巴芪柔肝方基准样品HPLC 特征图谱建立及其量值传递规律研究
2024-03-12耿赛龙孙水根赵立杰张继全
耿赛龙,周 琴,孙水根,李 曼,赵立杰,张继全∗,冯 怡∗
(1.上海中医药大学创新中药研究院,中药现代制剂技术教育部工程研究中心,上海 201203; 2.上海中医药大学附属曙光医院细胞免疫实验室,上海 201203)
巴芪柔肝方是上海中医药大学附属曙光医院治疗肝纤维化的中药复方,由巴戟肉、黄芪、地黄、泽兰、片姜黄、醋青皮6 味中药组成,功效补肾益气、活血化瘀,主治脾肾亏虚兼淤血阻络的慢性肝病纤维化,目前已申请相关专利[1]。如何建立有效的质量评价方法,确定合理的制备工艺,保证制剂的质量稳定,是临床经方走向院内制剂或中药新药过程中必须面临的问题[2-3]。在尊重临床应用实际的基础上,选择汤液基准样品作为实验对象,以特征/指纹图谱表征方剂质量整体性和个性,通过特征成分在制备过程中的转移变化佐证工艺参数的合理性,建立一套多维度的评价方式,已逐渐成为制剂质量研究的新趋向[4-5]。本实验建立巴芪柔肝方基准样品HPLC 特征图谱,并考察其量值传递规律,以期为该方质量评价体系开发提供参考。
1 材料
1.1 仪器 Agilent 1200/1260 型高效液相色谱仪,配置VWD、ELSD 检测器,购自美国安捷伦公司;XP205 型电子天平(十万分之一),购自梅特勒-托利多仪器(上海) 有限公司; FA2104N 型电子天平(万分之一),购自上海精密科学仪器有限公司; ZNHW 型电热套,购自巩义市予华仪器有限责任公司; HSH-6 型水浴锅,购自常州荣华仪器制造有限公司; R-210 型旋转蒸发仪,购自瑞士步琦公司; PB-10 型酸度计,购自赛多利斯科学仪器(北京) 有限公司。
1.2 试剂与药物 毛蕊异黄酮葡萄糖苷(批号111920-201907)、橙皮苷(批号110721-202019)、迷迭香酸(批号111871-202007)、柚皮苷(批号110722-202116) 对照品均购自中国食品药品检定研究院; 5-羟甲基糠醛(批号PS020460)、莪术烯醇(批号PU1007) 对照品均购自成都普思生物科技股份有限公司; 橘皮素(批号ST00630120)、芸香柚皮苷(批号ST05590120)、川橙皮素(批号ST00690120) 对照品均购自上海诗丹德标准技术服务有限公司。巴戟肉、黄芪、生地黄、片姜黄、泽兰、醋青皮均收集自药材市场,经上海中医药大学中药学院生药教研室倪梁红副教授鉴定为正品。乙腈、甲醇、甲酸为色谱纯,均购自国药集团化学试剂有限公司; 水为超纯水,由实验室自制。
2 方法与结果
2.1 基准样品制备 在前期实验室提取工艺研究中,分别对加水量、提取次数、提取时间等因素进行考察,参照临床使用情况,最终确定制备方法为饮片加10 倍量水提取2 次,每次1.5 h。饮片信息见表1,以随机数字表组合成15 批,具体见表2。

表1 饮片信息Tab.1 Information of decoction pieces
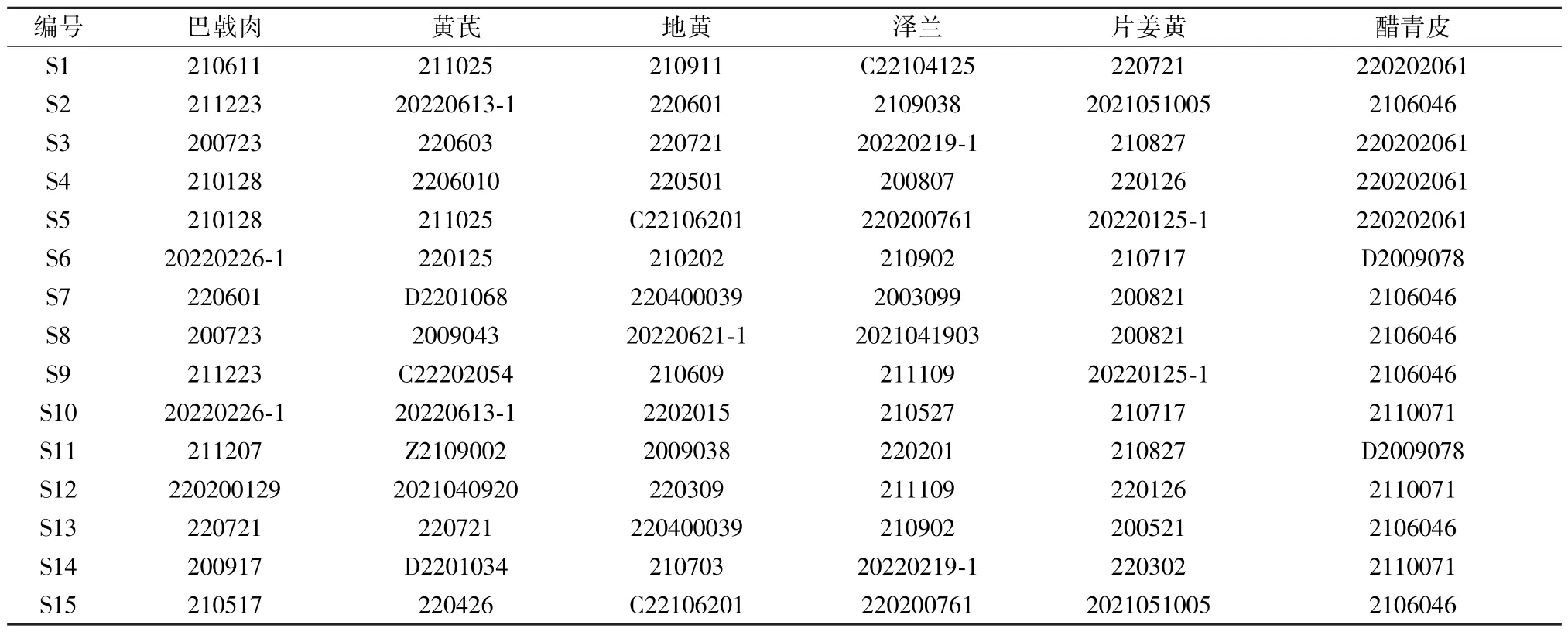
表2 饮片组合Tab.2 Combinations of decoction pieces
取巴戟肉、黄芪、地黄、泽兰各10 g,片姜黄9 g,醋青皮6 g,加550 mL 水煎煮2 次,每次1.5 h,300 目滤网趁热过滤,合并滤液,冷却至室温,减压浓缩至275 mL,即得。同法制备各单味饮片样品及其对应阴性样品。
2.2 HPLC 特征图谱建立
2.2.1 色谱条件 Shiseido CAPCELL PAK MG C18色谱柱(4.6 mm×250 mm,5 μm); 流动相乙腈-0.2%甲酸,梯度洗脱(0 ~10 min,4%乙腈; 10 ~22 min,4% ~13% 乙腈; 22 ~42 min,13% 乙腈;42 ~45 min,13% ~15%乙腈; 45 ~65 min,15% ~18%乙腈; 65 ~70 min,18% 乙腈; 70 ~85 min,18% ~21% 乙腈; 85 ~90 min,21% ~36% 乙腈;90~95 min,36%乙腈; 95~110 min,36% ~44%乙腈; 110 ~115 min,44% ~48% 乙腈; 115 ~120 min,48% ~50%乙腈); 体积流量1.0 mL/min; 柱温30 ℃; 检测波长260 nm; 进样量10 μL。
2.2.2 供试品溶液制备 精密吸取基准样品5 mL至10 mL 量瓶中,超纯水稀释定容至刻度,摇匀,超声(450 W、40 kHz) 提取5 min 后12 000 r/min离心10 min,取上清液,即得。
2.2.3 对照品溶液制备 精密称取5-羟甲基糠醛、毛蕊异黄酮葡萄糖苷、芸香柚皮苷、柚皮苷、橙皮苷、迷迭香酸、川橙皮素、莪术烯醇、橘皮素对照品适量,甲醇制成质量浓度分别为38.01、39.14、159.76、39.64、40.96、81.54、45.42、41.56、200.50 μg/mL 的溶液,即得。
2.2.4 方法学考察
2.2.4.1 精密度试验 取第13 批基准样品的供试品溶液适量,在“2.2.1” 项色谱条件下进样测定6 次,以橙皮苷为参照,测得各特征峰相对保留时间RSD 均小于0.15%,相对峰面积RSD 均小于2.02%,表明仪器精密度良好。
2.2.4.2 重复性试验 取第13 批基准样品的供试品溶液6 份,在“2.2.1” 项色谱条件下进样测定,以橙皮苷为参照,测得各特征峰相对保留时间RSD 均小于0.11%,相对峰面积RSD 均小于2.11%,表明该方法重复性良好。
2.2.4.3 稳定性试验 取第13 批基准样品的供试品溶液适量,于0、2、4、8、12、24 h 在“2.2.1”项色谱条件下进样测定,以橙皮苷为参照,测得各特征峰相对保留时间RSD 均小于0.27%,相对峰面积RSD 均小于2.33%,表明溶液在24 h 内稳定性良好。
2.2.5 特征峰归属和指认 取15 批基准样品的供试品溶液适量,在“2.2.1” 项色谱条件下进样测定,将相关数据导入“中药色谱指纹图谱相似度评价系统” (2012 年版) 软件,以第13 批数据为参照,采用平均数法,设置时间窗为0.5,自动匹配色谱峰,以共有模式色谱为对照测定相似度,结果见表3,可知均大于0.90,表明所选特征物质群在不同批次之间较稳定。HPLC 特征图谱见图1。

图1 15 批巴芪柔肝方基准样品HPLC 特征图谱Fig.1 HPLC characteristic chromatograms of fifteen batches of Baqi Rougan Decoction reference samples
综合实际分离情况与文献[6] 报道进行目标峰取舍,尽量使所选特征峰能反映药味特点,最终通过对照品比对在16 个特征峰中指认出9 个,见图2。再通过比对全方、单味药(图3)、阴性样品(图4) HPLC 特征图谱来进行归属,发现峰1归属于巴戟肉,峰2 (5-羟甲基糠醛) 为地黄、巴戟肉共有特征峰,峰12、5 (毛蕊异黄酮葡萄糖苷) 归属于黄芪,峰6、11 (迷迭香酸) 归属于泽兰,峰4、8、15 (莪术烯醇) 归属于片姜黄,峰3、7 (芸香柚皮苷)、9 (柚皮苷)、10 (橙皮苷)、13、14 (川橙皮素)、16 (橘皮素) 归属于醋青皮,表明所有药味均有特征峰,归属关系明确,可较稳定地从饮片传递到基准样品。
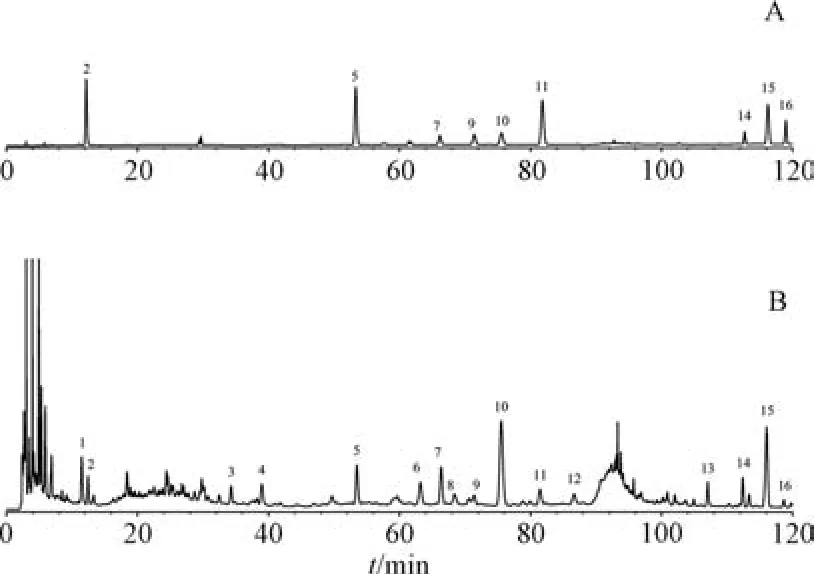
图2 对照品(A)、巴芪柔肝方基准样品(B) HPLC 特征图谱Fig.2 HPLC characteristic chromatograms of reference substances ( A) and Baqi Rougan Decoction reference sample (B)

图3 巴芪柔肝方基准样品、单味药HPLC 特征图谱Fig.3 HPLC characteristic chromatograms of Baqi Rougan Decoction reference sample and single drugs

图4 巴芪柔肝方基准样品、阴性样品HPLC 特征图谱Fig.4 HPLC characteristic chromatograms of Baqi Rougan Decoction reference sample and negative samples
2.3 成分含量测定及量值传递规律研究
2.3.1 毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇
2.3.1.1 色谱条件 同“2.2.1” 项。
2.3.1.2 供试品溶液的制备 同“2.2.2” 项。
2.3.1.3 对照品溶液制备 精密称取毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇对照品适量,甲醇制成质量浓度分别为1 117.07、639.46、1 032.99、1 240.68 μg/mL 的溶液,即得。
2.3.1.4 线性关系考察 精密吸取 “2.3.1.3”项下对照品溶液适量,甲醇稀释成系列质量浓度,在“2.2.1” 项色谱条件下进样测定。以对照品峰面积为纵坐标(Y),进样量为横坐标(X) 进行回归,并分别以信噪比(S/N) 3、10 为检出限、定量限,结果见表4,可知各成分在各自范围内线性关系良好。

表4 各成分线性关系Tab.4 Linear relationships of various constituents
2.3.1.5 精密度试验 按“2.2.4.1” 项下方法操作,测得毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇峰面积RSD 分别为0.69%、0.11%、0.90%、0.23%,表明仪器精密度良好。
2.3.1.6 重复性试验 按“2.2.4.2” 项下方法操作,测得毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇含量RSD 分别为0.85%、0.28%、0.77%、0.30%,表明该方法重复性良好。
2.3.1.7 稳定性试验 按“2.2.4.3” 项下方法操作,测得毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇峰面积RSD 分别为0.86%、0.11%、1.29%、0.23%,表明溶液在24 h 内稳定性良好。
2.3.1.8 加样回收率试验 取第13 批基准样品适量,按100%水平加入对照品(含毛蕊异黄酮葡萄糖苷0.052 mg、橙皮苷1.090 mg、迷迭香酸0.095 mg、莪术烯醇0.249 mg),按“2.2.2” 项下方法制备6 份供试品溶液,在“2.2.1” 项色谱条件下进样测定,计算回收率。结果,毛蕊异黄酮葡萄糖苷、橙皮苷、迷迭香酸、莪术烯醇平均加样回收率分别为 95.34%、99.55%、101.86%、98.38%、99.81%,RSD 分别为2.17%、1.84%、2.15%、1.87%。
2.3.2 耐斯糖含量测定
2.3.2.1 色谱条件 YMC-Triart C18色谱柱(4.6 mm×250 mm,5 μm); 流动相甲醇-0.1% 甲酸 (1 ∶99); 体积流量0.7 mL/min; 柱温20 ℃; 进样量10 μL; 蒸发光散射检测器雾化温度35 ℃; 蒸发温度80 ℃; 气体体积流量1.7 L/s; PMT 2.0。
2.3.2.2 供试品溶液制备 取基准样品的供试品溶液适量,12 000 r/min 离心10 min,精密移取上清液2.5 mL,超纯水稀释定容至10 mL 量瓶中,摇匀,即得。
2.3.2.3 对照品溶液制备 精密称取耐斯糖对照品适量,加水制成质量浓度为978.24 μg/mL 的溶液,即得。
2.3.2.4 专属性考察 分取吸取样品制备用水、对照品溶液、缺巴戟肉阴性样品溶液、供试品溶液适量,在“2.3.2.1” 项色谱条件下进样测定,发现阴性无干扰,表明该方法专属性良好。
2.3.2.5 线性关系考察 精密吸取对照品溶液适量,超纯水依次稀释至782.59、586.95、391.30、293.47、195.65、146.74 μg/mL,在“3.2.1” 项色谱条件下进样测定。以峰面积对数值(Y) 对进样量对数值(X) 进行回归,并分别以信噪比(S/N) 3、10 为检出限、定量限,结果见表4,可知耐斯糖在其范围内线性关系良好。
2.3.2.6 精密度试验 取第13 批基准样品的供试品溶液适量,在“2.3.2.1” 项色谱条件下进样测定6 次,测得耐斯糖峰面积RSD 为1.43%,表明仪器精密度良好。
2.3.2.7 重复性试验 取第13 批基准样品适量,按“2.3.2.2” 项下方法平行制备6 份供试品溶液,在“2.3.2.1” 项色谱条件下进样测定,测得耐斯糖含量RSD 为1.28%,表明该方法重复性良好。
2.3.2.8 稳定性试验 取第13 批基准样品的供试品溶液适量,于0、2、4、8、12、24 h 在“2.3.2.1”项色谱条件下进样测定,测得耐斯糖峰面积RSD为1.51%,表明溶液在24 h 内稳定性良好。
2.3.2.9 准确度试验 取第13 批基准样品适量,按100% 水平加入耐斯糖对照品1.770 mg,按“2.3.2.2” 项下方法制备6 份供试品溶液,在“2.3.2.1” 项色谱条件下进样测定,计算回收率。结果,耐斯糖平均加样回收率为99.81%,RSD为1.65%。
2.3.3 饮片-水煎液-基准样品中传递规律 分别按“2.3.1” “2.3.2” 项下方法测定各成分含量,计算转移率,结果见表5~6。由此可知,黄芪饮片中毛蕊异黄酮葡萄糖苷平均含量为(0.060±0.011)%,饮片-基准样品平均转移率为(77.81±8.31)%; 巴戟肉饮片中耐斯糖平均含量为(5.49±0.77%),饮片-基准样品平均转移率为(83.14±6.25)%。

表5 黄芪饮片-水煎液-基准样品毛蕊异黄酮葡萄糖苷含量、转移率测定结果Tab.5 Results for content and transfer rate determination of calycosin 7-O-glucoside in Astragali Radix decoction pieceaqueous decoction-reference sample

表6 巴戟肉饮片-水煎液-基准样品中耐斯糖含量、转移率测定结果Tab.6 Results for content and transfer rate determination of nystose in Morindae officinalis Radix decoction piece-aqueous decoction-reference sample
除了关注君药巴戟肉、黄芪中相对稳定成分的转移过程外,本实验对泽兰所含迷迭香酸、片姜黄所含莪术烯醇在水煎液-基准样品中的含量也进行了测定,结果见图5,可知两者平均转移率分别为(81.71±6.27)%、(72.16±5.91)%。另外,在热的水溶液中上述2 种成分均表现出不稳定性,可能与其结构密切相关,迷迭香酸中缩合咖啡酸、丹参素的酯键易受热水解[7-8],而莪术烯醇的烯醇式结构易受溶剂环境、温度影响发生转化[9-10]。在当前水溶液体系和热作用过程中,不同批次样品之间的差异可能会导致迷迭香酸、莪术烯醇变化更复杂,从而产生更离散的转移率分布。因此,不稳定化合物在制备过程中的量值变化规律可作为工艺条件对物料影响程度的指标[11],对其变化速率、程度的探索可为工艺参数选择提供重要参考。
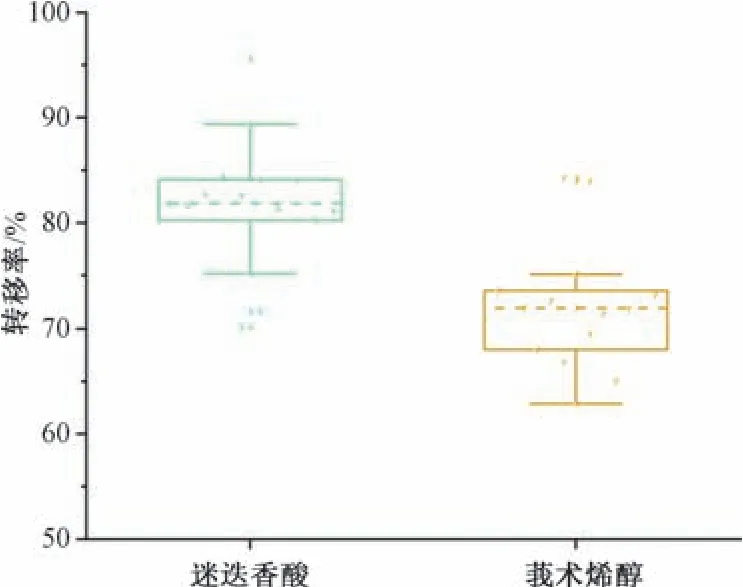
图5 迷迭香酸、莪术烯醇转移率Fig.5 Transfer rates of rosmarinic acid and curcumenol
2.4 出膏率、pH 值测定
2.4.1 出膏率 精密吸取基准样品供试品溶液10 mL,置于已恒重的蒸发皿中,水浴蒸干后在105 ℃下干燥3 h,取出,置于干燥器中冷却至室温,精密称定质量,以2 次称定结果之差计算出膏率。结果,15 批样品平均出膏率为 (38.91 ±1.46)%,稳定性较好。
2.4.2 pH 值 取基准样品水提液20 mL,测定pH 值,平行3 次,结果见表7。由此可知,15 批样品平均pH 值为5.13±0.08,即呈弱酸性。
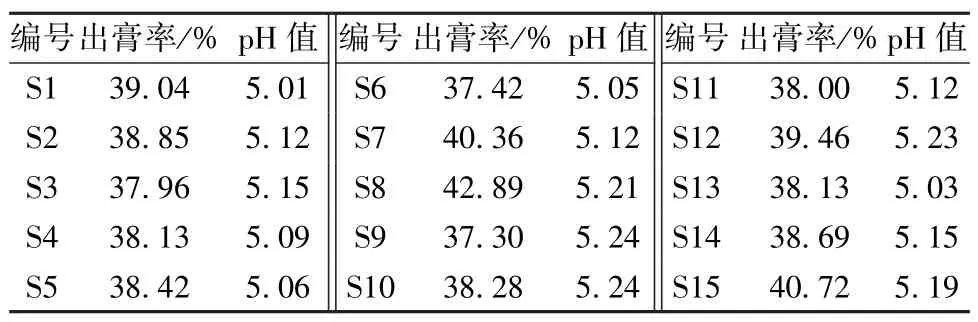
表7 出膏率、pH 值测定结果Tab.7 Results for paste-forming rate and pH value determination
3 讨论
3.1 特征成分选择 特征成分是否对方中药味具有一定的代表性,是进行指标筛选的重要考量依据[12]。去乙酰车叶草苷酸是巴戟肉中典型的环烯醚萜类成分之一,相较于巴戟天在炮制过程中寡糖类成分的裂解,其含量更稳定[13-14],但极性与其他成分差异过大,虽然前期实验已指认(保留时间约5 min),但考虑到整体协调未将该成分作为特征峰处理。基于色谱条件、专属性要求,绿原酸、槲皮素、芦丁等化合物也均未标示为特征峰。地黄中梓醇、地黄苷D 均在紫外末端吸收而不易被准确测定,前期发现两者在巴芪柔肝方中的专属性均不强,含量均过低,不适合作为该药材特征成分。5-羟甲基糠醛作为美拉德反应中的标志性产物,其含量变化与受热过程有关[15-16],在含糖丰富的地黄、巴戟肉中均能检测到,可间接反映两者炮制程度。毛蕊异黄酮葡萄糖苷作为黄芪中重要的黄酮类成分之一,被认为是该药材潜在质量标志物[17]。迷迭香酸是泽兰中酚酸类成分的代表[18]。莪术烯醇是片姜黄水提后保留的主要倍半萜类化合物[19-20]。橙皮苷作为青皮中标志性黄酮类成分,与柚皮苷、新橙皮苷含量的差异可区别于同属植物枳实、枳壳、化橘红,具有一定代表性[21-23]。
3.2 色谱条件选择 为了使包含酚酸、黄酮、倍半萜等多种类型成分的目标物质能协调地呈现在色谱图上,需结合波长扫描(210 ~400 nm) 来观察整体分离情况,最终选择260 nm 作为检测波长。在流动相考察过程中,本实验比较了冰醋酸、甲酸、磷酸对峰形的改善作用,发现加入甲酸时分离度最佳。在供试品溶液制备过程中,提高甲醇体积分数会使色谱前段的峰面积降低,故选择水作为稀释溶剂。在色谱柱筛选过程中,本实验对郁金香、月旭、Shiseido、SVEA、HICHROM、Kromasil 等品牌的C18色谱柱进行测试,最终选择分离度较好的Shiseido 色谱柱。
4 结论
本实验采用多批次来源饮片,筛选稳定存在、能体现药味特点的色谱信息建立巴芪柔肝方HPLC特征图谱,并进行多成分含量测定,同时结合工艺流程中热稳定或热不稳定指标成分的转移率,可为确定该方工艺参数、探索其关键质量属性提供参考。
