经导管三尖瓣缘对缘修复术的应用现状
2024-03-11谢春梅沈梦奇朱达王首正骆志玲潘湘斌
谢春梅 沈梦奇 朱达 王首正,3 骆志玲 潘湘斌,3
三尖瓣反流(tricuspid regurgitation,TR)是常见的心脏瓣膜病变,研究提示65岁以上老年人中度以上TR发病率>2.6%,75岁以上老年人中度以上TR发病率约3.96%[1]。我国一项基于医院就诊人群的14万例经胸超声心动图数据报道,中、重度TR的检出率分别为2.22%和1.39%[2]。根据发病机制,TR可分为原发性(器质性)和继发性(功能性)反流。原发性TR较少见,病因包括先天性(三尖瓣下移畸形)、风湿性疾病、黏液瘤、感染性心内膜炎、心内膜心肌纤维变性、创伤、医源性因素(起搏器/自动除颤器电极植入或右心室活检)等[3]。功能性TR最常见,超过90%[4],主要是由于右心室压力或容量负荷增加、右心室增大、瓣环扩张、瓣叶对合错位等。瓣环成形术是外科治疗TR的主要手段,通常推荐在左心疾病手术时同期进行。而对于孤立性TR患者,由于外科手术风险较高,需要慎重权衡手术利弊[5]。研究表明,目前TR的治疗需求远未被满足,美国流行病学数据显示,约有160万中、重度的TR患者,但接受手术治疗还不足0.5%[6]。由于三尖瓣患者症状隐匿,往往行外科干预前患者一般情况已较差,单纯外科三尖瓣手术风险高,其中既往行左心瓣膜术后再次单独行三尖瓣手术的院内死亡率高达10.6%[7];既往三尖瓣生物瓣置换术或瓣膜成形术后再次三尖瓣手术的术后30 d死亡率更是高达35%[8]。
对于长期药物维持治疗的TR患者,以及既往有开胸心脏手术史等高风险及手术禁忌人群,经导管介入治疗提供了新的治疗方式[9]。TR的经导管介入治疗包括介入瓣环成形、异位瓣膜置入、原位瓣膜置换、瓣叶修复术。早期研究表明,经导管三尖瓣介入成形或置换可以减少或消除TR,能够改善患者症状和血流动力学状态[10]。 经导管三尖瓣缘对缘修复术( transcatheter edge-to-edge tricuspid valve repair,T-TEER)通过夹闭瓣叶进而降低反流程度,是目前应用最多、证据最充分、器械进展最快的术式。本文就T-TEER的器械演变、循证医学证据以及未来面临的挑战进行综述。
1 T-TEER 技术原理及流程(图1)
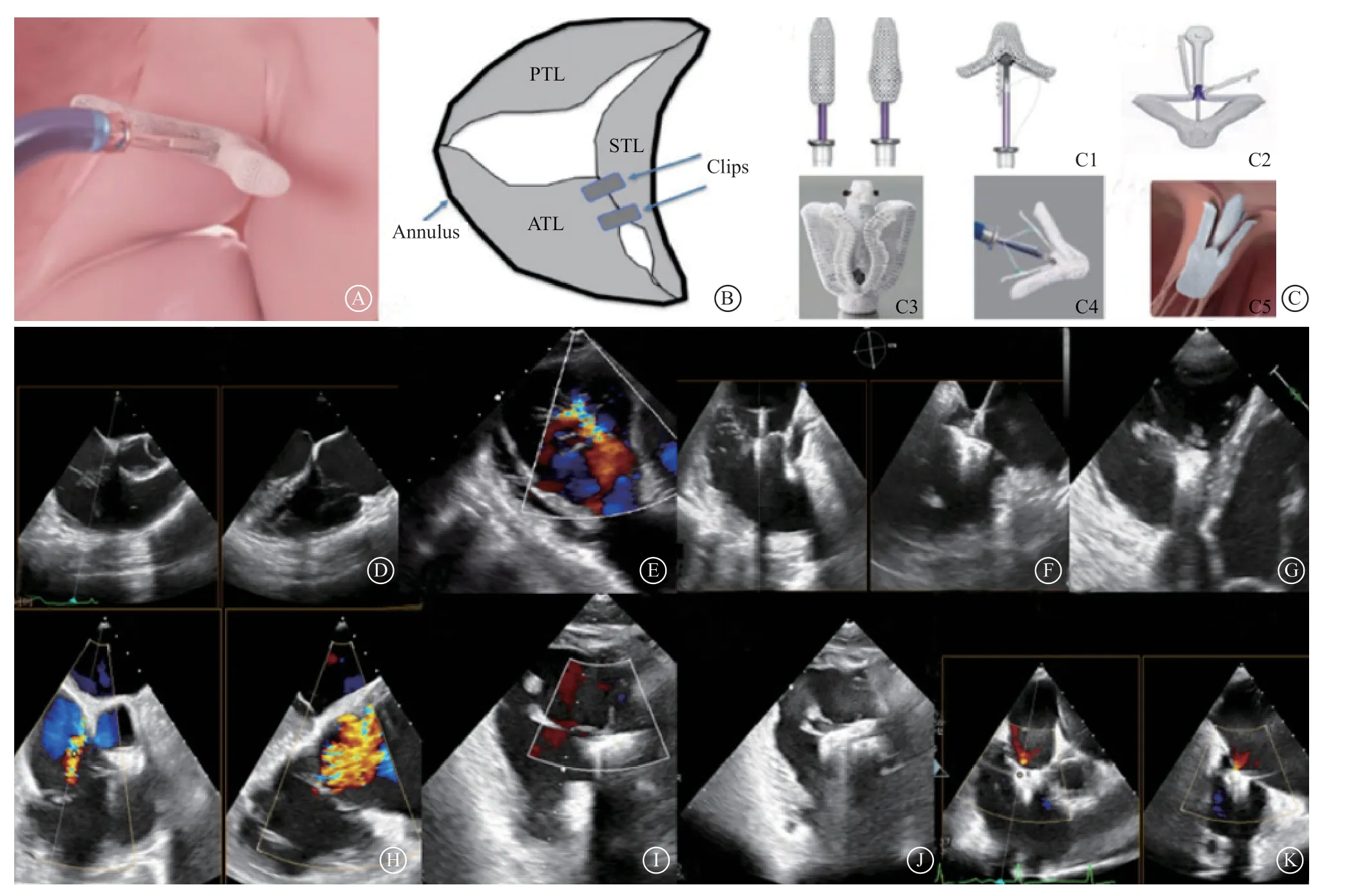
图1 T-TEER 技术原理及流程 A.T-TEER 的技术模拟图;B.T-TEER 瓣夹置入位置示意图;C1.TriClip G4 器械,其具备加宽瓣夹设计以及单瓣叶捕获功能;C2.PASCAL 系统Ace 瓣夹;C3.端佑NeoBlazarTM 系统瓣夹;C4.SQ-Kyrin-TTM 系统瓣夹;C5.DragonFly-TTM 系统瓣夹;D.TEE 核心切面,食管中段右心室流入道切面+利用X-Plane 获得反四腔心切面(靠近主动脉侧获取的图像为前隔交界图像);E.TEE 胃底短轴切面;F~G.SQ-Kyrin-TTM系统瓣夹抓捕前隔交界,胃底短轴确认瓣叶抓捕;H~K.端佑NeoBlazarTM 系统治疗三尖瓣反流,术前三尖瓣反流4+,置入2 枚瓣夹,反流基本消失Figure 1 Technical principle and f low chart of (T-TEER)
三尖瓣瓣膜由前叶、后叶、隔叶组成,瓣叶解剖变异时前、后及隔瓣瓣叶均可能分叶成为2个独立的瓣叶。功能性TR的主要解剖基础为瓣环朝后叶及前叶方向的右心室游离壁扩张,T-TEER治疗是通过在前隔/后隔瓣叶对合缘置入瓣夹,以达到降低TR、限制瓣环扩张的作用。T-TEER对于三尖瓣解剖要求较高,其核心筛选条件包括:(1)功能性TR且瓣叶组织正常(无挛缩、活动受限、钙化及明显增厚);(2)反流主要来源于前隔交界;(3)对合间隙不超过4 mm,且无金属导线跨越三尖瓣;(4)右心功能正常或仅轻度降低且无肺动脉高压。
其手术技术体系与经导管二尖瓣缘对缘修复术一脉相承,主要采用经食管超声心动图(transesophageal echocardiography,TEE)引导,切面采用 食管中段右心室流入道切面, 利用X线获得反四腔心切面 (靠近主动脉侧获取的图像即为前隔交界图像),此组切面可以帮助确定瓣夹是靠主动脉-下腔静脉(隔叶)还是右心室外侧壁(前叶/后叶)两个维度的定位(图1D),胃底短轴切面负责定位瓣夹是否垂直于对合缘,判定瓣夹是否捕获足够多的瓣叶(图1E)。通过上述3个切面,可以准确定位瓣夹位置,并引导准确夹合瓣膜病变区域[11]。为了确保更好的效果,T-TEER一般需置入2~3枚瓣夹,从而更好地关闭前隔交界,降低TR及达到更好的瓣环塑形作用。
2 T-TEER 器械演变及循证医学证据(表1)
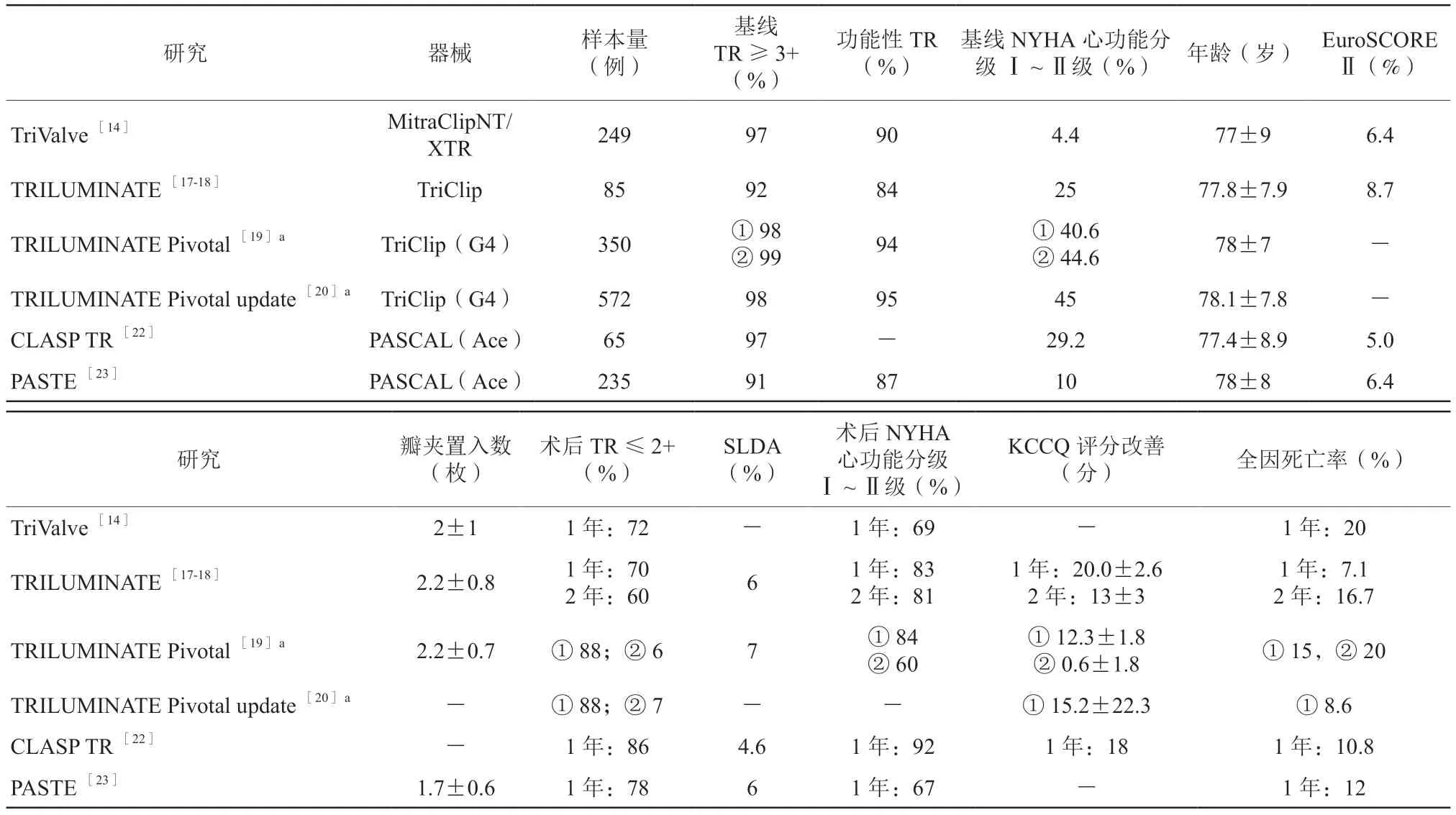
表1 经导管三尖瓣缘对缘修复术器械演变及循证医学证据进展Table 1 Evolution of instruments and progress of evidence-based medical evidence for transcatheter edge-to-edge tricuspid valve repair
2.1 MitraClip系统
MitraClip系统(Abbott Vascular,Santa Clara,Calif ornia,USA)是世界范围内临床应用最广泛的 经导管二尖瓣缘对缘修复系统,也是最早应用于T-TEER的器械。早期T-TEER多见于病例报道,Kowalski等[12]使用MitraClip器械经股静脉同期完成三尖瓣及二尖瓣的瓣叶修复。TriValve研究[13-14]是国际多中心回顾性注册研究,目的是收集使用不同器械进行经导管三尖瓣治疗的患者数据,采用TR 5级分类法:0+(无或微量)、1+(轻度)、2+(中度)、3+(重度)或4+(大量或汹涌)[15]。研究期间有249例TR患者使用MitraClip完成经股静脉T-TEER(占总样本数约60%),基线功能性TR 90%,纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅲ~Ⅳ级96%。96%患者成功放置至少1枚瓣夹,TR≥3+患者的比例从术前的97%降到出院前的23%(P<0.001),并且77%的患者TR≤2+,夹合后的平均跨瓣压差(2.5±1.4)mmHg(1 mmHg=0.133 kPa)。1年随访,44例(19%)患者死亡,76例(31%)患者因心力衰竭死亡或计划外再入院,T-TEER成功患者的死亡率显著低于失败患者(17.0%比30.8%,P=0.003),179例(72%)患者TR ≤2+,172例(69%)患者NYHA心功能分级≤Ⅱ级。该研究结果提示,使用MitraClip实施T-TEER安全可靠,能有效降低TR程度,并持续改善患者心功能。TriValve研究还分析了T-TEER失败的预测因素:非中心性/前隔联合部反流、较大的对合间隙大小(≥6.4 mm)、较大的三尖瓣隆起面积(≥3.2 cm2)和较大的有效反流口面积(≥0.70 cm2) 。Besler等[16]研究也提示,在使用MitraClip NTR器械时,三尖瓣较大对合间隙(>7 mm)已被确定为T-TEER失败的独立预测因素。
2.2 TriClip系统
TriClip系统(Abbott,Chicago,IL,USA)是专门设计用于T-TEER的器械,于2020年4月获得欧盟(Conformite Europeenne,CE)批准,是全球第一款获批的T-TEER器械,其瓣夹系统具备分开捕获的能力,并且根据三尖瓣的解剖位置和结构改进了输送系统,在引导鞘上设计了S-L调弯钮,便于更好地调整瓣夹轴向对准三尖瓣环,并且提供4种不同尺寸的瓣夹和可操控的夹持器驱动模式,可以优化瓣叶抓取。
TRILUMINATE第一阶段研究[17]是评价TriClip系统临床安全性及有效性的前瞻性多中心单臂研究。纳入85例TR≥2+的患者,其中功能性TR为84%,NYHA心功能分级Ⅲ~Ⅳ级75%。术后30 d内5例(6%)患者发生单瓣叶附着,之后的随访中无新增病例。63例患者完成1年随访,全因死亡率和主要不良心血管事件发生率均为7.1%,70%的患者TR≤2+,83%的患者NHYA心功能分级≤Ⅱ级(P<0.0001),6 min步行距离增加31 m(P=0.0023)。48例患者完成2年随访,心血管死亡率13.1%,全因死亡率16.7%,60%的患者TR≤2+,NYHA心功能分级、堪萨斯城心肌病问卷调查(Kansas city cardiomyopathy questionnaire,KCCQ)评分和6 min步行距离的临床改善主要发生在术后的30 d内,并在2年的随访期间基本维持不变[18]。
TRILUMINATE Pivotal研究[19]是首个在重度TR患者中评价T-TEER疗效的随机对照研究,共纳入350例患者,功能性TR为94%,基线T-TEER组(175例)和单纯药物治疗的对照组(175例)中各有169例、163例患者TR≥3+,T-TEER组中170例患者(98.8%)成功置入TriClip装置,平均置入(2.2±0.7)枚夹子(3例同意撤回)。术后30 d内共有12例患者发生夹子单瓣叶脱位,30 d后无相关不良事件发生。1年随访,T-TEER组(143例)和对照组(141例)中各有126例(88%)、8例(6%)患者TR≤2+,T-TEER组和对照组全因死亡率或三尖瓣外科手术率比较(15%比20%)、心力衰竭年再入院次数比较(0.35次/例比0.50次/例),差异均无统计学意义,但是T-TEER组和对照组的KCCQ-OS评分分别平均增加了(12.3±1.8)分和(0.6±1.8)分,差异有统计学意义(P<0.001),T-TEER组6 min步行距离平均变化(-8.1±10.5)m、对照组(-25.2±10.3)m,差异无统计学意义(P=0.25),T-TEER组NYHA心功能分级Ⅰ~Ⅱ级患者84%、对照组60%。在2023年10月美国经导管心血管治疗学术会议上公布了TRILUMINATE Pivotal研究[20]最新结果,分为2个队列:对于T-TEER术后预期TR≤2+的患者以1∶1的比例随机分配至TriClip组与药物治疗(对照)组,作为随机队列;对于预期TR程度降低至少1级(但未达到2+)的患者进行TriClip治疗,作为单臂队列。此次公布的数据除了包含之前公布的350例随机队列患者[19],另外纳入了222例随机队列患者和100例单臂队列患者。30 d时,单臂队列中单瓣叶附着的发生率为7.5%,与之前350例随机队列患者的7%相似,未发生其他重大不良事件。12个月时,572例随机队列中经过TriClip治疗后88%的患者TR≤2+,而对照组仅7%。此外,匹配后单臂队列中81%患者TR≤2+,随机队列中TriClip治疗组则89%患者TR≤2+。单臂队列的全因死亡率(15.0%比8.6%,P<0.05)和心力衰竭再入院率(24.0%比14.9%,P<0.05)显著高于随机队列中的TriClip治疗组。通过Win Ratio分析主要终点结局发现,随机队列中TriClip治疗组的胜率为1.53(P=0.0042)。在生活质量方面,TriClip组KCCQ评分提高了(15.2±22.3)分,单臂队列KCCQ评分则提高了(14.5±20.0)分[20]。研究提示,T-TEER虽然并未降低全因死亡或三尖瓣手术、心力衰竭再入院的复合终点事件发生率,但与单独药物治疗相比,使用TriClip设备进行T-TEER可快速、持续地改善患者的症状、功能状态和生活质量,基线KCCQ评分较低的患者更可能在T-TEER治疗后症状改善,这类患者可能是理想的干预对象[19-20]。
2.3 PASCAL系统
PASCAL系统(Edwards Lifesciences,Irvine,USA)是美国爱德华公司研发用于二尖瓣和三尖瓣疾病的TEER系统,采用超弹性的镍钛合金作为瓣夹骨架,其张力均匀分布可减少对瓣叶的损伤,已于2020年5月获得CE批准。PASCAL Ace器械的基本形态及工作原理同PASCAL,但其夹臂更窄、中央的隔离球(Spacer)更小[21]。
CLASP TR研究[22]是PASCAL系统用于治疗TR的早期可行性单臂研究,纳入65例TR≥3+患者,NYHA心功能分级Ⅲ~Ⅳ级70.8%,90.8%的患者成功置入瓣夹(62%置入PASCAL,33%置入PASCAL Ace,5%同时置入两者)。45例患者完成1年随访,全因死亡率10.8%,心血管死亡率7.7%,与器械无关的脑卒中发生率4.6%,术后30 d内的单瓣叶附着发生率4.6%,92%的患者NYHA心功能分级Ⅰ~Ⅱ级(P<0.001)、6 min步行距离增加94 m(P=0.014)、KCCQ评分提高18分(P<0.001),86%的患者TR≤2+(P<0.001)。与基线时相比,右心重构良好:右心室舒张末期内径[(4.0±0.9)cm比(3.5±0.7)cm,P<0.001]、三尖瓣环直径[(4.5±0.8)cm比(4.0±0.6)cm,P<0.001]。研究提示,在手术高风险的严重TR患者中,使用PASCAL(Ace)系统进行T-TEER安全性好、TR程度持续降低、生活质量改善明显。
PASTE回顾性多中心观察性队列研究[23]也观察到和CLASP TR研究相似的结果,该研究纳入235例TR患者,TR≥3+为91%,功能性TR 87%,NYHA心功能分级Ⅲ~Ⅳ级90%,63%置入PASCAL,35%置入PASCAL Ace,2%同时置入两者。196例患者完成1年随访,全因死亡率和心血管死亡率分别为12%和6%,器械失败率6%(多数为单瓣叶附着,1例无临床后遗症的器械栓塞),NYHA心功能分级Ⅰ~Ⅱ级67%,78%的患者TR≤2+,与基线相比6 min步行距离增加54 m[(264±115)m比(303±123)m,P<0.001]、右心室舒张末期内径[(56±9)mm比(53±9)mm,P<0.001]、右心房面积[(39±13)cm2比(37±12)cm2,P<0.001]。
3 T-TEER 技术在国内情况
目前,国内尚无注册上市的T-TEER器械,已进入临床研究的自主研发器械包括DragonFly-TTM(杭州德晋医疗科技有限公司)、SQ-Kyrin-TTM(上海申淇医疗科技有限公司)、NeoBlazarTM(江苏臻亿医疗科技有限公司)。
3.1 DragonFly-TTM系统
DragonFly-TTM系统的核心功能和技术参数可比拟TriClip和PASCAL(单侧瓣叶独立捕获技术及双调弯输送系统),另外还具有一些独特优势[24]:其瓣夹中央的球形垫片可伸展压缩,术中瓣夹完全夹闭后如果TEE提示瓣口面积小于最低标准或无法置入第2枚瓣夹,可于半夹闭的形态释放,且中央展开的球形垫片可减少瓣夹内的中心性反流。2020年12月,DragonFly-TTM系统首次应用于临床,术后TR由5+降到1+,2年随访时患者TR仍1+,NYHA心功能分级、右心房室结构、6 min步行距离改善明显,提示DragonFly-TTM系统治疗TR的可行性[25]。
3.2 SQ-Kyrin-TTM系统
SQ-Kyrin-TTM系统的独特优势包括:(1)4种尺寸的瓣夹(12/9 mm臂长,6/4 mm臂宽);(2)单侧瓣叶独立捕获技术;(3)导管多方向转向功能;(4)导管内标记有利于纯超声引导。在2023年的欧洲心血管介入会议上公布了SQKyrin-TTM系统用于治疗重度TR的首次人体试验(first in man,FIM)研究[26]结果,纳入12例功能性TR患者,基线NYHA心功能分级Ⅱ~Ⅲ级,术后30 d随访全因死亡率和严重不良事件发生率均为0,91.7%的患者TR程度至少降低2级,91.7%的患者NYHA心功能分级Ⅰ~Ⅱ级,提示SQ-Kyrin-TTM系统治疗TR的可行性。
3.3 NeoBlazarTM系统
该器械采用类似PASCAL的构架,具备独立捕获瓣叶的能力。2022年7月,NeoBlazarTM系统首次应用于临床。目前,NeoBlazarTM系统治疗TR的多中心前瞻性FIM研究,已有10例患者完成半年随访,TR≤2+的患者和NYHA心功能分级Ⅰ~Ⅱ级患者从基线时的0分别增加到80%和70%,半年无死亡,提示NeoBlazarTM系统治疗TR的初步有效性和安全性。
4 T-TEER 的未来展望和挑战
综上所述,虽然目前的证据尚不能表明T-TEER可以增加患者预期寿命,降低患者死亡率,但显示T-TEER技术的安全性良好,与药物治疗相比,并未增加死亡率、重大不良事件、心力衰竭再入院率,并且可以显著提高生活质量,而对于TR这类可以显著降低生活质量的慢性病变,一种安全有效并可改善生活质量治疗方式是必要的。进一步分析,反流量的改善及残余反流量与KCCQ评分明显相关,再次验证了T-TEER对生活质量改善的作用。 深入分析TRILUMINATE研究[17-20]在硬终点全因死亡或因心力衰竭再入院方面没有获益,可能因为:(1)三尖瓣患者耐受性较好,存活期相对较长,TRILUMINATE研究中两组患者基础年龄已高达78岁,但1年生存率均在90%水平,高龄患者影响生存因素本身就偏多;(2)TR自然病程相对较长,但该试验时间相对较短,随访时间只有1年,可能暂时体现不出差别;(3)三尖瓣是一个相对隐秘容易被忽视的瓣膜、疾病谱较宽、发病机制不尽相通,引起TR的病变很多(肺动脉高压、左心系统不良、右心功能差、心房颤动等),因此TR人群具有很大异质性。根据临床实践经验,反流量特别巨大、瓣环极度扩张患者解剖上是不适合TEER的,而此类患者可能是降低三尖瓣反流获益最明显的人群。然而,哪类重度TR患者行T-TEER可有临床获益,哪类患者临床获益有限甚至不能获益,未来应该进行更深入的研究和亚组分析。
目前,T-TEER多数应用于功能性TR且数量有限,对于原发性TR,经导管治疗的证据更不足。因此,需要选择合适的患者,才可以更好地提高T-TEER的临床效果。初期临床研究验证了T-TEER的安全性与有效性,但仍缺乏高质量的前瞻性对照研究和长期的有效性观察,加之三尖瓣解剖较复杂、右心室变异大、患者群体差异大等因素,T-TEER技术的循证医学之路还将面临诸多挑战。
利益冲突 所有作者均声明不存在利益冲突
