增强CT评估肝硬化患者自发性门体分流研究
2024-03-08史明君张祥林
史明君 张祥林


[摘要] 目的 探討增强CT评价肝硬化门静脉高压患者自发性门体分流(spontaneous portosystemic shunts,SPSS)的影像价值及相关临床特征。方法 回顾性收集2020年6月至2022年7月于盘锦市中心医院就诊的肝硬化患者,进行腹部增强CT检查评价自发性门体分流存在、大小及类型,进行统计学分析,并记录相关临床及实验室指标。结果 本研究共纳入119例肝硬化患者。无SPSS组、SPSS<8mm组与SPSS≥8mm组三组患者的总胆红素、白蛋白、凝血酶原时间、国际标准化比值、Child-Pugh分级、肝性脑病、门静脉血栓、肾静脉直径比较,差异有统计学意义(P<0.05)。多因素Logistic分析可以发现Child-Pugh C级、门静脉血栓为发生SPSS≥8mm的独立危险因素。无SSRS组、SSRS组中,尿酸值、胃左静脉直径、左肾静脉直径比较,差异有统计学意义(P<0.05)。结论 通过增强CT可尽早发现SPSS的存在,存在SPSS特别是直径≥8mm的患者肝功能更差,更易发生门静脉血栓。SPSS在一定程度上能反映患者的肝硬化状态。
[关键词] 肝硬化;门静脉高压;自发性门体分流;肝功能;肾功能
[中图分类号] R445 [文献标识码] A [DOI] 10.3969/j.issn.1673-9701.2024.05.013
Study of spontaneous portosystemic shunts in patients with cirrhosis evaluated by enhanced CT
SHI Mingjun, ZHANG Xianglin
Department of Radiology, the First Affiliated Hospital of Jinzhou Medical University, Jinzhou 121000, Liaoning, China
[Abstract] Objective To investigate the imaging value and associated clinical features of enhanced CT evaluation of spontaneous portosystemic shunts (SPSS) in patients with cirrhotic portal hypertension. Methods Patients with cirrhosis who attended Panjin Central Hospital from June 2020 to July 2022 were retrospectively collected to evaluate the presence, size and type of spontaneous portal shunts for statistical analysis, and relevant clinical and laboratory indices were recorded. Results A total of 119 patients with liver cirrhosis were included in this study. Total bilirubin level, albumin level, prothrombin time, international normalized ratio, Child-Pugh grade, hepatic encephalopathy, portal vein thrombosis, and renal vein diameter were all statistically significant difference (P<0.05) compared to the three groups of patients in the no-SPSS, SPSS<8mm and SPSS≥8mm groups. Multi-factor logistic analysis could identify Child-Pugh grade C and portal vein thrombosis as independent risk factors for the occurrence of spontaneous splenorenal shunt (SSRS) ≥8mm. In the group without SPSS and in the group with SSRS, there was a statistically significant difference (P<0.05). When comparing uric acid values, left gastric vein diameter and left renal vein diameter. Conclusion The presence of SPSS can be detected early by enhancing CT. The presence of SPSS, especially in patients with a diameter greater than or equal to 8mm, is associated with poorer liver function and a greater risk of portal vein thrombosis; the presence of SPSS reflects the patients cirrhotic state to some extent.
[Key words] Liver cirrhosis; Portal hypertension; Spontaneous portosystemic shunts; Liver function; Renal function
自发性门体分流的存在是严重门脉高压的一种的特异性表现[1],也被认为是一种降低门脉高压的代偿机制[2]。自发性脾肾分流(spontaneous splenorenal shunt,SSRS)是SPSS中较常见的一种,包括直接的脾肾分流和间接的胃肾分流两种[3]。通过影像学检查评估分流道的类型及大小[4-5],是介入治疗术前的重要一步,spontaneous portosystemic shunts(SPSS)直径能有效预测球囊闭合逆行静脉闭塞术的治疗结果[6]。本研究分析SPSS在其存在、大小及类型方面与肝硬化患者的实验室指标、临床相关并发症等的相关关系,进一步探讨SPSS是肝硬化患者的保护因素还是危险因素。通过增强CT这种常规检查手段尽早发现SPSS的存在,并指导临床诊疗。
1 资料与方法
1.1 研究对象
回顾性收集2020年6月至2022年7月在盘锦市中心医院就诊并行腹部增强CT检查的肝硬化患者。纳入标准:①组织学、内镜、影像学、实验室检查任一项符合肝硬化诊断患者[7];②具有完整的CT平扫及三期增强扫描影像;③具有完整临床资料。排除标准:①合并其他部位恶性肿瘤患者;②既往行介入或外科手术治疗者;③门静脉海绵样变性无法测量者。
1.2 增强CT扫描方法
采用上海联影医疗科技股份有限公司640层螺旋CT机扫描,患者取仰卧位。扫描范围至少包括患者上腹部(即膈肌上方至肝脏下缘)。行CT平扫及三期增强扫描(扫描时间分别为动脉期28s、门静脉期55s、延迟期150s)。增强扫描由肘正中静脉通过高压注射器(上海高朗医疗设备公司)注射对比剂碘海醇(北京北陆药业股份有限公司),浓度350mgI/ml,速率为2.5ml/s,注入100~150ml;同时以相同流速注入0.9%氯化钠溶液。扫描参数为120kV、100~400mA,重建层厚0.5mm,螺距0.994。
1.3 CT图像分析
所有增强CT扫描图像均由两名具有十年以上工作经验的放射科医师独立判断,对CT图像的分析包括①肝硬化影像评价:肝脏大小、轮廓、形态等;②门静脉、腔静脉系统走形及其分支;③肝硬化相关并发症:如腹水、食道胃底静脉曲张、门脉血栓、肝癌等。对于SPSS的识别,医师通过在轴向平面上滚动腹部增强CT扫描来筛选离开下腔静脉、门静脉系统的任何其他异常分支静脉,首选门静脉期,并在冠状面和矢状面验证SPSS的存在。合理应用后处理重建技术。若两人意见不相符时,再由一名经验丰富主任医师进行审核。对于CT图像测量,血管管径测量部位取其由主干分出后1.0~2.0cm管径均匀处。
1.4 統计学方法
采用SPSS 23.0统计学软件对数据进行处理分析,符合正态分布定量资料采用均数±标准差(![]() )表示,两组间比较采用t检验,多组间比较采用单因素方差分析;不符合正态分布的定量资料采用中位数(四分位数间距)[M(Q1,Q3)]表示,数据之间比较采用Mann-Whitney U检验及Kruskal-Wallis H检验;定性资料采用卡方检验或Fisher确切概率法。在SPSS大小分组实验中,选取合适因素作为自变量,进行Logistic多因素回归分析,以P<0.05为差异有统计学意义。
)表示,两组间比较采用t检验,多组间比较采用单因素方差分析;不符合正态分布的定量资料采用中位数(四分位数间距)[M(Q1,Q3)]表示,数据之间比较采用Mann-Whitney U检验及Kruskal-Wallis H检验;定性资料采用卡方检验或Fisher确切概率法。在SPSS大小分组实验中,选取合适因素作为自变量,进行Logistic多因素回归分析,以P<0.05为差异有统计学意义。
2 结果
2.1 增强CT诊断结果
本研究共纳入2020年6月至2022年7月在锦州医科大学附属第一医院行腹部增强CT检查患者119例。其中存在SPSS患者61例,附脐分流分流33例(64.7%),胃肾分流19例(31.1%)、脾肾分流17例(27.9%),并有8例患者同时存在两种分流。根据分流直径测量,SPSS≥8mm患者共17例(占所有患者的14.3%),SPSS<8mm为44例(占所有患者的37.0%)。
2.2 SPSS有无及直径大小对患者影响的单因素分析结果
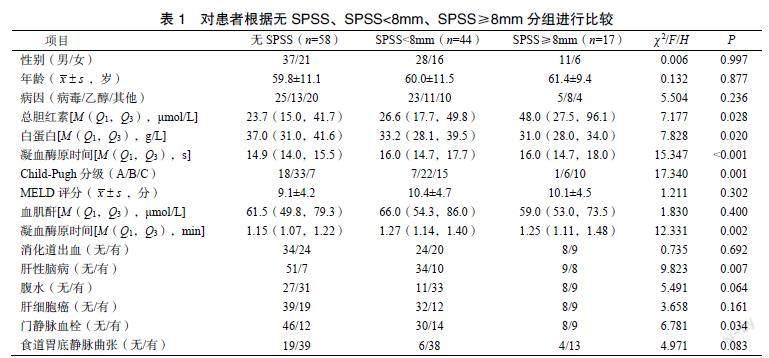
三组患者的性别、年龄、病因比较,差异无统计学意义(P<0.05)。三组患者的总胆红素水平、白蛋白水平、凝血酶原时间、(international normalized ratio,INR)国际标准化比值、Child-Pugh分级、肝性脑病、门静脉血栓发生率、左肾静脉直径相比,差异有统计学意义(P<0.05),见表1。
2.3 SPSS有无及直径大小对患者影响的多因素分析结果
将Child-Pugh分级、肝性脑病、门静脉高压纳入多因素分析,以无SPSS组作为参考类别,可以发现Child-Pugh C级是存在SPSS的独立危险因素,无论其直径大小,即相较于无SPSS患者,存在SPSS患者肝功能更差,Child-Pugh分级更高。与无SPSS组相比,门静脉血栓(OR=9.341,P=0.002)为发生SPSS≥8mm的独立危险因素,见表2。
2.4 有無SSRS对患者影响研究
在所有患者中,合并SSRS患者共36例(占30.3%)。与无SSRS患者相比,两组患者尿酸值相比,SSRS患者尿酸值较低(P=0.032)。与无SSRS患者组相比,SSRS患者胃左静脉直径、左肾静脉直径均较其更粗,差异有统计学意义(P<0.05),见表3。
3 讨论
根据患者分流部位不同,在所有存在SPSS患者中,分流类型最多的是附脐分流33例(64.7%),与Baveno Ⅵ共识相符,胃肾分流19例(37.3%)、脾肾分流17例(33.3%),并有8例患者存在两种不同位置分流[8]。在本研究中,与无SPSS患者相比,有SPSS患者肝功能分级为Child-Pugh C级的患者更多,无论分流道直径大小,Child-Pugh C级是出现SPSS的危险因素与Nardelli等[9]研究一致。另外,SPSS≥8mm患者较无SPSS患者更易门静脉血栓(OR=9.341,P=0.002)。对于存在SSRS的患者尿酸值较无SSRS患者低,其他收录反映肾功能的指标差异无统计学意义,CT图像上对相关静脉直径测量发现,胃左静脉、左肾静脉直径相较于无SSRS患者粗(P<0.05)。
存在SPSS会在一定程度上影响患者肝功能,包括患者实验室指标中总胆红素水平、白蛋白水平、凝血酶原时间、INR,肝功能Child-Pugh分级等级也会有差异,本研究在多因素Logistic回归分析中也印证了这一点。这是由于这种分流道的存在,将本该进入肝脏的血流直径进入体循环中,肝脏血流减少,肝功能变差。本组研究发现,存在SPSS时,其原因是由于这种分流道的存在,与文献病例报告一致,可以通过封堵门体分流道改善门静脉血流,进而提高患者肝功能水平[10]。相较于既往研究[11-12],本文中患者终末期肝病模型(model of end-stage liver disease,MELD)评分没有明显差异,这可能是因为本研究的研究中没有将血钠(Na)纳入研究,而研究显示,将Na纳入MELD评分模型,对于评估患者肝功能及生存率准确性更高[13]。
门静脉血栓症(portal vein thrombosis,PVT)是肝硬化失代偿期的一种常见并发症,包括非肿瘤性PVT和肝硬化肝癌时形成的门静脉癌栓两种。本研究发现SPSS≥8mm时,更易发现PVT的存在。分流道存在时,流经门静脉主干的血流减少、血流速度减慢,这是产生PVT的一项重要因素。研究表明,门静脉血流速度<15cm/s时,更易发现PVT的存在。当存在门体分流血管时,分流道流量大、流速高时,易于预测PVT[14-15]。
SPSS的存在有一定的双面性,之前本研究讨论了较大直径的SPSS增加了患者产生PVT,而对于肝硬化门脉高压的另一并发症“腹水”,在之前研究中表示,患者存在较大直径的SPSS,患者更不易产生腹水[16],在本研究中SPSS的有无级直径大小与腹水的发生差异无统计学意义,这可能是因为本研究将患者入院前后腹水发生作为一项统计结果,未具体记录SPSS产生后是否产生腹腔积液。
有研究表明存在任何形式的SPSS都会可能导致“门体分流综合征”,其特征包括肝功能进行性恶化、肝性脑病、门静脉血栓形成。特别是持续的、反复的肝性脑病,被发现与大的门体分流有关,有研究显示分流相关的肝性脑病可以通过介入治疗得到改善[17-21]。而在本研究中,患者肝性脑病的发生差异无统计学意义,这可能是由于本对于肝性脑病的评估没有为统一医师,在患者回忆既往肝性脑病时有一定误差,都可能产生信息偏倚。
“肝肾综合征”指的是失代偿期肝硬化合并腹水患者,门脉高压导致的肾灌注不足、循环中炎症介质增加进一步造成肾功能受损[22]。而SSRS作为一种门脉高压的代偿机制,使存在SSRS的患者左肾静脉直径较无SSRS患者直径明显增加,可能是导致其尿酸值较无SSRS患者低的原因。但是,本研究存在SSRS患者的尿酸值虽然减低,但而两者尿酸值均在正常值范围内,且其他可以反映肾功能的指标未见明显差异,特别是可以诊断肝肾综合征的重要指标肌酐值。因此,本研究认为SSRS的产生并不会改变患者的肾功能,这也需要进一步的研究来证实这一点。
总之,本研究的研究表明Child-Pugh C级是出现SPSS的危险因素,存在SPSS特别是直径>8mm的患者肝功能更差,更易发生门静脉血栓。SPSS的存在在一定程度上能反映患者的肝硬化状态。因此,增强CT可以作为肝硬化患者常规的检查手段,尽早发现SPSS的存在并引起重视是十分必要的。
利益冲突:所有作者均声明不存在利益冲突。
[参考文献]
[1] BERZIGOTTI A, ROSSI V, TIANI C, et al. Prognostic value of a single HVPG measurement and Doppler- ultrasound evaluation in patients with cirrhosis and portal hypertension[J]. J Gastroenterol, 2011, 46(5): 687–695.
[2] GARCIA-TSAO G, ABRALDES J G, BERZIGOTTI A, et al. Portal hypertensive bleeding in cirrhosis: Risk stratification, diagnosis, and management: 2016 practice guidance by the American Association for the study of liver diseases[J]. Hepatology, 2017, 65(1): 310–335.
[3] YI F, GUO X, ZENG Q, et al. Computed tomography images of spontaneous portosystemic shunt in liver cirrhosis[J]. Can J Gastroenterol Hepatol, 2022, 2022: 3231144.
[4] RODRIGUEZ E A, PEREZ R, ZHANG N, et al. Clinical outcomes of portosystemic shunts on the outcome of liver transplantation[J]. Liver Transpl, 2020, 26(5): 693–701.
[5] DOWNING T M, KHAN S N, ZVAVANJANJA R C, et al. Portal venous interventions: how to recognize, avoid, or get out of trouble in transjugular intrahepatic portosystemic shunt (TIPS), balloon occlusion sclerosis (ie, BRTO), and portal vein embolization (PVE)[J]. Tech Vasc Interv Radiol, 2018, 21(4): 267–287.
[6] TATSUMI A, MAEKAWA S, OSAWA L, et al. Spontaneous portosystemic shunt diameter predicts liver function after balloon-occluded retrograde transvenous obliteration[J]. JGH Open, 2022, 6(2): 139–147.
[7] 中華医学会肝病学分会. 肝硬化诊治指南[J]. 中华肝脏病杂志, 2019, 27(11): 846–865.
[8] DE FRANCHIS R, BAVENO VI FACULTY. Expanding consensus in portal hypertension: report of the baveno Ⅵconsensus workshop: Stratifying risk and individualizing care for portal hypertension[J]. J Hepatol, 2015, 63(3): 743–752.
[9] NARDELLI S, RIGGIO O, TURCO L, et al. Relevance of spontaneous portosystemic shunts detected with ct in patients with cirrhosis[J]. Radiology, 2021, 299(1): 133–140.
[10] ISHIKAWA T, HAMAMOTO K, SASAKI R, et al. Significant improvement in portal-systemic liver failure symptoms and successful management of portal-splenic venous hemodynamics by the combination of interventional radiology and pharmacotherapy[J]. Hepatol Res, 2020, 50(10): 1201–1208.
[11] QI X, QI X, ZHANG Y, et al. Prevalence and clinical characteristics of spontaneous splenorenal shunt in liver cirrhosis: A retrospective observational study based on contrast-enhanced computed tomography (CT) and magnetic resonance imaging (MRI) scans[J]. Med Sci Monit, 2017, 23(5): 2527–2534.
[12] LIPINSKI M, SABOROWSKI M, HEIDRICH B, et al. Clinical characteristics of patients with liver cirrhosis and spontaneous portosystemic shunts detected by ultrasound in a tertiary care and transplantation centre[J]. Scand J Gastroenterol, 2018, 53(9): 1107–1113.
[13] KIM W R, MANNALITHARA A, HEIMBACH J K, et al. MELD 3.0: The model for end-stage liver disease updated for the modern era[J]. Gastroenterology, 2021, 161(6): 1887–1895.
[14] STINE J G, WANG J, SHAH P M, et al. Decreased portal vein velocity is predictive of the development of portal vein thrombosis: A matched case-control study[J]. Liver Int, 2018, 38(1): 94–101.
[15] MARUYAMA H, OKUGAWA H, TAKAHASHI M, et al. De novo portal vein thrombosis in virus-related cirrhosis: Predictive factors and long-term outcomes[J]. Am J Gastroenterol, 2013, 108(4): 568–574.
[16] YI F, GUO X, WANG L, et al. Impact of spontaneous splenorenal shunt on liver volume and long-term survival of liver cirrhosis[J]. J Gastroenterol Hepatol, 2021, 36(6): 1694–1702.
[17] KUMAMOTO M, TOYONAGA A, INOUE H, et al. Long-term results of balloon-occluded retrograde transvenous obliteration for gastric fundal varices: hepatic deterioration links to portosystemic shunt syndrome[J]. J Gastroenterol Hepatol, 2010, 25(6): 1129–1135.
[18] PRAKTIKNJO M, SIM?N-TALERO M, R?MER J, et al. Total area of spontaneous portosystemic shunts independently predicts hepatic encephalopathy and mortality in liver cirrhosis[J]. J Hepatol, 2020, 72(6): 1140–1150.
[19] DAJTI E, RENZULLI M, COLECCHIA A, et al. Size and location of spontaneous portosystemic shunts predict the risk of decompensation in cirrhotic patients[J]. Dig Liver Dis, 2022, 54(1): 103–110.
[20] LENG X, ZHANG F, ZHANG M, et al. Comparison of transjugular intrahepatic portosystemic shunt for treatment of variceal bleeding in patients with cirrhosis with or without spontaneous portosystemic shunt[J]. Eur J Gastroenterol Hepatol, 2019, 31(7): 853–858.
[21] HE C, LV Y, WANG Z, et al. Association between non-variceal spontaneous portosystemic shunt and outcomes after TIPS in cirrhosis[J]. Dig Liver Dis, 2018, 50(12): 1315–1323.
[22] Chinese Society of Hepatology, Chinese Medical Association, XU X, et al. Chinese guidelines on the management of ascites and its related complications in cirrhosis[J]. Hepatol Int, 2019, 13(1): 1–21.
(收稿日期:2023–04–06)
(修回日期:2023–11–24)
![]()
《中國现代医生》杂志征订征稿启事
《中国现代医生》杂志是由国家卫生健康委员会主管、中国医学科学院主办的国家级医学综合类杂志。国内统一刊号:CN11–5603/R,国际标准期刊号:ISSN1673–9701,邮发代号80–611。本刊为旬刊,国内外公开发行。《中国现代医生》官方网址:http://www.zgxdys.ac.cn。
本刊系世界卫生组织西太区医学索引(WPRIM)、中国核心期刊(遴选)数据库、解放军医学图书馆CMCC和CMCI收录期刊,所刊登的文章被万方数据-数字化期刊群和万方医学网、中国知网和中国学术期刊网络出版总库、中文科技期刊数据库全文收录。
本刊紧跟医学发展趋势,对医学热点予以适时追踪,内容新颖、及时,信息量大,学术水平较高。以报道医学领域的前沿性重大科研成果、国家重点课题的医学进展、医疗新技术和诊疗经验为主要内容,突出科学性、先进性、创新性和实用性,促进医学领域的学术交流。主要栏目有论著、药学研究、医学信息技术、医学教育、医院管理、护理研究、综述、个案报道等,是全国各医疗机构广大临床医生和医学院校师生工作、学习交流的园地。
本刊已经启用新远程投稿系统,作者和读者可登录《中国现代医生》官方网址:http://www.zgxdys.ac.cn,进行注册投稿等操作,杂志官方信箱:zgxdys@imicams.ac.cn。
