NUDT15基因多态性与巯嘌呤类药物所致白细胞减少相关性的Meta分析
2024-03-07李剑钦杨星辰陈连云黄苏莉
李剑钦,杨星辰,陈连云,黄苏莉
1. 上海中医药大学附属龙华医院药学部(上海 200032)
2. 上海市杨浦区精神卫生中心药剂科(上海 200093)
巯嘌呤类药物是常见的免疫调节剂,临床上被广泛使用的主要有6-硫鸟嘌呤(6-thioguanine,6-TG)、6-巯基嘌呤(6-mercaptopurine, 6-MP)及硫唑嘌呤(azathioprine, AZA)[1]。巯嘌呤类药物在体内经过一系列反应,首先通过负反馈作用抑制酰胺转移酶,起到干扰嘌呤核苷酸合成的作用,继而抑制复杂的嘌呤间相互转变,使得肿瘤细胞不能增殖,最终发挥免疫抑制作用[2]。目前相关指南推荐巯嘌呤类药物为治疗急性淋巴细胞白血病(acute lymphoblastic leukemia, ALL)、克罗恩病(Crohn's disease, CD)等的首选用药,但巯嘌呤类药物存在骨髓抑制、感染、肝功能损伤等不良反应,其中以白细胞减少最为常见,许多患者因严重的白细胞减少反应而减少巯嘌呤类药物用量甚至停药[3]。研究发现,亚洲人群对巯嘌呤的耐受性较差,这与亚洲人群的NUDT15基因突变率高有密切关系[4]。因此,本研究通过Meta分析探究NUDT15基因多态性与巯嘌呤所致白细胞减少症的相关性,以期为临床应用巯嘌呤类药物提供循证依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准
①研究对象:治疗方案均选用巯嘌呤类药物的患者;②终点事件:需包括白细胞减少症情况,并有明确的白细胞减少症判定标准。此外,将3~4 级白细胞(white blood cell, WBC)减少(WBC <2 000/mm3)定义为严重白细胞减少;③随访时间:随访时间8 周内的终点事件为早期事件,超过8 周的终点事件为中后期事件;④基因检测:纳入研究的人群均参与NUDT15c.415C>T(rs116855232)检测,基因型频率分布必须符合Hardy-Weinberg 平衡。其中,C 为野生型基因,T 为突变型基因,等位基因模型(C vs T),显性基因模型(CC vs CT+TT),杂合基因模型(CT vs TT)。
1.1.2 排除标准
①重复发表;②临床经验、综述、个案报道;③纳入患者诊断不明确;④无明确随访时间。
1.2 文献检索策略
计算机检索中国知网、万方、维普、中国生物医学文献、PubMed、Embase 数据库,检索年限为建库至2023 年6 月,中文检索词包括白细胞减少、基因多态性、巯嘌呤,英文检索词包括NUDT15、NUDT15c.415C>T、leukopenia、gene polymorphism、thiopurine、6-thioguanine、6-mercaptopurine、azathioprine。以Pubmed 为例,具体检索策略见框1。
1.3 文献筛选与资料提取
由两名研究人员独立对检索所得的文献进行筛选。首先,通过阅读标题和摘要进行初筛,以排除重复发表的研究和与本研究不相关的文献。然后,根据纳入与排除标准阅读全文进行复筛。资料提取内容包含:①纳入研究的基本信息,如作者、发表年份等;②结局指标;③纳入研究患者的基因型频率分布;④随访时间。

框1 PubMed检索策略Box 1. Search strategy in PubMed
1.4 文献质量评价
采用纽卡斯尔-渥太华量表(Newcastle-Ottawa Quality Assessment Scale, NOS)进行文献质量评价,该量表包括研究患者选择、组间可比性、暴露因素测量3 个方面,共8 个条目,总分9 分,得分6 分以上表示质量为优,4~5 分表示质量中等,低于4 分表示质量较差[5]。由两名研究人员独立评价纳入文献的质量,如遇分歧通过讨论解决或咨询第三方专家判定。
1.5 统计分析
采用Stata 14.0 软件进行统计分析。采用比值比(odds ratio, OR)和95%可信区间(confidence interval, CI)分别作为分析的统计量和效应量,同时计算Z检验的P值,以P<0.05 为差异具有统计学意义。使用Q检验和I2检验对纳入文献的异质性进行评估,当P>0.1 且I2<50%时,表明各研究结果之间无明显异质性,采用固定效应模型,反之,则采用随机效应模型。对具有异质性的基因模型进行Meta 回归分析,通过多个协变量引入回归模型后,根据研究间方差的变化,解释异质性的来源。绘制发表偏倚的漏斗图,并采用Egger's 回归评估发表偏倚,当P>0.05 时,认为不存在发表偏倚[6]。
2 结果
2.1 文献筛选流程及结果
检索共获取154 篇文献,经过筛选,最终纳入17 篇文献[7-23],文献筛选流程见图1。
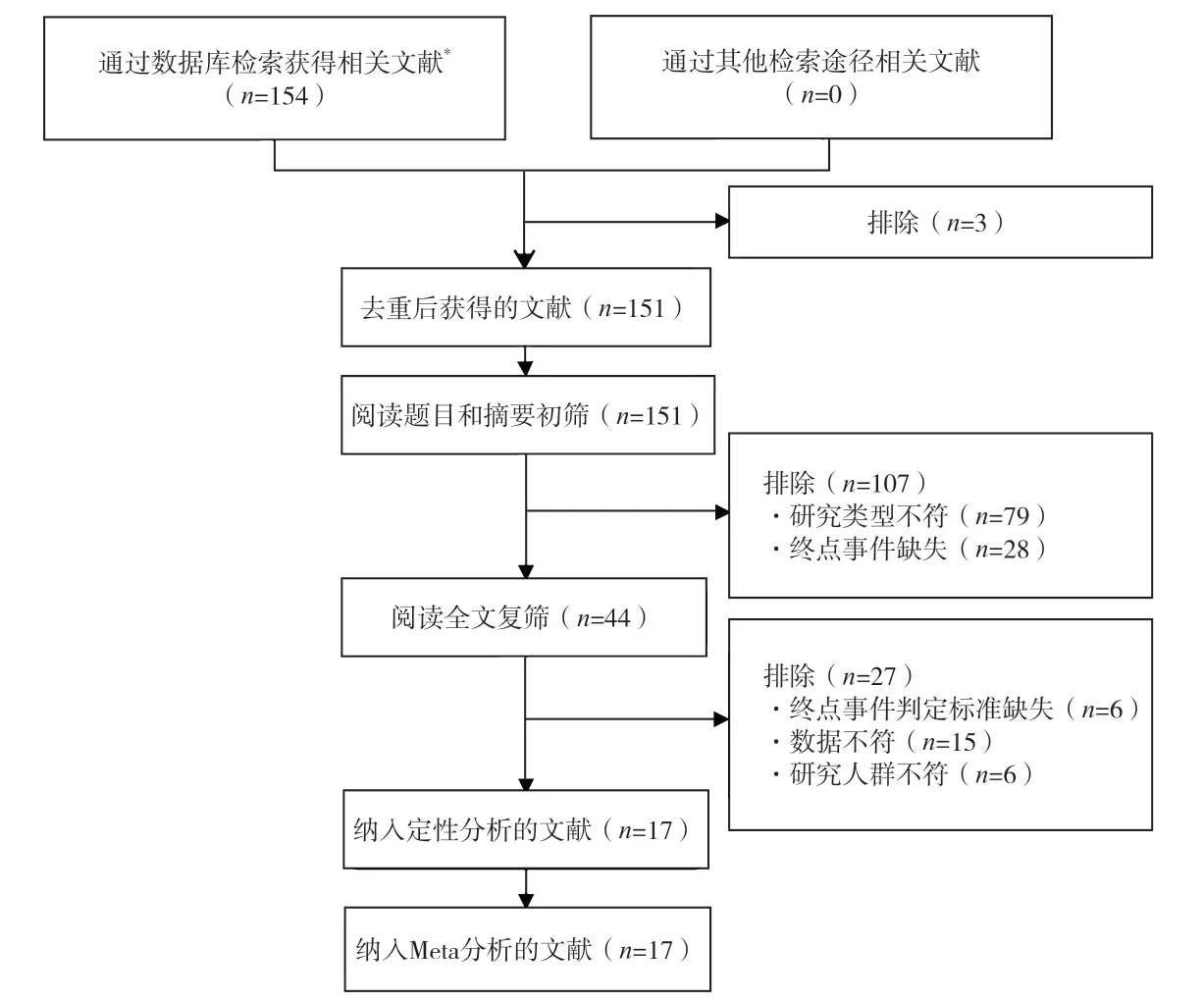
图1 文献筛选流程图Figure 1. Flowchart of literature screening
2.2 纳入文献的基本特征及质量评价结果
纳入文献基本特征见表1,共纳入患者4 057例。按照NOS 对纳入的17 篇文献[7-23]进行质量评价,得分为6~8 分,提示这些研究的质量相对较高。
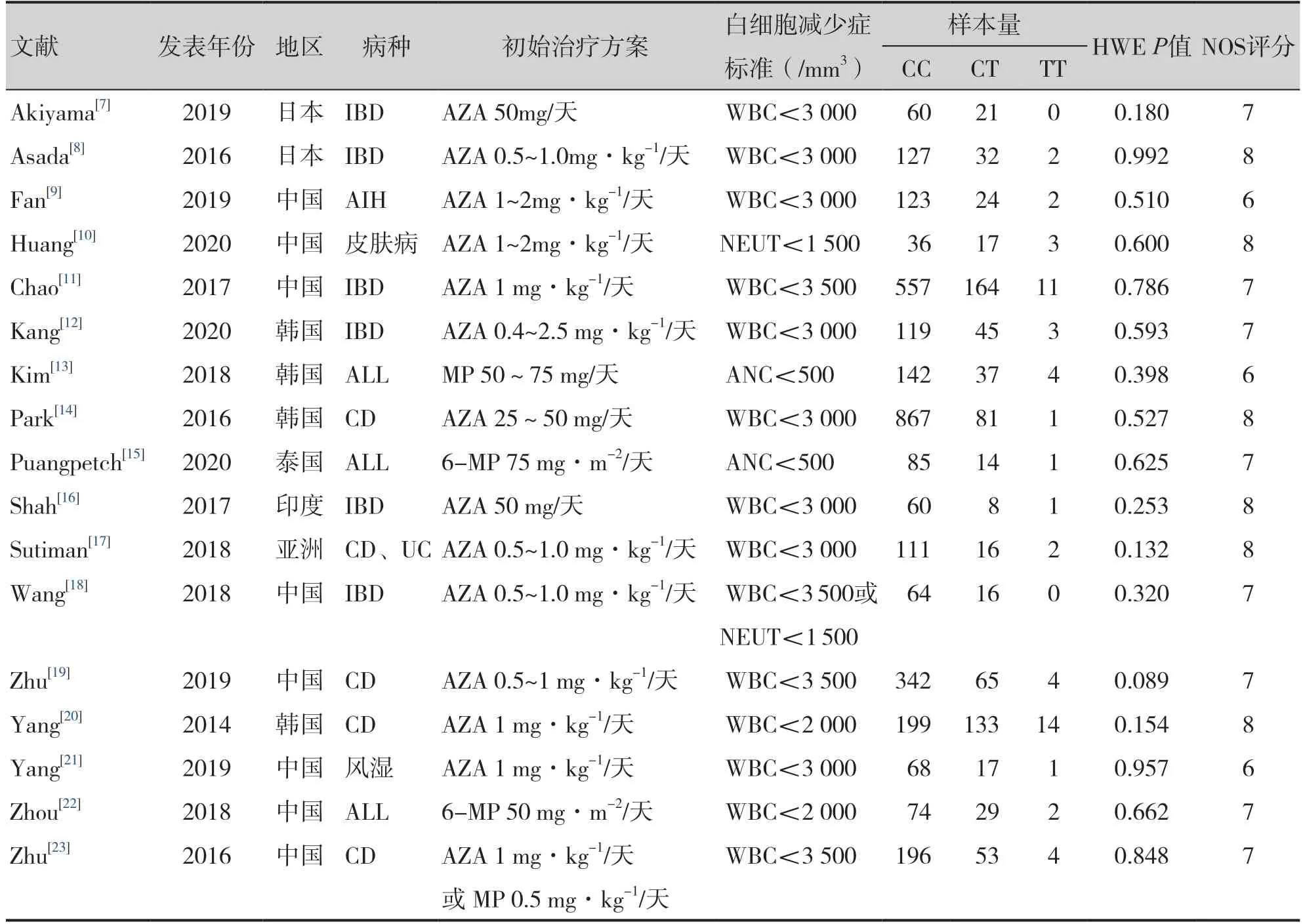
表1 纳入文献的基本特征Table 1. Basic characteristics of the included literature
2.3 Meta分析结果
2.3.1 异质性检验
对纳入的17 篇研究进行异质性检验,所有的杂合基因模型中8 周内:I2=45.40%,P=0.05;超过8 周:I2=26.50%,P>0.1,严重白细胞减少显性基因模型:I2=0.00%,P>0.1,提示各研究间的异质性不具有统计学意义,采用固定效应模型;其余各组I2均大于50.00%,P<0.1,提示各研究间的异质性具有统计学意义,采用随机效应模型。
2.3.2 基因分组模型
Meta 分析结果显示,巯嘌呤类药物所致白细胞减少症与NUDT15c.415C>T基因位点多态性的相关性差异存在统计学意义。服用巯嘌呤类药物8 周内所致白细胞减少症中,等位基因模型[OR=0.15,95%CI(0.10,0.22),P<0.001]、显性基因模型[OR=0.13,95%CI(0.08,0.20),P<0.001]、杂合基因模型[OR=0.04,95%CI(0.01,0.19),P<0.001]与白细胞减少显著相关,见图2-A、图2-B、 图2-C。服用超过8 周巯嘌呤类药物所致白细胞减少症中,等位基因模型[OR=0.18,95%CI(0.11,0.30),P<0.001]、显性基因模型[OR=0.17,95%CI(0.09,0.31),P<0.001]、杂合基因模型(图3-C)[OR=0.05,95%CI(0.02,0.15),P<0.001]与白细胞减少具有显著相关性,见图3-A、图3-B。严重白细胞减少的显性基因模型[OR=0.09,95%CI(0.05,0.15),P<0.001]与白细胞减少具有显著相关性,见图4。

图2 8周内NUDT15 c.415C>T与巯嘌呤类药物所致白细胞减少症的Meta分析Figure 2. Meta-analysis of NUDT15 c.415C>T and thiopurine-induced leukopenia within 8 weeks

图3 超过8周NUDT15 c.415C>T与巯嘌呤类药物所致白细胞减少的Meta分析Figure 3. Meta-analysis of NUDT15 c.415C>T and thiopurine-induced leukopenia over 8 weeks
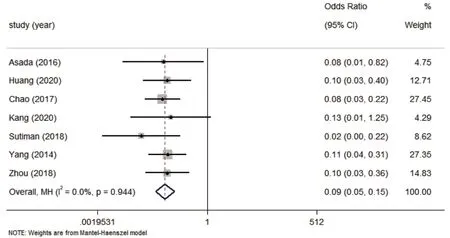
图4 严重白细胞减少显性基因模型组的Meta分析Figure 4. Meta-analysis of the severe leukopenia dominant gene model group
2.3.3 发表偏倚和Egger's回归
如图5 所示,不论是8 周内或是超过8 周的随访终点事件,等位基因模型和显性基因模型的散点分布有一定的偏向性,因此存在一定的发表偏倚;杂合基因模型的散点分布基本对称,提示无明显的发表偏倚。在严重白细胞缺乏症事件中,显性基因组无明显发表偏倚。

图5 NUDT15 c.415C>T各基因分组漏斗图Figure 5. Funnel plot of NUDT15 c.415C>T gene subgroups
采用Egger's 检验进行发表偏倚分析,结果显示,8 周内随访终点事件中等位基因中偏倚[t=-0.81,95%CI(-3.56,1.68),P=0.436];显性基 因中偏倚[t=-1.19,95%CI(-3.17,0.97),P=0.262];杂合基因中偏倚[t=2.25,95%CI(-0.05,23.29),P=0.051]。超过8 周随访终点事件中等位基因中偏倚[t=-1.61,95%CI(-7.11,1.11),P=0.137];显性基因中偏倚[t=-1.77,95%CI(-5.36,0.56),P=0.102];杂合基因中偏倚[t=-1.11,95%CI(-11.45,3.83),P=0.292]。在严重白细胞缺乏症事件中,显性基因中偏倚[t=-0.84,95%CI(-2.27,1.15),P=0.440]。提示纳入的研究不存在明显发表偏倚。
2.3.4 Meta回归分析
在NUDT15c.415C>T各基因分组中,等位、显性基因模型中存在异质性,因此,以各研究的治疗方案、白细胞减少症判定标准以及发表年份、患者的病种和地区为协变量进行Meta 回归分析,结果显示,对于早期(8周内)白细胞减少症,等位、显性基因模型同时引入五个协变量,P值均大于0.05;对于中后期(超过8 周)白细胞减少症,等位基因模型和显性基因模型同时引入五个协变量,治疗方案的P值均小于0.05。
3 讨论
本Meta 分析主要通过观察NUDT15c.415C>T基因多态性与巯嘌呤类药物所致白细胞减少症的相关性,对纳入的17 项研究的数据进行分析比较。结果表明,不论是早期(8 周内)白细胞减少症,或是随着药物持续使用的中后期(超过8 周)白细胞减少症中,等位基因模型、显性基因模型、杂合基因模型均提示NUDT15c.415C>T的基因多态性与巯嘌呤类药物所致白细胞减少症具有显著相关性。
在本研究之前,李惠英等[24]已有同类研究发表,与其相比,本Meta 分析具有三个优势:一是所纳入的研究数量、病例数更多。李惠英等[24]研究纳入7 篇文献,总病例数1 198 人,本研究纳入17 篇文献,总病例数4 057 人;二是本Meta分析剔除了不符合Hardy-Weinberg 平衡的文献,而李惠英等的研究并未进行Hardy-Weinberg 平衡检验,其纳入的部分文献不符合Hardy-Weinberg平衡;三是本研究通过对不同随访周期、严重不良反应事件进行Meta 分析,结论对临床实践具有一定的参考意义。
本研究结果显示,NUDT15c.415C>T基因多态性与巯嘌呤类药物所致白细胞减少症存在明显的相关性。有研究显示,日本患儿NUDT15 c.415C>T基因多态性对巯嘌呤类药物诱导的骨髓抑制有重要影响[25]。另一项Meta 分析也显示,在亚洲人群中,NUDT15c.415C>T可能是硫嘌呤类药物导致的白细胞减少症的重要预测因子[26]。一项队列研究发现,NUDT15c.415C>T的检测可能有助于减少韩国IBD 患者服用巯嘌呤类药物所致的白细胞减少症[27]。在本研究中,等位基因模型(C vs T)、显性基因模型(CC vs CT+TT)、杂合基因模型(CT vs TT)均提示NUDT15c.415C>T的基因多态性与巯嘌呤类药物所致白细胞减少症具有显著相关性。由此可见,T 是风险等位基因,与巯嘌呤所致不良反应存在显著相关性。
在中后期(超过8 周)白细胞减少症中,等位基因模型和显性基因模型中各研究存在异质性,在同时引入五个协变量后发现治疗方案的P值均小于0.05,研究间方差分别由0.752 7 降为0.450 3、0.944 1 降为0.463 5,表明中长周期终点事件的研究中,有40.18%和50.91%的异质性来源于治疗方案差异。因此,通过Meta 回归提示,治疗方式的差异可能是导致各文献数据存在异质性的原因之一。
本研究结果具有一定的临床指导意义。首先,纳入研究的人群均为亚洲人群,降低人种差异对结果产生的异质性;其次,本研究严格按照Hardy-Weinberg 平衡的标准筛选符合群体基因遗传平衡的文献;此外,本次研究纳入的病种具有多样性,具有一定的参考意义。
本研究存在以下不足:首先,部分病种的文献数量过少,如风湿、皮肤病等,导致证据相对缺乏,对整体结果可能产生一定影响;其次,目前对于白细胞减少症缺少统一的标准定义,虽然大部分的研究定义白细胞减少症的标准为WBC <3 000/mm3,但也有少部分研究将其定义为WBC <3 500/mm3或WBC <2 000/mm3,这可能导致部分基因分组产生异质性,也可能对最终结果产生一定的影响;最后,在早期(8 周内)白细胞减少症中,等位基因模型和显性基因模型中各文献数据虽存在差异,但通过Meta 回归发现,其异质性均不来源于各研究的发表年份、研究人群的病种和地区、治疗方案、白细胞减少症判定标准的不同,其原因尚未明确。
综上,NUDT15基因多态性与巯嘌呤类药物所致白细胞减少具有相关性,未来仍需大样本、高质量的临床研究加以验证,以进一步评估NUDT15c.415C>T基因多态性与巯嘌呤类药物所致白细胞减少症之间的关系,为临床合理用药提供依据。
