三苯基秘与三对甲苯基秘的合成*
2024-03-05何仕艳蒲娅玲黎凤娇
陈 静,何仕艳,蒲娅玲,谢 竹,唐 薇,黎凤娇
(四川文理学院化学化工学院,四川 达州 635000)
元素周期表的第六周期第VA族的元素是秘,原子序数为83。金属秘具有优良的物理化学性质,它的密度大、原子半径大、熔点低、电负性小、质地柔软,有利于制作保险丝等易熔合金材料[1]。秘左右两边的元素分别是铅与钋,铅是重金属,能够阻挡放射性射线,具有耐腐蚀性、熔点低、韧性好、导电性能低等优良性能,但是铅及其化合物进入人体后对消化、肝脏、中枢神经等多个系统造成危害。钋是著名科学家居里夫人与丈夫在1898年发现的银白色金属,它主要通过人工合成得到,毒性非常强。秘有绿色金属之称,它有很多特殊的性质,在生物医药、能源环境等领域展现出重要的应用前景。我国的秘储量世界第一,主要分步在湖南、广东、江西等地,其产量长期居世界首位。秘及其化合物的毒性小,与同族元素氮、磷、砷、锑相比较,对生态环境的影响较弱,可以取代毒性大的金属应用于有机合成、医药、催化等领域。研究发现,一些秘类化合物具有较为强大的杀菌、消炎等药物作用,可用于腹泻、胃溃疡、消化不良等疾病的治疗,例如果胶秘、铝酸秘等[2]。部分新型秘类化合物可以有效地抑制肿瘤,具有抗癌的功效,利用其成像性、载药性等特点,可作为放射性药剂用于诊断和治疗[3-4]。
三芳基秘类化合物是比较稳定的化合物,其中三苯基秘是重要的有机合成中间体与催化剂[5-6]。三苯基秘的合成方法主要使用格氏试剂与三氯化秘的金属互换法,合成路线如图1所示。使用嗅苯、镁在无水乙醚溶液中制备格氏试剂,即苯基嗅化镁,然后加入三氯化秘继续反应,反应完成后经过一系列后续处理得到相应的产物[7]。该反应使用嗅苯为原料,用量大且成本较高,因此其他研究者探讨使用氯苯来代替嗅苯合成三苯基秘[8]。合成方法如图2所示,氯苯与镁在无水乙醚溶液中制备苯基氯化镁,然后加入三氯化秘发生金属与格氏试剂的互换反应,反应完成后水解、萃取、干燥、过滤并除去溶液可以得到三苯基秘。
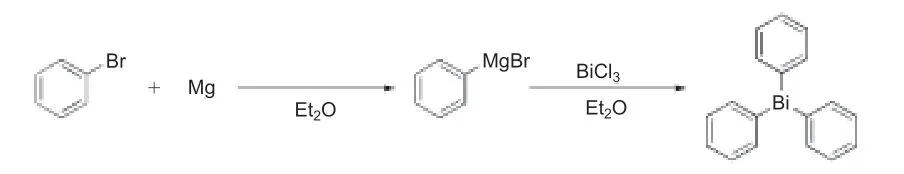
图1 三苯基铋的合成路线1Fig. 1 Synthetic route 1 of triphenylbismuth
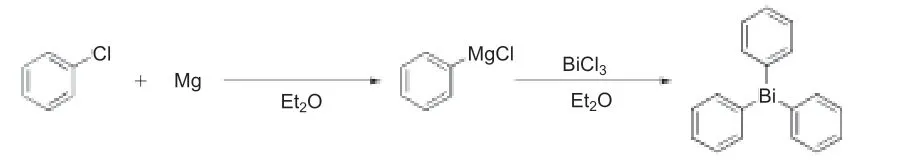
图2 三苯基铋的合成路线2Fig. 2 Synthetic route 2 of triphenylbismuth
由于乙醚的沸点低,易挥发,而且易燃易爆,在格氏试剂的制备阶段不容易控制反应过程。有研究者使用四氢呋喃作为反应溶剂对实验进行改进,使用芳基嗅代物、镁与三氯化秘或三氯化锑采取一锅法合成三价有机秘、锑化合物[9]。合成方法如图3所示。
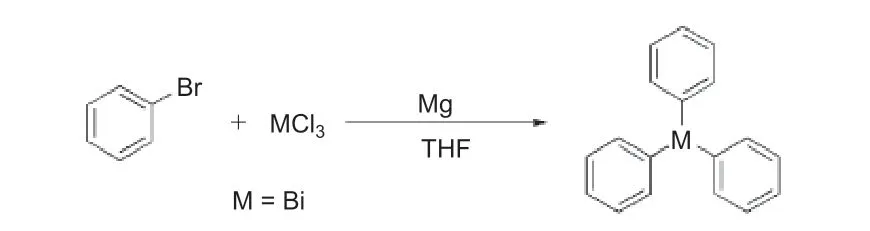
图3 三芳基铋的合成Fig. 3 Synthesis of triarylbismuth compounds
以上的合成方法主要探讨了三苯基秘的合成,对主要的反应条件如反应温度、反应时间对产物产率的影响尚不明确。为了优化合成条件,本文主要探讨反应温度、反应时间对三苯基秘与三对甲苯基秘产率的影响,探索有效可行的合成路线。
1 实验部分
1.1 实验仪器
DF-101S型集热式加热磁力搅拌器,河南予华仪器有限公司;101-2AB型电热鼓风干燥箱,天津市泰斯特仪器有限公司;SHZ-D(III) 型循环水式真空泵,巩义市予华仪器有限责任公司;WFH-204B型手提式紫外分析仪,杭州齐威仪器有限公司;JY501B型电子天平,上海浦春计量仪器有限公司;旋转蒸发仪,上海贤德实验仪器有限公司;RY-1G熔点仪,天津光学仪器厂;Bruker Avance 500 MHz核磁共振仪。
1.2 实验试剂
嗅苯、对嗅甲苯、四氢呋喃、三氯化秘,均为分析纯,上海麦克林生化科技股份有限公司;乙醚、甲醇、硫酸镁、碘粒(均为分析纯),镁条(化学纯),成都科隆化学品有限公司。
1.3 合成路线(图4)

图4 三苯基铋与三对甲苯基铋的合成Fig. 4 Synthesis of triphenylbismuth and tri-p-tolylbismuth
1.4 合成步骤
格氏试剂的制备需要在无水的条件下进行,实验仪器使用前在烘箱内烘干1h。将250mL的三颈圆底烧瓶安装在磁力搅拌器中,分别安装回流冷凝管和滴液漏斗,在回流冷凝管上口安装无水氯化钙干燥管。称取1.2g(0.05moL)除去氧化膜的镁条,加入250mL的三颈烧瓶内,取20mL的无水四氢呋喃以及5.4mL(0.05moL)的嗅苯加入滴液漏斗中。将滴液漏斗中的四氢呋喃和嗅苯混合溶液部分滴加至三颈烧瓶内,几分钟后可观测到溶液微沸,控制滴加的速度继续滴加剩余的混合液,保持反应液微沸的状态。滴加完成后,在80℃油浴下加热搅拌30min,使镁屑尽量反应完全生成苯基嗅化镁。
将三颈圆底烧瓶取出油浴锅,冷却至室温。然后将三颈烧瓶置于冰水浴中冷却数分钟,在搅拌下加入四氢呋喃和4.73g(0.015moL)三氯化秘的混合液,溶液立即由浅黑色变为深绿色,搅拌数分钟后在设定温度下加热一定时间使反应完全。加热完成后将三颈圆底烧瓶置于冰水浴中,在搅拌下加入40mL的饱和氯化铵溶液,分解混合物。静置后抽滤,用分液漏斗分出有机层,水层用10mL乙醚萃取两次,合并有机层加入适量无水硫酸钠干燥。将干燥后的滤液倒入圆底烧瓶使用旋转蒸发仪蒸发溶剂,冷却后烧瓶内加入适量甲醇,静置后抽滤、洗涤,干燥后得到白色晶体三苯基秘。表征数据如下:
三苯基秘:mp:76~78 ℃;1H NMR(500MHz, CDCl3):δ7.71(d,J= 10.0Hz, 6H), 7.31(t,J= 7.5Hz, 6H), 7.22(t,J= 5.0Hz, 3H);13C NMR(125MHz, CDCl3):δ155.52,137.86,130.82,128.06。数据与文献[9-10]基本相同。
三对甲苯基秘的合成步骤与三苯基秘基本相同,得到白色晶体。表征数据如下:
三对甲苯基秘:mp: 116~118 ℃ ;1H NMR(500 MHz, CDCl3):δ7.69(d,J= 5.0Hz, 6H), 7.25(d,J= 5.0Hz, 6H), 2.37(s, 9H);13C NMR(125MHz,CDCl3):δ151.16,137.56,137.36,131.30,21.52。数据与文献[9-10]基本相同。
2 结果与讨论
2.1 三苯基铋合成条件的优化
2.1.1 反应温度的筛选
其他反应条件不变,保持苯基嗅化镁与三氯化秘的反应时间为3h,考察反应温度对三苯基秘产率的影响。从表1可以看出,三苯基秘的产率随着反应温度的升高而发生变化,反应温度为80℃时,三苯基秘的产率仅为23%,当反应温度上升为95℃时产物的产率可以达到52%,当反应温度为100℃时产物的产率为45%。因此,反应温度在95℃时得到的产率最佳。
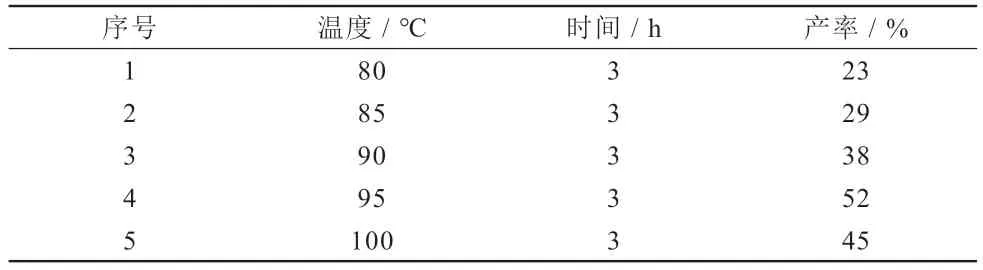
表1 反应温度对三苯基铋产率的影响Table 1 The effect of reaction temperature on the yield of triphenylbismuth
2.1.2 反应时间的筛选
其他条件不变,保持反应温度为95℃时,考察反应时间对三苯基秘产率的影响。从表2可以看出,改变反应时间三苯基秘的产率会随之发生变化。反应时间为2h时三苯基秘的产率仅为18%,当反应时间为3h时产物产率增加到52%,继续延长反应时间为4h和5h时,产物的产率下降,副产物增加。因此,反应时间为3h时得到的产率最佳。

表2 反应时间对三苯基铋产率的影响Table 2 The effect of reaction time on the yield of triphenylbismuth
由于该反应需要在无水的条件进行,所有仪器都需要充分干燥,极少量的水也会抑制反应的进行,并分解已生成的格氏试剂,进而影响下一步的反应,而且整个反应在无氮气保护情况下进行,因此三苯基秘的产率低于文献值[9-10]。
2.2 三对甲苯基铋合成条件的优化
将原料中的嗅苯换变为对嗅甲苯,按照1.4合成步骤,其他条件不变,保持对甲苯基嗅化镁与三氯化秘的反应时间为3h时,考察反应温度对甲苯基秘产率的影响,结果见表3。

表3 反应温度对三对甲苯基铋产率的影响Table 3 The effect of reaction temperature on the yield of tri-p-tolylbismuth
从表3可以看出,三对甲苯基秘的产率随着反应温度的升高而发生变化,反应温度为80℃时,三对甲苯基秘的产率为44%,当反应温度上升为90℃时产物的产率可以达到63%,当反应温度为100℃时产物的产率为53%。因此,反应温度在90℃时得到的产率最佳。对嗅甲苯中由于甲基的给电子效应,与嗅苯相比最终产物的产率上升,反应温度则有所下降。
此外,其他条件不变的情况下,保持反应温度为90℃时,考察了反应时间(2h、3h和4h)对三对甲苯基秘产率的影响,结果发现反应时间为3h时得到的产率最佳,延长反应时间会导致副产物增多,产率下降。
3 结论
通过三苯基秘的反应温度与反应时间的探索,明确了最优反应条件,当反应温度为95 ℃时,反应3h得到的三苯基秘产率为52%。在此基础上三对甲苯基秘的反应条件也进行了优化,结果表明,反应温度为90℃时,反应3h得到的三对甲苯基秘产率可达到63%。该反应路线简单,反应时间短,产物的产率较高。由于苯环上的碳原子与秘原子直接成键,因此苯环上不同取代基的电子效应对三芳基秘化合物的物理和化学性质产生较大的影响。今后会探讨不同三芳基秘的合成方法,并对其进行结构分析,明确不同配体对中心秘原子的配位作用,为有机秘化合物的基础研究提供理论依据。
