天然产物山奈酚的聚集诱导发光特性及在铝离子检测中的应用
——推荐一个大学化学综合实验
2024-03-04王小青卢雯徐莉
王小青,卢雯,徐莉
南京林业大学理学院,南京 210037
1 概述
随着荧光探针与荧光显微技术的发展,用荧光成像来示踪生物体中的金属离子引起了人们越来越多的研究兴趣[1–3],然而利用该方法来示踪植物中金属离子,在本科实验教学中基本没有涉及。传统的化学实验教学主要以理论验证和基本操作为培养目标,缺乏对于学生解决实际问题和创新意识等综合能力的培养。在双一流建设背景下,在全面提高人才培养质量的目标下,以科研反哺教学,与思政协同育人[4,5],对于学生的创新意识培养和综合能力提高具有重要的作用。
山奈酚(Kaempferol,Kae)是从银杏叶中分离提取的一种黄酮类天然产物分子,已被广泛研究并被发现具有抗癌、抗氧化、抗炎、抗菌等多种药理特性。最近的研究表明,该类天然产物分子还可被用于荧光传感领域[3,6]。大多数荧光分子通常在稀溶液中强烈发光,但在聚集状态下会遇到不同程度的聚集引起的猝灭效应(Aggregation induced quenching,ACQ)。为了避免ACQ,探针通常被控制在较低的浓度下进行检测。然而,在荧光传感和成像过程中,由于光漂白作用,低浓度的探针会导致弱荧光信号和检测效率降低。聚集诱导发光(Aggregation induced emission,AIE)已成为解决这一问题的一种普适的策略。AIE生色团(AIEgens)在稀溶液中不发光,而在聚集状态下高效发光。到目前为止,AIEgens在生物检测和成像、医学诊断和治疗领域显示出巨大的潜力,值得骄傲的是,中国科学家在AIE材料的研究方面一直处于世界领先水平[7,8]。山奈酚的物理和化学特性取决于自身的结构和聚集程度。基于山奈酚的特性,可发展出具有高选择性、高灵敏度和高稳定性的生物成像和检测手段。以山奈酚聚集体为探针的分析方法,具有简便、高效、抗光漂白等优点,并能应用于实际样品的检测与成像。铝及其化合物被广泛应用于人类的生产和日常生活中,铝元素摄入超标可诱发神经退行性疾病和植物中毒。目前已报道的对Al3+的检测中,荧光探针法由于其操作简单、灵敏度高、实时无损等优势而受到了广泛的关注。
在本综合实验中,向山奈酚的良溶剂溶液中加入不良溶剂,可以观察到山奈酚溶液由不发光到发出蓝色荧光,同时伴随荧光逐渐变强的变化;然后向含山奈酚聚集体的溶液中加入Al3+后,可以观察到发出的荧光由蓝色变为蓝绿色;结合紫外-可见吸收和荧光光谱仪的测试结果和数据分析,学生可以直观地了解AIE的特点及其检测应用,并能够学会检测限的计算方法。同时,通过对比山奈酚与ACQ荧光分子(以罗丹明B为例)在分散和聚集状态下的不同荧光性能,学生也可以直观地了解ACQ的特点。该实验适合作为化学、材料化学等专业本科高年级学生的化学综合实验。
2 实验部分
2.1 实验目的
(1) 了解荧光的基本原理与应用。
(2) 了解AIE与ACQ的区别。
(3) 掌握紫外-可见吸收和荧光光谱仪的基本操作和图谱分析。
(4) 掌握检测限的计算方法。
(5) 加强绿色发展理念、增强民族自豪感和激发学习热情。
2.2 实验原理
2.2.1 荧光的产生原理
荧光是一种常见的光致发光现象,具体产生过程如图1所示[9]。处于基态(S0)的分子吸收合适能量的光子后,其电子从基态跃迁到激发态,具有较高能量的激发态分子很快以振动驰豫(VR)和内转换(IC)的方式释放出热量达到单重激发态的最低能级(S1),然后电子直接以辐射衰变释放出光子的形式返回至基态的最低能级(S0),发出荧光。在某些情况下,如果受激发分子的电子在激发态时经系间窜越(ISC)形成三重激发态,再经过VR达到三重激发态的最低能级(T1),也会伴随热量的释放。其中,振动驰豫、内转换和系间窜越都属于非辐射衰变,不利于荧光的产生。
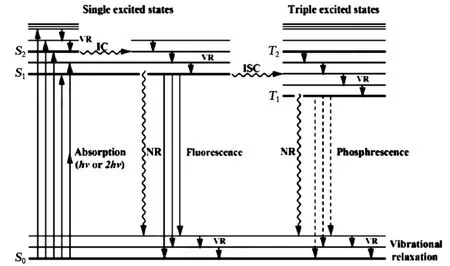
图1 雅布隆斯基的分子激发和发射能级图
2.2.2 ACQ分子与AIE分子的发光机制
经典的荧光分子一般具有大的π共轭结构,在稀溶液状态下发出较强的荧光,但在高浓度或聚集状态下,由于分子之间的π–π堆积作用,使得激发态的能量以非辐射衰变的形式消耗掉从而产生聚集诱导荧光猝灭,即ACQ现象。与经典的ACQ分子不同的是,AIE荧光分子通常具有“螺旋桨”状结构。该类分子在溶液中由于取代基绕单键的自由旋转消耗了激发态能量,从而导致荧光较弱;而在聚集状态下,取代基的自由旋转受到阻碍,非辐射衰变被有效抑制,从而使荧光显著增强。另外,AIE型分子的“螺旋桨”状分子结构还能够有效抑制分子间紧密的π–π堆积,从而有利于提高分子聚集体发光效率。本文中报道的山奈酚分子,亦具有部分“螺旋桨”状结构[10],通过碳碳单键将苯酚与2,5,7-三羟基色原酮这两个共轭基团相连接,形成具有AIE特性的荧光分子(图2)。

图2 山奈酚的结构图
2.3 试剂和仪器
本实验所用试剂与仪器如表1和表2所示。
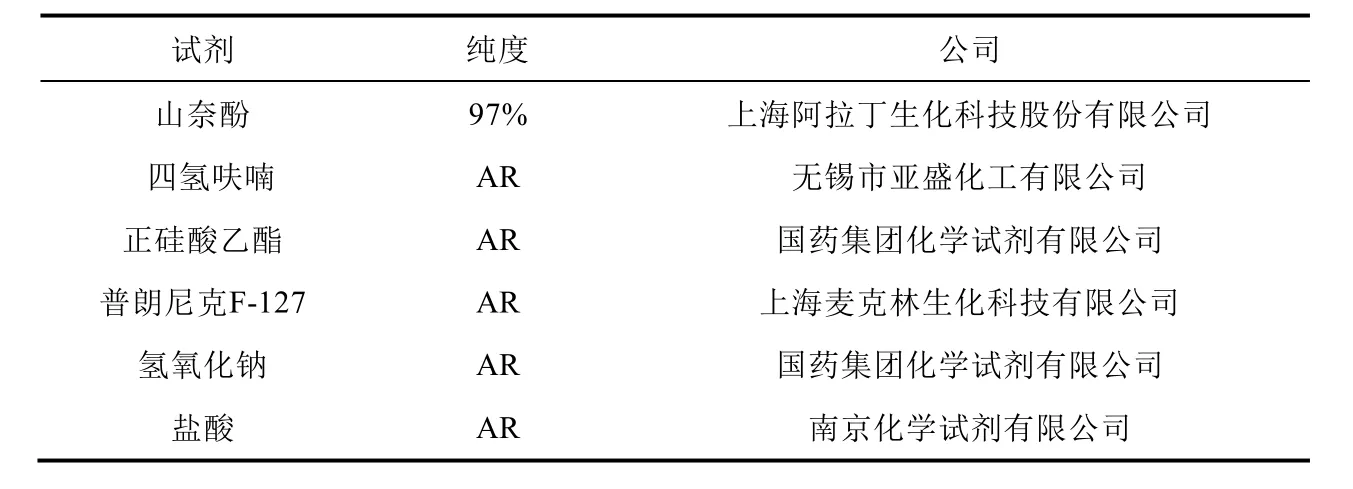
表1 实验试剂

表2 实验仪器
2.4 实验内容
2.4.1 山奈酚与罗丹明B的荧光比较实验
分别取少量山奈酚和罗丹明B置于载玻片上,在365 nm紫外灯的照射下,观察两者的荧光强度。
分别称取山奈酚和罗丹明B各0.01 g装入试管中,加入10 mL四氢呋喃,配成溶液。在365 nm紫外灯的照射下,观察两者的荧光强度。
2.4.2 山奈酚聚集体的制备
制备山奈酚(3 mmol·L−1)的四氢呋喃(THF)储备液1.5 mL。用移液管量取100 μL储备溶液转移到10 mL容量瓶中。加入一定量的水和THF,定容至10 mL,得到30 μmol·L−1山奈酚的THF/水溶液,水的体积分数分别被调至fw= 0、10%、20%、30%、40%、50%、60%、70%、80%、90%和99%,以365 nm为激发波长,测试溶液在375–600 nm范围内的荧光光谱。
2.4.3 山奈酚聚集体的粒径分布表征
取1 mL山奈酚(30 μmol·L−1)的THF/水溶液(fw= 80%)放入比色皿中,通过粒径分布测试仪进行表征。
2.4.4 检测离子的配制和荧光测试
分别将CaCl2、CdCl2、CoCl2、CrCl3、CuCl2、FeCl2、FeCl3、KCl、MgCl2、MnCl2、NaCl、Ni(CH3COO)2、Pb(CH3COO)2、ZnCl2、AlCl3、KBr、NaCl、NaF、KI、H2O2和FeSO4、NaNO2、Na2SO3、Cu(ClO4)2、Na2HPO4、NH₄HSO₄、CH3COONa固体溶解在适量水中,然后在10 mL的容量瓶中进行定容,配成3 mmol·L−1储备液。分别取30 μL以上储备液加入到3 mL Kae (30 μmol·L−1)的H2O/THF(8 : 2,V/V)二元溶液中,以365 nm为激发波长,测试溶液在375–600 nm范围内的荧光光谱。
2.4.5 紫外滴定测定Kae与Al3+配位比的实验
分别取0–50 μL (10 μL之前体积梯度为1 μL,10 μL之后体积梯度为5 μL) Al3+储备液加入到3 mL Kae (30 μmol·L−1)的H2O/THF (8 : 2,V/V)二元溶液中,测试溶液在325–550 nm范围内的紫外-可见吸收光谱。
2.4.6 测试检测限的实验
分别取0–200 μL (70 μL之前体积梯度为5 μL,70 μL之后体积梯度为50 μL) Al3+储备液加入到3 mL Kae (30 μmol·L−1)的H2O/THF (8 : 2,V/V)二元溶液中,以365 nm为激发波长,测试溶液在375–600 nm范围内的荧光光谱。
取3 mL THF/水溶液(fw= 80%)放入4 mL的比色皿中,然后用365 nm激发波长,测试溶液在375–600 nm范围内的荧光光谱。重复10次,分别记录486 nm和421 nm处的荧光强度值,计算两者的比值然后获得标准方差σ值,再结合拟合后线性关系的斜率,根据公式DL = 3σ/k计算检测限。
2.4.7 光稳定测试
取3 mL山奈酚(30 μmol·L−1)的THF/水溶液(fw= 80%)放入4 mL的比色皿中,用365 nm的紫外灯进行照射1 h,然后测其荧光光谱。
2.4.8 pH稳定性实验
取适量山奈酚(30 μmol·L−1)的THF/水溶液(fw= 80%)放入小烧杯中,测其pH,在此基础上用1 mol·L−1盐酸和1 mol·L−1氢氧化钠溶液调pH范围1–12 (梯度为1),以365 nm为激发波长,测试溶液在375–550 nm范围内的荧光光谱,记录486 nm处的荧光强度值。
取30 μL Al3+储备液加入到3 mL Kae (30 μmol·L−1)的H2O/THF (8 : 2,V/V)二元溶液中,测其pH,在此基础上用1 mol·L−1盐酸和1 mol·L−1氢氧化钠溶液调pH范围1–12 (梯度为1),以365 nm为激发波长,测试溶液在375–550 nm范围内的荧光光谱,记录486 nm处的荧光强度值。
2.4.9 拟南芥根部组织的Al3+成像(演示)
用水洗涤拟南芥根部三次以除去杂质。之后,将清洗过的根分别在水中和含Kae (30 μmol·L−1)的THF/水(2 : 8,V/V)溶液中孵育1 h,用365 nm激发波长的激光共聚焦扫描显微镜进行荧光成像。
2.4.10 山奈酚聚集体及与Al3+螯合物的形貌表征(演示)
分别取适量山奈酚(30 μmol·L−1)的THF/水溶液(fw= 80%)以及与加入Al3+后的溶液滴在铜网上,待溶剂挥发后进行透射电子显微镜(TEM)表征。
3 结果与讨论
3.1 山奈酚的AIE特性
山奈酚在THF中表现出良好的溶解性。由于分子内旋转诱导的非辐射衰变,其稀溶液的荧光基本被猝灭。当水作为不良溶剂加入并且其体积含量(fw)增加到50%前,山奈酚的荧光强度几乎保持不变。当fw达到60%时,观察到以421 nm为中心的发射带,随着fw增加到80%时,发射强度急剧增加(图3a、3b)。动态光散射(DLS)结果表明,此时形成了直径为180 nm左右的聚集体(图3c)。当fw超过90%时,由于沉淀的形成,山奈酚的溶液变得浑浊,发射强度明显降低。这些结果表明山奈酚具有AIE特性。另外,山奈酚聚集体表现出优异的抗光漂白能力。如图3d所示,即使在紫外线照射60 min下,fw为80%的山奈酚聚集体的AIE荧光强度也保持不变,表明其具有高度光稳定性。
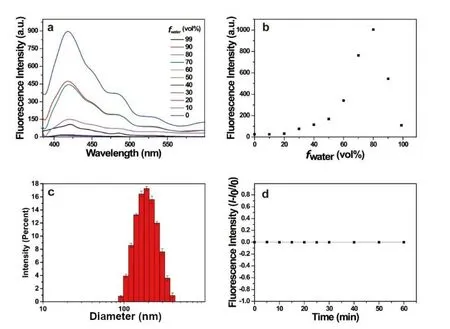
图3 (a) 山奈酚在不同体积比的水与THF中的荧光发射谱图;(b) 随着水的体积含量变化,山奈酚在421 nm处的荧光强度变化;(c) 山奈酚聚集体的粒径分布;(d) 山奈酚聚集体的光稳定性
3.2 山奈酚聚集体探针的Al3+响应机理
为了了解山奈酚聚集体对Al3+的响应机制,在THF/水二元溶剂(8 : 2,V/V)中进行了紫外滴定实验。如图4a所示,随着Al3+浓度的增加,吸收光谱370 nm处的吸收峰逐渐减小,同时425 nm处产生了一个新的吸收峰。这一结果表明山奈酚与Al3+发生反应形成了Kae-Al配合物。从吸光度(425 nm)与Al3+浓度之间的关系曲线来看,Kae-Al配合物的Kae与Al3+的配位比为3 : 1 (图4b),基于上述结果,聚集的Kae对Al3+的响应机制可能如图5所示。最初,Kae分子聚集成纳米颗粒,分布在THF/水的二元溶剂(8 : 2,V/V)中,由于AIE特性,聚集的Kae发出强烈的蓝色荧光。随着Al3+的加入,Kae聚集体将与其螯合,并且与Kae聚集物相比发射波长红移,发出蓝绿色荧光。从TEM照片可以看出,在THF/水的二元溶剂(8 : 2,V/V)中,Kae分子以及与Al3+形成的螯合物均以聚集体的形式存在。
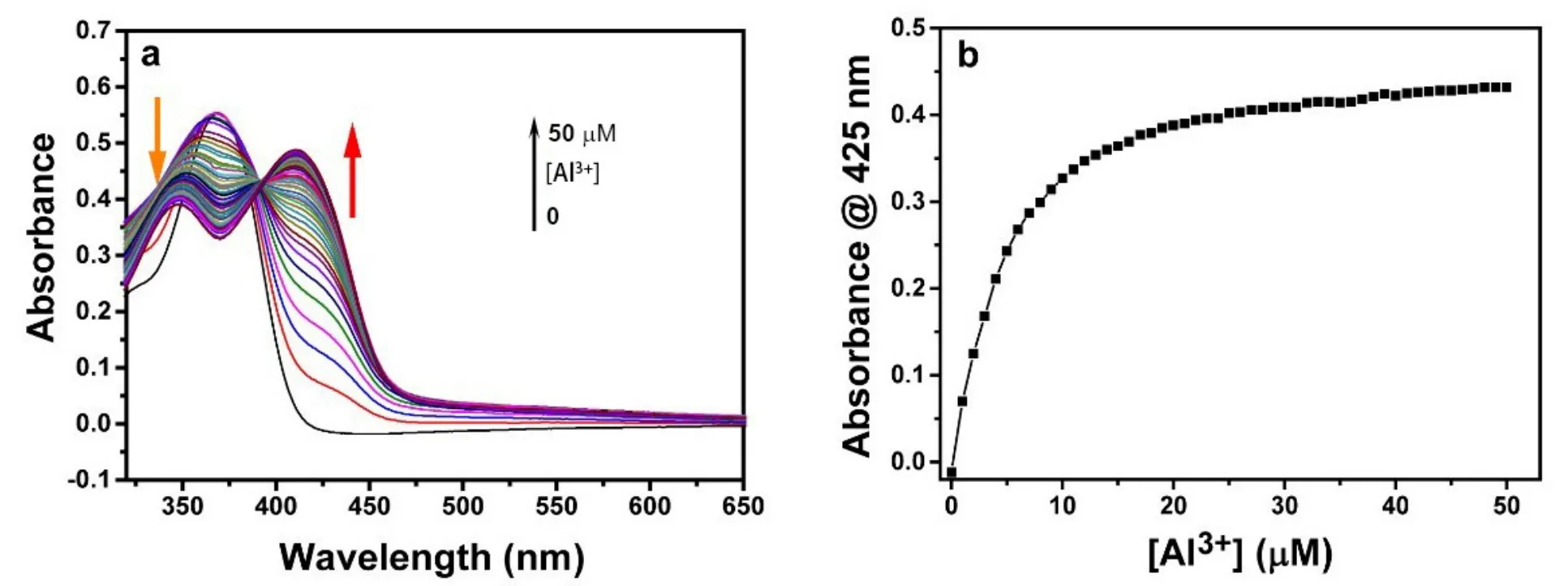
图4 (a) 山奈酚聚集体对Al3+的紫外滴定实验;(b) 425 nm吸光度与Al3+浓度的关系曲线
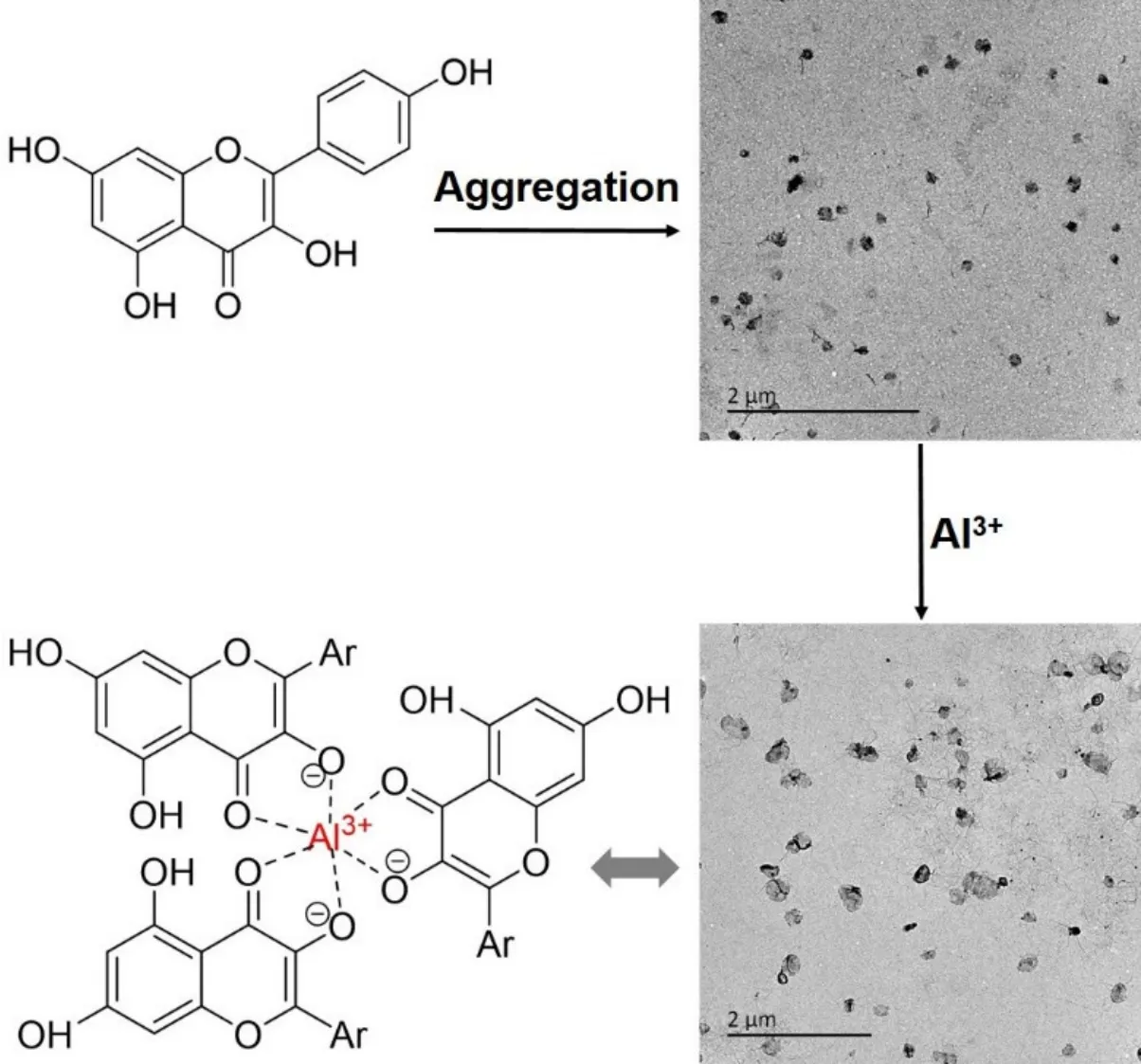
图5 山奈酚聚集体与Al3+的作用机制示意图
3.3 山奈酚聚集体探针的Al3+响应选择性和灵敏性
为了研究该探针对Al3+的特异性响应能力,我们考察了其他生物相关物种对Kae聚集体(THF/水,2 : 8,V/V)的AIE性质的影响(图6a、6b)。加入30 μmol·L−1的Al3+后,在421 nm处的发射峰明显减弱,同时在486 nm的发射峰明显增加。发射峰红移表明Kae和Al3+的络合作用导致分子内电荷转移增强。I486nm/I421nm的荧光比增加超过12倍,表明Kae聚集体对Al3+显示出高选择性。此外,加入30 μmol·L−1的Cu2+、Fe3+、Fe2+或Pb2+后,荧光几乎被淬灭,Kae对各种其他金属离子和阴离子的响应几乎可以忽略不计。
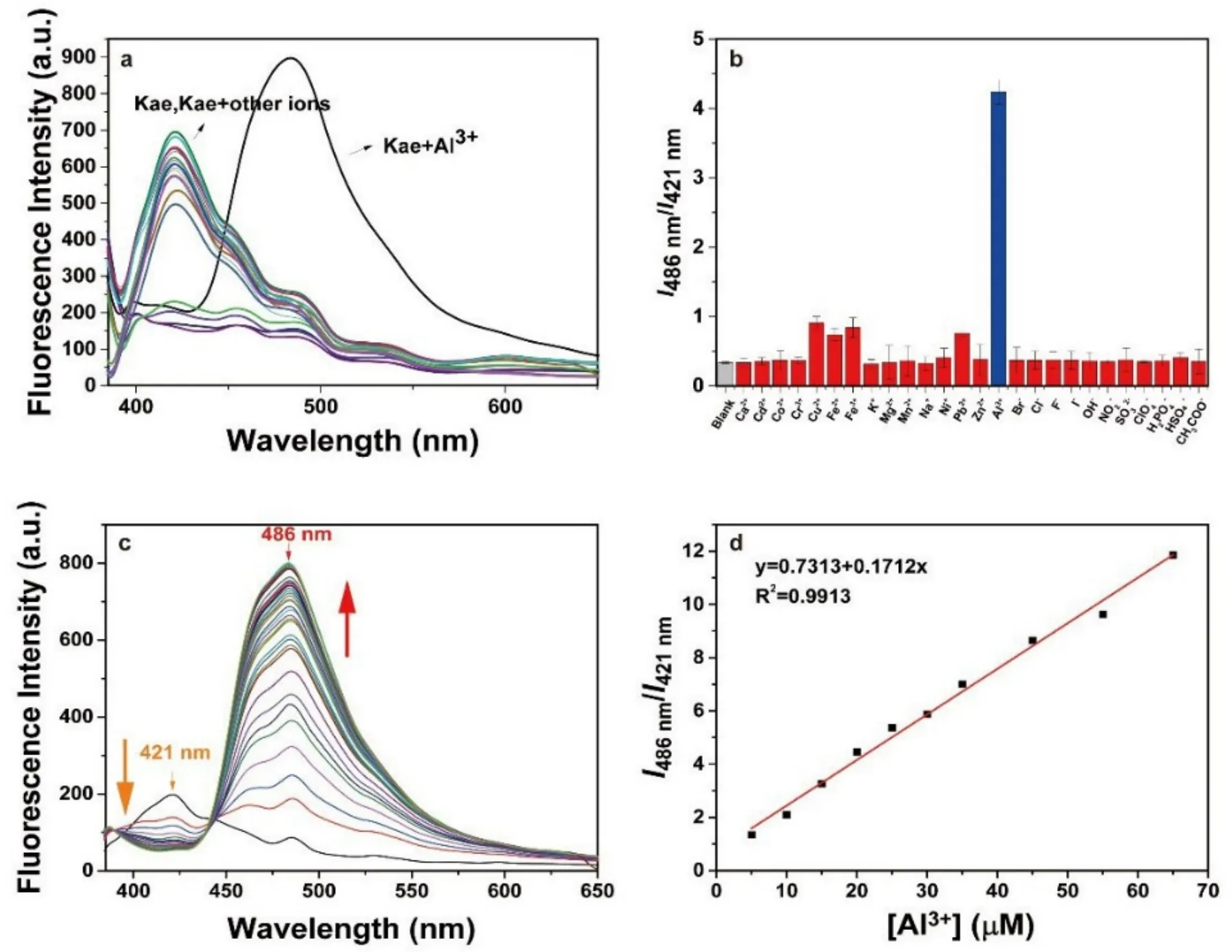
图6 (a) 探针对Al3+或各种干扰离子响应的荧光光谱和(b) 荧光强度比(I486 nm/I421 nm);(c) 探针与不同浓度Al3+响应的荧光强度变化;(d) I486 nm/I421 nm比值与Al3+浓度的函数图
为了研究Kae聚集体对Al3+响应的灵敏度,我们进行了Al3+的荧光滴定实验(图6c)。加入Al3+后,在421 nm处的发射强度缓慢降低,同时在486 nm处的发射峰强度缓慢增加。此外,观察到I486nm/I421nm荧光比和Al3+浓度在5–65 μmol·L−1范围内的呈线性关系(图6d),表明Kae聚集体可以用于定量检测Al3+。检出限(DL)是根据DL = 3σ/k的方程确定的,计算为0.37 μmol·L−1,其中σ为空白样品10次测量值的标准差,k为滴定实验中线性方程的斜率。
3.4 酸碱度对Kae聚集体检测Al3+的影响
为了研究探针在生物酸度条件下的稳定性,我们对探针在pH = 1–12的条件下进行了检测Al3+实验(图7)。结果表明Kae聚集体在pH值6–12范围内荧光稳定。加入Al3+后,在pH值4–9范围内,发射强度明显增加。值得注意的是,在pH值6–8范围内,Kae-Al的荧光非常稳定,表明Kae聚集体在生理条件下对Al3+具有稳定的检测能力。
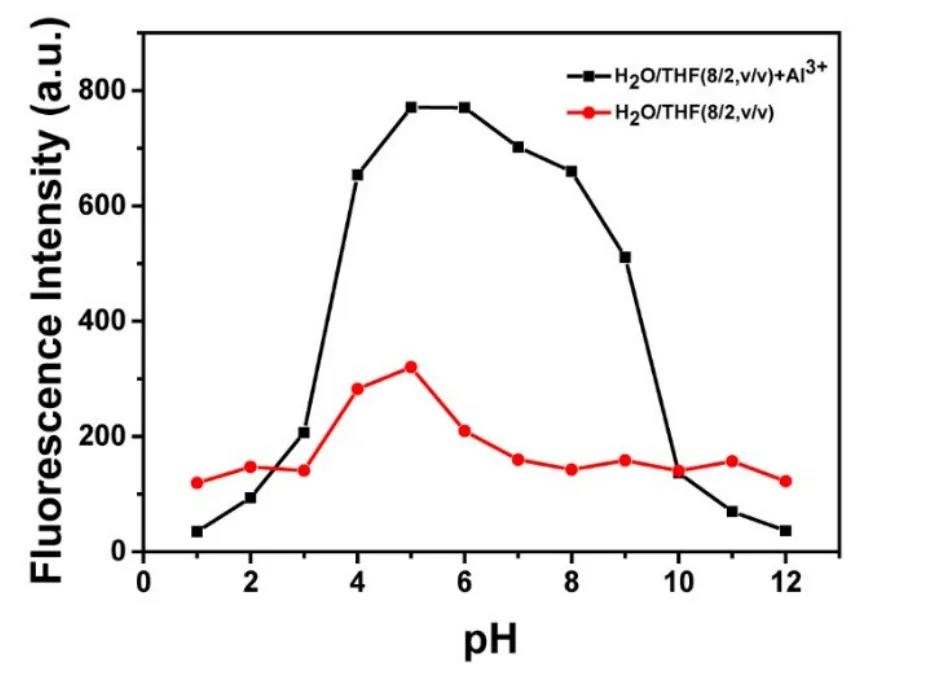
图7 探针对Al3+响应的pH稳定性
3.5 拟南芥根部组织的Al3+成像
如上所述,当pH在6–8范围内,Kae聚集体对Al3+具有高效的响应特征,这表明该探针可能具备在植物根部环境检测Al3+的能力。我们在拟南芥根部进行了Kae聚集体对Al3+成像的能力评估。如图8所示,首先将根部与水一起孵育1 h,然后利用荧光共聚焦显微镜对其成像,发现在410–450 nm(通道1)范围内不能获得荧光信号,而在465–600 nm (通道2)范围内可以捕获拟南芥微弱的自发荧光;之后,将根部与Kae聚集体溶液再一起孵育1 h,在通道1中可以看到微弱的荧光信号,而在通道2中可以获得明显增强的荧光信号。这些结果表明,Kae聚集体可以有效地实现拟南芥根部Al3+的可视化。
4 实验教学安排
实验总学时为16学时,分4次完成。具体安排如下:第一次课,4学时,学生经过文献调研后汇报荧光产生的原理以及AIE分子的发光机制;演示如何利用软件进行作图。第二次课,4学时,山奈酚与罗丹明B的荧光比较测试,含不同比例四氢呋喃/水溶剂的山奈酚的荧光光谱测试,交叉进行山奈酚聚集体的光稳定性测试、聚集体的粒径分布测试。第三次课,4学时,紫外滴定实验和荧光滴定实验、选择性测试、pH稳定性测试。第四次课,4学时,进行拟南芥根部的处理和激光共聚焦显微镜成像的观察、聚集体的TEM测试样品的制备和形貌表征。
5 结语
本实验将前沿和热点研究与基础教学相结合,能够满足双一流建设中人才培养的需求,实验贴近自然和生活,容易激发学生的兴趣。一方面,学生通过查阅文献,对天然产物的结构和应用有一定认识和了解,同时引导学生利用天然产物来解决与自身密切相关的环境问题,加强绿色发展理念;另一方面,通过对AIE提出背景和特点的了解,在拓展学生视野的同时,培养学生提出问题和分析问题的能力,并增强学生民族自豪感和激发学习的热情。
