动脉瘤栓塞后非缺血性脑增强病变1例
2024-02-03范雪怡钱海蓉
于 瑾,范雪怡,邓 馨,李 华,钱海蓉
1 病例报告
患者,女,63岁,因头痛伴左侧肢体力弱3 d,2019-12-23入住解放军总医院第三医学中心神经内科。既往高血压、糖尿病、动脉硬化病史,起病1个月前因蛛网膜下腔出血行右侧后交通动脉瘤支架辅助栓塞术。吸烟30年,40支/d,无饮酒史,无特殊个人史、家族史。入院体格检查:体温36 ℃,血压116/78 mmHg,内科查体未见异常。神经系统查体:神清,言语清晰。记忆力、理解力、计算力正常。颅神经(-),左侧肢体肌力4级,右侧肢体肌力5级,肌张力正常。左侧指鼻试验、跟膝胫试验欠稳准,右侧稳准。双侧肢体痛觉对称存在,四肢腱反射(++),对称存在。双侧Babinski征(-)。颈软,Kernig征(-)。入院后空腹葡萄糖 8.41mmol/L(正常范围:3.9~6.1 mmol/L),糖化血红蛋白 7.9%(正常范围:4.5%~6.0%);维生素B1294 pmol/L(正常范围:133~675 pmol/L)。结核γ干扰素释放试验(-)。
腰椎穿刺脑脊液压力130 mmH2O,潘氏试验 (+),细胞总数11×106/L(正常范围:0~50/L),白细胞数 11×106/L,蛋白0.24 g/L(正常范围:0~0.45 g/L),糖 4.59 mmol/L(正常范围:2.8~3.9 mmol/L),氯129 mmol/L(正常范围:120~132 mmol/L),乳酸脱氢酶 26 U/L(正常范围:114~240 U/L),腺苷脱氨酶 1.0 U/L(正常范围:4~24 U/L);未找到抗酸杆菌及新型隐球菌。结核病明确诊断的三项指标(简称结明三项)(血+脑脊液)均阴性。脑脊液自身免疫性脑炎、副肿瘤相关抗体及细胞学均阴性。脑脊液NGS(细菌、真菌、寄生虫、DNA病毒)均阴性。
2019-12-23颅脑MRI示右侧额顶颞枕叶异常信号,T1增强序列示右侧额顶叶多发强化病灶(图1A);T2Flair序列示右侧额顶叶血管源性水肿(图1B);弥散加权成像示右侧额顶叶不规则斑片状稍高信号(图1C)。诊断:颅内病变待查,予以双重抗血小板聚集、降脂稳斑及降压、降糖治疗。患者2020-01-13出院时头痛稍缓解,肢体无力未恢复。出院诊断:迟发性NICE病变。患者1年后随访,头痛缓解,左侧肢体肌力恢复,2021-01-07外院复查颅脑磁共振强化病灶消失(图1D),既往病灶消散(图1E、F)。
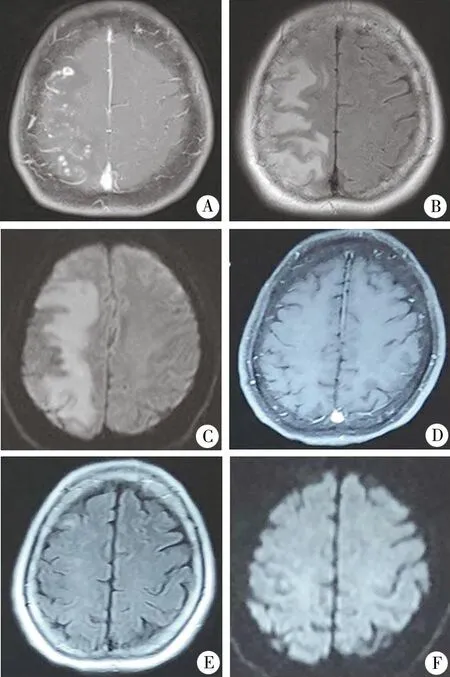
图1 右侧后交通动脉瘤栓塞术后NICE病变患者(女,63岁)颅脑MRI影像A.T1增强序列示右侧额顶叶多发环形、点状、小结节状强化病灶;B.T2 Flair序列示右侧额顶叶血管源性水肿;C.弥散加权成像示右侧额顶叶不规则斑片状稍高信号;D~F. 出院后1年随访,外院T1增强序列示原有增强病灶消失,相应部位T2 Flair序列和弥散加权成像示水肿消散。
2 讨 论
2.1 NICE病变的概念 2008年,Fealey等[1]报道了1例患者,颈内动脉眼段动脉瘤栓塞术后9个月,患者出现左侧肢体麻木、力弱,随后出现癫痫发作,行颅脑MRI检查示大脑皮质多发增强病灶,病理学证实肉芽肿组织中存在非折射性丝状蓝灰色异物,性状与亲水聚合物栓塞剂(hydrophilic polymer embolic, HPE)一致。2016年,Shotar等[2]提出迟发性NICE病变概念。2022年,Shotar 等[3]将NICE定义为迟发的,有症状或无症状的,分布在脑膜、皮层和皮层下的点状、结节状或环形增强病灶,伴病变周围水肿,病灶血管分布为EVT流域,排除其他可以解释其临床和影像的疾病。
2.2 临床特点 迟发性NICE病变的临床表现大多是非特异性的,包括癫痫发作、头痛、运动障碍、不自主运动、视觉障碍和言语障碍。Shotar等[2]报道,症状出现或发现无症状病变的平均延迟时间为12周,范围为2周至12个月。多项研究显示发病率为0.05%~0.9%,个别研究报道高达2.3%,患者大多数为女性[3-8]。NICE病变具有自愈性,多数患者MRI增强病灶可完全消失[6]。但仍有少数患者在皮质类固醇治疗下发生病情波动,并可能复发。
2.3 发病机制 NICE的发病机制主要有两种假说:一是EVT设备涂层HPE栓塞引发的异物肉芽肿性反应,二是EVT金属材料的过敏反应[2]。HPE进入血管后可引发血管内皮的损伤,导致Ⅳ型迟发型超敏反应,类似于异物肉芽肿性反应[9]。这是一种非过敏性慢性炎症反应,属于细胞介导的免疫应答。HPE与血液相互作用,发生蛋白质吸附,形成临时基质,引发急性炎症反应,表现为中性粒细胞浸润,并由肥大细胞脱颗粒介导,释放组胺、IL-4、IL-13和纤维蛋白原吸附。急性炎症在1周内消退,慢性炎症随着单核细胞的涌入而发生。由于炎症部位的细胞释放出各种趋化因子,巨噬细胞被吸收到HPE中并被激活,融合成多核巨细胞。巨噬细胞分泌炎症介质,促进肉芽组织形成,最终导致纤维化。
有研究表明,含有镍钛合金的颅内支架可能会引起短暂的偏头痛,最可能的原因是镍产生了过敏反应[10]。在使用置入装置治疗房间隔缺损后,血清镍水平升高,在24 h时显著升高,1个月时达到最高水平,12个月时降至基线水平[10]。
2.4 EVT的治疗 EVT作为颅内动脉瘤的一线治疗,最初使用的弹簧圈材料主要是不锈钢、铂和镍钛合金,通过诱导炎症和血栓形成促进动脉瘤的闭塞。早期的血管造影随访显示,超过20%的裸线圈填充动脉瘤发生再通[11]。在裸线圈表层覆盖可降解的HPE,如聚乙二醇-聚乳酸(polyethylene glycol-polylactic acid,PGLA)和聚乙烯吡咯烷酮(polyvinylpyrrolidone,PVP),可减少再通。PGLA在体内2~3个月可被完全吸收[12]。术后影像发现的无症状的动脉瘤壁强化可能代表弹簧圈的正常愈合反应。然而,过度的炎症反应可能导致严重的并发症,包括动脉瘤周围瘤样水肿和无菌性脑膜炎[13]。
HPE也被广泛用作EVT导管和装置的涂层,以减少血管内创伤和动脉痉挛。文献[14]报道PVP可以从导管中释放出来。模拟微导管使用的体外试验表明,HPE能够从导管中分离出来[15]。HPE栓子可能被免疫系统识别为异物,发生3种不同的脑内损伤模式,包括炎症反应、栓塞现象和动脉病变[16]。脑内损伤持续时间的长短因栓塞物的大小和分布而不同,也会受到患者发生过敏反应倾向的影响[9]。
美国食品和药物管理局针对EVT提出相关要求避免HPE脱落,包括规范使用导管,在导管插入器和导管套之间留足空间,必要时更换设备以避免过度使用[17]。一些作者也提出相关建议:正确储存器材;停止正压生理盐水冲洗微导管;微导管通过内径小、尖端有角度的导管时注意减少移动次数;对于多导管情况,考虑双腹股沟入路;有过敏史的患者,应避免使用生物活性弹簧圈[5,18,19]。
NICE的确切病因及机制尚不清楚,但这一罕见并发症的医源性原因未得到充分认识。设备涂层技术的进步能否降低或消除 HPE 的风险有待确定。颅内EVT后出现意想不到的神经症状时应高度怀疑迟发性NICE,在没有脑活检的情况下,识别典型的脑成像结果对其诊断至关重要。
