噻托溴铵联合莫西沙星治疗轻中度慢性阻塞性肺疾病急性加重期的临床研究
2024-01-29赵晶晶李亚楠于立为张小杰
赵晶晶,李亚楠,于立为,张小杰
首都医科大学附属北京友谊医院平谷医院 呼吸科,北京 101200
慢性阻塞性肺疾病是一种呼吸系统常见疾病,其发病率逐年上升,数据显示,我国2007—2018 年发病率由8.2%上升至13.7%,总患病人数约1 亿[1]。该病作为一种常见异质性肺部病变,其急性加重期对疾病进展和社会经济负担的负面影响尤为明显,该阶段是与气道和(或)肺泡异常有关、以14 d 内慢性呼吸道症状(呼吸困难、咳、痰等)急性加重为特征的临床过程,患者肺功能快速下降,可伴全身不适、心动过速、精神紊乱等症状[2]。临床上针对慢性阻塞性肺疾病急性加重期以改善肺泡通气量和控制感染为关键环节,轻中度患者主要采用支气管扩张剂、抗菌药等治疗策略以达到减少本次损害和未来发作频率的治疗目标[3]。莫西沙星为喹诺酮类药物,抗菌谱较广、可覆盖多种慢性阻塞性肺疾病合并感染病原菌,是慢性阻塞性肺疾病急性加重期的常用抗菌药[4]。噻托溴铵具有强大、持久的支气管扩张作用,利于改善肺通气、减轻呼吸道症状,属于长效抗胆碱能(LAMA)吸入粉剂[5]。故而本研究将噻托溴铵联合莫西沙星治疗慢性阻塞性肺疾病急性加重期。
1 资料与方法
1.1 一般资料
回顾性收集2019 年12 月—2022 年11 月首都医科大学北京友谊医院平谷医院呼吸科收治的78例轻中度慢性阻塞性肺疾病急性加重期患者的病例资料,其中男51 例,女27 例;年龄44~74 岁,平均(62.34±8.85)岁;慢性阻塞性肺疾病病程2~20年,平均(10.35±3.12)年;病情严重程度:轻度16 例,中度62 例。
纳入标准:(1)轻中度慢性阻塞性肺疾病[6];(2)符合慢性阻塞性肺疾病急性加重期诊断标准[7];(3)病例资料完整;(4)无噻托溴铵、莫西沙星使用禁忌证;(5)有抗菌治疗指征[7];(6)年龄44~75 岁;(7)近1 个月无抗感染药物、免疫调节剂及支气管舒张剂应用史;(8)均签订知情同意书。
排除标准:(1)严重充血性心力衰竭、心律失常、心肌梗死急性期;(2)出现严重肺内外并发症、如气胸等危重情况;(3)合并严重肝肾功能不全;(4)存在其他系统感染或慢性消耗性疾病;(5)伴有血液或内分泌等系统疾病;(6)新发脑血管疾病;(7)合并精神疾患或恶性肿瘤。
1.2 药物
噻托溴铵粉雾剂由正大天晴药业集团股份有限公司生产,规格18 μg/粒,产品批号190104202、200215064、210314109、220 620302;盐酸莫西沙星氯化钠注射液由海南爱科制药有限公司生产,规格250 mL∶盐酸莫西沙星0.4 g 与氯化钠2.0 g,产品批号191007、201289、211146、220918。
1.3 分组和治疗方法
根据治疗方案的不同将患者分为对照组和治疗组,每组各39 例。其中对照组男27 例,女12 例;年龄46~74 岁,平均(62.79±8.65)岁;慢性阻塞性肺疾病病程3~20 年,平均(10.74±3.23)年;病情严重程度:轻度9 例,中度30 例。治疗组男24 例,女15 例;年龄44~72 岁,平均(61.48±8.36)岁;慢性阻塞性肺疾病病程2~19 年,平均(10.08±2.96)年;病情严重程度:轻度7 例,中度32 例。两组基线资料比较差异无统计学意义,具有可比性。
所有患者均接受生活调摄、维持液体和电解质平衡、痰液引流、雾化吸入祛痰药物处理伴随并发症等相同的基础治疗措施。对照组静脉滴注盐酸莫西沙星氯化钠注射液,0.4 g/次,每次输液时间≥90 min。治疗组在对照组基础上使用噻托溴铵吸入粉雾剂,1 粒/次,通过粉雾吸入器吸入给药装置吸入使用,1 次/d。两组疗程为10 d。
1.4 临床疗效判定标准[8]
以肺部体征和呼吸道症状(咳嗽、咳痰、喘息)的改善情况作为疗效评定依据。临床控制:肺部哮鸣音和呼吸道症状恢复至急性发作前状态;减轻:肺部哮鸣音和呼吸道症状未达发作前状态,但有好转;无效:肺部哮鸣音和呼吸道症状与入院前无明显变化。
1.5 观察指标
1.5.1 咳痰评估问卷(CASA-Q)评分 覆盖咳嗽症状和影响、咳痰症状和影响共4 个方面20 个条目,各条目均按严重程度计0~4 分,各方面评分及其总分均采用百分制转换,评分越高则咳嗽、咳痰症状越轻[9]。
1.5.2 血气指标 使用德国SIEMENS 公司产的RAPIDPoint500 型血气分析仪测定患者动脉血氧分压(pO2)、动脉血二氧化碳分压(pCO2)。
1.5.3 改良版英国医学研究委员会呼吸困难问卷(mMRC)评分 按患者呼吸困难严重程度分为0 级(剧烈活动时感受到)、1 级(快走或上坡时感受到)、2 级(平地行走需停下呼吸或较同龄人走得慢)、3级(平地步行数分钟或100 m 需停下呼吸)、4 级(感受明显无法离开房屋),评分(0~4 分)越高则呼吸困难越严重[10]。
1.5.4 血常规相关指标和血清C 反应蛋白(CRP)运用深圳迈瑞公司BC-6800 型血液细胞分析仪对患者行血常规和CRP 检查,由检查结果计算中性粒细胞与淋巴细胞比值(NLR)、血小板与淋巴细胞比值(PLR),并记录CRP 水平。
1.6 不良反应观察
记录患者药物相关不良反应,包括皮疹、恶心、口干、头痛。
1.7 统计学分析
使用SPSS 25.0 统计软件包处理数据,计量资料、计数资料分别以、百分比表示,分别行t、χ2检验。
2 结果
2.1 两组临床疗效比较
治疗后,治疗组总有效率是97.44%,较对照组的79.49%显著提高(P<0.05),见表1。

表1 两组临床疗效比较Table 1 Comparison on clinical efficacy between two groups
2.2 两组CASA-Q 评分比较
治疗后,两组CASA-Q 中咳嗽症状、咳嗽影响、咳痰症状、咳痰影响评分及其总分均较治疗前显著增加(P<0.05);且治疗后,治疗组CASA-Q 评分高于对照组(P<0.05),见表2。
表2 两组CASA-Q 评分比较( )Table 2 Comparison on CASA-Q scores between two groups ()

表2 两组CASA-Q 评分比较( )Table 2 Comparison on CASA-Q scores between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05。*P < 0.05 vs same group before treatment;▲P < 0.05 vs control group after treatment.
2.3 两组血气指标比较
治疗后,两组pO2均显著上升,而pCO2均显著下降(P<0.05);且治疗后,治疗组血气指标改善优于对照组(P<0.05),见表3。
表3 两组血气指标比较( )Table 3 Comparison on blood gas indicators between two groups ()
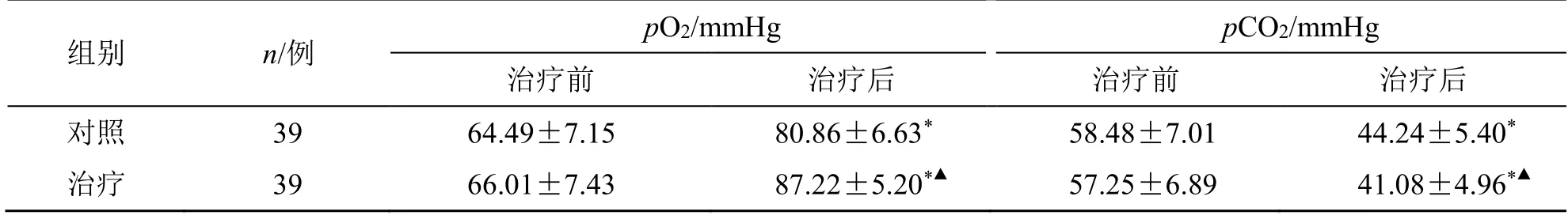
表3 两组血气指标比较( )Table 3 Comparison on blood gas indicators between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05(1 mmHg=133 Pa)。*P < 0.05 vs same group before treatment;▲P < 0.05 vs control group after treatment (1 mmHg=133 Pa).
2.4 两组mMRC 评分比较
治疗后,两组mMRC 评分均显著降低(P<0.05);且治疗后,治疗组mMRC 评分低于对照组(P<0.05),见表4。
表4 两组mMRC 评分( )Table 4 Comparison on mMRC scores between two groups ()
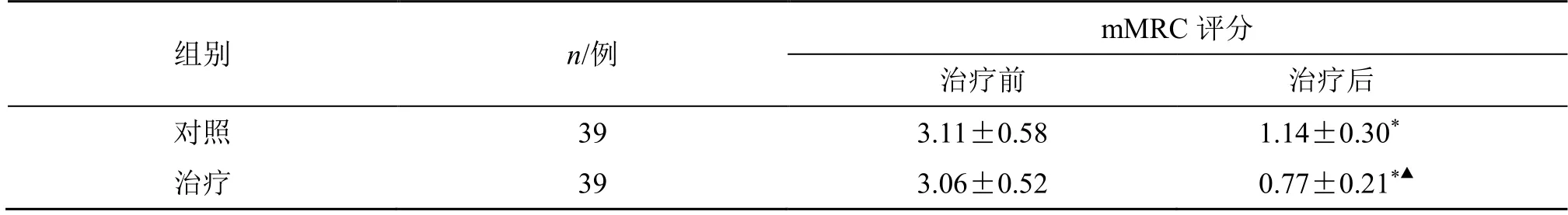
表4 两组mMRC 评分( )Table 4 Comparison on mMRC scores between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05。*P < 0.05 vs same group before treatment;▲P < 0.05 vs control group after treatment.
2.5 两组外周血NLR、PLR 和血清CRP 水平比较
治疗后,两组NLR、PLR 和CRP 水平均显著下降(P<0.05);且治疗后,NLR、PLR 和血清CRP水平均以治疗组降低更显著(P<0.05),见表5。
表5 两组外周血NLR、PLR 和血清CRP 水平比较( )Table 5 Comparison on peripheral blood NLR,PLR,and serum CRP levels between two groups ()

表5 两组外周血NLR、PLR 和血清CRP 水平比较( )Table 5 Comparison on peripheral blood NLR,PLR,and serum CRP levels between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05。*P < 0.05 vs same group before treatment;▲P < 0.05 vs control group after treatment.
2.6 两组不良反应比较
对照组发生皮疹、恶心各1 例,不良反应发生率是5.13%;治疗组发生口干2 例,头痛1 例,不良反应发生率是7.69%,两组不良反应发生率比较差异无统计学意义。
3 讨论
急性加重期作为慢性阻塞性肺疾病自然病程中多见的临床事件,每年发生0.5~3.5 次,且首次发生后未来再次发生风险明显增加,与患者的健康状况、肺功能减退、劳动力丧失、生活质量下降等密切相关,是该病医疗费用的主要部分和患者首位死亡因素。目前研究指出,慢性阻塞性肺疾病急性加重近80%由呼吸道感染触发,病毒感染、吸入过敏原、空气污染等因素引起和(或)加重气道炎症,进而诱发下呼吸道细菌感染,造成气流阻塞加剧,是该病程分期的主要发生机制[11]。因此,合理使用抗菌药物是慢性阻塞性肺疾病急性加重期的常用治疗策略之一。莫西沙星可作为无铜绿假单胞菌感染风险的慢性阻塞性肺疾病急性加重期患者抗菌治疗的优选之一,其主要通过干扰细菌脱氧核糖核酸拓扑异构酶Ⅱ和Ⅳ,起到抑制慢性阻塞性肺疾病急性加重期绝大部分常见病原体(如肺炎链球菌、流感嗜血杆菌、金黄色葡萄球菌、卡他莫拉菌等)的效果,且耐药率低;同时本品具有肺组织浓度高、杀菌效能强、不良反应较少等优点,对呼吸系统感染具有良好疗效[12]。1 项多中心、随机对照研究显示,莫西沙星治疗慢性阻塞性肺疾病急性加重的疗效和细菌清除率与β 内酰胺类抗生素相似,能达到快速减轻症状、降低治疗失败率、延长发作间期的作用,且可明显缩短住院和抗生素使用时间,利于减少医疗费用及抗生素选择压力[13]。
慢性阻塞性肺疾病急性加重期以持续、进展性气流阻塞为特征,长期气道阻力增加可引起呼吸肌疲劳和肺通气功能障碍,从而导致呼吸衰竭、肺心病等不良后果。支气管舒张剂能有效缓解气流受限、降低急性发作风险,是慢性阻塞性肺疾病急性加重期的核心治疗措施[14]。噻托溴铵为新型吸入粉剂,其扩张支气管、抑制炎性细胞浸润、抗气道重塑等作用主要通过与气道平滑肌M1、M3 胆碱受体结合实现,从而可达到纠正气流阻塞、减少肺过度充气、改善肺功能、增加运动耐量、遏止病情恶化等治疗目的。此外,该药物与M1、M3 受体解离缓慢,能24 h 获得气道舒张效应,作用持久、应用方便,患者依从性高;而其局部抗胆碱能作用及与M2 受体快速解离的特点则有助于降低不良反应[15]。庞晶琳等[16]研究表明,慢性阻塞性肺疾病急性加重期在常规治疗基础上予噻托溴铵治疗有助于纠正呼吸困难症状、改善肺功能和运动功能、防治肺部感染。本研究将噻托溴铵与莫西沙星联合应用于轻中度慢性阻塞性肺疾病急性加重期的治疗中,发现其总有效率(97.44%)优于单纯莫西沙星治疗的对照组(79.49%);且联合治疗组对CASA-Q、mMRC 评分及血气指标(pO2、pCO2)和肺功能指标(FEV1占预计值%、MVV、FEV1/FVC)的改善效果均显著优于对照组;表明噻托溴铵与莫西沙星的联合方案对减轻轻中度慢性阻塞性肺疾病急性加重期患者咳、痰、呼吸困难症状及改善肺通气和降低肺功能损害具有良好效果;另外,治疗组患者的不良反应并未明显增加,故安全性较佳。
遍及气道、肺实质和肺血管的慢性炎症是慢性阻塞性肺疾病急性加重期的重要病理特征。NLR、PLR 为新兴的炎症标志物,均由全血细胞计数衍生而来,具有使用广泛、经济、高效、简便等优点,二者在慢性阻塞性肺疾病急性加重期呈现数值上升的特点,其水平变化可反映机体炎症状态及预警风险[17]。其中由于炎性刺激,气道内会大量聚集活化的中性粒细胞,可通过释放活性氧基、金属蛋白酶、细胞因子等多种介质,加速炎症反应及肺组织破坏;感染应激促进了儿茶酚胺类物质与糖皮质激素分泌,致使淋巴细胞功能下降与凋亡,故其数量减少;低氧、酸中毒及大量炎症因子的释放导致肺血管内皮损伤,引起血小板过度激活,从而加重肺实质炎症、增加心血管事件风险[18]。CRP 为常用炎症指标,可用于评估细菌感染、抗菌药物使用及预后。罗立等[19]研究显示,慢性阻塞性肺疾病急性加重期患者血清CRP 水平较健康人群明显上升,且与病情严重程度密切相关。本研究中,治疗后治疗组外周血NLR、PLR 和血清CRP 水平均显著低于对照组;提示噻托溴铵联合莫西沙星在抑制轻中度慢性阻塞性肺疾病急性加重期患者机体炎性反应方面的效果更为突出。
综上所述,噻托溴铵联合莫西沙星治疗轻中度慢性阻塞性肺疾病急性加重期患者具有良好的疗效,能安全有效地缓解患者呼吸道症状,改善动脉血气和肺功能,调节机体炎症状态,值得临床推广应用。
利益冲突所有作者均声明不存在利益冲突
