单操作孔电视胸腔镜肺癌根治术治疗非小细胞肺癌患者的疗效观察
2024-01-24章静娴聂云飞
严 琳,赵 倩,曹 彬,章静娴,聂云飞
(郑州大学第一附属医院,河南 郑州 450000)
非小细胞肺癌( NSCLC)早期无明显症状,确诊时已发展到早中期[1]。传统开胸术创伤大、并发症多[2]。微创术逐渐应用于NSCLC治疗中,目前多采用胸腔镜下肺癌根治术治疗,其创伤小、恢复快[3]。胸腔镜肺癌根治术一般是三孔法,包括主操作、观察和副操作孔,但副操作孔对肌层损伤大,且空间狭窄,可加重对机体的损伤,增加疼痛感[4]。研究发现,三孔胸腔镜肺癌根治术治疗后存在感觉障碍、背部切口疼痛等问题[5]。目前随着胸腔镜技术的发展,手术过程逐步缩减为单操作孔电视胸腔镜(VATS)手术,其是在三孔术式上进行改进,保留了主操作孔和观察孔,可减少对肌肉和神经的损伤,减轻疼痛,且切口美观[6]。但该手术方法在临床中详细报道较少,故本研究进一步分析该术式对NSCLC围术期指标、疼痛程度、肺功能、炎性因子、肿瘤标志物及血清血管内皮生长因子受体2(VEGFR2)、胸苷激酶1(TK1)水平和并发症的影响,现报道如下。
1 资料与方法
1.1 一般资料2020年6月至2022年6月我院收治的245例NSCLC患者。纳入标准:①符合《中国原发性肺癌诊疗规范》[7]诊断,并经术后病理学确诊。②具备手术指征,年龄25~78岁,TNM分期:Ⅰ~Ⅱ期;③病历资料完整。排除标准:①心力衰竭及心律失常;②既往具有开胸手术史;③术前接受过化疗、免疫或靶向治疗;④术中腔镜手术中转开胸。按手术方式分为对照组(三孔胸腔镜肺癌根治术,n=115)和观察组(单操作孔VATS肺癌根治术,n=130)。对照组男62例、女53例,年龄25~78岁[(55.87±7.16)岁];体质量指数(BMI)19~24 kg/m2[(22.78±1.70)kg/m2];病灶直径3~7 cm[(4.32±0.48)cm];TNM分期:Ⅰ期47例,Ⅱ期68例;腺癌81例,鳞癌34例。观察组男72例、女58例,年龄26~77岁[(56.49±7.22)岁];BMI 19~24 kg/m2[(23.14±1.77)kg/m2];病灶直径3~7 cm[(4.09±0.52)cm];TNM分期:Ⅰ期52例,Ⅱ期78例;腺癌92例,鳞癌38例。两组一般资料比较差异无统计学意义(P>0.05)。本研究经医院伦理委员会批准通过。
1.2 方法患者全麻,取侧卧位。对照组采用三孔胸腔镜肺癌根治术:腋前线和腋中、后线7、8肋间为操作、观察、操作孔。胸腔镜确定病灶,操作孔置入手术器械,游离、切除病变,清扫淋巴结,留置引流管。观察组采用单操作孔VATS肺癌根治术:腋中线7肋间为观察孔,置入Trocar、胸腔镜,4~5肋间隙切口为操作孔。打开纵膈胸膜并游离肺静脉、动脉、支气管,切割器切断,取出病灶组织,清除肺门和纵隔系统性淋巴结,检查有无创面出血,冲洗胸腔,留置引流管,缝合切口,术闭。
1.3 观察指标①记录术中出血量、手术和引流时间及淋巴清扫数。②VAS评分[8]:总分10分,无痛及轻、中、重度疼痛分别为0分、<3分、4~6分和7~10分。③肺功能:肺功能仪测定第1秒用力呼气容积(FEV1)、用力肺活量(FVC)、最大呼气流量(PEF)。④ELISA检测肿瘤坏死因子-α(TNF-α)、C反应蛋白(CRP)、白细胞介素-6(IL-6)、白细胞介素-1β(IL-1β)。⑤肿瘤标志物及VEGFR2、TK1水平:术前及术后7d采用ELISA检测糖类抗原5(CA50)、癌胚抗原(CEA)、细胞角质蛋白19片段抗原21-1(CYFRA21-1)、VEGFR2、TK1水平。⑥观察并记录两组并发症。
1.4 统计学方法采用SPSS 24.0统计学软件处理数据。计量资料以均数±标准差表示,不同时间点比较采用重复测量方差,两组比较采用t检验,计数资料以例数(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组围术期指标比较观察组出血量较对照组少(P<0.05),两组其他指标比较,差异无统计学意义(P>0.05)。见表1。
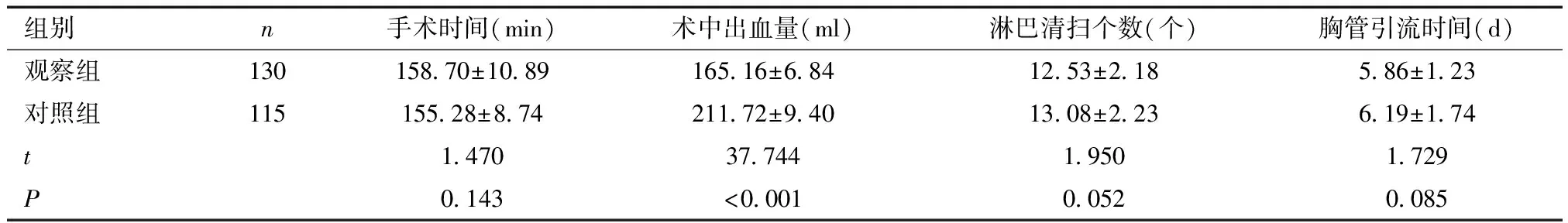
表1 两组围术期指标比较
2.2 两组VAS评分比较观察组术后各时间点VAS评分均低于对照组(P<0.05)。见表2。

表2 两组VAS评分比较 (分)
2.3 两组肺功能指标比较术前两组肺功能比较差异无统计学意义(P>0.05);术后1个月两组肺功能指标均较术前升高,且观察组肺功能指标高于对照组(P<0.05)。见表3。
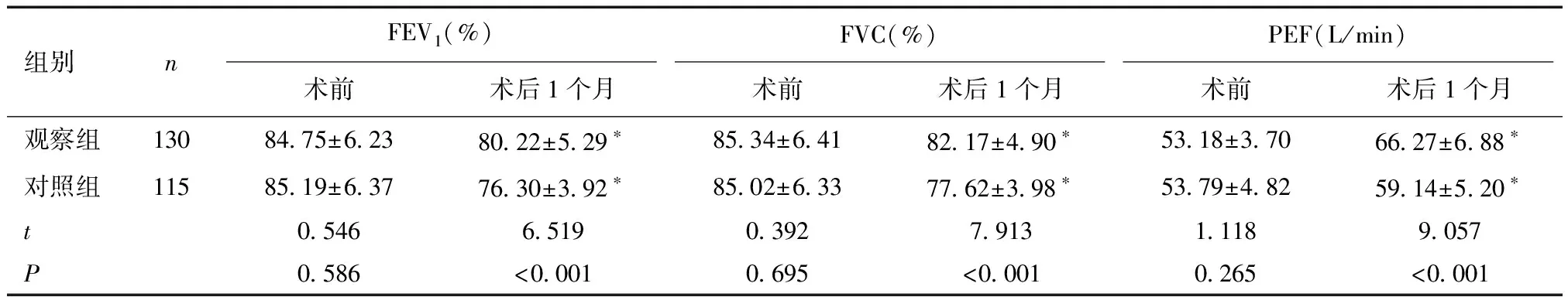
表3 两组肺功能指标比较
2.4 两组炎性因子水平比较术前两组炎性因子水平比较,差异无统计学意义(P>0.05);术后3 d两组炎性因子水平均较术前降低,且观察组炎性因子水平低于对照组(P<0.05)。见表4。

表4 两组炎性因子水平比较
2.5 两组肿瘤标志物水平比较术前两组肿瘤标志物水平比较,差异无统计学意义(P>0.05);术后7 d两组肿瘤标志物水平均较术前降低,且观察组各肿瘤标志物水平低于对照组(P<0.05)。见表5。
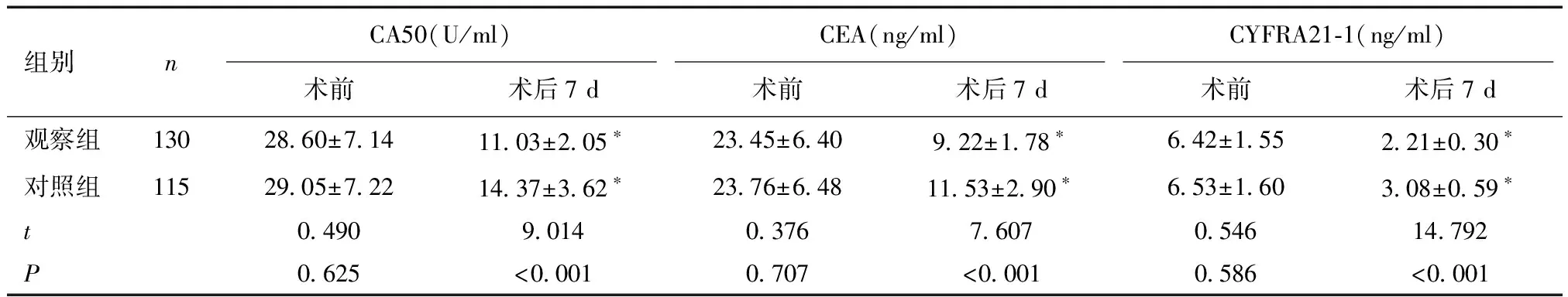
表5 两组肿瘤标志物水平比较
2.6 两组VEGFR2、TK1水平比较术前两组VEGFR2、TK1水平比较,差异无统计学意义(P>0.05);术后7 d两组VEGFR2、TK1水平均较术前降低,且观察组VEGFR2、TK1水平低于对照组(P<0.05)。见表6。
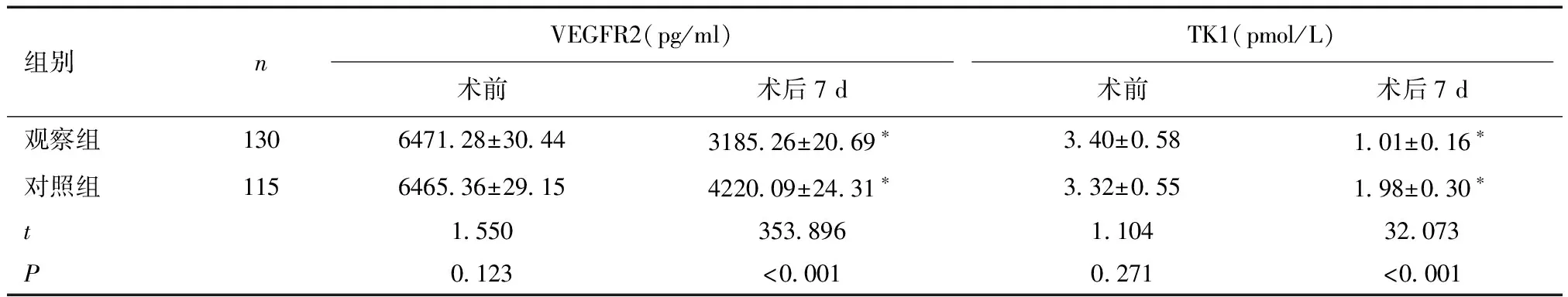
表6 两组VEGFR2、TK1水平比较
2.7 两组并发症发生情况比较两组并发症发生情况比较,差异无统计学意义(P>0.05)。见表7。

表7 两组并发症发生情况比较[n(%)]
3 讨论
近年来,NSCLC发病率逐渐上升,其发病隐匿、侵袭性高[9]。传统开胸术创伤大、并发症较多,且术中易损伤神经、疼痛感强烈,不利于患者恢复。随着微创理念与技术的革新,胸腔镜术具有创伤小、操作简单、恢复快、切口小及位置隐蔽等优点,逐渐应用于NSCLC治疗中,临床以三孔胸腔镜肺癌根治术较为常见,但其副操作孔位于肋间隙,并经阔肌,血供丰富,易损伤神经,术后可致感觉、运动障碍,加重疼痛[10,11]。近年来单操作孔VATS肺癌根治术逐渐应用于治疗NSCLC中,减少了副操作孔切口,且切口长度短,减少了切口引起的渗血、渗液,促进了了胸腔引流,能有效缓解术后疼痛;且操作孔处肌肉群少、肋间隙宽,出血量少,可避免肌肉和神经组织受损情况,促进术后恢复[12,13]。
蒲睿智等[14]等研究显示,单操作孔VATS肺癌根治术中由于操作器械和辅助器械均从同一位置放入,导致操作过程中容易彼此受到影响,在调整时延长手术时间可延长手术时间。与本研究结论不一致,与例数少有关。且观察组术中出血量少,说明单操作孔VATS肺癌根治术可减少出血量;同时观察组术后12、24、48及72 h的VAS评分低于对照组,提示单操作孔VATS肺癌根治术可降低术后疼痛,究其原因:三孔胸腔镜肺癌根治术切口数较多,可加大对肋间神经刺激和挤压的损伤,因此疼痛程度较高,而单操作孔VATS肺癌根治术切口少且短,创伤小,故可降低疼痛。且研究发现,术后1个月,观察组肺功能高于对照组,说明单操作孔VATS肺癌根治术对肺功能损伤更小,有利于患者肺功能恢复,这是由于单操作孔VATS肺癌根治术切口少,可减少对肺部的损伤,有利于肺功能恢复。研究表明,手术可损伤机体,引起炎症反应[15]。TNF-α、CRP、IL-6、IL-1β为常见炎症因子,可反应组织损伤程度[16]。本研究显示,术后3 d,观察组TNF-α、CRP、IL-6、IL-1β较对照组低,说明单操作孔VATS肺癌根治术可抑制炎症因子,这是由于单操作孔VATS肺癌根治术创伤小,急性期炎症反应也相应有所减轻。而CA50、CEA、CYFRA21-1是肿瘤标记物,可反映肿瘤治疗情况。研究显示,术后7 d,观察组肿瘤标志物低于对照组,与沈荣强等[17]研究相符,说明单操作孔VATS肺癌根治术可降低肿瘤标志物水平。肿瘤发生、生长依赖于新生血管,VEGF是血管新生的启动剂子,而VEGFR-2在VEGF和血管内皮生成中起主导作用[18];而TK1是DNA合成的嘧啶补救途径激酶,可反映肿瘤细胞增殖速率[19,20]。本研究发现,术后7 d,观察组VEGFR2、TK1水平低于对照组,提示单操作孔VATS肺癌根治术可抑制新血管生成,延缓肿瘤增长、转移。此外,两组并发症率无差异,提示两种术式安全性均高。
综上,单操作孔VATS肺癌根治术可改善NSCLC患者肺功能,降低炎性因子、肿瘤标志物和VEGFR2、TK1水平,下一步将随访远期疗效,旨在为临床提供充足论证。
