靶向补体的IgA肾病治疗进展
2024-01-24李贵森
李贵森
(1.四川省医学科学院·四川省人民医院肾脏内科,四川 成都 610072;2.电子科技大学医学院,四川 成都 610056 )
从最早命名IgA肾病(IgA nephropathy,IgAN)开始,临床医生就注意到在肾小球系膜区伴随IgA分子沉积,同时有补体成分如C3的沉积,提示补体活化在IgAN的发病中起重要作用。近年来,针对补体活化在IgAN发病和进展中的作用,以及靶向补体的治疗,已经成为IgAN的研究热点,本文对相关的进展进行综述。
1 补体活化是IgAN发病的重要环节
早期大量研究已经证实,IgAN患者血清或肾组织中补体C3水平与患者的蛋白尿水平、肾功能损害程度,或者疾病进展风险相关。2003年Suzuki等对肾移植的供肾进行零点肾活检,显示供肾IgA阳性率16.1%,但仅同时伴有C3沉积时,部分患者才可能出现病理改变[1]。对GWAS数据进行分析显示,IgAN易感位点相关的基因包括补体H因子相关蛋白1(CFHR1)和3(CFHR3)等[2]。IgAN患者肾组织中多种补体成分阳性,如C1q、MBL、L-Ficolin、Collectin 11、MASP 2、MASP 1/3、Bb、C4d、C3c、C5b-9等[3]。通过尿液蛋白组学分析也显示,与健康对照相比,IgAN患者尿液多种补体成分异常[4]。多项研究显示,IgAN患者存在血清、肾组织和尿液中补体成分异常和补体活化的证据[5~7]。IgAN患者血液中含IgA1的大分子复合物中也包含多种补体成分,其具体作用还需要进一步探索[7]。这些证据均表明,IgAN发病和肾组织损害过程中,补体活化起重要的作用。实质上,IgAN发病机制的四重打击学说中,糖基化缺陷IgA1(Gd-IgA1)与其相应的自身抗体结合,沉积肾组织后,补体活化是刺激系膜细胞及导致后续肾组织病理生理改变的重要环节[8]。
2 补体活化与IgAN的临床表现及预后相关
早期大量研究已经证实,IgAN患者血清、肾组织和尿液中的补体活化证据与患者临床及病理表现相关,与患者肾功能损害严重程度及疾病进展相关[5~7]。目前研究重点关注的补体成分包括替代途径的C3、C3a、Bb、CFH、CFHR1、CFHR5;凝集素途径的MBL、C4d、MASP2、MASP1/3、MAP19、Ficolin;共同通路的C5、C5a、C5a受体、C5b-9等[5~7]。
近年来的GWAS研究数据显示IgAN易感位点与补体编码蛋白相关,例如位于1q32的rs6677604,既位于补体H因子编码基因CFH的内含子区,也与CFHR1和CFHR3的调节区相关,会影响IgAN患者补体活性[9]。近期一项研究对1781例患者的年随访显示,尽管系膜区C3沉积与基因的变异相关,但仅有系膜区更强的C3沉积与IgAN患者严重的肾功能损害,更重的肾脏病理表现和严重的不良结局[eGFR下降>40%、终末期肾病、全因死亡]相关[10]。循环CHFR5的水平高的IgAN患者肾功能损害更严重,更易发生肾功能进展及终末期肾病[11,12]。多种尿液补体成分异常与IgAN患者蛋白尿,肾功能损害和严重病理表现相关[4]。
3 靶向补体治疗是IgAN治疗的重要方向
基于前期的临床和基础研究结果,证实补体活化在IgAN发病和进展中起至关重要的作用,因此靶向补体的治疗是目前探索的热点之一[5~7,13~15]。目前很多药物已经进入临床研究,见表1。
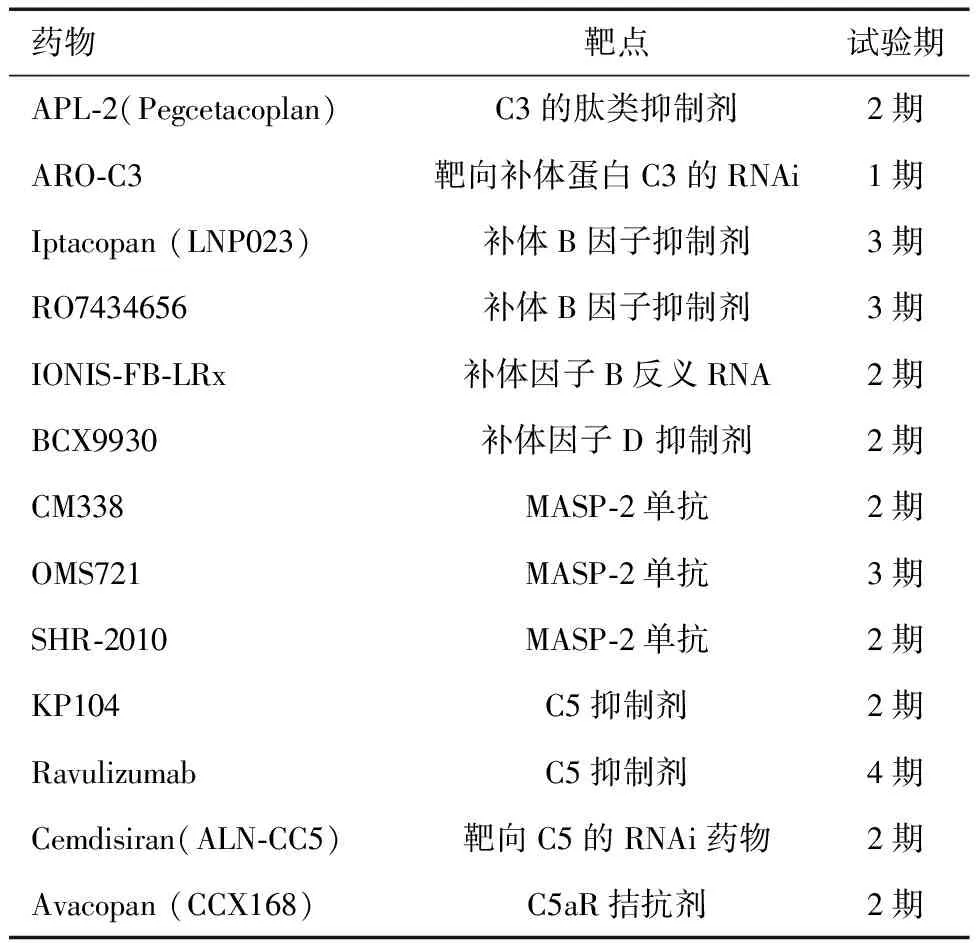
表1 靶向补体系统药物治疗IgA肾病的临床研究
3.1 甘露聚糖相关凝集素结合丝氨酸蛋白酶(mannan-associated lectin-binding serine protease,MASP)MASP是凝集素通路的重要成分。Narsoplimab作为MASP2的抗体,已经在血栓性微血管病中做了系列临床研究。近期的一项2期临床试验,纳入18岁以上IgAN患者,24小时尿蛋白排泄>1 g/d,eGFR>30 ml/(min·1.73 m2),充分RAS系统抑制剂等支持治疗后,使用激素者进入亚组1,逐渐激素减量,同时使用Narsoplimab每周一次输注,12周后停止,随访6周;未用激素者进入亚组2,分成Narsoplimab和安慰剂的随机对照试验[16]。亚组1 的4例患者,用药后尿蛋白显著下降,但eGFR相对稳定;亚组2患者治疗及延长后尿蛋白有较明显下降[16]。其后一项在美国肾脏病年会公布的研究数据(未发表)显示,Narsoplimab对54例IgAN治疗18周后尿蛋白下降与对照相似,但延长至31周后,治疗组尿蛋白下降达到61%。
MASP3是MASP1的剪接异构体,MASP1基因敲除鼠导致MASP1/3缺乏,导致D因子缺乏,使B因子不能活化,替代途径活化受阻。MASP1/3和D因子也可能成为IgAN的重要干预靶点。
3.2 B因子B因子在IgAN患者血清和肾组织表达增加,与临床表现相关[7]。LNP023是诺华研发的B因子口服抑制剂,II期临床试验纳入112例IgAN患者,eGFR30>30 ml/(min·1.73 m2),尿蛋白> 0.75 g/24 h,稳定剂量RAS抑制剂。患者分成不同剂量,观察3月时尿蛋白的变化情况[17]。结果显示,患者3月时尿蛋白下降23%,呈明显的剂量依赖性[17]。目前已经开始III期研究(APPLAUSE-IgAN),拟纳入450例IgAN患者,观察iptacopan对患者蛋白尿和肾功能的影响[18]。
在2022年ASN年会上公布了针对B因子,基于配体共轭反义技术设计的反义核苷酸IONIS-FB-LRx治疗IgAN的II期临床试验,25例IgAN患者,29周时尿蛋白下降44%,其安全性和耐受性良好。
3.3 补体C3补体C3在IgAN发病和进展中的作用已经得到证实。Pegcetacoplan(APL-2)是C3和C3b的一种肽抑制剂。II期的临床试验证实,对于C3肾病,该药显著降低患者48周的蛋白尿,但对于IgAN和狼疮性肾炎,治疗效果不明显[19]。
3.4 补体C5补体C5活化与IgAN发病及进展相关,也是一个重要的干预靶点。目前已经针对C5开发了多种药物,例如依库珠单抗(Eculizumab)是C5的抑制剂,已经有一些个案报道在IgAN患者取得较好的效果。直接针对C5的药物还有Ravulizumab (ALXN1210) 单抗,靶向C5的GalNAc-偶联的小干扰RNA (siRNA) (ALN-CC5) cemdisiran来沉默C5的表达,都已经开展临床试验[5,7,13,15]。
针对C5aR的抑制剂Avacopan,在IgAN的II期试验,尿蛋白>1 g/g的IgAN患者中,在RAASi基础上,予以avacopan 30mg,Bid,治疗4周,7例IgAN患者中有6例尿蛋白改善,其中3例患者尿蛋白下降>50%[20]。
总之,IgAN患者预后仍然较差,近年来新的治疗药物和措施不断涌现,有助于改善患者的预后。其中,靶向补体系统的关键成分治疗IgAN是一个重要的方向,已有的临床试验证据支持我们积极进一步研究,以改善患者预后。
