制备乙酸乙酯若干问题的再探究
2024-01-16马凯旋
马凯旋


摘要:针对制备乙酸乙酯过程中反应物添加顺序及吸收剂选择问题再次展开实验探究和讨论。从热效应角度,通过测量混合溶液的温度,证明了按照乙醇、乙酸、浓硫酸的添加顺序效果最好;通过探究吸收剂的选择,证明在一定的实验条件下,制备过程中有乙醚和水副产物生成;选择饱和碳酸钠溶液和30%氢氧化钠溶液作吸收剂效果最好,选择15%氢氧化钠溶液却得不到乙酸乙酯层;进一步探究乙酸乙酯与氢氧化钠溶液反应的本质,推测乙酸乙酯碱性水解的临界点在氢氧化钠溶液质量分数为15%~30%之间。通过再探究,有助于教师和学生解决制备乙酸乙酯实验中存在的困惑和对某些知识点的深入理解。
关键词:乙酸乙酯制备;实验探究;添加顺序;吸收剂选择
文章编号:10056629(2023)12007805
中图分类号:G633.8
文献标识码:B
1 问题提出
在高中化学必修第二册“乙酸”的教学中,乙酸乙酯的制备是教学重点[1]。教材上,这个实验中试剂的添加顺序是3mL乙醇→2mL98%的浓硫酸→2mL冰醋酸,这种添加顺序是否最合理?此外,在制备乙酸乙酯的过程中,吸收剂的选择是否有唯一性,氢氧化钠溶液是否一定不能作为吸收剂?对于上述两个问题,不少学者也曾对其进行了探究[2]。笔者从另一角度思考:在试剂添加顺序中,加入浓硫酸后,必然存在热效应,那么温度变化是否会
对实验结果产生影响?另外对于吸收剂的选择,陆燕海等人进行模拟实验,只研究了30%氢氧化钠溶液对结果的影响,并未考虑其他浓度[3]。为探究真实的实验情境,消除存在的疑惑,笔者设计了改进实验,作进一步深入研究。
2 实验仪器及药品
实验仪器:100mL烧杯、玻璃棒、2mL和5mL吸量管、量筒、试管、试管架、碎瓷片、酒精燈、铁架台、酒精温度计和电子天平(型号:HCC 1002)
实验药品:98%浓硫酸(分析纯)、无水乙醇(分析纯)、乙酸(分析纯)、氯化钠(分析纯)、碳酸钠(分析纯)、碳酸氢钠(分析纯)、氢氧化钠(分析纯)和酚酞指示剂
3 实验原理
乙酸和乙醇在浓硫酸催化下加热可制备乙酸乙酯,苏教版必修第二册教科书中,用如图1A所示装置进行实验[4];苏教版选择性必修3中,用如图1B所示装置进行实验[5]。实验过程中发现用图1B装置进行实验,反应速率很慢,反应约10分钟,油层高度仅为0.3cm(文中乙酸乙酯产量均以高度计)且液体呈米黄
色,表明产物杂质也较多[6]。为提高实验效率,不考虑杂质影响,本实验选用图1A装置进行实验。
4 实验设计
4.1 实验探究一:按不同顺序添加试剂过程中温度变化对乙酸乙酯产量的影响
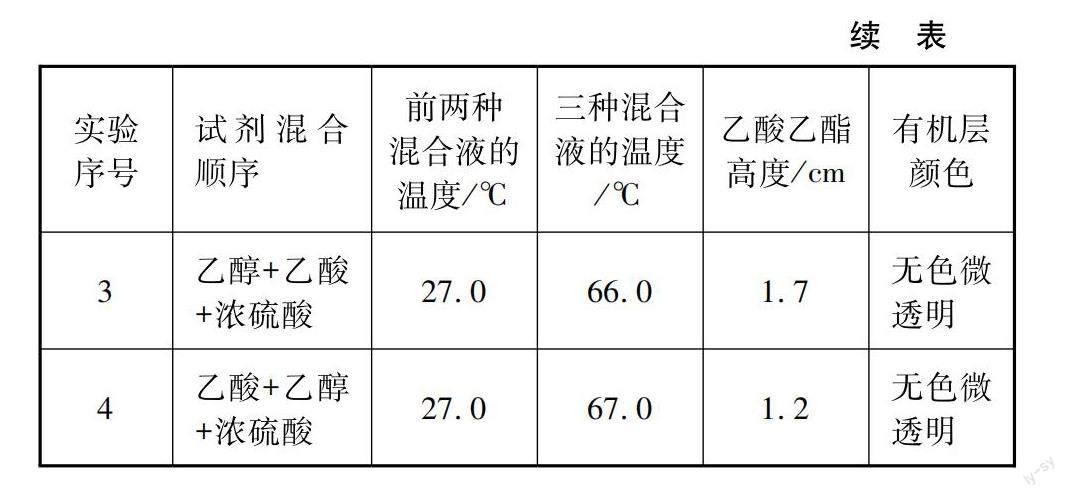
分别测前两种试剂混合溶液的温度和加最后一种试剂后溶液的温度,记录温度最大值,平行测定三次并计算平均值,然后按照对应顺序以水作吸收剂,制备乙酸乙酯并测其高度,结果见表1,相关试剂性质与用量见表2。
从实验结果可见,溶液混合后,温度均未超过任一反应试剂的沸点,故实验过程中,试剂的挥发结果近似,反应液体积的变化可以忽略不计。我们发现第3种加料方式得到的乙酸乙酯的量最大,这里可以通过三个角度进行解释:第一,在有液体参与的反应中,添加液体的顺序,一般按照密度由小到大的顺序添加,这样有利于反应液的充分混合。第二,先加乙醇再加乙酸,可以把乙醇看作分散剂,把乙酸看作分散质,这样有利于乙酸分子充分分散,并且根据反应机理,乙酸的质子化是酯化反应的决速步骤[12],因此乙酸充分分散,不在最后加入,均有利于后续浓硫酸对其质子化,进而有利于乙酸乙酯产量的提高。第三,如果乙酸最后加入,由于乙酸密度较小会浮于乙醇和浓硫酸混合溶液表面,且乙醇和浓硫酸混合时会放热,由表1数据知此两种溶液混合时温度升高最大,因此易造成乙酸的挥发且不利于乙酸质子化,这也可以解释表1中实验1得到的乙酸乙酯高度很小。因此,在后续实验中即按照先加乙醇,然后加乙酸,最后再加浓硫酸的顺序进行。
4.2 实验探究二:不同吸收剂的实验现象分析及其对乙酸乙酯产量的影响
分别选取水、饱和氯化钠溶液、饱和碳酸氢钠溶液,饱和碳酸钠溶液、质量分数分别为15%和30%氢氧化钠溶液作吸收剂,实验过程中保持所取吸收剂体积、所用试管均相同,探究吸收剂对乙酸乙酯产量的影响。分别配制好对应的溶液后,用移液管量取5mL对应吸收剂于试管中,分别向饱和碳酸氢钠溶液,饱和碳酸钠溶液、15%氢氧化钠溶液、30%氢氧化钠溶液滴入两滴酚酞指示剂(由于15%和30%氢氧化钠溶液浓度较大,溶液碱性很强,滴入酚酞溶液后,振荡试管溶液红色很快退去),分别向水和饱和氯化钠溶液中滴入两滴水作对照,进行乙酸乙酯制备实验。实验结果如表3所示。
由表3可见,不同的吸收剂对反应结果颇有影响,为此,笔者对其进行深入探究,进而说明不同吸收剂影响乙酸乙酯产量的原因。我们以15%氢氧化钠溶液和饱和碳酸钠溶液吸收剂为例,制备乙酸乙酯实验结束,对吸收剂所在试管振荡前后进行对比。结果发现,试管振荡前,含有饱和碳酸钠溶液的试管,三层溶液分层清晰,而含有15%氢氧化钠溶液的试管,中层和下层溶液分层不清晰。对此,笔者研究用饱和碳酸钠溶液为吸收剂,所得的三层溶液的主要成分的实验结果如表4所示。
由表4可知,上层溶液主要为乙酸乙酯,该层溶液呈酸性且与下层溶液混合会使其退色,混合过程中有气泡产生,说明上层溶液中还含有乙酸,由于乙酸的量较少,下层溶液退色的主要原因是乙酸乙酯对酚酞的萃取[13]。下层溶液呈碱性,且几乎无刺激性气味,说明主要溶质为碳酸钠。中层溶液有刺激性气味,与乙醚气味相似,已知乙醇成醚的反应温度在140℃,用酒精灯加热试管,会达到并超过这一数值,笔者推测含有乙醚,但根据资料所知常温下乙醚可燃烧,与钠不发生反应[14]且微溶于水,易溶于乙酸乙酯[15],又根据表2知乙醚密度为0.714g·mL-1,小于乙酸乙酯密度,且根据反应温度来看,应该先生成乙酸乙酯再生成乙醚,故理论上乙醚应该完全溶于乙酸乙酯。然而,在实验过程中,导管口刚开始是悬在液面上方,后来随着产物增多,导管口逐渐被溶液淹没,后面产生的乙醚没有与乙酸乙酯充分接触,有少部分乙醚溶于水中,且中层溶液不燃烧,会与钠剧烈反应,故推测中层溶液中大部分是水。中层和下层液体混合,红色不退去,说明中层溶液几乎不含乙酸,对于是否含有乙醇可采取更高级的检测方法,比如红外光谱等。故中间层主要是含少量乙醚的水溶液,但是为何这种溶液会与碳酸钠溶液分层?仔细观察发现,中下层溶液的分层与上中层之间的分层状态不同,也就是其与有机液体和水溶液间的明显分层有较大差距,且将中下层液体混合后,溶液不再分层,故中下层液体实际不是严格意义上的分层,而是由于未经外力作用,溶液密度和酸碱性不同而导致颜色的分界。经过振荡,三层溶液充分混合,乙酸乙酯萃取碳酸钠溶液中的酚酞而使红色退去,同时也萃取了水中的乙醚,最终溶液分为两层。
用15%氢氧化钠溶液作为吸收剂时,未振荡试管前,中下层分层处隐约出现红色,这说明氢氧化钠溶液浓度在减小,达到使酚酞变红的浓度。振荡后,乙酸乙酯充分与氢氧化钠溶液接触,导致乙酸乙酯发生水解,溶液不再分层。水解过程中,氢氧化钠溶液浓度进一步减小,使溶液的红色变得更加明显。仔细观察还可以发现试管上部分溶液红色较深,下部分较浅,这是由于上部分溶液中,还含有浓度较大的乙酸钠,使溶液碱性增强。
通过上述讨论,当用水和饱和氯化钠溶液作吸收剂时,保持其他实验条件不变,也会出现乙醚、水等副产物,只是由于没有指示剂使下层溶液显色,看上去溶液分为两层。
由表3可见,不同吸收剂会影响乙酸乙酯的产量。其中水、饱和氯化钠溶液和饱和碳酸氢钠溶液对乙酸乙酯产量的影响差别不大,但是都小于以饱和碳酸钠溶液、30%氢氧化钠溶液为吸收剂的情况。以水作吸收剂时,乙酸乙酯在水中的溶解度较小,且乙酸和乙醇极易溶于水,在水的体积固定的情况下,乙酸乙酯没有溶解太多。饱和碳酸氢钠可以与乙酸反应,且能溶解较多的乙酸乙酯,故得到油层高度最小[16]。15%氫氧化钠溶液会直接导致乙酸乙酯的水解。饱和碳酸钠溶液、30%氢氧化钠溶液除去乙酸的效果很好,且乙酸乙酯在其中的溶解度小,故得到的油层高度最高。为探究氢氧化钠溶液浓度不同导致实验结果不同的原因以及乙酸乙酯与氢氧化钠溶液反应的本质,待反应结束后,将分别含有15%和30%氢氧化钠溶液的试管充分振荡静置后的结果进行对比。
探究发现,含有30%氢氧化钠溶液的试管中溶液依然分层,且上下层液体均无红色出现。与含有15%氢氧化钠溶液的试管中溶液颜色及状态对比,可以推知乙酸乙酯与氢氧化钠溶液反应的本质是乙酸乙酯和水发生水解反应,即乙酸乙酯中的乙酰基和乙氧基分别与水中的羟基和氢结合。若氢氧化钠浓度过高,则会抑制水的电离,从而不利于乙酸乙酯水解正向进行,因此用30%氢氧化钠溶液作为吸收剂仍会得到乙酸乙酯层。
由此也可以推测出,乙酸乙酯在氢氧化钠溶液中的水解存在一个临界点,该点氢氧化钠溶液溶质质量分数在15%~30%之间。综上,在实验室制备乙酸乙酯时可以选择饱和碳酸钠溶液或30%氢氧化钠溶液。
5 结语
在制备乙酸乙酯添加反应物过程中,从热效应角度进一步说明按照乙醇、乙酸、浓硫酸顺序添加效果最好。实验结束,吸收剂所在试管溶液分为三层,中下层并非严格意义上的分层,中间层主要是含少量乙醚的水溶液。选择饱和碳酸钠溶液和30%氢氧化钠溶液作吸收剂,得到的乙酸乙酯产量最高,而选择15%氢氧化钠溶液作吸收剂则得不到乙酸乙酯层,因此乙酸乙酯的水解受氢氧化钠溶液浓度的影响很大。
参考文献:
[1][4]王祖浩主编. 普通高中教科书·化学·必修第二册[M]. 南京:江苏凤凰教育出版社,2022:72.
[2][3][12][16]陆燕海,江旭峰. 制备乙酸乙酯若干问题的实证与教学分析[J]. 化学教学,2020,(5):87~92.
[5]王祖浩主编. 普通高中教科书·化学·选必3[M]. 南京:江苏凤凰教育出版社,2022:101.
[6]鲍文亮,林美凤,刘丽君. 水浴条件下乙酸乙酯制备实验的改进[J]. 化学教学,2019,(10):64~66.
[7][8]曾洁萍,李金燕,许旋,罗一帆. 建模教学在发展高阶思维中的研究——以“乙酸乙酯的制备”复习为例[J]. 中学化学教学参考,2022,(4):45~46.
[9]大连理工大学无机化学教研室编. 无机化学(第五版)[M]. 北京:高等教育出版社,2011:497.
[10]李景宁等. 有机化学(第五版下册)[M]. 北京:高等教育出版社,2012:40.
[11][14]李景宁等. 有机化学(第五版上册)[M]. 北京:高等教育出版社,2013:321~322.
[13]谢雕,唐娅. 乙酸乙酯制备实验中酚酞褪色原因的探究[J]. 化学教学,2016,(12):64~66.
[15]吴朝辉. 乙酸乙酯的水溶性及制备时碳酸钠溶液的作用[J]. 化学教学,2016,(8):50~52.
