固体推进剂用硝酸酯增塑剂的热安定机制研究进展①
2024-01-12曹华文唐秋凡郑启龙李吉祯
曹华文,唐秋凡,郑启龙,屈 蓓,李吉祯
(西安近代化学研究所,西安 710065)
0 引言
随着大型舰船、高性能战斗机、直升机作战平台、车载作战平台等高性能武器平台的不断涌现及“立体攻防、全域作战”能力的着力构建[1-3],对武器系统提出了更宽的温度适应能力的要求,如机载和舰载武器系统必须适应远洋(赤道周边舰面温度可达80 ℃以上)作战、车载或机载武器系统等必须适应沙漠(撒哈拉沙漠夏季白天地表最高温度达70 ℃以上)作战等极端环境要求,保证其在极端环境下工作稳定可靠。因硝酸酯的热安定机制未掌握,其热安定控制技术方面仍存在明显不足,目前以硝酸酯作为增塑剂的固体推进剂的使用温度上限尚无法满足武器平台环境适应能力的要求[4],这已成为制约该类推进剂应用拓展的关键瓶颈。
硝酸酯是对含有O—NO2基团的一类物质的总称,因其优异的能量特性和塑化能力,成为固体推进剂中不可或缺的含能增塑剂。固体推进剂中应用的硝酸酯种类繁多,如双基推进剂和改性双基推进剂中常用的硝酸酯增塑剂有硝化甘油(NG)、N-硝基-二乙醇胺二硝酸酯(DINA)、三羟甲基乙烷三硝酸酯(TMETN)等[5-6],硝酸酯增塑聚醚(NEPE)推进剂常用的有硝化甘油(NG)、1,2,4-丁三醇三硝酸酯(BTTN)等[7-8],叠氮推进剂中主要使用的有硝化甘油(NG)、二缩三乙二醇二硝酸酯(TEGDN)、1,2,4-丁三醇三硝酸酯(BTTN)等[9],端羟基聚醚(HTPE)不敏感推进剂中常用的有丁硝胺乙基硝酸酯(BuNENA)等[10-11]。因为硝酸酯分子中O—NO2键键强度和化学稳定性相对较弱,所以硝酸酯键在温度升高时会发生分解,释放出氮氧自由基。氮氧自由基会对硝酸酯的分解产生催化作用[4, 12],这种催化作用会加速硝酸酯的分解。硝酸酯的分解过程还会放出大量的热,这会导致体系温度的升高,甚至发生燃烧、爆炸。硝酸酯增塑的固体推进剂的使用温度上限取决于硝酸酯增塑剂的热分解温度。硝酸酯的分解无法被阻止,但是加入化学安定剂可以有效吸收硝酸酯热分解初期产生的氮氧化物[13-14],从而抑制其自催化反应,延缓硝酸酯分解速率,使固体推进剂体系安定、长时间储存(25 ℃下有效贮存期可达十年到几百年[15]),具有一定的高温环境适应能力。国内外化学安定剂在推进剂中的应用多以经验及试验为主[5-6, 8, 13, 14, 16-40],对化学安定剂安定机理研究较少,硝酸酯的热安定性机制未掌握,新型安定剂设计及应用缺乏理论依据,硝酸酯增塑的固体推进剂的温度适应上限不能满足使用要求。鉴于此,急需对固体推进剂硝酸酯增塑剂的热安定机制开展深入研究,用于指导新型安定剂体系的设计及应用,为提升武器装备的环境适应温度能力提供理论支撑。
深入开展固体推进剂硝酸酯增塑剂的热安定机制的研究,不仅是目前固体推进剂应用的要求,也是未来固体推进剂领域发展的重要方向。本文综述了固体推进剂硝酸酯增塑剂热安定机制的研究进展,并且提出未来该领域研究的重点。
1 硝酸酯常用的安定剂
安定剂在推进剂中占比很少,通常添加量不超过5%,但其是硝酸酯增塑的固体推进剂不可或缺的组分。安定剂能迅速地吸收硝酸酯组分释放的氮氧自由基,且不生成对推进剂有害的产物。安定剂本身不具有强碱性或者强酸性,其与推进剂组分有良好的相容性,具有良好的贮存稳定性。目前常用的化学安定剂主要有苯胺类、苯脲类及苯酚类化合物等,可以单独使用也可以复配使用[4, 41-43],如图1。

图1 固体推进剂中常用的化学安定剂(二苯胺(DPA)、2-硝基苯胺(2-NDPA)、N-甲基-硝基苯胺(MNA)、2号中定剂(1,3-二甲基-1,3-二苯脲,C2)和3-甲基-1,1-二苯基脲(AK-Ⅱ)、间二苯酚(Res))
苯胺类安定剂主要有二苯胺(DPA)、2-硝基苯胺(2N-DPA)、N-甲基-硝基苯胺(MNA)。二苯胺从1905年开始就被用作安定剂[44],其常温下是结晶状的白色固体,熔点54 ℃,沸点302 ℃。但因为二苯胺具有较强的碱性,这导致其与推进剂组分的相容性较差,所以限制了其在固体推进剂中的广泛应用。2N-DPA比DPA碱性弱,所以应用则更加广泛。MNA与氮氧自由基反应活性高、吸收速率快,是硝酸酯类含能材料极为有效的安定剂,但由于其在硝酸酯中溶解度低,易于晶析,导致其固体推进剂的加入量受到极大限制,一般不超过0.5%。
苯脲类安定剂包括1号中定剂(1,3-二乙基-1,3-二苯脲,C1)、2号中定剂(1,3-二甲基-1,3-二苯脲,C2)和3-甲基-1,1-二苯基脲(AK-Ⅱ)等。1号中定剂在和氮氧化物反应时会产生大量气体,这会使药柱开裂,故目前应用很少。2号中定剂碱性较弱,和氮氧化物反应速率慢,常与间苯二酚复配应用于改性双基推进剂中。AK-II是一种新型的安定剂,其在N原子上引入酰氧基,增大了分子的共轭效应,这有效降低了N原子上的碱性,使其不与硝酸酯发生皂化反应,同时其苯环上的π电子具有供电子效应,使其能与亲电试剂(如NO)发生反应,吸收硝酸酯释放出的氮氧自由基,起到良好的安定作用[14, 45-47]。
苯酚类安定剂含有富电子基团,可以与氮氧自由基发生反应。目前广泛应用的苯酚类安定剂是间二苯酚(Res),但是Res和交联剂(如异氰酸酯)存在竞争性反应,这会降低推进剂的交联度[4],减少了其在推进剂中的应用范围。目前也有一些新的酚类安定剂,但其安定效率相对较低,推测可能是由于空间位阻过大导致的[28, 41]。
目前国内外也开发出一些新的安定剂种类,包括天然组分[48]、富勒烯类[49]、丙二苯酰胺类[26]、无机类[50]、高分子类安定剂[51]等。有些化合物性能不亚于传统的安定剂,但因对其研究还不够成熟,尚未见相关应用报道。
单组分安定剂的使用有一定的局限性,如DPA会导致硝化甘油皂化、MNA易于晶析、2号中定剂反应速率过慢等,为了解决这些问题,人们提出了安定剂复配的解决方法[5, 52-58]。
目前对于安定剂复配的研究主要集中在两种安定剂的复配。BELLAMY等[5]提出现有的复配安定剂中第二组分安定剂的作用是减少第一组分安定剂的消耗,使复配安定剂的工作时间更长,达到更好的安定效果。安定剂C2/2N-DPA[54]、C2/DPA[19]、MNA/C2[59]、三苯胺(TPA)/C1[53]、TPA/Ak-II[53]和MNA/2N-DPA[5, 60]等的复配都有应用或者报道。唐秋凡等[61]研究指出单组分苯脲型安定剂或者复配的苯脲型安定剂都无法满足改性双基推进剂(CMDB)未来提升使用温度的需求。对于复配安定剂来说,以MNA为主组分,以2N-DPA、C2和Res中的一种及一种以上(以不同时添加C2和Res为前提)为第二组分的复配安定剂的安定效果最佳:在推进剂配方中添加1.0%MNA和0.3%的2-NDPA,或者添加0.5%MNA,0.5%2-NDPA和0.3%的C2,推进剂的5 s爆发点温度都可达 305 ℃,只添加单组分安定剂的推进剂5 s爆发点温度都小于303 ℃。
虽然复配安定剂比单组分的安定剂性能更为优异[4-5],但因为当前安定剂安定机理及安定作用机制理论依据不足,相关新型安定剂的设计、固体推进剂安定剂的优选和复配使用等研究工作仍然以实验为主。
2 硝酸酯的热安定机制
2.1 硝酸酯的热分解机理
开展硝酸酯的热安定机制研究,首要任务是全面掌握硝酸酯的热分解过程,尤其是其使用温度条件下的热分解速率,热分解产物组成等。关于硝酸酯的分解机理的研究很多[22-24, 33, 62-85],并且已经取得了许多成果。硝酸酯的分解分为两步——硝酸酯键的断裂与硝酸酯的自催化。硝酸酯的部分分解过程如图2所示。

图2 硝酸酯的分解机理
根据目前的研究结果,可以知晓NG、TEGDN等常用的硝酸酯的初步反应是O—NO2键的均裂,其遵循接近典型的一级反应动力学方程;第二步反应则是自催化反应[22-24, 62-76]。
NO2催化的硝化甘油的分解反应分为α位和β位夺氢催化反应两种,并且α位的夺氢催化反应更迅速。根据目前的研究结果可以将硝化甘油的分解反应分为两步,第一步O—NO2基团消去反应为主反应通道,第二步α夺氢反应为主反应通道[75, 77-80],如图3所示。

图3 硝化甘油的α位与β位夺氢反应
季戊四醇四硝酸酯(PETN)热分解机理研究结果表明PETN的分解活化能为125~292 kJ·mol-1之间[67, 81-82]。根据分解温度可以将PETN的分解划分为两个部分(如图4):低温下(353.15、363.15、 373.15、383.15 K)分解缓慢,部分分解;高温下(393.15、403.15 K)存在相变过程,分解迅速,产生大量气体,403.15 K下达到0.1%分解深度的时间仅为8 min,远低于353.15 K下的30 964 min[67],如图4所示。

图4 (a)各温度下PETN的压力-时间曲线;(b) 各温度下PETN的压力-时间曲线(换算到298.15 K)
SUN等[83]在B3LYP/6-31G**水平下计算了1,2-二硝基丙二醇(DNP),二硝基乙二醇(EGDN),二乙二醇二硝酸酯(Di-EGDN),三乙二醇二硝酸酯(Tri-EGDN)和四乙二醇二硝酸酯(Tetra-EGDN)的NO2催化反应和夺氢反应的的能垒(ΔE≠)、焓(ΔH)和吉布斯自由能(ΔG),发现硝酸酯的夺氢反应的能垒低于NO2催化自分解反应 (见表1),这表明夺氢反应更易于发生。

表1 NO2催化硝酸酯自分解的能垒硝酸酯的夺氢反应的能垒
目前硝酸酯的反应动力学相关研究也比较多,并且取得了一定的成果。姚子云等[78]发现硝化甘油在压力下的热分解反应可以用自催化动力学方程来描述,即式(1),并且提出硝化甘油的热分解存在两种并行的反应,自身的热分解反应和NO2自催化的硝酸酯分解反应。
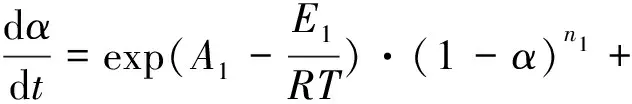
(1)
SUN等[33]使用DFT计算方法对硝酸酯的分解机理进行了计算,分别模拟了乙基硝酸酯(EN)、异丙基硝酸酯(IPN)、丙基硝酸酯(NPN)、硝酸异戊酯(EHN)及丁三醇三硝酸酯(BTTN)五种硝酸酯在NO2存在和无NO2存在的条件下的分解,并计算了热力学数据和反应常数k,计算结果表明有NO2存在的条件下硝酸酯分解活化能降低了11.82~17.86 kJ·mol-1的能量(见表2),这表明NO2会催化硝酸酯的分解。

表2 五种硝酸酯在有NO2催化(Ea)和无NO2催化(ΔE1)分解的活化能
从上述的研究中可以初步得出硝酸酯分解遵守阿伦尼乌斯方程,分解的第一步均为O—NO2键的断裂,生成大量的氮氧自由基,氮氧自由基对硝酸酯的分解产生催化作用,NO2使硝酸酯键的分解能垒降低了11.82~17.86 kJ·mol-1[33]。自催化分解反应中氮氧自由基会和硝酸酯同时发生α位和β位的夺氢反应,其中α位的夺氢反应更为迅速[79]。
综上所述,国内外针对硝酸酯的热分解研究大多采用非等温方法,且研究对象均为在高温条件下的集中放热分解过程,与硝酸酯增塑的固体推进剂贮存及使用的环境温度(-55~80 ℃)未形成良好的对应关系,并且未涉及硝酸酯使用温度下的分解产物组成、等温分解速率等。因此,已有的硝酸酯热分解历程及机理的研究成果难以对其热安定机制研究起到有效的指导作用,仍需开展使用工况条件下等温分解历程、分解速率、分解产物组成等研究工作。
2.2 硝酸酯的热安定机理
国内外在常用的化学安定剂对硝酸酯的热安定机理方面的研究较少[13, 14, 19, 20, 22, 23, 33, 38, 43, 76, 83, 86]。曾秀琳团队[23]对化学安定剂的分子性质进行了计算。唐秋凡团队[20, 43]、SUN团队[33]、SUN团队[76, 83]对苯胺、苯脲类和苯酚类安定剂与氮氧化物的反应历程等进行了量化计算,提出了部分安定剂的反应机理。VENTER团队[38]、LINDBLOM团队[22]报道了DPA的安定产物二硝基二苯胺等。牛加新团队[19]、LUO团队[86]、国外LUSSIER团队[13-14]等对苯脲类、苯胺类安定剂的反应历程进行了研究,得到部分安定剂与氮氧化物反应过程的活化能、过渡态产物,推断了反应历程。
2.2.1 苯胺类安定剂
苯胺类安定剂的安定反应涉及两个反应,即硝化和亚硝化[13, 19, 20, 22, 23, 33, 38, 43, 76, 83, 86]。以DPA为例,研究发现NO和DPA不发生反应[20],因此在安定反应中DPA的反应试剂是硝酸酯分解产生的NO2。LUSSIER等[13]研究发现NO2和DPA会发生两种反应,即N-亚硝化和C-硝化。N-亚硝化反应生成亚硝基二苯基胺(N-NO-DPA),这是消耗DPA的主反应;C-硝化反应生成N-(2-硝基苯基)苯胺(2-NO2-DPA)和N-(4-硝基苯基)苯胺(4-NO2-DPA)。这三个反应是并行反应(图5)。在这三种反应中N-亚硝化是最易发生的反应。
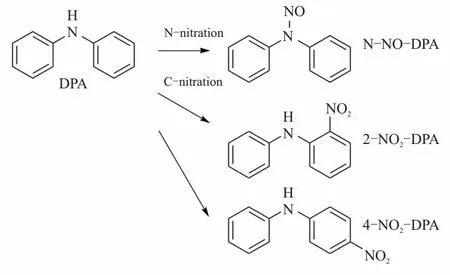
图5 DPA和NO2反应的C-硝化和N-亚硝化机理
LUO等[21]通过等温热分解动力学研究了四种苯胺安定剂(MNA、N-乙基-对硝基苯胺(ENA)、N-异丙基-4-硝基苯胺(i-PNA)、N-正丁基-4-硝基苯胺(n-BNA))对硝化棉(NC)热分解的影响,采用阿伦尼乌斯(Arrhenius)方程和模型拟合法评价了安定剂对NC等温热分解动力学的影响,采用贝特洛(Berthelot)方程估算了稳定剂对NC储存时间的影响,得出MNA的安定性最佳。
SUN等[33]在(U)B3LYP/6-31G**的基组水平上对NO2和苯胺类安定剂反应活化能进行了计算,发现同一种安定剂和NO2反应中,NO2的O进攻安定剂的活化能小于NO2的N进攻安定剂的活化能(2~16 kJ/mol),并且提出安定剂通过消耗NO2来抑制硝酸酯的自催化反应(见图6)。
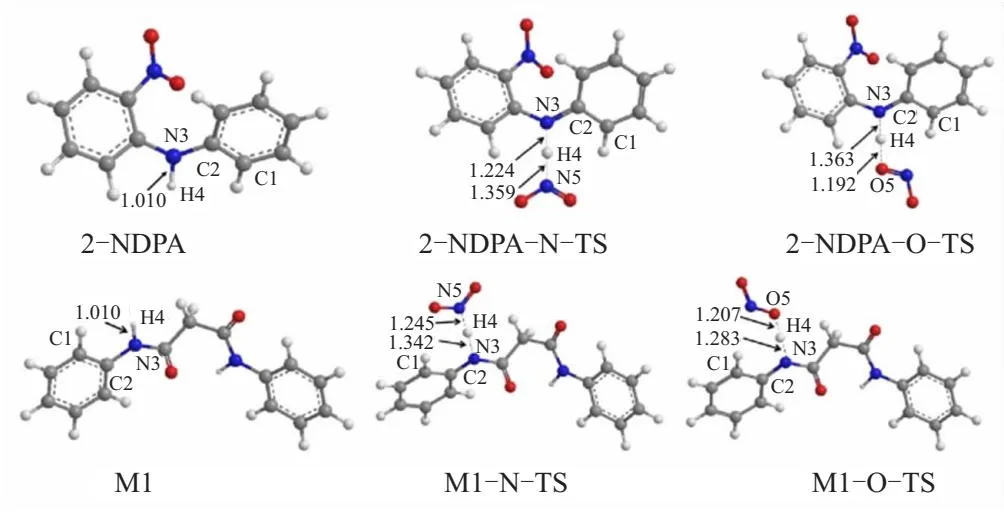
图6 NO2进攻安定剂2-NDPA的O进攻途径和N进攻途径的过渡态
SUN等[83]在B3LYP/6-31G**的基组水平上计算12种安定剂(苯胺(PA)、二苯胺(DPA)、对氨基苯酚(p-HPA)、对甲氨基苯酚(p-MAP)、间甲氨基苯酚(m-MAP)、邻甲氨基苯酚(o-MAP)、4-硝基二苯胺(4-NDPA)、对羟基二苯胺(p-HDPA)、2-(甲基氨基)-5-硝基苯酚(o-HMN)、5-(甲基氨基)-2-硝基苯酚(m-HMN)、2-(甲基氨基)-5-亚硝基苯酚(o-HAN)、5-(甲基氨基)-2-亚硝基苯酚(m-HAN))和NO2的双分子反应的活化能,同样发现NO2的O进攻安定剂途径的能垒低于NO2的N进攻安定剂途径的能垒(图7),说明了NO2和安定剂的反应的O途径更容易发生,同时也说明了在安定剂中引入给电子基团有利于安定剂吸收NO2。
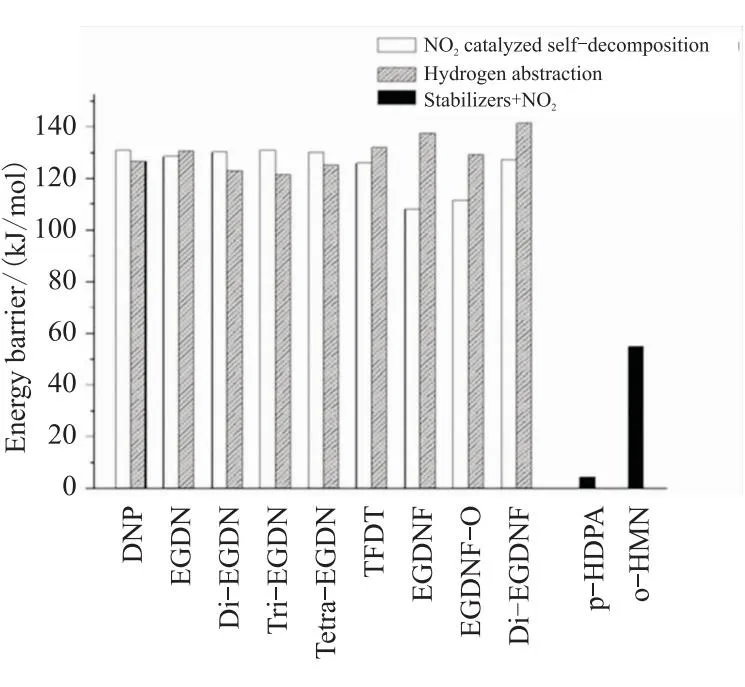
图7 硝酸酯和安定剂与NO2反应的能垒对比图
唐秋凡等[20]提出了苯胺类安定剂的安定反应的反应历程:NO2夺取安定剂氨基N上的H,生成自由基和HNO2;HNO2分解产生NO和NO2;硝酸酯分解产生的NO和HNO2分解产生的NO与自由基结合生成亚硝基产物(如图8)。
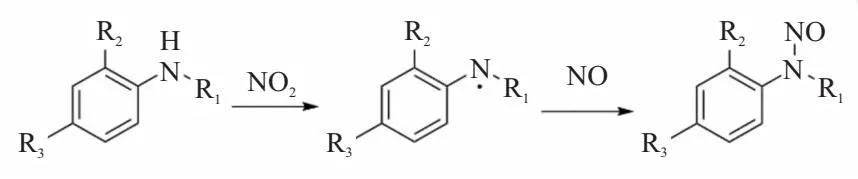
图8 苯胺类安定剂安定机理
唐秋凡等[43, 61]设计并合成了5种新型安定剂(N-乙基-对硝基苯胺(ENA)、N-正丙基-对硝基苯胺(n-PNA)、N-异丙基-对硝基苯胺 (i-PNA)、N-正丁基-对硝基苯胺(n-BNA)和N-叔丁基-对硝基苯胺(t-BNA)),并基于密度泛函理论(DFT)中的B3LYP方法在6-31g(d)基组水平上对不同安定剂(ENA、n-PNA、i-PNA、n-BNA、t-BNA)与氮氧化物(NO2和NO)反应过程中的分子结构(包括反应物、过渡态和产物)进行了计算(见图9)。理论分析结果表明,在五种新的安定剂中,n-BNA 是最有潜力的安定剂。将n-BNA应用于典型改性双基推进剂中进行了实验验证,结果表明,n-BNA和NG相容性良好,加入n-BNA组分的推进剂的120 ℃甲基紫实验变色时间长达98 min,90 ℃真空放气量0.74 mL/g,相比于C2和Res作为安定剂的实验结果(120 ℃甲基紫变色时间51 min,真空放气量 1.72 mL/g),推进剂的热安定性得到明显提高。

图9 在B3LYP/6-31G(d)水平下计算的安定剂n-BNA与氮氧化物反应过渡态图
2.2.2 苯脲类安定剂
相比于苯胺类安定剂,苯脲类安定剂的安定机理更为复杂[14, 19, 20, 23, 33],但目前尚无完整的机理提出。以AK-Ⅱ为例,一种可能的AK-Ⅱ与氮氧化物反应的反应机理如图10[14]。最先发生的是N-硝化,然后发生C-硝化,其中N—NO键不稳定,易发生脱硝反应,最后生成单硝基化合物。

图10 AK-Ⅱ的安定机理
苯胺类安定剂常用的还有乙基中定剂,乙基中定剂和氮氧化物反应有两条可能路径[87]:一是发生硝化反应,氮氧化物加成到苯环上;二是中定剂发生脲键的断裂,形成单芳族衍生物,以亚硝基铵离子作为中间体,如图11所示。

图11 乙基中定剂的安定机理
LUSSIER等[14]采用高效液相色谱的方法对AK-II和NO2的反应产物进行了分离,发现共有五种衍生物,如图12(峰1为1-(甲基氨基)-N-(2-硝基苯基)-N-苯基甲烷酰胺(2-NO2-AK-II),峰2为 1-(甲基氨基)-N-(4-硝基苯基)-N-苯基甲烷酰胺(4-NO2-AK-II), 峰3为2-甲基-4-(2-硝基苯基)-1-氧亚基-4-苯基氨基脲(N-NO-2-NO2-AK-II),峰4为2-甲基-1-氧亚基-4,4-二苯基氨基脲(N-NO-AK-II),峰5为2-甲基-4-(4-硝基苯基)-1-氧亚基-4-苯基氨基脲(N-NO-4-NO2-AK-II))。在五种产物中N-NO-AK-II第一个产生,在其达到最大值后,其他产物才开始生成,如图13。根据色谱分析,AK-II的单硝基取代衍生物可能是N-NO-单硝基取代衍生物脱硝得到的。

图12 AK-Ⅱ和150 ml NO2反应后的液相色谱图

图13 AK-Ⅱ和其反应产物的色谱峰强度随NO2加入量的分布
丁黎等[24]采用B3LYP方法在6-31g(d)基组水平上,比较了C2和AK-Ⅱ上羰基结合质子的能力,结果表明C2结合质子的能力弱于AK-Ⅱ。同时95 ℃的热减量实验表明,AK-Ⅱ吸收硝酸酯分解产物的能力优于C2,即AK-Ⅱ对硝酸酯的安定能力比C2更强。同时发现,安定剂和硝酸酯之间存在明显的相互作用,安定剂的亲核能力越强,硝酸酯键越易被破坏,因此选择安定剂也要考虑安定剂和硝酸酯的相互作用。
3 结束语
国内外在硝酸酯的热分解、热安定性等方面已经开展了大量的研究工作,得到了系列研究成果,对硝酸酯的合成和应用以及固体推进剂的研究工作起到了非常积极的促进作用。
硝酸酯的热分解研究大多集中于非等温条件下硝酸酯高温快速分解热行为和动力学的阐释,得到硝酸酯的部分分解机理——硝酸酯键的断裂和硝酸酯的自催化反应。当前对其在实际工况条件下的等温热分解历程,分解速率、分解产物构成等方面研究不足,需要进一步开展研究。
硝酸酯的热安定性的研究大多集中于安定剂的安定效果及与氮氧化物安定反应历程的推断。根据目前对安定机理的研究结果推测,苯胺和苯脲型的安定剂的安定机理的初步反应是二氧化氮和安定剂中的氨基上的氢发生夺氢反应生成HNO2。目前对安定剂与不同氮氧自由基、氮氧化物气体、酸、醛产物的反应速率、反应活化能等量化表达以及安定剂和硝酸酯的定量配比关系研究不足,无法有效指导目前硝酸酯的新型安定剂的设计、固体推进剂安定剂的优选和复配使用。
针对当前拓宽硝酸酯增塑的固体推进剂使用温度范围的迫切需求(硝酸酯增塑的固体推进剂可靠工作温度上限提高至80 ℃),急需开展如下工作:
(1)使用温度条件下典型硝酸酯的等温分解历程、分解速率、分解产物构成研究;使用温度条件下混合硝酸酯的等温分解历程、分解速率、分解产物构成研究。
(2)针对硝酸酯的热分解,典型安定剂安定反应的历程、速率和安定剂的复配效应等安定机制研究,以及安定剂吸收硝酸酯分解产物过程的机理性研究。
