显微镜下去血管化技术切除颈动脉体瘤20例临床分析
2024-01-11宜若男岳波张昌明乔燕查定军
宜若男,岳波,张昌明,乔燕,查定军
(空军军医大学西京医院 耳鼻咽喉头颈外科,陕西 西安 710032)
颈动脉体瘤(carotid body tumor,CBT)一种化学肿瘤,是源自神经嵴外胚层细胞的最常见的副神经节瘤类型[1]。这是一种罕见的颈部肿瘤,占头颈部副神经节瘤的60%~70%[2],位于颈总动脉分叉处[3]。CBT是良性肿瘤,发病率低、生长缓慢、癌变率低,与年龄无关[4-5]。本研究主要将我科2016年8月—2022年5月收治的CBT患者的临床资料进行分析总结,并探讨CBT的临床特点、诊断、治疗及术后并发症。
1 资料与方法
1.1 一般资料
收集20例CBT患者,其中男5例,女15例;年龄18~67岁,平均年龄为46岁。肿瘤位于左侧11例,右侧7例,双侧均有肿瘤2例;病程最短为1个月,最长为7年;肿瘤最小为2.0 cm×2.0 cm×1.5 cm,最大为5.5 cm×6.0 cm×4.0 cm;临床表现为发现颈部包块18例,不能负重1例,颈部胀痛感1例; Shamblin分型:Ⅰ型15例,Ⅱ型3例,Ⅲ型2例。
1.2 诊断方法
20例患者采用颈部B超、CT、MRI和DSA专科检查。CBT患者B超的特点:低回声为主,无包膜,边界清除,形态比较规则,包绕颈动脉分叉平面,使颈内外动脉夹角增大,起始部距离增大,肿块内部有丰富的血流信号[6]。CBT患者CT的影像学显示肿瘤位于颈动脉间隙,轮廓清晰,无钙化,血供非常丰富;增强扫描明显强化,动脉期比较明显,与周围动脉的密度相似。CBT患者MRI影像学特点[7]为“椒-盐征”,即T1WI上所见为点片状等或稍高信号,T2WI所见不均匀高信号,“椒”代表快血流的血管流空信号,“盐”代表亚急性期出血或慢血流所致的高信号,后者少见,因此在瘤体内多见到血管流空信号。CBT患者DSA图像显示颈总动脉分叉,肿瘤压迫下颈内外动脉移位。可以清楚地显示供应肿瘤的血管。
1.3 手术治疗
20例患者CBT患者均在显微镜下切除,其中15例患者采用的手术方式为单纯瘤体切除术;3例患者伴有颈部淋巴结肿大,采用的手术方式为瘤体切除术+颈部淋巴结清扫术;1例患者采用的手术方式为瘤体切除术+颈外动脉结扎术,此例患者因压迫颈总动脉可致晕厥,在家属的看护下回家进行Metas训练,训练1个月后持续压迫颈总动脉无不适症状后行手术治疗;1例患者术中可见瘤体质坚硬,完全包绕颈总动脉、颈内动脉、颈外动脉、颈内静脉,并粘连紧密,术中难以完全分离,取粘连部位处组织和迷走神经近心端周围组织送冷冻快速病理检查,回报考虑CBT,考虑恶性肿瘤,如果继续切除肿瘤极易造成大血管破裂出血危及生命,建议手术结束,根据术后病理检查可考虑辅助放疗,与家属沟通后同意结束手术。
20例患者根据肿瘤的位置,沿颈部皮纹做一弧形切口,游离颈阔肌皮瓣,暴露颈鞘,注意保护瘤体周围的血管及神经,显露肿物,当肿物显露时在显微镜下双极射频凝闭瘤体表面的微血管,用组织剪、显微弹簧剪完整剥离肿物,我们将其称之为去血管化技术(图4)。
2 结果
2.1 颈部专科辅助检查的诊断率
2.1.1 颈部超声 20例患者中,19例患者查颈部超声,1例未查,此患者查颈部CT及MRI。在19例查超声的患者中5例未诊断CBT,其余均诊断为CBT,诊断率为74%。
2.1.2 颈部CT 20例患者中,19例患者查颈部CT,1例未查,此患者查颈部超声、MRI及DSA。在19例查超声的患者中1例未诊断CBT,其余均诊断为CBT,诊断率为95%。见图1。
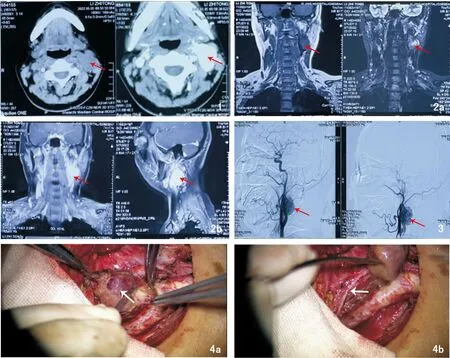
图1 颈部CT,箭头所指为CBT 图2 颈部MRI,箭头所指为CBT 2a:平扫; 2b:增强 图3 DSA检查,箭头所指为CBT 图4 显微镜下去血管化技术切除肿瘤 4a:箭头所指为肿瘤; 4b:箭头所指为迷走神经
2.1.3 颈部MRI 20例患者中,10例患者查颈部MRI,10例未查,此10例患者查颈部超声和/或CT和/或DSA。在10例查MRI的患者中1例未诊断CBT,其余均诊断为CBT,诊断率为90%。见图2。
2.1.4 DSA检查 20例患者中,11例患者查DSA,9例未查,此9例患者查颈部超声和/或CT和/或MRI。在11例查超声的患者均诊断为CBT,诊断率为100%。见图3。
2.2 术后并发症及随访
20例CBT患者术后有4例出现声音嘶哑,1例出现吞咽困难,1例出现饮水呛咳,4例出现伸舌偏斜,术后出现并发症可能与术中牵拉导致迷走神经、舌下神经水肿所致。经随访后,4例患者声嘶均好转,1例患者吞咽困难好转,1例患者饮水呛咳好转,3例患者伸舌偏斜好转,1例患者伸舌偏斜无好转,1例患者后期出现抬肩困难,可能是因为术中导致副神经损伤。1例患者术中未完全切除肿瘤,术中取组织送冷冻快速病理检查回报考虑恶性CBT,随访2年后,一般情况可,继续密切随访。
3 典型病例
患者,女,49岁,以“左侧颈部胀痛感7年”为主诉入院。伴有左耳疼痛及听力下降。患者既往有糖尿病,高血压。查体:左侧颈部可触及直径约4 cm质韧肿物,可触及搏动感,表面无红肿及破溃。查MRI提示左侧颞骨及左侧颈血管鞘肿块影。入院诊断为:①CBT(左);②颈静脉孔区副神经节瘤(左)。拟行手术方式为颞下窝A型径路左侧颈静脉孔区及左侧颈部肿物切除术、外耳道封闭,面神经移位、颈部血管解剖,腹部取脂肪术腔填塞,备耳大神经移植面神经修复术,颈内静脉结扎术,右侧颈部肿物切除术。但由于术中术中可见瘤体质坚硬,完全包绕颈总动脉、颈内动脉、颈外动脉、颈内静脉,并粘连紧密,术中难以完全分离,取粘连部位处组织和迷走神经近心端周围组织送冷冻快速病理检查,回报考虑恶性CBT,如果继续切除肿瘤极易造成大血管破裂出血危及生命,建议手术结束,根据术后病理可考虑放疗,与家属沟通后同意结束手术。术后随访至今,患者一般情况可,密切随访中。
4 讨论
4.1 CBT的临床表现
CBT于1743年首次被描述和报道[8],从血管瘤组织生长和演变而来的[9],是一种罕见的化学感受器肿瘤。其中大多数为良性和单侧,恶性约占2%~8%[10],30~40岁人群多发,女性的发病率略高于男性[11]。CBT的病因不清,有文献报道高海拔地区长期慢性缺氧暴露可能与该病有关[12],也有可能与基因突变有关,雌激素是加速CBT形成的重要因素。但是在陈飞等[13]的研究中,23例(29侧)CBT患者,只有2例患者有高海拔生活史。CBT位于颈动脉分叉,毗邻颈总动脉、颈内动脉、迷走神经、舌下神经和喉返神经等许多重要血管和神经,在手术过程中严重干扰脑组织的血液供应,术中和术后都可导致严重并发症[14-15]。CBT主要的临床症状表现为颈部肿块,多数无症状,当肿块增大压迫到周围的神经血管、或侵犯到颅底压迫到后组脑神经时引起相应的症状,比如声音嘶哑、吞咽困难、伸舌偏斜、眩晕及Adams-Stokes综合征[16]。约3%的CBT患者与颈动脉窦综合征有关,颈动脉窦综合征是由肿瘤压迫颈动脉体引起的颈动脉窦过敏反应[17]。主要表现为心功能抑制、心跳突然缓慢、血压下降,导致脑缺血缺氧和昏厥[18]。
4.2 CBT的分型
临床上,CBT可分为以下两种类型:家族型(6.5%),多为双侧;散发型,主要是单侧[19]。Shamblin等[20]将CBT分为3类:Ⅰ级,肿瘤局限于颈动脉分叉,不粘附在颈内外动脉壁上;Ⅱ级,肿瘤延伸至颈动脉分叉以下,部分包裹颈动脉分叉处的血管,粘附颈内外动脉壁;Ⅲ级,肿瘤完全包裹颈动脉及颈动脉分叉处,紧贴颈动脉。以上分型有助于手术方案的选择。
4.3 CBT的影像学检查
超声可作为CBT初步筛查检查,可清晰反映肿瘤和颈动脉的血液供应、大小和位置,有助于诊断,但很难显示肿瘤和血管之间的关系[21]。颈部CT有助于确定CBT的大小和范围以及肿瘤与周围组织结构之间的关系[22]。MRI具有很高的组织分辨率能力,可以清楚地显示肿瘤的大小,形态,范围和位置,可以直观地显示肿瘤与血管之间的关系,具有很高的诊断价值[23]。DSA检查,它可以观察颈动脉的变化,定位肿瘤,确定肿瘤的供血状态,确认肿瘤与颈动脉之间的位置关系。它可以显示双侧脑动脉的交通量,并清楚地显示Willis环的侧支循环,这是CBT的确切诊断方法之一[24]。
4.4 CBT的治疗
4.4.1 显微镜下去血管化技术的应用 显微镜下去血管化技术是手术切除CBT的有效安全切除方法。显微镜下可以更清楚的辨别血管及神经,双极可以精准射频凝闭瘤体表面的微血管,可以避免损伤重要血管及神经。
4.4.2 常规CBT的治疗 CBT的首选治疗方案尽早手术[25],以防止肿瘤进展,避免侵犯邻近神经或血管,减少术后并发症,术中应当保护颈动脉,血压应保持稳定,以确保一定的颅内灌注压,预防脑缺血。手术主要分为以下几种方式[26]:①单纯瘤体切除术,适合瘤体较小的Shambin Ⅰ型CBT患者以及血管形态良好的Shambin Ⅱ型、Ⅲ型CBT患者,在术前准备充分的前提下也可考虑此方法;②瘤体切除+颈外动脉结扎术,适用于血管比较丰富的Shambin Ⅰ型、Ⅱ型CBT患者;③瘤体切除+颈动脉重建术,适合与血管壁粘连紧密,血液灌流量较高的Shambin Ⅱ型、Ⅲ型CBT;④瘤体切除+颈内、颈总动脉结扎术,患者患侧血管重建比较困难,对侧脑侧支循坏代偿较好,可采用此方法[25],但是结扎颈内动脉可导致偏瘫、甚至危及生命,术前准备应当充分。有研究[27]表明术前栓塞可以减少术中出血量,但是也有研究[28]表明术前栓塞对手术并没有多大的作用。而且血管栓塞术如果栓子返流会误栓颈内动脉等导致严重并发症[29]。所以目前对CBT术前栓塞无一致的认识。
4.4.3 特殊CBT的治疗 对于恶性CBT,手术切除肿瘤仍然是首选治疗方法[25]。对于发生颈部淋巴结转移的恶性CBT,原发部位仍可选手术切除,同时可行区域性淋巴结清扫,如果发生全身转移,手术切除已不适用,可以考虑放疗。对于双侧CBT患者的治疗方案目前存在争议,有学者[30]建议先做瘤体较大一侧,择期形瘤体较小的一侧,如果两侧同时手术,如果损伤双侧喉返神经,可能导致窒息。有文献报道[31]11.8%的CBT患者可局部切除,但是局部控制率为69%。放疗可终止CBT的进展,其原理是通过诱发闭塞性动脉炎引起血管纤维化。以下情况患者可以考虑放疗[32]:①全身基础疾病较大并且不适于手术的老年患者;②瘤体比较大,无法完整切除,并且靠近颅底;③术后复发或已发生远处转移的CBT。
4.5 术后并发及预防
CBT术后最常见的并发症为出血,双极电刀的使用可以减少出血,出血较多可以考虑输血治疗。CBT最严重的并发症为缺血性脑卒中,术前应当准备充分,了解Willis环情况以及对侧脑代偿供血情况, 并进行Matas训练;术中应当尽量减少血管损伤, 术中阻断颈动脉时间尽量短,麻醉应将血压控制在适当范围, 围手术期注意保持血流动力学的平稳, 适当使用抗凝药物、扩张脑血管药物[33-34]。CBT最主要的并发症是脑神经损伤,有文献报神经损伤率高达20%~40%[35],最常见的神经损伤是迷走神经和舌下神经,术中应当仔细识别并进行保护,避免过度牵拉及钳夹。双侧CBT患者在切除双侧肿瘤术后,同时双侧颈动脉压力感受器失去血压调节的功能时,可出现压力感受器衰竭综合征。其治疗的主要目的是防止血流动学不稳定引起的并发症,目前治疗压力感受器衰竭综合征的首选药物是可乐定。
5 总结
CBT是临床上比较罕见的疾病,术前诊断主要依靠B超、CT、MRI、DSA,确诊以后手术治疗为首选方案,显微镜下去血管化技术是一种有效安全的切除方法,根据CBT的分型应当制定合理的手术方案,并为术中、术后发的并发症制定出合理的解决措施。
