星状风毛菊药材分析及质量标准研究
2024-01-05马家麟乔亚玲杲秀珍李玉林
马家麟 ,王 硕 ,陈 涛 ,宋 霞 ,乔亚玲 ,杲秀珍 ,申 诚 ,海 平 ,李玉林
(1.中国科学院西北高原生物研究所,青海 西宁 810001;2.青海省药品检验检测院 中药(藏药)质量控制重点实验室,青海省中药(藏药)现代化研究重点实验室,青海 西宁 810016)
星状风毛菊为菊科凤毛菊属植物星状风毛菊(Saussurea stellaMaxim.)的干燥全草,又名星状雪兔子,藏文名为“苏尔公玛保”[1-2],主要分布于青海、西藏、甘肃、四川、云南省及自治区,生长于海拔2 500~5 400 m 的高山草甸、河边或沼泽草地.星状风毛菊是藏区较常用的藏药材,性味苦,微寒,具有清热利湿、解毒、接骨、消炎止血的功效,主要用于治疗中毒性热症、跌打损伤、骨折、创伤化脓等症状[3-5].
在《青海植物志》中对星状风毛菊仅载有形态和资源分布,文献调研仅有少量关于其理化鉴别项、化学成分研究,究其原因是相关基础研究较少,缺乏质控指标,难以制订完善的质量标准,严重影响星状风毛菊药材的开发利用.因此,本研究以星状风毛菊为对象,通过对药材性状、粉末显微特征、薄层色谱鉴别、检查(水分、灰分、醇溶性浸出物)和含量测定5 项内容进行深入研究,找到检验该药材的专属性方法,制定合理的限度,对星状风毛菊药材质量进行有效的控制提供方法和依据.
1 试验部分
1.1 仪器与试剂
梅特勒-托利多AG135 精密电子天平(梅特勒-托利多仪器上海有限公司);CAMAG 薄层点样和成像系统(瑞士卡玛公司);Shimadzu LC-2030C 高效液相色谱仪(日本岛津公司);PDA 检测器(日本岛津公司);Axio IMAGE Z2 光学显微镜(德国ZISSI公司);DZKW-4 电子恒温水浴锅(北京中兴伟业);SX2-4-10 马弗炉(上海实验仪器厂).
星状风毛菊来自青海、四川省,样品信息如表1所列.经中国科学院西北高原生物研究所孙菁研究员鉴定11 批样品均为菊科凤毛菊属植物星状风毛菊Saussurea stellaMaxim.干燥全草.绿原酸对照品(中国食品药品检定研究院,批号:110753-202018);硅胶G 薄层板(上海麦克林);甲醇为色谱纯(市售);其余试剂为分析纯(市售);水为超纯水.

表1 星状风毛菊药材采集信息Table 1 Sample collection informations of Saussurea stella Maxim.
1.2 薄层鉴别
对照品溶液配制:精密称取绿原酸对照品10.0 mg,置于10 mL 容量瓶中,加甲醇超声溶解后定容,即得对照品溶液(1.0 mg/mL).
供试品溶液配制:取本品粉末约1.0 g,加50%乙醇50 mL 置于热水浴中热回流1 h,过滤,滤液减压浓缩蒸干,精密加入5 mL 甲醇溶解即得.
在室温、相对湿度70%条件下,依照《中华人民共和国药典》四部2020 年版通则0502[6]薄层色谱法,分别量取对照品溶液及供试品溶液5 µL,点于同一硅胶G 薄层板上,以乙酸乙酯-丙酮-甲酸-水(体积比10∶6∶1∶2)为展开剂展开,取出晾干后,喷以含1%亚硝酸钠的甲醇溶液,105 ℃加热至斑点显色清晰,日光下检视.
1.3 水分、总灰分、浸出物检查
精密称定各批次星状风毛菊药材粉末2.0 g,平行试验2 份,依照《中华人民共和国药典》四部2020 年版通则0832[6]烘干法测定11 批药材水分;依照2302 总灰分测定法测定11 批药材总灰分;依照2201 热浸法,以45%乙醇为溶剂测定11 批药材浸出物含量.
1.4 绿原酸含量测定
1.4.1 色谱条件
色谱柱:Shim-pack GIST C18(4.5 mm×260 mm,5 µm);流动相:甲醇为A 相,0.1%乙酸-水为B 相;分离条件:A∶B(体积比为25∶75);流速:1.0 mL/min;检测波长:326 nm;柱温:30 ℃;进样量:10 µL.
1.4.2 对照品溶液配制
精密称取绿原酸对照品10.0 mg,置于10 mL容量瓶中,加甲醇超声溶解后定容,即得对照品储备液(1.0 mg/mL).
1.4.3 供试品溶液配制
精密称定本品粉末(过5 号筛)1.0 g,置于具塞锥形瓶,精密加入50%乙醇50 mL,称定重量,置于水浴中加热回流1 h,放冷,再称定重量,用50%乙醇补足减失的重量,摇匀,过0.45 µm 滤膜后待测.
2 结果与讨论
2.1 定性鉴别
2.1.1 性状鉴别
星状风毛菊原植物及药材性状如图1 所示.药材根圆柱形,表皮黄褐色,断面灰白色,有少量须根.几乎无茎,叶皱缩,呈褐色,完整叶呈披针形,叶基部紫红色,无毛.头状花序呈紫红色,在莲座状叶丛中密集成半球形.瘦果,表面黑色.冠毛淡褐色,外层较短,糙毛状,长约0.3~0.6 cm,内层羽毛状,长约0.8~1.3 cm.花果期为每年7~9 月.气微,味微苦.

图1 星状风毛菊性状鉴别图(a)原植物形态,(b)药材性状Fig.1 Photos of Saussurea stella Maxim.(a) original plant morphology, (b) medicinal materials properties
2.1.2 显微鉴别
通过光学显微镜,观察星状风毛菊药材粉末样品的结构特征,其显微特征如图2 所示.由图2 可见,本品粉末呈棕褐色.花粉粒呈椭圆形或圆球形,外壁有短刺及疣状雕纹,萌发孔3 个.导管短,多为环纹.非腺毛,单细胞.纤维成束,壁平直,含有草酸钙方晶.木栓细胞较多,呈类长方形.淀粉团充满细小淀粉粒.长管道状分泌细胞,细胞内充满棕色物.表皮细胞呈长方形或多角形,均有气孔.
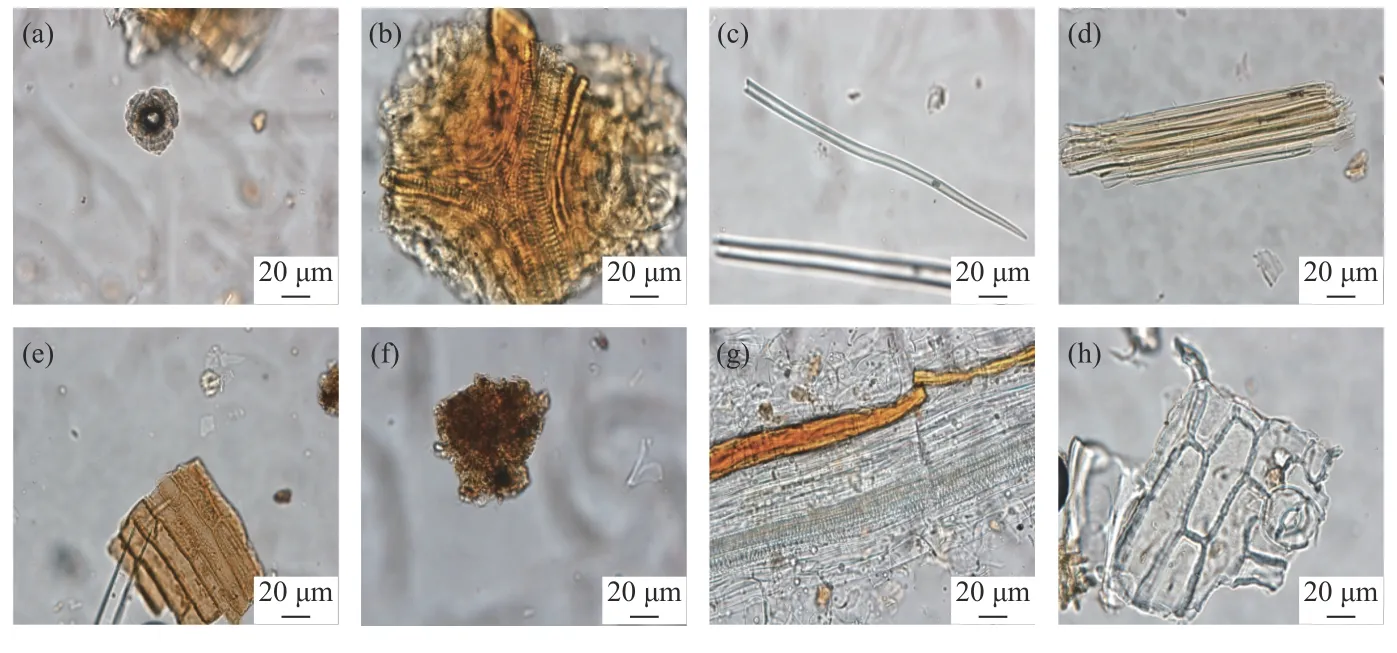
图2 星状风毛菊显微特征图(a)花粉粒,(b)环纹导管,(c)非腺毛,(d)纤维束,(e)木栓细胞,(f)淀粉团,(g)长管道状分泌细胞,(h)表皮细胞Fig.2 Microscopic characteristics images of Saussurea stella Maxim.(a) pollen grain, (b) annular vessel, (c) non-glandular hair, (d) fiber bundle, (e) cork cell, (f) starch granule,(g) secretory cell, (h) epidermal cell
2.1.3 薄层鉴别
按1.2 项下薄层鉴别方法进行分析,其结果如图3 所示.可见供试品、绿原酸对照品色谱相应的位置上,显相同的黄色斑点,且分离度高.

图3 星状风毛菊TLC 鉴别图谱(S1~S11)供试品,(A)绿原酸对照品Fig.3 TLC identification of Saussurea stella Maxim.(S1~S11) test samples, (A) reference substance of chlorogenic acid
2.2 水分、灰分、浸出物测定
本试验分别按照《中华人民共和国药典》2020年版[6]水溶性浸出物、醇溶性(45%、稀乙醇、70%)浸出物测定法项下的冷浸法、热浸法(附录XA)测定浸出物.相比于冷浸法,热浸法测定星状风毛菊浸出物效果更佳,因此采用热浸法提取.最终试验结果表明,浸出物含量:45%乙醇浸出物>水溶性浸出物>稀乙醇浸出物>70%乙醇浸出物.因此采用醇溶性浸出物测定法项下的热浸法测定药材浸出物.
11 批药材水分、灰分、浸出物测定结果如表2所列.根据测定结果并结合《中华人民共和国药典》2020 年版中药材的标准,水分、总灰分均以平均值的120%设限,浸出物以平均值的80%设限,拟定星状风毛菊药材水分含量不得大于10.0%,灰分含有量均不得大于11.0%,醇溶性浸出物含有量不得小于16.0%.

表2 星状风毛菊水分、灰分、浸出物和绿原酸含量测定结果Table 2 Determination results of water content, total ash,ethanol soluble extractives and chlorogenic acid/(%,n=2)
2.3 绿原酸含量测定
2.3.1 条件优化
经文献调研,国内外针对星状风毛菊展开的研究较少,现有资料表明,星状风毛菊主要含有黄酮、黄酮醇、木质素、酚醛等多类成分[7-11],但对其主要有效成分的研究未见报道.前期研究表明,星状风毛菊全草乙醇浸提物用石油醚-乙酸乙酯-正丁醇萃取后由高效液相色谱仪(HPLC)检测显示化合物A、B 含量较高(如图4 所示),经核磁共振法鉴定以及文献对比,确定化合物A、B 分别为洋蓟素和绿原酸.现代药理学研究绿原酸具有抗菌、抗病毒、利肝胆、抗肿瘤等作用[12-13],而且对于创伤的治愈、润滑关节、防止炎症等有治疗效果[14-15],这与星状风毛菊清热利湿、解毒、接骨、消炎止血的功效相吻合.因此,本标准以绿原酸为指标成分考察星状风毛菊药材质量具有合理性.

图4 星状风毛菊正丁醇相HPLC 色谱图(A)洋蓟素,(B)绿原酸Fig.4 HPLC chromatogram of n-butanol fraction of Saussurea stella Maxim.(A) cynarin, (B) chlorogenic acid
本试验对星状风毛菊药材提取条件进行了优化,分别测试了提取溶媒(40%~80%乙醇溶液)、提取方式(冷浸法、超声提取法、加热回流法)和提取时间(30、45、60、90 min)对绿原酸提取效率的影响,试验结果如图5 所示.最终选择提取溶剂为50%乙醇,热回流提取方法,加热回流60 min 进行提取.

图5 绿原酸提取方法考察(a)提取溶剂,(b)提取方式,(c)提取时间Fig.5 Study on extraction methods of chlorogenic acid(a) extraction solutions, (b) extraction methods, (c) extraction times
2.3.2 系统适用性
精密吸取对照品溶液、供试品溶液进行测定.结果如图6 所示.结果表明,试样中绿原酸与相邻色谱峰的分离度均大于1.5,对称因子在0.95~1.05区间内,峰形对称,理论塔板数≥8 000,符合药典相关规定.

图6 HPLC 色谱图(a)对照品溶液,(b)供试品溶液,(1)绿原酸Fig.6 HPLC chromatograms(a) reference solution, (b) sample solution, (1) chlorogenic acid
2.3.3 线性关系考察
精密量取不同体积对照品溶液用甲醇稀释并配制成系列浓度对照品工作液,质量浓度分别为1.00、50.0、100、200、500 µg/mL.精密吸取对照品工作液各10 µL,注入HPLC 测定.以绿原酸质量浓度X(µg/mL)为横坐标,峰面积Y为纵坐标绘制标准曲线,得到线性回归方程为Y=307 03X−116 887(R2=0.999 6,n=6).结果表明,在1.00~500 µg/mL 范围内绿原酸质量浓度与峰面积线性关系良好.
2.3.4 精密度试验
精密吸取1.4.2 项下对照品溶液10 µL,注入HPLC 中测定,连续进样6 次.测得绿原酸峰面积的相对标准偏差(RSD)为0.12%(n=6),表明仪器精密度良好.
2.3.5 重复性试验
取样品粉末(S11)6 份,按1.4.3 项下方法配制供试品溶液,测得供试品溶液中绿原酸含量均值为1.34%,RSD 为0.15%(n=6),表明该方法重复性良好.
2.3.6 稳定性试验
取同一份供试品溶液(S11)置于室温,分别在0、2、4、8、12、24 h 进行测定,绿原酸峰面积RSD 为0.19%(n=6),表明供试品溶液在24 h 内稳定.
2.3.7 加样回收试验
采用加样回收法,精密称定已知含量的星状风毛菊药材粉末(S11)0.5 g,平行9 份,置具塞锥形瓶中,分别精密加入含有0.3、0.6、0.9 倍绿原酸的对照品溶液,按1.4.3 项下方法配制供试品溶液,进样测定并计算回收率.结果如表3 所列,3 个添加水平的平均回收率在97.6%~98.7%范围内,表明试验回收率良好,准确度高,符合药典要求.

表3 绿原酸的回收率Table 3 Recoveries of chlorogenic acid
2.3.8 含量测定
取11 批样品(S1~S11),按1.4.3 项下方法制备供试品溶液.精密吸取供试品溶液和对照品溶液各10 µL,按1.4.1 项下色谱条件进行测定.测定结果如表2 所列,11 批星状风毛菊中绿原酸含量的测定结果均值为0.65%,按《中华人民共和国药典》2020 年版规定将均值的80%拟为含量限度,即本品按干燥品计算,含绿原酸不低于0.50%.
3 结论
本试验通过对青海、四川省多个采样点星状风毛菊药材进行性状描述、显微鉴别及薄层色谱鉴别,可知该药材性状及显微鉴别特征较为明显,薄层色谱图斑点清晰,分离度高,可作为星状风毛菊药材定性鉴别的依据.通过对星状风毛菊药材水分、灰分及浸出物测定,初步确定各项限量.通过所建立的绿原酸含量测定方法,初步确定星状风毛菊药材指标性化学成分及限量要求,为民族药星状风毛菊药材质量标准的制定及进一步开发利用奠定基础.
