菊甘蓝多糖片的制备工艺及含量测定方法研究
2024-01-04朱鹤云吉林医药学院药学院吉林吉林132013
桑 野,关 皎,潘 旭,朱鹤云,冯 波 (吉林医药学院药学院,吉林 吉林 132013)
糖尿病和高血脂是临床十分常见的疾病,这些疾病会引发多种疾病症状与体征,从而对人体健康造成不同程度的损害[1]。随着时代的发展和进步,人们的健康意识不断增强,开始从治疗疾病向预防疾病转变,这一时代背景极大地促进了保健品行业的发展。植物多糖具有较多的生物功能,例如增强人体免疫力、降低血糖、促进造血、抗利尿、抗衰老、抗菌抗炎、抗肿瘤等[2-3]。研究表明,菊芋多糖具有降糖、抗氧化等作用[4-5];绞股蓝多糖具有抗炎、抗肿瘤、降血压、降血脂、降血糖、抗衰老、抑制血栓形成等作用[6];甘草为药食两用物品,其多糖具有抗氧化、降血糖等作用[7-8]。以上述植物多糖为基础,制备了具有降糖、降脂作用的多糖片剂,具有方便运输、储藏、便于携带、服用方便等优点。本次研究拟制备一种具有降低血糖、血脂的菊甘蓝多糖片,该片剂主要以菊芋、绞股蓝、甘草多糖为主原料,其他辅料相复配,经研磨、过筛、制粒、压片而成,并对其含量进行测定,以期为其工业化生产提供理论基础。
1 材料与方法
1.1 试剂与仪器
菊芋粗多糖、绞股蓝粗多糖、甘草粗多糖(实验室自制);硬脂酸镁(北京泽平科技有限责任公司);聚乙烯比咯烷酮[PVP(K30)](武汉普洛夫生物科技有限公司);羧甲基淀粉钠(CMS-Na,江苏奥福生物科技有限公司);乙醇(济南普莱华化工有限公司);微晶纤维素(山东六佳药用辅料股份有限公司);葡萄糖(江苏成谦生物科技有限公司);浓硫酸(分析纯,深圳市华亚新材料有限公司);苯酚(分析纯,山东旭晨化工科技有限公司);蒸馏水(实验室自制)。
电子天平(ME54,海圣科仪器设备有限公司),单冲式压片机(TDP-5,上海天峰制药设备有限公司),片剂四用测定仪(78X-2,天津市嘉鑫海机械设备有限公司),紫外分光光度计(UV-1800,上海昂拉仪器有限公司)。
1.2 处方筛选及优化
1.2.1 苯酚硫酸法处理
因所制片剂主要成分为多糖,而多数辅料为多糖类,为防止对主成分紫外分析产生影响,故对多种辅料进行苯酚-硫酸法处理,测定吸光度。吸光度值越小,对多糖紫外吸收影响越小,从而确定菊甘蓝多糖片剂处方中辅料组成。
1.2.2 单因素试验
通过单因素试验筛选填充剂、崩解剂、黏合剂的用量,以片剂外观、黏合度、崩解时限和硬度为评价指标,确定菊甘蓝多糖片剂最优处方。
1.3 制备工艺确定
使用普通片剂的几种常用制备方法,对苯酚硫酸法和单因素试验筛选出的辅料种类和用量进行片剂的制备,根据辅料的性质、粉体或颗粒的流动性及片剂的成型性选择最佳制备方法,并确定辅料和原料药的添加顺序。
1.4 片剂一般检查
1.4.1 片重差异检查
取3 批样品,每批抽取20 片,精密测定总重量,计算平均片重。再分别精密测定各片重量,每片重量与平均片重比较不得超出±5%,要求超出差异限度的片剂不得超过2片,并不得有1片超出限度1倍。
1.4.2 硬度检查
取3 批样品,每批抽取10 片,用片剂四用测定仪测每片硬度,要求硬度在45~55 N之间。
1.4.3 崩解时限检查
取3 批样品,每批分别抽取6 片置吊篮玻璃管中,启动片剂四用测定仪检查崩解时间,各片均应在15 min内全部崩解。
1.5 含量测定
1.5.1 方法的建立
应用紫外分光光度计采用苯酚硫酸法进行菊甘蓝多糖片的含量测定。检测波长为490 nm。
1.5.2 溶液配制
对照品溶液制备:称取葡萄糖对照品0.1005 g,加入到100 mL容量瓶中,以水为溶剂,稀释并定容至刻度,摇匀,即得浓度为1.005 g/L 对照品储备液;精密量取不同体积(0.0、0.8、1.6、2.4、3.2、4.0 mL)的上述对照品储备液,加入到50 mL 容量瓶中,得到浓度分别为0、16.08、32.16、48.24、64.32、80.40 mg/L 对照品溶液。供试品溶液制备:取菊甘蓝多糖片剂5片研磨成粉,取样品1 g,加入适量的75%乙醇溶液进行溶解、摇匀、过滤。滤液转移至50 mL容量瓶中,以水为溶剂稀释至刻度,作为供试品溶液。
1.5.3 标准曲线与线性范围
吸取不同体积(0、16.08、32.16、48.24、64.32、80.40 mg/L)的对照品溶液各1 mL,转移至10 mL 容量瓶中(苯酚硫酸法处理),测定吸光度A(检测波长:490 nm),绘制标准曲线(横坐标为对照品浓度,纵坐标为吸光度),计算回归方程。
1.5.4 精密度实验
吸取浓度为32.16 mg/L 的对照品溶液1 mL,测定6次吸光度,计算RSD值,RSD值应小于2%。
1.5.5 稳定性试验
取供试品溶液,室温下放置不同时间(0、2、4、8、12、24 h)后测吸光度,计算吸光度的RSD 值应小于2%。
1.5.6 回收率试验
分别量取供试品溶液9 份,每份0.5 mL,置于9个容量瓶中。分别加入低、中、高浓度(16.08、48.24、80.40 mg/L)的对照品溶液各0.5 mL,每个浓度各3份,测定吸光度,计算回收率及RSD 值,RSD 值应小于2%。
1.5.7 含量测定
按“1.5.2”方法制备三批样品溶液,苯酚硫酸法处理,测定吸光度,带入回归方程计算多糖含量。
2 结果
2.1 处方筛选及优化
2.1.1 辅料种类筛选
对淀粉、糊精、微晶纤维素、PVP(K30)、蔗糖、硬脂酸镁等多种辅料进行苯酚-硫酸法处理,紫外吸收情况见表1。结果显示,微晶纤维素、PVP(K30)、硬脂酸镁紫外吸光度值较小,对多糖紫外吸收影响较小,可以用作辅料。因此确定菊甘蓝多糖片剂处方中辅料组成,填充剂为微晶纤维素,黏合剂选择PVP(K30),硬脂酸镁为润滑剂,考虑成本因素,崩解剂选择CMS-Na。

表1 辅料苯酚-硫酸法测定结果Tab.1 Determination results of auxiliary material phenolsulfuric acid method
2.1.2 填充剂用量筛选
以外观、硬度、崩解时限为考察指标,选择最佳微晶纤维素用量。结果显示,微晶纤维素用量逐渐增多时,外观变整洁,且硬度及崩解时间相应减小。当微晶纤维素用量为4 g 时,外观及硬度符合片剂要求,但崩解时间仍大于15 min,所以下一步对崩解剂CMS-Na的用量进行考察。
2.1.3 崩解剂用量筛选
以硬度和崩解时限为指标对片剂进行评价,选择最佳CMS-Na 用量。因微晶纤维素也具有崩解作用,所以CMS-Na 用量不需太多。结果显示,随着CMS-Na 用量增加,片剂崩解时间减少,硬度减小。当用量为1 g时,崩解时间<15 min,硬度适中。
2.1.4 黏合剂用量筛选
以黏合效果、崩解时限和硬度为指标对片剂进行评价,从而选出最佳的PVP(K30)浓度。该片剂主料为多糖,本身黏合性较好,故黏合剂PVP(K30)需求不大。结果显示,当PVP(K30)用量逐渐增加,片剂黏度增大,崩解时间及硬度也逐渐增大。当PVP(K30)浓度为1.5%时,黏度适中,且崩解时限和硬度符合要求。
2.1.5 处方确定
根据单因素试验结果,确定最优处方:以20 g计,菊芋粗多糖10 g,甘草粗多糖3 g,绞股蓝粗多糖2 g,微晶纤维素4 g,CMS-Na1g,聚乙烯吡咯烷酮浓度为1.5%,硬脂酸镁0.2%。
2.2 制备工艺
制备方法选择湿法制粒压片法。将原料药菊芋、甘草、绞股蓝粗多糖及所有辅料分别研磨,加入微晶纤维素,过100目筛充分混匀,得到无结块粉末。加入1.5% PVP(K30)溶液(溶剂为80%乙醇),制备软材,制粒(18 目筛),50 ℃烘箱中干燥后整粒(10 目筛),最后加硬脂酸镁,充分混合。将所得粉末用单冲压片机压片,即得菊甘蓝多糖片。
2.3 片剂一般检查
2.3.1 片重差异检查
样品片重检查结果如表2 所示。3 批样品(每批20片)总片重分别为8.02、8.09、8.04 g,平均片重分别为0.401、0.405、0.402g,因此3 批样品每片的重量应分别在0.381~0.421 g、0.385~0.425 g、0.382~0.422 g范围内,3批样品均符合要求。

表2 片剂一般检查结果Tab.2 General inspection results of tablets
2.3.2 硬度检查
供试品硬度检查结果如表2 所示,3 批样品硬度均在45~55 N之间,平均硬度为51 N,符合要求。
2.3.3 崩解时限检查
崩解时限结果见表2。结果显示,3 批样品均在15 min内崩解完毕,符合规定。
2.4 含量测定
2.4.1 标准曲线与线性范围
根据对照品溶液吸光度A(检测波长:490 nm),绘制标准曲线(横坐标为对照品浓度,纵坐标为吸光度),计算得到回归方程(A=0.009 7C+0.096 1;R=0.999 7)。由此可知,该方法在16.08~80.40 mg/L范围内线性关系良好。
2.4.2 精密度实验
根据精密度测定结果,RSD 为0.53%,符合相关要求,仪器精密度良好。
2.4.3 稳定性试验
结果显示,RSD为1.62%,样品在24 h内稳定。
2.4.4 回收率试验
结果显示,菊甘蓝多糖片的平均回收率为99.89%,RSD为1.03%,样品回收率符合要求。
2.4.5 含量测定
含量测定结果如表3 所示,3 批样品中,多糖含量平均值为0.215 g/片,RSD为0.22%。
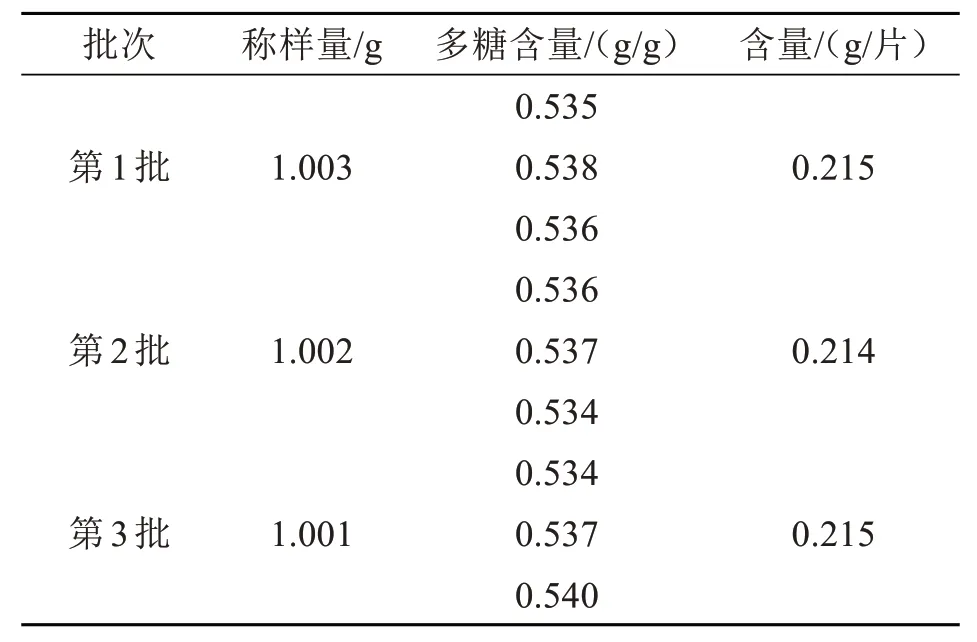
表3 菊甘蓝多糖片中多糖含量Tab.3 Polysaccharide content in chrysanthemum cabbage polysaccharide tablets
3 讨论
多糖片主成分为多糖,黏性较大,且遇水黏合性更强,对崩解时间影响较大。此外,本着绿色健康的原则,应尽量添加较少的辅料。片剂制备中,填充剂直接选用主成分菊芋多糖,片剂崩解时间超过2 h,可能是由于多糖占处方比例过大,黏性太强。通过考察多种填充剂,微晶纤维素对多糖含量测定影响最小,考虑成本因素,崩解剂最终选择CMS-Na。由于主成分本身黏性大,黏合剂PVP(K30)浓度也不需太高,以免发生黏冲、硬度过大等问题。通过对以上辅料进行单因素试验考察,获得最佳处方:每20 g 含有菊芋粗多糖10g,甘草粗多糖3 g,绞股蓝粗多糖2 g,微晶纤维素4 g,CMS-Na 1g,加入1.5%聚乙烯吡咯烷酮适量,湿法制粒,得干颗粒后,加约总量0.2%硬脂酸镁,压片,即得。
湿法制粒压片制备工艺得到的片剂具有外观美观、流动性好、耐磨性较强、压缩成形性好等特点,是一种优良的片剂制备工艺。但湿法制粒压片法过程较为复杂,需要使用较多的水和有机溶剂,并严格把控制粒条件和干燥温度等参数。本试验为保证片剂流动性,且减小辅料对多糖含量测定的影响,故黏合剂溶剂选择80%乙醇,干燥温度为50 ℃。
为了对菊甘蓝多糖片剂的质量进行评价,根据中华人民共和国药典(2020 版)对其一般性能进行检查。经检查制备的片剂的硬度、片重差异和崩解时限均符合标准。进一步建立了苯酚硫酸法处理采用紫外分光光度计进行含量测定方法,在使用硫酸苯酚法测定多糖时,由于反应的时间以及温度会对溶液的显色反应有一定的影响,从而导致误差[11]。所以在实际测定过程中,应尽量保证反应时间与要求时间相符。最终得到多糖含量平均值为0.215 g/片。
综上所述,通过本次试验,筛选得出菊甘蓝多糖片最佳处方与制备工艺,制成片剂含量均匀、性状稳定、表面光滑圆整,为菊甘蓝多糖片工业化生产提供数据,并为质量控制标准提供了可靠依据。
