果胶酶对灵武长枣果实发育中阿拉伯半乳糖蛋白分布的影响
2024-01-02章英才陶珊珊
王 静 章英才 陶珊珊 杨 雪
(宁夏大学生命科学学院,银川 750021)
果实的组织特性是决定品质和消费者选择标准的关键特征,果实的品质特性主要取决于特定果实细胞代谢等过程[1]。细胞壁使果实具有一定的形状和弹性,其结构和物质成分的改变被认为是引起果实质地变化的主要原因[1]。所有导致果实成熟和软化的过程都与细胞壁的重塑有关,主要与细胞壁聚合物网络的松散紧密相关[2-4],细胞壁在其中起着至关重要的作用。纤维素主要作为细胞壁的骨架,而果胶等则有序的分布在纤维素和半纤维素微丝中,并与之交联。多糖组装体的修饰,尤其是果胶的修饰对果实生长和成熟过程中细胞壁的变化具有重要影响。在番茄(Solanum lycopersicum)果实成熟过程中,果胶半乳糖醛酸表达量下降,这与酶促降解导致果胶解聚有关,细胞壁的破坏表现为细胞与细胞的粘附减少,同时受果胶的空间分布及其在细胞连接处流失的影响[5-6]。然而,果胶结构的改变不仅会直接导致细胞壁的改变,而且会导致与其他成分连接的重新排列,进而引起细胞壁的改变[7]。其中之一是阿拉伯半乳聚糖蛋白(AGPs),其具体分布与果实成熟阶段有关[8-10]。AGPs 参与了细胞壁-质膜连续体的建立,以及与其他细胞壁成分的交联。
AGPs 是植物细胞壁蛋白中富含羟脯氨酸糖蛋白家族(HRGPs)的高度糖基化蛋白,是无定形植物细胞外基质中普遍存在的组分,具有可变的核心蛋白和富含阿拉伯糖、半乳糖的糖基侧链[11]。AGPs 的特点是高比例的糖基部分,以及蛋白质骨架和碳水化合物链的异质性。碳水化合物链对AGPs 的正常功能有较大的影响,高度分支的碳水化合物结构域、特别是它们的异质性,对AGPs 功能的多样性十分重要[12-15]。AGPs 是GPI 锚定的蛋白(GAPs),由蛋白骨架C 末端的糖磷脂酰肌醇紧密结合在质膜上[16-17]。此外,AGPs 通过阿拉伯半乳聚糖的分子共价连接到细胞壁半纤维素和果胶多糖上,形成阿拉伯木聚糖果胶-阿拉伯半乳聚糖蛋白1(APAP1)结构。AGPs 与不同组分的相互作用有助于它们作为细胞壁-质膜连续体的锚定物发挥作用[18-20]。自果实组织中发现阿拉伯半乳聚糖蛋白(AGPs)以来,前人已有的研究表明,细胞壁的组装可能会受到这些糖蛋白的影响,这对果实的特性非常重要。
从干旱缺水到营养器官和生殖器官的热胁迫,AGPs 被认为有助于植物应对生物和非生物胁迫[21]。各种因素对果实中阿拉伯半乳糖蛋白的分布产生影响。就果实而言,有报道称低氧和缺氧可调节AGPs 编码基因的mRNA 水平,提示它们在番茄生长中的适应过程和维持细胞壁稳定性中的作用[22]。此外,葡萄(Vitis vinifera)成熟过程中的细胞扩增与AGPs 的丰度增加有关,LM2 抗体识别的AGPs 表位β-D-GlcA 是葡萄果实成熟的潜在生物标志物[8]。在苹果(Malus×domestica)果实中,AGPs 表位的定位取决于采后衰老过程中细胞壁-质膜发生变化的条件,此外,还发现AGPs 具有组织特异性[23]。
果实软化的酶机制与细胞壁多糖的解聚有关。AGPs 的结构修饰和碳水化合物部分的降解是由α-L-阿拉伯呋喃糖苷酶(α-L-Af)、β-半乳糖苷酶(β-Gal)和β-木糖苷酶(β-xylosidases)几种糖苷酶引起。其中,α-L-Af 的活性与AGPs 中L-阿拉伯呋喃糖残基的释放和对β-半乳糖苷酶敏感的糖部分的形成有关[24],可导致阿拉伯糖的丧失,对果实成熟过程中阿拉伯糖的代谢及果实软化有重要作用[2]。β-半乳糖苷酶水解细胞壁的半乳糖苷键,切除多糖侧链中非还原末端半乳糖残基,导致细胞壁多糖中半乳糖、阿拉伯糖含量的降低,以及阿拉伯半乳聚糖等多聚物的解聚,改变细胞壁中一些组分的稳定性,促使细胞壁膨胀进而使其软化,半乳糖和阿拉伯糖在细胞壁结构中扮演很重要的角色[25]。为了阐明AGPs 的作用,人们利用AG 糖链的降解酶,鉴定了2 个编码β-葡萄糖醛酸酶的基因,它们能够水解AGPs 的β-Glc A 和4-Me-β-Glc A残基[26]。这些研究结果表明,酶对阿拉伯半乳糖蛋白具有作用,糖苷酶的激活可能导致寡糖链的损伤和释放,这些寡糖链对于高等植物蛋白聚糖的生理功能必不可少。
果胶酶是一种复合酶,主要包括解聚酶类和水解酶类,在果实发育过程中催化细胞壁果胶类物质的降解过程,促进细胞壁解体和果实成熟软化具有重要作用[1-2]。使用酶降解和细胞壁多糖定向探针是研究果实结构发育修饰的有效分析工具。众所周知,AGPs 与细胞壁中的其他基本组分形成了一个复杂的网络,果胶酶影响了AGPs 在细胞壁中的分布以及AGPs 抗原表位排列的改变,AGPs 在果实软化过程中发挥重要作用[10]。灵武长枣(Ziziphus jujuba‘Lingwu Changzao’)为宁夏优良药食同源鲜食枣品种,在果实贮藏保鲜、生理特性等方面已有较多的研究[27-28],而有关果胶酶对果实AGPs 分布及果实成熟过程的影响鲜见报道。因此,本研究的目的是揭示果胶酶对4个不同发育时期灵武长枣果实AGPs 分布的影响,以明确果胶降解酶对AGPs 分布的影响。通过果胶酶处理不同时期果实材料,采用免疫细胞化学技术,在细胞水平上对AGPs 表位进行原位分析检测,研究AGPs 作为果实细胞壁多糖-蛋白聚糖网络的重要组成部分在灵武长枣果实细胞壁中排列的影响和分布的变化,为明确果胶酶对果实成熟过程的影响提供解剖学依据。
1 材料与方法
1.1 试验材料
以位于宁夏灵武市的宁夏红枣工程技术研究中心试验基地(38°12′N,106°34′E)6 年生灵武长枣为供试材料,采用随机设计,3次重复,每次重复选择5~10 株生长发育良好、树势适中、长势和花期相似、栽培管理水平一致的植株,用毛线于2022年6 月10 日标记同一天开放的花朵,每个重复标记3 000朵[27-28]。
在灵武长枣开花坐果到果实成熟的发育过程中共设计4 次试验,具体分别在果实膨大前期(7月10日)、果实快速膨大期(8月9日)、果实着色期(9月8日)、果实完熟期(9月28日)[28],每次试验时间均设定于09:00—11:00 进行,按所标记植株从树冠的东、西、南、北4个方位以及上、中、下、里、外各个方向选择标记花朵的枣吊作为试验对象,将枣吊采摘用冰壶带回实验室[27-28]。
果胶酶来自黑曲霉(Aspergillus niger)、购自Sigma Aldrich 公 司,AGPs 单 克 隆 抗 体JIM13、JIM8、MAC204 购自美国乔治亚大学,其相应二抗Anti-mouse-IgG-FITC购自Sigma公司。
1.2 方法
1.2.1 果胶酶处理
果实组织的酶处理是根据Leszczuk 等[29]进行,作了一些修改。选取4 个发育时期果实,用锋利的刀片从外果皮开始切取2 mm×2 mm×4 mm 的果实组织,立即放入E1(0.028 U·mL-1)、E2(0.056 U·mL-1)、E3(0.084 U·mL-1)3种不同浓度果胶酶的醋酸盐缓冲液(pH=5.5),22 ℃酶解3 h[29]。
1.2.2 树脂包埋和切片
样品经10 mmol·L-1的PBS 漂洗后放入4%多聚甲醛-0.5%戊二醛的PBS(10 mmol·L-1,pH=7.4)固定液中(对照不用果胶酶处理,分割后直接固定),盖紧瓶盖后多次抽气至样品沉落瓶底,冰上(或4 ℃)固定4 h,再分别转移至新鲜的固定液中,冰上(或4 ℃)固定4 h。
样品在4 ℃下摇床中以PBS(10 mmol·L-1,pH=7.4)漂洗3 次,每次15 min。在4 ℃下摇床中分别以30%、50%、70%、90%乙醇脱水,每次15 min;100%乙醇15 min,100%丙酮30 min,共3~4 次。样品经脱水后渗透包埋于Spurr 树脂。在超薄切片机(LEICA EM UC6,德国)下制作1 μm 厚的半薄切片。
1.2.3 免疫细胞化学分析
将有切片的载玻片放入10%过碘酸(高碘酸)中腐蚀树脂,在温箱中60 ℃静置15 min,蒸馏水冲洗,PBS(10 mmol·L-1,pH=7.4)冲洗;0.3%H2O2中5 min[30]。切片放入PBS(10 mmol·L-1,pH=7.4)淋洗(浸泡)5 min,然后用含50 mmol·L-1甘氨酸、2%BSA 的PBS (10 mmol·L-1,pH=7.4) 封闭液封闭10 min。PBS(10 mmol·L-1,pH=7.4)淋洗5 min,再用PBS(含1% BSA)以1∶50 体积比稀释后的单克隆抗体,4 ℃下孵育过夜[27-28]。对照组采用含1%BSA 的PBS 溶液代替一抗。用PBS 淋洗3 次,每次5 min,以去除多余抗体;再用PBS(含1%BSA)以1∶200 体积比稀释后的Anti-mouse-IgG-FITC 二抗37 ℃黑暗条件下孵育2 h;标记后,PBS 淋洗3 次,每次5 min,除去未标记的二抗;0.01% Toluidine blue 染色5 min,以去除植物本身的自发荧光,PBS(10 mmol·L-1,pH=7.4)淋洗10 min[27-28]。
1.2.4 Calcofluor染色
为进行对比染色,将半薄切片用0.01% Calcofluor White 水溶液在黑暗中染色10 min[29],以显示细胞壁纤维素的分布和存在情况。
1.2.5 成像观察
切片PBS(10 mmol·L-1,pH=7.4)淋洗10 min,稍微晾干后,取甘油少许滴在样品上封片,指甲油将盖玻片的四周封固。尽快在LEICA STELLARIS 5 激光共聚焦显微镜下观察绿色荧光和蓝色荧光叠加图,并拍照。
FITC的激发波长为490 nm,发射波长为525 nm,显示绿色荧光。Calcofluor染色切片在激发波长为355 nm、发射波长为433 nm 的条件下显示蓝色荧光。每个果实样品至少分析15 个组织切片,每个抗体重复试验数次,选取有代表性的图像利用photoshop软件进行图像编辑。
2 结果与分析
2.1 果实成熟过程中果皮AGPs和纤维素分布的变化
成熟过程诱导了果实组织外果皮、中果皮结构的形态学变化,果实成熟过程中的一个明显特征是外果皮表皮细胞外壁角质层的显著增厚变化,膨大前期表皮细胞外壁角质层相对较薄(图1:A~C),快速膨大期(图1:D~F)、着色期(图1:G~I)、完熟期(图1:J~L)显著增厚;且内部组织的细胞变得更大和更圆(图1:D~L)。除了表皮细胞组织学上的差异外,内部组织也表现出结构上的差异,果实发育前期果皮中细胞紧密排列(图1:A~C),在发育后期成熟过程中出现解体和松散(图1:D~L)。
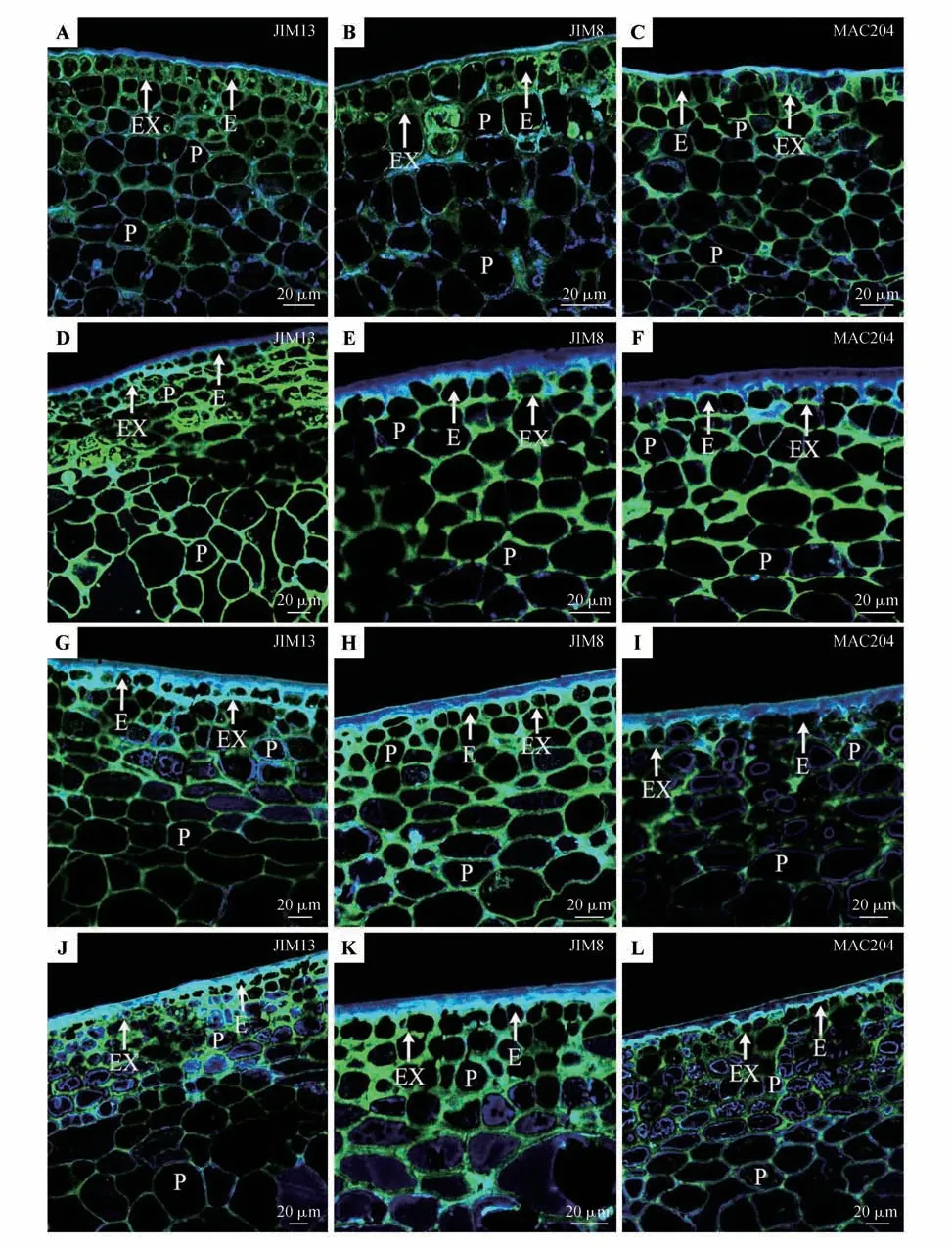
图1 不同发育时期果皮AGPs的分布A~C.膨大前期;D~F.快速膨大期;G~I.着色期;J~L.完熟期;EX.外果皮;E.表皮细胞;P.薄壁细胞;下同。Fig.1 AGPs distribution of fruit pericarp during different development periods A-C.The early bulking period;D-F.The rapid enlargement period;G-I.The coloring period;J-L.The maturation period;EX.Exocarp;E.Epidermal cells;P.Parenchymal cells;the same as below.
为了检测AGPs 的分布特征,本研究采用一系列识别AGPs 糖链特异性表位的单克隆抗体标记了果实组织切片,呈现绿色荧光。此外,具有β-Dglycans 亲和力的Calcofluor White 被用于对比染色和显示细胞壁纤维素的分布,呈现蓝色荧光,结果显示所有形态变化都与细胞壁组成的改变有关。在果实发育过程中,JIM13、JIM8 和MAC204 抗体所识别的抗原绿色荧光表位在4 个时期果实的外果皮(图1:A~L),以及相邻的内部数层排列紧密的中果皮小细胞的细胞壁和邻近细胞壁内部均有分布(图1:A~L)。内部的中果皮大型卵圆形薄壁细胞的细胞壁和邻近细胞壁处在膨大前期和快速膨大期,均有JIM13、JIM8 和MAC204 抗体所识别的抗原绿色荧光表位分布(图1:A~F),而着色期和完熟期果实JIM13、JIM8 和MAC204 抗体所识别的抗原表位均主要分布于薄壁细胞的细胞壁上,大部分细胞内部无分布(图1:G~L)。随着果实发育成熟,内部中果皮薄壁细胞间隙拉大排列更加松散,出现细胞破裂,JIM13、JIM8 和MAC204 抗体所识别的抗原表位分布逐渐减少(图1:G~L)。识别βGlcA(1→3)-αGalA(1→2)Rha 残基的JIM13、识别AGPs 糖基表位的JIM8 和MAC204 抗体所标记的抗原荧光强弱在各时期果实的不同组织存在一定差异。在果实发育的膨大前期至快速膨大期早期阶段,标记保持在同一区域,即在细胞壁的边缘靠近质膜的区域,荧光信号较强烈;而在果实逐渐成熟的着色期至完熟期红色果实阶段,荧光信号比之前时期果实组织中减弱,且标记的规律性较差,表明随果实成熟过程,AGPs 的数量有所减少。此外,在纤维素分布变化方面,膨大前期至快速膨大期果实外果皮细胞壁纤维素显著增多,在这一过程中,外果皮细胞的形状发生了变化,主要表现在表皮层由细胞壁加厚的细胞组成,这些细胞的细胞壁被Calcofluor White 强烈地标记为蓝色荧光(图1:A~F),而着色期和完熟期果实外果皮细胞壁纤维素有所减少,内部组织细胞近细胞膜处纤维素显著增多(图1:G~L),与同期AGPs 的减少相反。
2.2 果胶酶处理后果皮AGPs 和纤维素分布的变化
果实用低浓度酶0.028 U·mL-1(E1)处理后,在膨大前期(图2:A~C)、快速膨大期(图3:A~C)、着色期(图4:A~C)、完熟期(图5:A~C)均未观察到果皮组织结构的明显变化。比较显著的变化出现在酶浓度0.056 U·mL-1(E2)处理后,在膨大前期(图2:D~F)、快速膨大期(图3:D~F)、着色期(图4:D~F)、完熟期(图5:D~F)果实组织的各部位均可见细胞形态的变化和细胞壁的紊乱。经最高酶浓度0.084 U·mL-1(E3)处理后,膨大前期(图2:G~I)、快速膨大期(图3:G~I)、着色期(图4:G~I)、完熟期(图5:G~I)果实不均匀增厚的细胞壁解体程度增加,内部薄壁细胞细胞壁的增厚较明显。
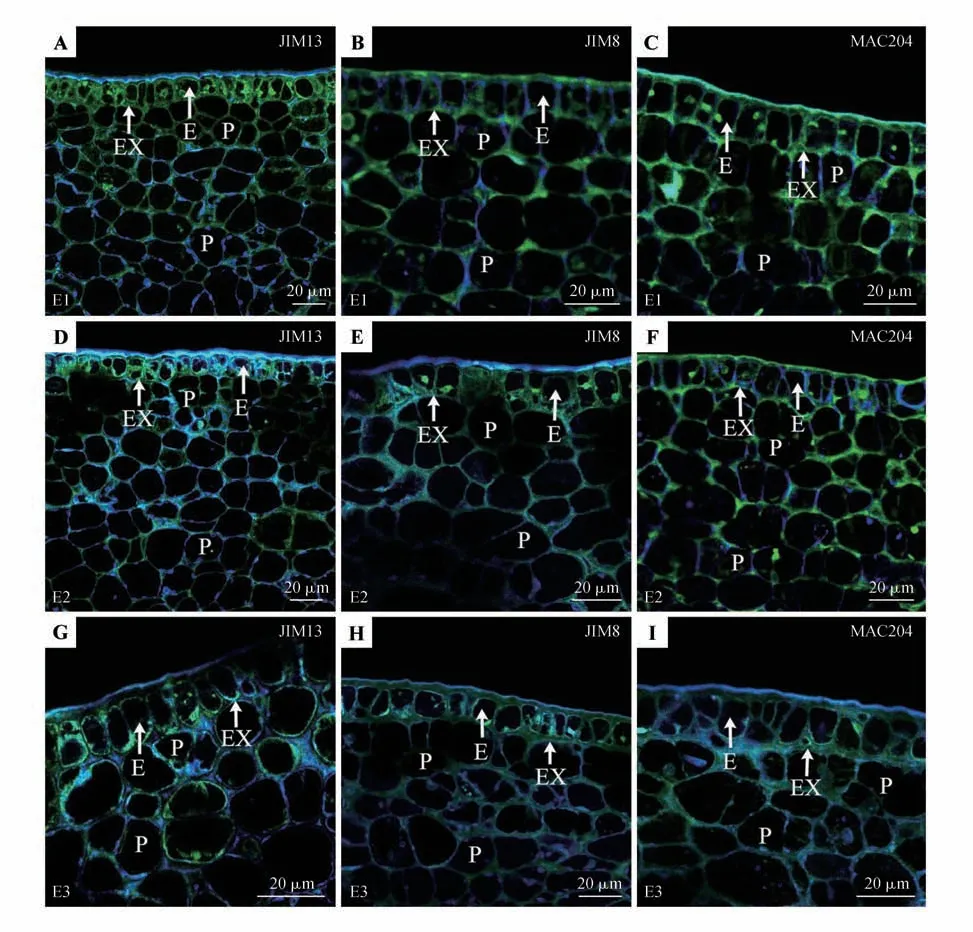
图2 3种不同浓度酶处理后膨大前期果实AGPs的分布Fig.2 The distribution of AGPs in the early bulking period fruit pericarp after treatment with three different concentrations enzymes
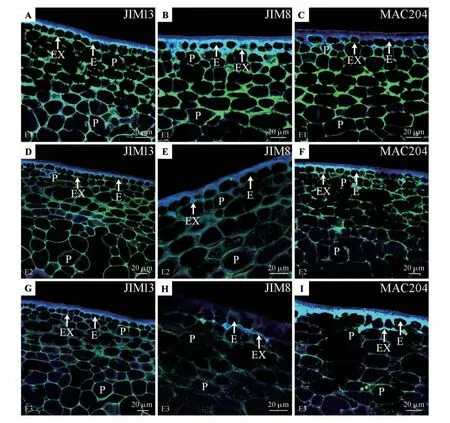
图3 3种不同浓度酶处理后快速膨大期果皮AGPs的分布Fig.3 The distribution of AGPs in the rapid enlargement period fruit pericarp after treatment with three different concentrations enzymes

图4 3种不同浓度酶处理后着色期果皮AGPs的分布Fig.4 The distribution of AGPs in the coloring period fruit pericarp after treatment with three different concentrations enzymes
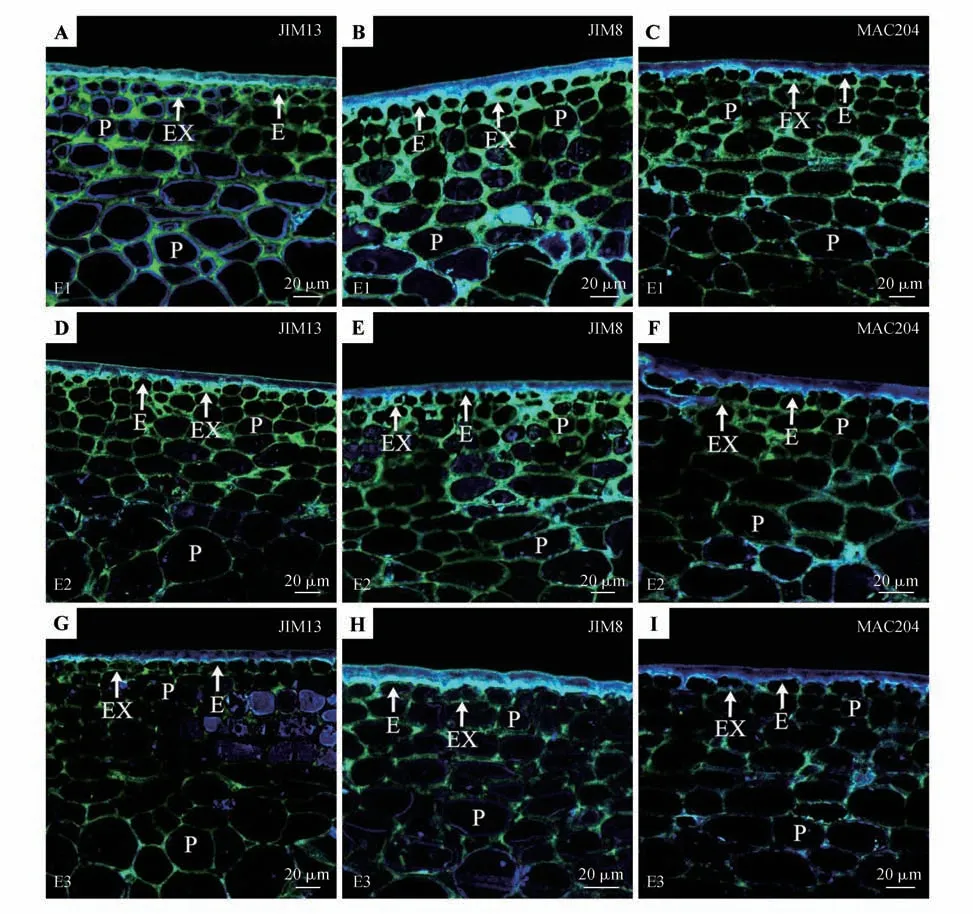
图5 3种不同浓度酶处理后完熟期果皮AGPs的分布Fig.5 The distribution of AGPs in the maturation period fruit pericarp after treatment with three different concentrations enzymes
利用酶解法,本研究揭示了AGPs 抗原表位排列的改变。作为酶处理的结果,这些表位的破坏显示了AGPs 的变化。当果实组织用较低浓度的酶(E1:0.028 U·mL-1)处理,膨大前期(图2:A~C)、快速膨大期(图3:A~C)、着色期(图4:A~C)、完熟期(图5:A~C)果皮及内部薄壁细胞细胞壁中的AGPs抗原表位减少,但没有完全消除,0.056 U·mL-1(E2)和0.084 U·mL-1(E3)处理的果实中AGPs抗原表位检测量逐渐降低,在许多情况下,只可见小的荧光斑点(图2:D~I;图3:D~I;图4:D~I;图5:D~I)。酶浓度的增加导致AGPs在果实所有表位排列的影响更大和荧光信号较弱,果胶酶浓度与AGPs 抗原荧光强弱具有明显负相关性。同样,最高浓度的果胶降解酶处理后,Calcofluor White染色显示不同发育时期果实外果皮表面及果皮内部组织细胞壁区域蓝色荧光也不同程度减弱或降低,纤维素分布有所减少(图2:G~I;图3:G~I;图4:G~I;图5:G~I)。
2.3 果胶酶处理后果实维管束和薄壁组织AGPs和纤维素分布的变化
AGPs在4个时期外果皮内维管束和薄壁组织的分布变化,果实发育前期薄壁组织和维管束细胞壁区域在所观察的AGPs表位中最为丰富(图6:A,D),着色期至完熟期薄壁组织细胞变大,细胞间隙拉长,AGPs 表位减少(图6:G,J)。Calcofluor White 标记的纤维素分布于整个细胞壁表面,在细胞壁及靠近内壁的质膜上出现较强的荧光信号,突出了细胞壁AGPs 的分布特征(图6:A,D,G,J),在果实发育成熟过程中纤维素影响组织完整性和细胞壁形状,从而观察到细胞解离和AGPs 表位重排(图6:A,D,G,J)。
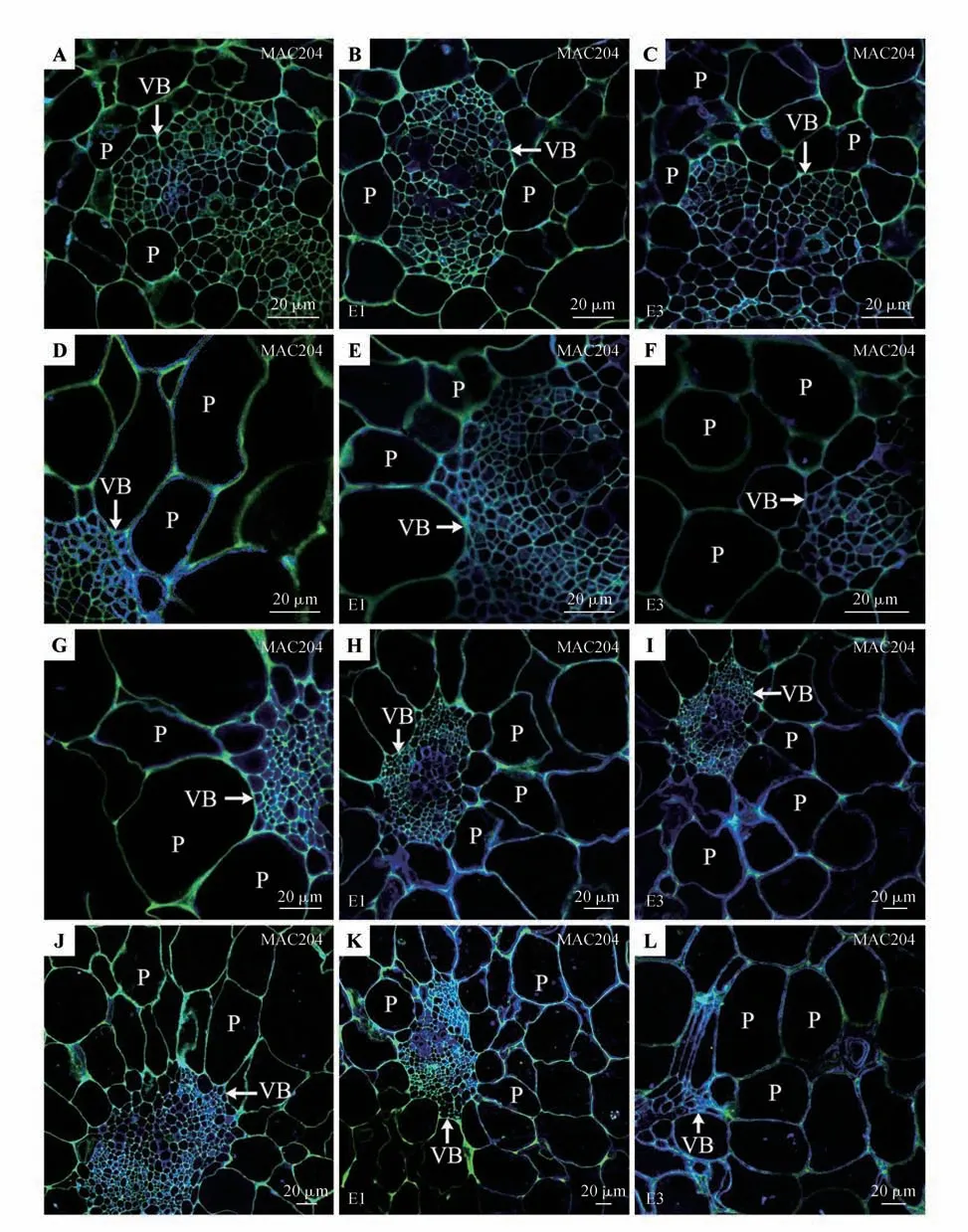
图6 酶处理后4个发育时期的外果皮内薄壁组织及维管束AGPs的分布A~C.膨大前期;D~F.快速膨大期;G~I.着色期;J~L.完熟期;VB.维管束。Fig.6 The distribution of AGPs in parenchyma tissues and vascular bundle beside exocarp after treatment with different concentrations enzymes during 4 development stages A-C.The early bulking period;D-F.The rapid enlargement period;G-I.The coloring period;J-L.The maturation period;VB.Vascular bundle.
果胶酶处理后AGPs 和纤维素分布变化的观察显示,细胞壁的酶解特征表现为荧光信号较少且无序。经0.028 U·mL-1(E1)浓度的酶处理后,AGPs抗原表位标记不局限于细胞壁/质膜,分布在整个细胞壁表面和细胞间隙,在薄壁细胞中,AGPs 抗原表位有时会出现在被破坏的细胞壁边缘(图6:B,E,H,K)。经最高浓度酶0.084 U·mL-1(E3)的处理后,在纤维素蓝色荧光对比下,抗体与AGPs结合的绿色荧光信号显得相当弱(图6:C,F,I,L)。因此,AGPs 分布模式的紊乱和抗原表位的缺失与组织中纤维素组装的变化有关。
3 讨论
3.1 果胶酶导致AGPs排列的中断和果实组织结构的变化
高等植物细胞壁的共同特征是均由纤维素、半纤维素、果胶质和糖蛋白等大分子组成。利用多项生化技术和过表达技术的研究揭示了细胞壁酶在果实成熟中的功能,在苹果果实中,甲酯化聚半乳糖醛酸、结晶纤维素和岩藻糖基化木葡聚糖侧链等3 种关键多糖的水解对薄壁组织的机械性能有重大影响[31]。AGPs 作为纤维素微纤丝与半纤维素、果胶交联的共外延网络的元素,在细胞壁中的分布因果胶酶而改变。本研究的目的是揭示果胶酶的诱导对灵武长枣果实AGPs 碳水化合物分布的影响。
果胶酶混合物中含有果胶裂解酶(PL)EC 4.2.2.2、内切多聚半乳糖醛酸酶(PG)EC 3.2.1.15、果胶甲酯酶(PME)EC 3.1.1.11,以及少量半纤维素酶(EC3.2.1.8,EC 3.2.1.89)和 纤 维 素 酶Cx(EC 3.2.1.4)。细胞壁修饰酶,如果胶裂解酶(PL)、多聚半乳糖醛酸酶(PG)和果胶甲酯酶(PME),负责重塑果胶网络[32-33]。果胶甲酯酶在整个果实生长过程中催化半乳糖醛酸残基的C6 羧基的去甲基化,使果胶(多聚半乳糖醛酸)降解,细胞壁解体,果实软化[1-2];PME 对于果实软化具有前导或启动作用,在果实成熟过程中参与了果实的降解代谢,影响组织结构完整性[34];果胶裂解酶催化果胶聚合物中去甲基化的半乳糖醛酸残基的裂解[35];在果实成熟过程中,PG 对于果胶多聚物的降解和溶解有重要作用,其活性在番茄成熟软化过程中均可检测到[36];PG 在许多果实成熟软化后期作用明显,但其并非果实软化的决定性因素[37]。在果胶发生降解的同时,半纤维素多糖也被不断修饰而参与了果实软化的进程[38]。在整个灵武长枣成熟过程所有被检测的AGPs 表位中,与质膜相邻的细胞壁及细胞间隙区域较为丰富,细胞壁修饰酶处理与果实细胞壁组装中AGPs 表位的丢失或重塑有关,这与AGPs 碳水化合物结构域的降解紧密相关。因此,果实中特异的阿拉伯聚糖沉积并附着在细胞壁及细胞间隙很可能是导致果实成熟的关键因素。
果实软化与纤维素的合成,以及纤维素微纤丝的物理特性及其沉积有关[3]。细胞外基质中纤维素的定位与细胞壁中其他成分的存在有关[39]。纤维素微纤丝被阿拉伯聚糖和半乳糖侧链直接连接,因此AGPs 碳水化合物的损失与纤维素微纤丝的解体有关,这导致果实软化和细胞分离的变化[40]。有证据表明,果胶酶的最高浓度对所检测的番茄果实AGPs 表位的分布有影响,也对纤维素的存在有影响[29];这与本研究结果相似。众所周知,纤维素酶是由多种纤维素酶类组成的混合酶,通过纤维素的分解参与了果实发育和成熟阶段细胞壁物质降解[41]。Cx 酶作用于纤维素,使细胞壁中纤维素微纤丝-半纤维素-果胶连接的结构松散,导致果实软化。本研究结果表明,同样缺乏另一种细胞壁成分,即AGPs 蛋白聚糖导致纤维素不同程度的解体。这些结果表明,荧光信号的降低与碳水化合物链的降解、细胞壁的扩张以及纤维素组装的变化相联系。
随着果实成熟衰老,多聚半乳糖醛酸酶(PG)、果胶甲酯酶(PME)和纤维素酶等活性增加,果胶、纤维素组分降解,导致果肉软化[1]。李欢等[42]测定了鲜食枣‘冬枣’(Z.jujuba‘Dongzao’)、制干枣‘木枣’(Z.‘Muzao’)和‘骏枣’(Z.‘Junzao’)果实成熟和软化7 个发育时期细胞壁物质(果胶和纤维素)含量及相关酶类(PG、PE或PME、Cx)活性,比较结果表明,鲜食枣灵武长枣、冬枣与木枣、骏枣果实质地和成熟软化机制不同,枣果实成熟过程与果胶酶、纤维素酶和半纤维素酶基因等细胞壁代谢网络的调控相关;揭示了鲜食枣与制干枣成熟过程的细胞壁物质及酶类生理和分子调控的不同机制,为深入探究枣果实成熟品质调控提供了理论基础。
3.2 酶促因素和非酶促因素影响均可能导致AGPs排列中断
果实的成熟软化受到多种内外因素的影响。果实软化主要是在多种胞壁水解酶的作用下,细胞壁多糖发生降解和解聚合,从而导致细胞壁结构改变,胞壁结构分离造成的。除外源果胶酶的作用外,内源PG、PME、Cx、β-Gal 等与果实细胞壁多糖降解或解聚密切相关,在果实成熟软化的不同时期起着不一样的作用[43]。除酶促因素外,内源乙烯[43]、抗坏血酸[44]等非酶促因素也可能导致果实细胞壁多糖的降解,引起细胞壁疏松,促进果实软化。因此,果实的软化可能是多种因素共同作用引起细胞壁多糖的降解进而导致AGPs 与细胞壁中的其他基本组分复杂网络破坏的结果,影响了AGPs 在细胞壁中的分布以及AGPs 抗原表位排列的改变。
由此看来,适宜浓度的果胶酶逐渐溶解灵武长枣果实中大部分的果胶多糖和纤维素、半纤维素,内源细胞壁修饰酶促进了果胶、纤维素、半纤维素的酶切,导致果胶多糖的断裂,纤维素-半纤维素-果胶连接的结构松散,因而果实自然软化。成熟的果实细胞AGPs 减少、细胞壁硬度降低与果胶多聚体等细胞壁物质分解增加有关,这是细胞壁修饰酶活性较高的机制,其参与了阿拉伯半乳糖-果胶复合物的降解增溶作用,导致熟化过程中细胞壁松弛。因而,针对不同AGPs 抗原表位抗体的标记模式不同,荧光信号呈现多样性。
3.3 果胶酶的作用影响了果实成熟过程
影响果实结构的成熟关联变化与许多因素有关,但其中最显著的决定因素之一是果胶酶的活性[3,7]。果实发育初期果皮细胞壁结构致密均匀而连续,在发育后期成熟过程中出现解体和松散。说明果胶的溶解和解聚合会导致细胞壁之间空隙增大,细胞间粘合力降低,细胞间隙不断增大,使胞壁水解酶更好接触底物,从而导致果实的软化[45]。本研究表明,果胶酶的作用引起组织的微结构改变,但诱导细胞壁的改变与自然成熟果实中发生的改变不具有可比性。本研究采用不同浓度水平的细胞壁水解酶对细胞壁进行酶解,观察结果表明果胶酶的作用可能影响了果实成熟过程。由此看来,根据果实质地和成熟软化机制不同,通过果胶酶等调控果实成熟进程,对果实成熟软化及品质调控具有重要意义。
因此,4个不同发育时期果皮细胞壁结构的差异对细胞壁功能具有影响,也与AGPs 分布相关。果实AGPs 碳水化合物的分布因多种因素而不同,这与果实组织结构的变化有关。尽管组成果实细胞壁的纤维素和果胶多糖是果实成熟的基本要素和关键因素,但笔者认为各成分之间的相互作用在控制成熟和采后生理方面的作用最为显著。AGPs 聚糖链的缺失使所有细胞壁成分之间相互作用的建立发生中断和重塑,诱导整个细胞壁结构的改变。
