特瑞普利单抗联合XELOX化疗对晚期胃癌患者的效果及肿瘤标志物的影响
2024-01-01潘娜冯继李明蔚



[摘" "要]" "目的:探讨特瑞普利单抗联合卡培他滨+奥沙利铂(XELOX)化疗对晚期胃癌患者疾病控制率及血清肿瘤标志物的影响。方法:回顾性选取120例晚期胃癌患者,依据治疗方案不同分组,对照组60例采用XELOX方案化疗,观察组60例采用特瑞普利单抗联合XELOX化疗,治疗3个周期。比较两组疾病控制率、治疗前后血清肿瘤标志物[癌胚抗原(carcino-embryonic antigen,CEA)、糖类抗原19-9(carbohydrate antigen 19-9,CA19-9)、糖类抗原724(carbohydrate antigen 724,CA724)、血管内皮生长因子(vascular endothelial growth factor,VEGF)]水平、T淋巴细胞亚群(CD3+细胞、CD4+细胞、CD4+/CD8+)、Th1/Th2相关因子[干扰素-γ(interferon-γ,IFN-γ)、白介素-12(interleukin-12,IL-12)、白介素-13(IL-13)]水平。比较两组治疗后QLQ-C30评分、卡氏功能状态评分(Karnofsky performance status,KPS)、Piper疲乏修订量表评分(revised Piper fatigue scale,RPFS)以及毒副反应发生率。结果:观察组疾病控制率91.67%,高于对照组的65.00%(P<0.05);治疗1个周期、3个周期后,观察组血清CEA[(20.01±6.85)μg/mL vs(26.77±4.27) μg/mL,(13.28±3.24) μg/mL vs(21.05±2.63) μg/mL]、CA19-9[(185.63±41.87)U/mL vs(200.41±32.63)U/mL,(133.96±24.65)U/mL vs(172.05±17.35)U/mL]、CA724[(66.30±12.10)U/mL vs(75.06±15.02)U/mL,(42.01±4.16)U/mL vs(60.08±10.02)U/mL]、VEGF[(188.29±32.76)pg/mL vs(200.71±26.38)pg/mL,(124.17±31.39)pg/mL vs(168.92±36.30)pg/mL]水平低于对照组(均P<0.05),CD3+细胞[(68.99±3.25)% vs(60.01±3.62)%,(78.24±4.41)% vs(59.66±3.37)%]、CD4+细胞[(36.71±2.06)% vs(28.11±2.15)%,(39.66±2.01)% vs(28.07±2.24)%]、CD4+/CD8+[(1.80±0.25)vs(1.40±0.18),(1.97±0.20)vs(1.38±0.11)]高于对照组(均P<0.05),血清IFN-γ[(17.22±1.74)ng/mL vs(15.02±1.06)ng/mL,(23.96±3.18)ng/mL vs(18.77±2.25)ng/mL]、IL-12[(19.66±2.55)ng/mL vs(16.38±2.16)ng/mL,(26.39±3.19)ng/mL vs(20.01±2.07)ng/mL]水平高于对照组,IL-13[(18.27±2.09)pg/mL vs(21.19±2.06)pg/mL,(6.33±1.11)pg/mL vs(13.38±2.46)pg/mL]水平低于对照组(均P<0.05)。与对照组比较,观察组治疗3个周期后QLQ-C30评分[(83.26±8.25)分vs(71.14±7.37)分]、KPS评分[(82.33±3.51)分vs(76.10±3.28)分]升高,RPFS评分[(3.88±0.85)分vs(4.25±1.12)分]降低(均P<0.05)。两组毒副反应发生率比较,差异无统计学意义(均P>0.05)。结论:特瑞普利单抗联合XELOX化疗治疗晚期胃癌患者,可提高疾病控制率,降低血清肿瘤标志物水平,改善免疫功能,提升生活质量,缓解癌因性疲乏,且具有一定安全性。
[关键词]" "晚期胃癌;特瑞普利单抗;卡培他滨;奥沙利铂;肿瘤标志物
[中图分类号]" "R735.2 [文献标志码]" "B [DOI]" "10.19767/j.cnki.32-1412.2024.05.010
胃癌早期症状较隐匿,确诊时多数患者已处于中晚期。晚期胃癌患者常采用化疗方案治疗,但目前仍无标准化疗方案[1]。卡培他滨+奥沙利铂(XELOX)方案用于晚期胃癌可阻滞肿瘤进展,延长患者生存期,但大部分患者会出现毒副反应,疗效欠佳[2]。近年来分子靶向药物已在临床应用,程序性死亡受体-1(program cell death receptor-1,PD-1)抑制剂特瑞普利单抗通过阻断PD-1/(PD-L1)通路,激活淋巴细胞抗肿瘤活性,阻止肿瘤免疫逃逸,增强机体免疫功能[3]。本研究回顾性选取2021年8月—2023年11月我院收治的120例晚期胃癌患者,分析特瑞普利单抗联合XELOX方案的疗效及其对血清肿瘤标志物、免疫功能、生活质量的影响。
1" "资料与方法
1.1" "一般资料" "晚期胃癌患者120例,依据治疗方案不同分为对照组和观察组各60例。对照组男性34例,女性26例;年龄61~71岁,平均(66.28±2.26)岁;体质量指数18~26 kg/m2,平均(22.68±1.29)kg/m2;病程12~21个月,平均(16.32±2.15)个月;临床分期:Ⅲb期23例,Ⅳ期37例;分化程度:低分化45例,中高分化15例;病理类型:腺癌41例,印戒细胞癌19例;原发部位:胃38例,胃-食管结合部22例。观察组男性32例、女性28例;年龄59~73岁,平均(65.93±3.05)岁;体质量指数20~26 kg/m2,平均(23.01±1.41)kg/m2;病程11~22个月,平均(17.05±2.20)个月;临床分期:Ⅲb期25例,Ⅳ期35例;分化程度:低分化41例,中高分化19例;病理类型:腺癌39例,印戒细胞癌21例;原发部位:胃33例,胃-食管结合部27例。两组一般资料比较,差异均无统计学意义(P>0.05)。纳入标准:(1)符合胃癌诊断标准[4],经双重造影、组织病理学检查等确诊;(2)美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力评定量表评分0~1分,预计生存时间>6个月;(3)可测量靶病灶≥1个;(4)既往未使用过XELOX方案化疗;(5)临床资料完整。排除标准:(1)肿瘤全身广泛转移;(2)合并造血系统疾病、凝血功能障碍、肝肾功能不全、其他恶性肿瘤;(3)对本研究药物过敏。本研究经医院医学伦理委员会审核批准。
1.2" "治疗方法" "对照组:采用XELOX化疗。第1 d静脉滴注奥沙利铂(哈药集团生物工程有限公司,国药准字H20133094)130 mg/m2,2 h/次;口服卡培他滨片(上海罗氏制药有限公司,国药准字H20073024),1 000 mg/m2,2次/d,连续口服14 d,21 d为1个周期,连续治疗3个周期。观察组:采用特瑞普利单抗联合XELOX化疗。XELOX方案同对照组,于第4 d静脉滴注特瑞普利单抗(上海君实生物医药科技股份有限公司,国药准字S20180015)3 mg/kg,21 d为1个周期,连续治疗3个周期。
1.3" "观察指标" "(1)疾病控制率:治疗3个周期后评估疾病控制率[5],肿瘤病灶完全消失视为完全缓解(complete remission,CR),基线病灶直径总和缩小≥30%视为部分缓解(partial remission,PR),基线病灶直径总和增加>20%视为疾病进展(progressive disease,PD),介于PR和PD之间视为稳定(stable disease,SD),CR、PR、SD计入疾病控制。(2)血清肿瘤标志物:治疗前、治疗1个周期、3个周期后采集患者空腹外周静脉血,采用电化学发光免疫法检测血清癌胚抗原(carcino-embryonic antigen,CEA)、糖类抗原19-9(carbohydrate antigen,CA19-9)、糖类抗原724(carbohydrate antigen,CA724)水平(上海梵态生物公司试剂盒),酶联免疫吸附试验检测血清血管内皮生长因子(vascular endothelial growth factor,VEGF)水平(上海联祖生物公司试剂盒)。(3)T淋巴细胞亚群:采用Attune NxT流式细胞仪(美国赛默飞世尔科技公司)于治疗前、治疗1个周期、3个周期后检测患者外周血CD3+、CD4+细胞数量,计算CD4+/CD8+比值。(4)Th1/Th2相关因子:治疗前、治疗1个周期、3个周期后采用酶联免疫吸附试验检测患者血清干扰素-γ(interferon-γ,IFN-γ)、白介素-12(interleukin-12,IL-12)、白介素-13(IL-13)水平(美国Ramp;D公司试剂盒)。(5)生活质量:采用欧洲癌症研究与治疗组织(European Organization for Research and Treatment of Cancer,EORTC)生命质量量表EORTC QLQ-C30(以下简称QLQ-C30)评估生活质量。该量表包括4项:运动、健康状态、活动、生活行为,每项0~25分,总分为100分,得分越高则生活质量越好。卡氏功能状态评分(Karnofsky performance status,KPS):包括20个条目,总分100分,得分与健康状况呈正相关。Piper疲乏修订量表(revised Piper fatigue score,RPFS)评分[6]:包括认知、情感、感知、行为4个维度,总分10分,得分越高则癌因性疲乏越严重。
1.4" "统计学处理" "采用SPSS 26.0软件进行统计学分析;计量资料以±s表示,两组间比较采用独立样本t检验;计数资料以n(%)表示,两组间比较采用χ2检验;P<0.05为差异有统计学意义。
2" "结" " " 果
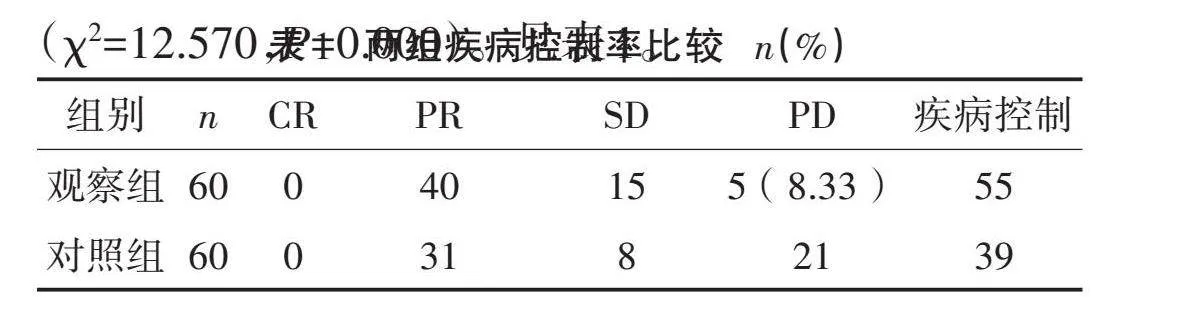
2.1" "两组疾病控制率比较" "观察组疾病控制率91.67%,高于对照组的65.00%,差异有统计学意义(χ2=12.570,P=0.000)。见表1。
2.2" "两组血清肿瘤标志物比较" "治疗前两组血清CEA、CA19-9、CA724、VEGF水平比较,差异均无统计学意义(P>0.05);与治疗前比较,两组治疗1个周期、3个周期后血清CEA、CA19-9、CA724、VEGF水平降低;观察组治疗后血清CEA、CA19-9、CA724、VEGF水平较对照组更低,差异均有统计学意义(P<0.05)。见表2。
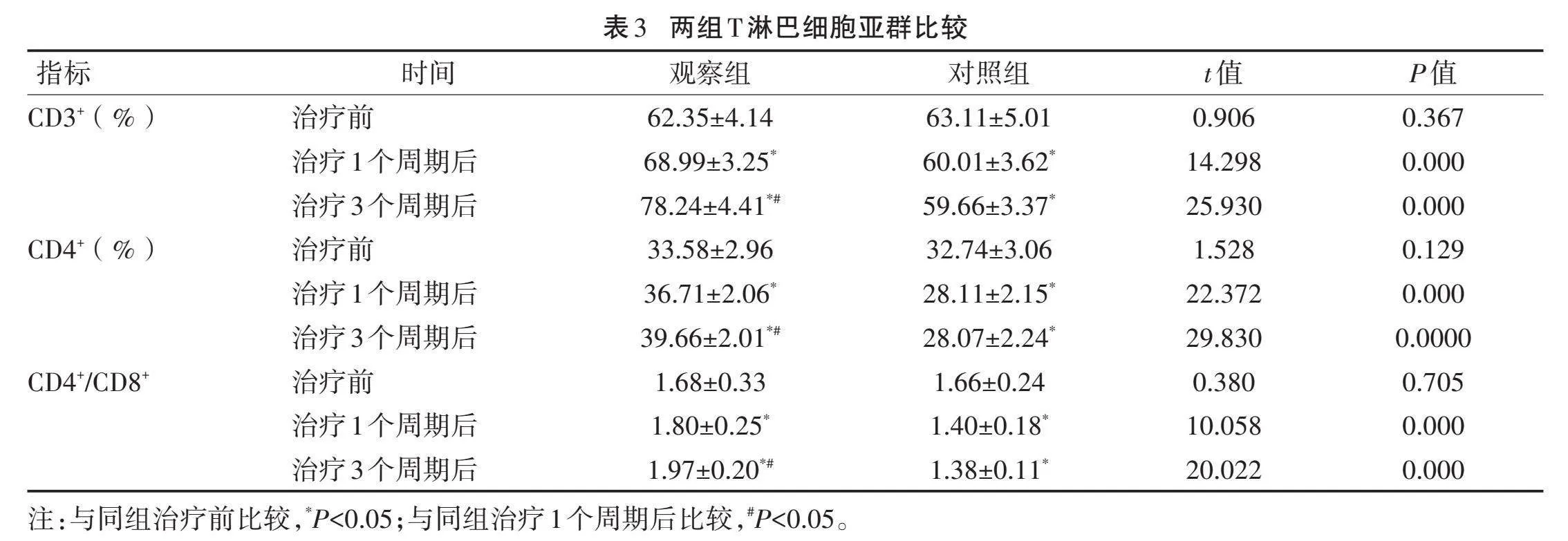
2.3" "两组T淋巴细胞亚群比较" "治疗前两组CD3+、CD4+细胞、CD4+/CD8+比较,差异均无统计学意义(P>0.05);治疗1个周期、3个周期后对照组CD3+、CD4+细胞、CD4+/CD8+低于治疗前,观察组CD3+、CD4+细胞、CD4+/CD8+高于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05)。见表3。
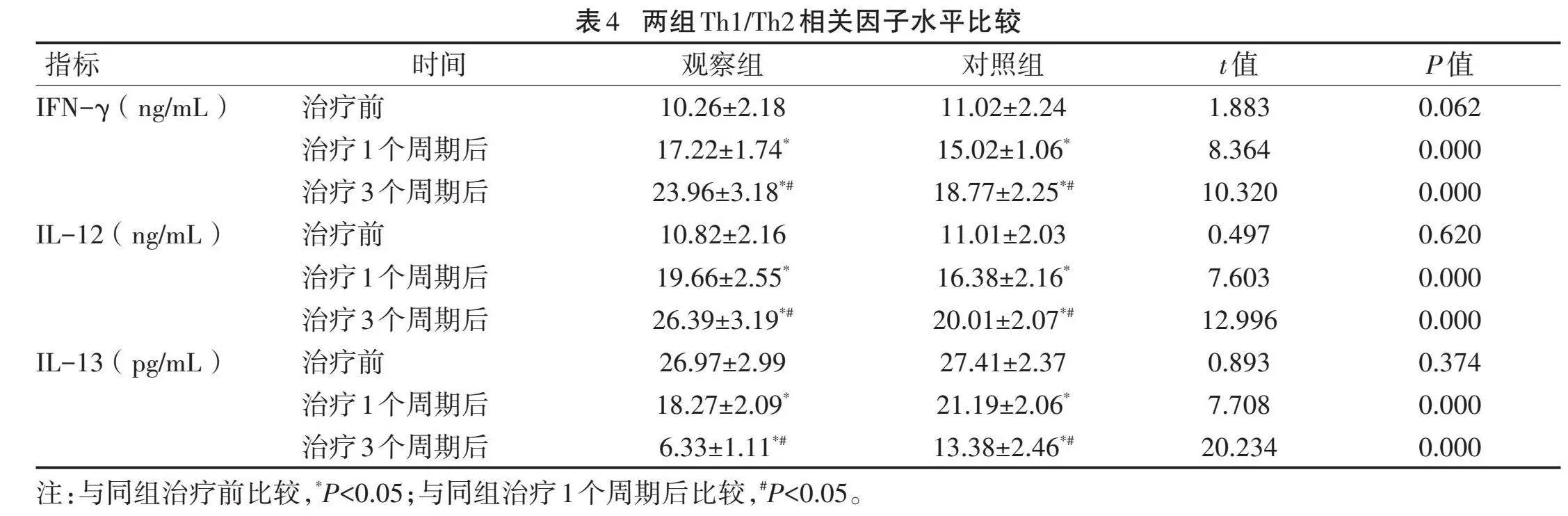
2.4" "两组Th1/Th2相关因子水平比较" "治疗前两组Th1/Th2相关因子水平比较,差异均无统计学意义(P>0.05)。与治疗前比较,两组治疗后血清IFN-γ、IL-12水平升高,IL-13水平降低;与对照组比较,观察组治疗后血清IFN-γ、IL-12水平升高,血清IL-13水平降低,差异均有统计学意义(P<0.05)。见表4。
2.5" "两组QLQ-C30评分、KPS评分及RPFS评分比较" "治疗前两组QLQ-C30评分、KPS评分及RPFS评分比较,差异均无统计学意义(P>0.05)。治疗3个周期后两组QLQ-C30评分、KPS评分高于治疗前,RPFS评分低于治疗前,且观察组改善幅度大于对照组,差异均有统计学意义(P<0.05)。见表5。
2.6" "两组毒副反应比较" "两组各种毒副反应发生率比较,差异均无统计学意义(P>0.05)。见表6。
3" "讨" " " 论
胃癌发病机制可能与饮食习惯、幽门螺杆菌感染、癌基因活化、抑癌基因失活、遗传基因等有关,临床常采用化疗方案治疗晚期胃癌患者,但可引起胃肠道反应等毒副反应[7],因此寻找新的有效治疗方案具有重要意义。
卡培他滨可干扰肿瘤细胞RNA、蛋白质生成,抑制肿瘤细胞增殖,奥沙利铂能抑制肿瘤细胞DNA复制和增殖[8]。特瑞普利单抗通过抑制PD-1/PD-L1通路,阻止肿瘤细胞增殖,诱导癌细胞凋亡,减少肿瘤负荷,并可降低肿瘤细胞侵袭能力,重建免疫监视体系,增强T细胞免疫反应能力[9-10]。本研究结果显示,观察组疾病控制率高于对照组。与李文娟等[11]研究结果一致,提示联合治疗具有协同增效作用。CEA、CA724、CA19-9可用于辅助诊断胃癌,动态监测其水平变化可用于疗效评估;VEGF调节血管通透性,参与胃癌发生发展过程[12]。与对照组比较,观察组治疗后血清CEA、CA19-9、CA724、VEGF水平降低,差异有统计学意义(P<0.05),其原因可能为联合治疗增强抗肿瘤效果,特瑞普利单抗可抑制炎症反应,改善肿瘤内环境,防止肿瘤细胞侵袭,抑制肿瘤组织血管生成,进而降低肿瘤标志物表达。
胃癌发生发展与免疫功能紊乱有关,CD3+细胞水平反映机体细胞免疫功能,免疫功能受损时CD3+细胞减少;CD4+细胞可诱导细胞免疫,调控体液免疫;CD4+/CD8+比值降低表明机体免疫发生损伤[13]。杨宁等[14]研究表明,特瑞普利单抗治疗Ⅲ期非小细胞肺癌患者,可降低肿瘤标志物水平,提高机体免疫力。本研究观察组治疗后CD3+、CD4+细胞、CD4+/CD8+明显升高,高于对照组,差异均有统计学意义(P<0.05),与有关研究结果类似。推测可能因为特瑞普利单抗解除免疫抑制,增强T细胞对肿瘤细胞杀伤能力,促进肿瘤免疫应答反应,改善T淋巴细胞亚群的紊乱状态。Th1细胞分泌IFN-γ、IL-12等细胞因子,激活细胞毒性T细胞和巨噬细胞,增强机体抗肿瘤能力;Th2细胞分泌IL-13等细胞因子,抑制抗肿瘤免疫功能,Th1/Th2失衡可促进肿瘤发生发展[15]。与对照组比较,观察组治疗后血清IFN-γ、IL-12水平升高,血清IL-13水平降低,差异均有统计学意义(P<0.05),提示联合治疗可纠正Th1/Th2失衡。此外,与对照组比较,联合治疗后患者QLQ-C30评分、KPS评分升高,PFS评分降低,差异均有统计学意义(P<0.05),提示联合治疗可改善患者生活质量,缓解癌因性疲乏。两组毒副反应发生率的差异无统计学意义(P>0.05),说明XELOX方案化疗时增加特瑞普利单抗并不增加药物不良反应。
综上所述,特瑞普利单抗联合XELOX化疗治疗晚期胃癌患者,可提高疾病控制率,降低血清肿瘤标志物水平,改善免疫功能,提升生活质量,缓解癌因性疲乏,且具有一定安全性。
[参考文献]
[1] 王俊斌,王栓虎,张露,等. 低剂量阿帕替尼联合化疗二线治疗对晚期胃癌患者的疗效[J]. 中国临床研究,2022,35(5):622-626.
[2] 章海斌,丁晓娇,王练,等. 甲磺酸阿帕替尼联合XELOX方案一线应用于晚期胃癌的疗效与安全性评价[J]. 蚌埠医学院学报,2023,48(2):170-173.
[3] LU S,ZHANG W,WU L,et al. Perioperative toripalimab plus chemotherapy for patients with resectable non-small cell lung cancer: the neotorch randomized clinical trial[J]. JAMA,2024,331(3):201-211.
[4] 国家卫生健康委员会. 胃癌诊疗规范(2018年版)[J]. 中华消化病与影像杂志(电子版),2019,9(3):118-144.
[5] EISENHAUER E A,THERASSE P,BOGAERTS J,et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J]. Eur J Cancer,2009,45(2):228-247.
[6] 陈伟霞,李佳,牛垚飞,等. 基于网络药理学探讨加味四君子汤治疗胃癌的作用机制研究[J]. 中医肿瘤学杂志,2021,3(2):48-55.
[7] 徐泽宇,汪海岩,田园. 卡瑞利珠单抗联合白蛋白紫杉醇二线治疗晚期胃癌的疗效及安全性[J]. 现代肿瘤医学,2023,31(1):130-134.
[8] 尹婷立. 自拟抑癌汤联合XELOX化疗方案对胃癌术后的疗效及相关情况的影响[J]. 医学临床研究,2020,37(5):705-707,711.
[9] SHI G M,HUANG X Y,WU D,et al. Toripalimab combined with lenvatinib and GEMOX is a promising regimen as first-line treatment for advanced intrahepatic cholangiocarcinoma: a single-center,single-arm,phase 2 study[J]. Signal Transduct Target Ther,2023,8(1):106.
[10] WANG Y,DENG L,WANG J,et al. Induction PD-1 inhibitor toripalimab plus chemotherapy followed by concurrent chemoradiotherapy and consolidation toripalimab for bulky locally advanced non-small-cell lung cancer: protocol for a randomized phase II trial (InTRist study)[J]. Front Immunol,2023,14:1341584.
[11] 李文娟,刘虎,周守兵,等. 特瑞普利单抗单药或联合治疗在晚期恶性肿瘤中的疗效和安全性[J]. 安徽医学,2020,41(4):413-417.
[12] 张盛,熊伟杰,万涛,等. 复方苦参注射液联合SOX化疗方案治疗晚期胃癌的临床研究[J]. 现代药物与临床,2023,38(10):2531-2535.
[13] 白慧霞,武春燕,段春霞,等. 西妥昔单抗联合伊立替康对晚期胃癌患者血清肿瘤标志物、T淋巴细胞亚群水平及生活质量的影响[J]. 现代生物医学进展,2022,22(21):4157-4162.
[14] 杨宁,张轶群,于芳. 放化疗联合特瑞普利单抗治疗Ⅲ期非小细胞肺癌的疗效观察[J]. 癌症进展,2024,22(1):88-91.
[15] 卫春燕,宋丽丽. 信迪利单抗联合改良DCF方案治疗晚期胃癌的临床研究[J]. 检验医学与临床,2022,19(14):1970-1974.
[收稿日期] 2024-09-11
(本文编辑" "王晓蕴)
