杜梨响应低钾和盐胁迫基因PbHAK17的克隆及功能分析
2023-12-25金雨濛申长卫徐阳春董彩霞
金雨濛,杨 晗,申长卫,徐阳春,董彩霞*
(1 有机(类)肥料国家重点实验室(筹)/ 江苏省固体有机废弃物资源化高技术研究重点实验室 /南京农业大学资源与环境科学学院,江苏南京 210095;2 河南科技学院资源与环境学院,河南新乡 453003;3 盐城市盐都区果蔬园艺技术指导站,江苏盐城 224000)
盐胁迫通常是由于氯化钠在土壤中积累引起植物的渗透胁迫,会严重制约农业生产[1-2]。据估计,全球20%的农业土地为含盐用地,约为8×108hm2,占总土地面积的6%。盐胁迫首先会由于渗透胁迫抑制植物生长,其次是有毒离子浓度过高对植物生长产生不利影响。在盐胁迫下,细胞质中过多的钠离子(Na+)会抑制钾离子(K+)和镁离子(Mg2+)的吸收,从而破坏离子稳态并限制诸多代谢途径。钾是植物细胞中最丰富的阳离子,在维持离子稳态和植物正常生长过程中起到至关重要的作用[3]。充足的K+可以在一定程度上保护植物免受Na+毒害[1,4]。K+还能提高对霜冻、干旱和盐度的耐受性,并提高作物的品质和产量[5]。
有研究表明,外部培养基中高浓度的Na+降低了植物组织中的K+/Na+比值,部分原因是通过HKT 转运体和非选择性阳离子通道增加了质膜上对Na+的摄取[6-7]。K+吸收是通过K+通道和高亲和K+转运体实现,其中 KUP/HAK/KT 家族成员数量最多、研究最为深入[8],不仅与钾离子吸收和利用有关,而且与植物的耐盐能力关系密切[9-10]。不同KT/HAK/KUP 转运体对盐胁迫的响应不同,大麦HvHAK1和芦苇PhaHAK2[11-12]受Na+诱导调控其高亲和转运;AtHAK5和OsHAK1通过竞争性机制抑制对Na+的吸收[13];水稻中OsHAK5则通过降低对Na+的敏感性,阻止Na+流入,增加K+吸收来维持细胞稳态[14]。总之,K+与Na+的摄取、易位、吸收和隔离方面的相互作用很强[15],通常认为盐胁迫下植物通过促进Na+的排出和K+的吸收,从而维持Na+/K+平衡,然而,目前对盐胁迫下植物K+吸收和维持K+/Na+平衡的分子机制了解较少[16]。因此,研究不同K+水平对Na+胁迫下植物生长发育响应的影响,对阐明相关过程具有重要意义。
杜梨(Pyrusbetulifolia)是我国梨树栽培中广泛使用的砧木,具有较强的耐盐性[17-18],以杜梨为砧木可提高梨树的耐盐能力[19-20],但对钾钠离子运输调控的耐盐机制研究较少。本课题组前期利用梨全基因组测序鉴别到21 个HAK/KUP/KT 钾转运蛋白基因,根据基因序列间的同源性和遗传距离将其分为5 个进化簇,通过杜梨根系的转录组数据和实时荧光定量PCR 分析,筛选到对钾胁迫和盐胁迫都有响应的差异表达基因PbHAK17,为AtHAK5的同源基因,推测与AtHAK5有相似功能,可参与响应Na+和K+的吸收。本研究通过克隆耐盐砧木品种杜梨PbHAK17基因,明确钾转运体基因PbHAK17在不同钾钠水平下的时空表达模式,利用钾缺陷型酵母和转基因拟南芥进行异源功能验证,以期从分子水平上揭示PbHAK17在梨钾素吸收转运及响应盐胁迫方面的作用,为提高杜梨耐盐胁迫提供理论依据。
1 材料与方法
1.1 试验设计
选择大小基本一致的杜梨种子,经2.5%次氯酸钠消毒后,用去离子水清洗杜梨种子表面并进行浸泡处理后,放于铺有湿润纱布的玻璃培养皿中,在4℃冰箱中低温冷藏3~4 周左右发芽,期间每3 天用去离子水清洗种子表面分泌物。将发芽的种子播入装有m(营养土)∶m(蛭石)为1∶1 的穴盘中培养,生长期间的温度控制在22℃~28℃,光照周期16 h/8 h(昼/夜),湿度控制在60%左右,光强设置在280~300 μmol/(m2·s)。杜梨幼苗长出4~6 片真叶时,将长势一致的杜梨苗移至1/4 霍格兰营养液[21]中培养缓苗,期间用加氧泵保持氧气浓度。待幼苗长至适宜大小,选取生长发育良好且大小较为一致的幼苗进行不同钾钠水平处理。设置适钾(+K,3 mmol/L K+)、缺钾(-K,0 mmol/L K+)、适钾低盐(3 mmol/L K++50 mmol/L NaCl,即+K+50 mmol/L NaCl)、适钾高盐(3 mmol/L K++200 mmol/L NaCl,即+K+200 mmol/L NaCl)、缺钾低盐(0 mmol/L K++50 mmol/L NaCl,即-K+50 mmol/L NaCl,)、缺钾高盐(0 mmol/L K++200 mmol/L NaCl,即-K+200 mmol/L NaCl)6 个处理。根据胁迫处理杜梨幼苗的生理变化,选取处理6 h 和15 天为采样时间点,每个处理采集9 株杜梨幼苗,分离其根、茎和叶于液氮中速冻,3 株为1 组重复,装入离心管于-80℃超低温冰箱冷藏,待提取RNA。
1.2 PbHAK17 基因的克隆
杜梨总RNA 提取采用上海美吉生物有限公司多糖多酚RNA 提取试剂盒,参考NCBI 数据库收录的梨基因组序列(Pyrus)得到PbHAK17(LOC103950380)总长序列。通过NCBI 对梨钾转运体基因PbHAK17进行搜索获得目的基因全长序列,通过DNAMAN和SnapGene Viewer 软件设计特异性引物(表1)。分别提取根、茎和叶中RNA,反转录后放于-20℃保存备用。PCR 反应体系:10 µL 2×Phanta Max Buffer,0.5 µL dNTP Mix,0.5 µL Phanta MaxSuper-Fidelity DNA Polymerase 高保真聚合酶,正、反向引物各1 µL,模板cDNA 1 µL,ddH2O 补至20 µL。PCR 反应程序:95℃ 3 min;95℃ 15 s,56℃ 15 s,72℃ 2 min,共35 个循环;72℃ 5 min。特异性RT-PCR 产物纯化回收后连接至T 载体上(擎科,北京),转入大肠杆菌,于LB+Ampicillin 固体培养基上培养过夜,挑取单克隆菌株于液体LB 培养基摇菌培养至OD600=0.6~1.0,菌液PCR 鉴定出阳性单克隆,然后进行测序鉴定。

表1 本研究中使用的引物Table 1 Primers used in this study
1.3 PbHAK17 基因生物信息学分析
使用NCBI(https://www.ncbi.nlm.nih.gov/)对两个目的基因进行核苷酸同源比对分析;用Prot-Param(http://web.expasy.org/protparam)预测蛋白的理化特征;用Prot Scale(http://web.expasy.org/cgi-bin/protscale/protscale.pl)推测蛋白的疏水性;用TMHMM Server v.2.0(http://www.cbs.dtu.dk/services/TMHMM/)预测蛋白的跨膜结构;用Signal P 4.1 Server(http://www.cbs.dtu.dk/services/Signal P)预测蛋白的信号肽;利用DNAMAN 软件比对氨基酸序列;利用MEGA 6.06软件中的邻接法(neighbor-joining,NJ)构建基因系统发育进化树。
1.4 PbHAK17 蛋白的亚细胞定位
将测序正确的 pEASY-PbHAK17阳性克隆提取质粒,利用同源重组的方法连接到经Hind Ⅲ和BamHⅠ(NEB 公司,北京)双酶切后的表达载体pRCS2(南京农业大学,植物营养与肥料系分子实验室),引物设计时应保证基因不发生移码突变。并将该质粒转化到农杆菌(Agrobacteriumtumefaciens)EHA105 感受态细胞(唯地生物,南京)中,筛选阳性克隆并保存。培养农杆菌至OD600为0.8,注射到4 周龄的本氏烟草(Nicotianabenthamiana)叶片中,黑暗条件下正常生长48 h 后,通过激光共聚焦显微镜(Olympus FV1000,日本)在488 nm 的激发光下观察 GFP 的表达情况,在610 nm 的激发光下观察细胞膜染料FX™ 4-64(fixable analog of FM™ 4-64 membrane stain)激发的红色荧光,确定基因位置[22]。
1.5 PbHAK17 基因的相对表达量分析
分别提取不同钠钾处理6 h 和15 天的杜梨幼苗根、茎和叶中的RNA。以反转录的cDNA 为模板,使用全式金公司的TransStart® Tip Green qPCR Super Mix 荧光定量试剂盒进行qRT-PCR。以梨Actin 作为内参基因,每个样品qRT-PCR 采用3 次重复,Step One Plus 荧光定量仪测定后采用2-△△CT法[23]分析基因表达量。
1.6 PbHAK17 在缺陷型酵母中的功能验证
对 pEASY-PbHAK17进行质粒提取,质粒经PCR 扩增后利用同源重组技术将目的基因连接到具有Hind Ⅲ 和KpnⅠ 双酶切位点的表达载体 pYES2中,以空载体质粒作为阴性对照,利用钾离子缺陷型酵母菌株R5421 进行酵母转化(感受态细胞购于上海唯地生物技术有限公司),调节PbHAK17酵母转化子和空载体转化子菌液(OD600=1.0),无菌ddH2O将菌液依次稀释倍数为1、10、100、1000 为打点液体。每次吸取3 µL 含有目的基因PbHAK17的酵母转化子和转空载体酵母菌株,对应在不同 K+浓度(0.05、0.1、0.5、1、5、10、20、50 mmol/L)的酵母AP培养基以及分别在高钾(50 mmol/L)和低钾(5 mmol/L)设置的不同盐浓度(50、100、200、300 mmol/L)的酵母AP 培养基上进行打点培养,置于28℃培养箱倒置培养3~5 天后观察拍照。
1.7 PbHAK17 基因遗传转化拟南芥与鉴定
根据目的基因及空载体 pCAMBIA1301 序列设计相应的酶切位点EcoRⅠ和KpnⅠ引物序列,以保存的pEASY-PbHAK17为模板,利用诺唯赞高保真酶进行PCR 扩增、产物回收、同源重组、挑单克隆和测序,成功获得目的基因。通过前期试验建立的花序浸蘸法,用农杆菌将超量表达载体转入野生型拟南芥 Col-0 中,经 PCR 检测确定阳性植株。连续继代后,获得稳定遗传的T2代转基因拟南芥。
1.8 钾钠处理下 PbHAK17 过表达拟南芥的生物量测定
将野生型拟南芥WT 及PbHAK17拟南芥T2代种子播种于MS(20 mmol/L K+)培养基平板上,于4℃冰箱低温避光层积处理2 天,转移到光照培养箱正常培养至4 片叶子,移栽到m(河沙)∶m(珍珠岩)为2∶1 的混合沙土中,置于人工气候室内培养,配制适钾1/2 MS 营养液和缺钾1/2 MS 培养液,用适钾1/2 MS 营养液配置0、50、200 mmol/L的NaCl 培养液,分别处理5 组拟南芥,每个处理下转基因材料用2 株,重复3 次,选用单株进行拍照。处理6 天后,测定拟南芥叶片和根系的鲜重和干重。
1.9 钾钠处理下 PbHAK17 过表达拟南芥钾钠元素含量的测定
将烘干的拟南芥装入5 mL 离心管,加入两个小钢珠,使用TL2010S 高通量组织研磨仪粉碎成粉末状,称取粉末样品0.0200~0.0500 g,放入圆柱形消煮管底部,加入混酸[v(浓硝酸)∶v(高氯酸)=4∶1]6 mL 摇匀后过夜,设置控温消解仪的温度梯度,120℃,1 h;150℃,1 h,190℃,赶酸。到高氯酸分解出现白色烟雾约1 mL,取下冷却,过滤,滤液转移到50 mL 容量瓶中,采用ICP-AES 测定[24]。
1.10 数据分析
采用SPSS 20 统计分析软件对数据进行分析,使用Prism 9.0 和Origin 9.0 进行图表制作。
2 结果与分析
2.1 PbHAK17 基因的克隆
PbHAK17的凝胶电泳条带对应2000~3000 bp标记(marker)位置(图1)。阳性克隆测序结果与目的基因一致,PbHAK17基因cDNA 长度为2370 bp。
图1 克隆PbHAK17 基因电泳图Fig.1 Electropherogram of cloned PbHAK17 gene
2.2 PbHAK17 蛋白结构分析
PbHAK17基因编码的蛋白质含789 个氨基酸,相对分子量88.15 kD,等电点(pI)为8.66,平均亲水指数GRAVY 为0.270,因此,预测该蛋白属疏水性蛋白,不稳定系数为27.58,预测该蛋白为稳定蛋白,并且具有KUP/HAK/KT 家族典型的12 个跨膜结构域(图2)。PbHAK17 蛋白中缬氨酸(Val,9.5%)、异亮氨酸(Ile,9.1%)、亮氨酸(Leu,8.9%)、丝氨酸(Ser,8.0%)、甘氨酸(Gly,7.0%)和丙氨酸(Ala,6.6%)这6 种氨基酸所占比例较高,合计达49.1%,比例最低的为色氨酸(Trp)和半胱氨酸(Cys),占比均仅为1.1%。酸性氨基酸残基天冬氨酸Asp 和谷氨酸Glu 的总数为66,占总氨基酸比例为8.4%,碱性氨基酸组氨酸His、赖氨酸Lys 和精氨酸Arg 残基总数为89,占总氨基酸比例为11.3%,由此可见,该蛋白属于碱性蛋白。
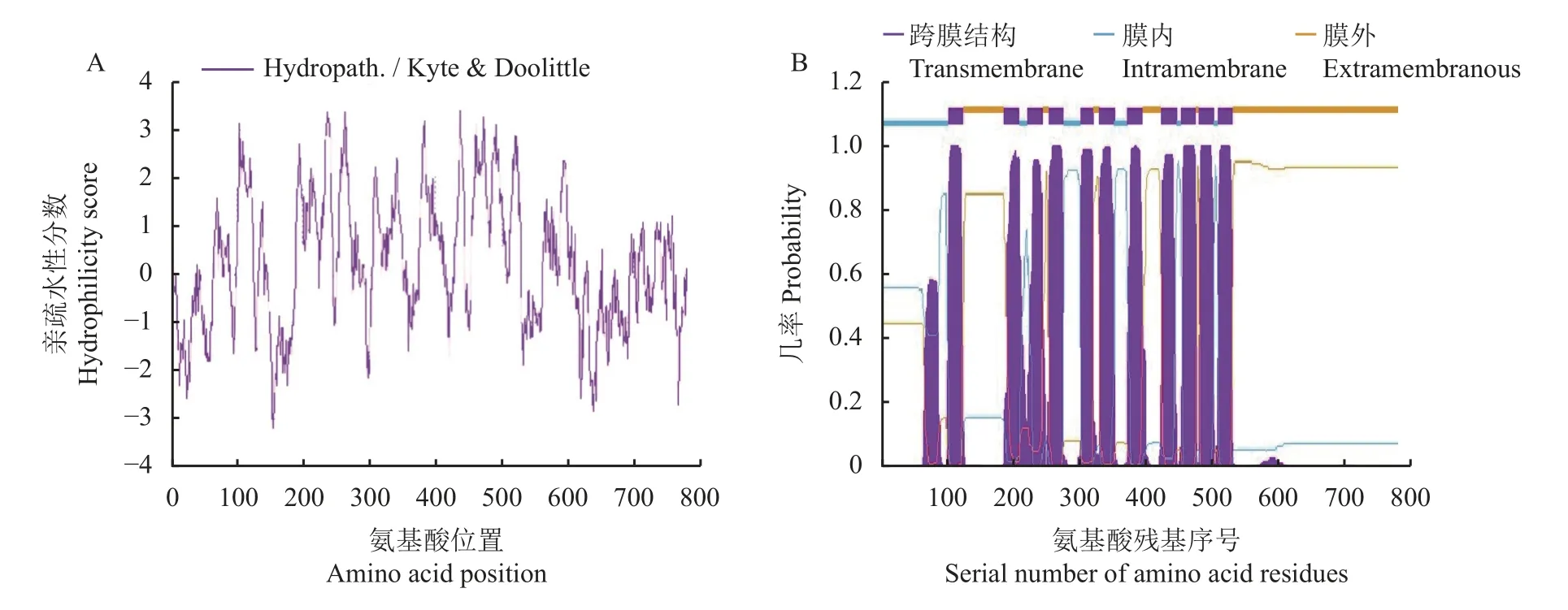
图2 PbHAK17 基因蛋白的一级结构分析Fig.2 Primary structure of PbHAK17 protein
2.3 PbHAK17 核苷酸序列比对和进化分析
PbHAK17 蛋白序列存在保守序列,其中GVVYGDLGTSPLY(高度保守氨基酸)序列属于KUP/HAK/KT 钾转运蛋白家族的标志性序列(图3)。采用MEGA 6.06 中的邻接法(NJ)构建基于HAK 基因的系统发育进化树(图4),结果显示,与模式作物蔷薇科苹果MdHAK5基因亲缘关系最近,同源序列高达96.96%。PbHAK17基因与模式作物拟南芥AtHAK5基因亲缘关系最近,与核苷酸同源性比对分析结果一致。

图3 杜梨PbHAK17 与其他植物相同蛋白同源序列间多重比较Fig.3 Multiple comparisons between the homologous sequences of PbHAK17 protein in pear and other plants
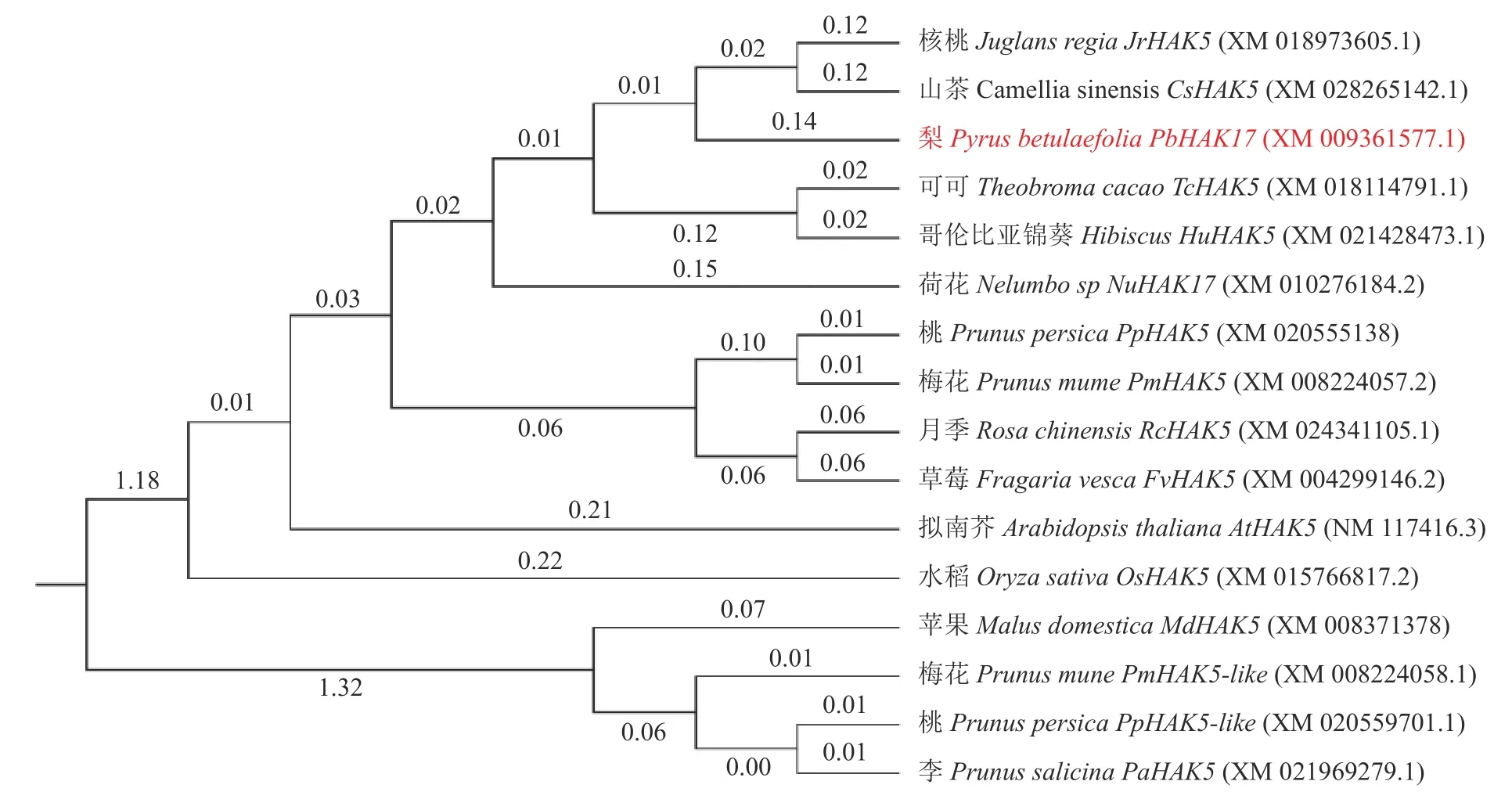
图4 杜梨PbHAK17 与其他植物相同蛋白的进化树分析Fig.4 Evolutionary tree analysis of the same protein of PbHAK17 from pear and other plants
2.4 PbHAK17 蛋白在烟草表皮细胞上的表达定位
由图5 可知,FMTM4-64FX 质膜特异性染料在烟草叶片细胞质膜上呈现红色荧光信号。转入表达载体的烟草 PbHAK17-GFP 融合蛋白在激发光下,只有质膜上有强烈的较为清晰的绿色荧光信号,并与细胞质膜的红色荧光信号完全重合呈现黄色。
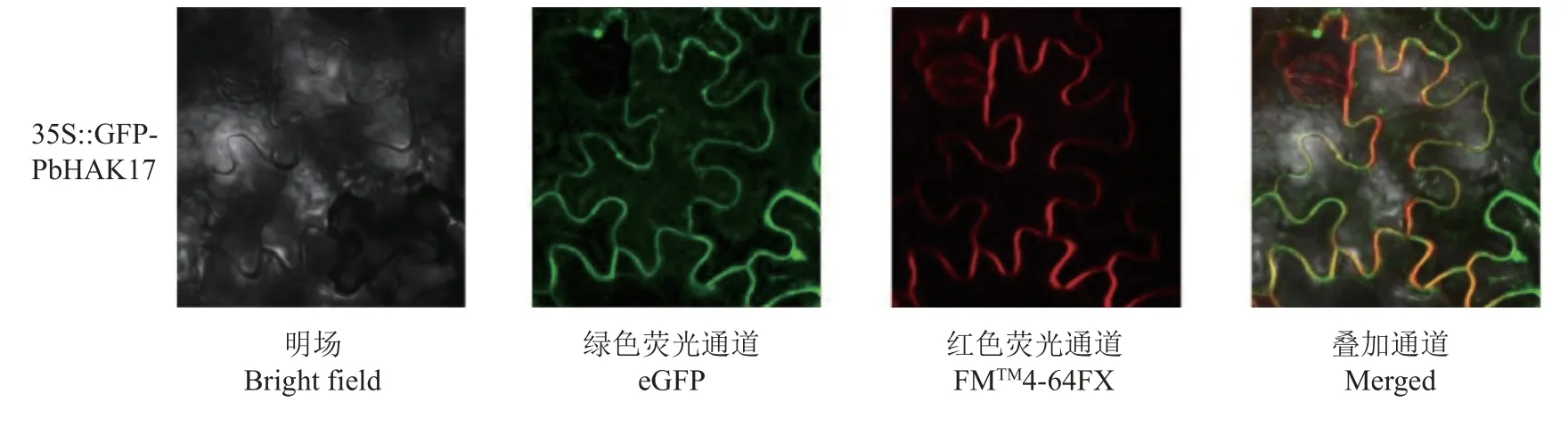
图5 PbHAK17 基因表达产物的亚细胞定位Fig.5 Subcellular localization of PbHAK17 gene expression products
2.5 PbHAK17 在不同钾钠胁迫下的表达模式
图6 结果显示,PbHAK17基因在杜梨中的相对表达量呈现根部显著高于茎部和叶部的特征;相比之下,杜梨叶中的相对表达量很低。PbHAK17在根部短期6 h 的相对表达量普遍高于15 天的表达量。PbHAK17在根、茎中均受缺钾(0 mmol/L)和低盐胁迫(50 mmol/L NaCl)诱导显著增强表达,PbHAK17在缺钾条件下根系中的表达量是正常供钾条件下的2.45 倍。在缺钾条件下同时进行不同程度盐胁迫,PbHAK17的相对表达量较仅缺钾诱导增强的表达量显著下降,但在6 h 内根系中缺钾高盐条件下表达量是正常供钾条件下表达量的1.2 倍,且表达量在6 h内均随盐浓度的增加而增加。
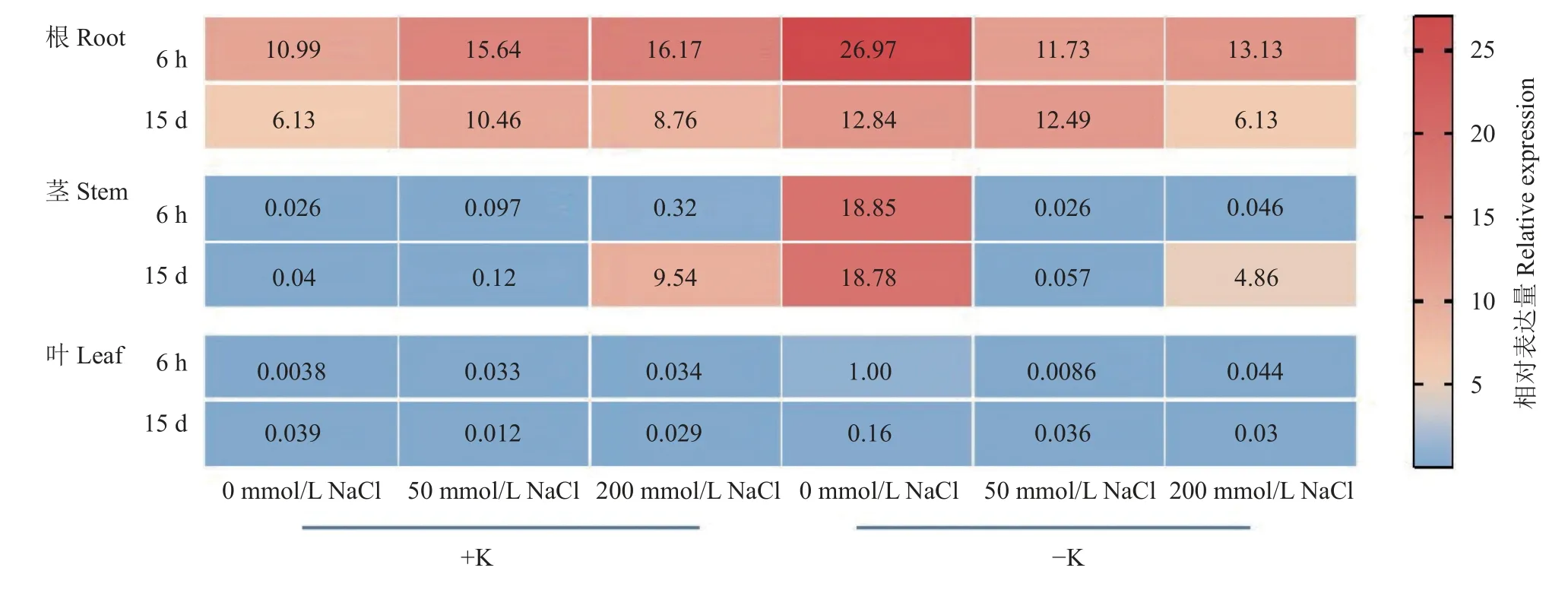
图6 PbHAK17 在不同钾钠胁迫下的表达模式Fig.6 Expression pattern of PbHAK17 under different potassium and sodium stresses
2.6 酵母异源验证PbHAK17 在钾吸收方面的功能
如图7所示,当K+浓度在0.05~50 mmol/L 时,PbHAK17酵母转化子的生长能力显著优于转空载体的酵母。随着 K+浓度降低,PbHAK17酵母转化子菌株长势逐渐减弱,但一直明显优于转空载体菌株。酵母异源回补试验结果表明,PbHAK17能恢复K+吸收缺陷型酵母突变体在低钾培养基中的生长。盐胁迫处理下,随着盐浓度的提高转空载体的酵母生长逐渐受到抑制,尤其在200 和300 mmol/L NaCl 胁迫下,生长受到明显抑制(图8)。PbHAK17酵母转化子长势则明显优于转空载体的酵母,尤其在50~200 mmol/L 盐浓度下其生长均不受抑制。
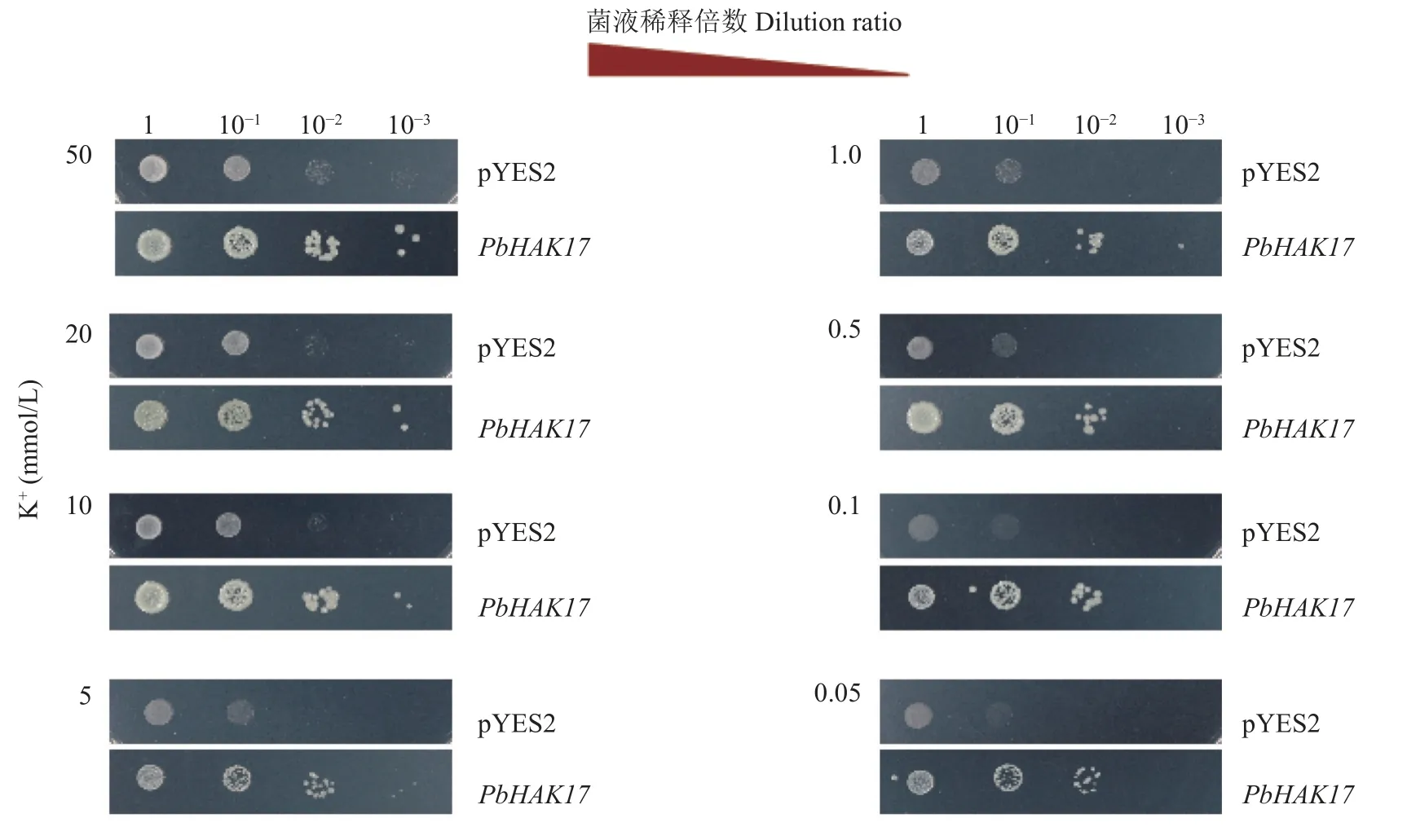
图7 PbHAK17 和pYES2 在不同钾供应浓度下的生长Fig.7 Growth of PbHAK17 and pYES2 under different potassium ion concentrations
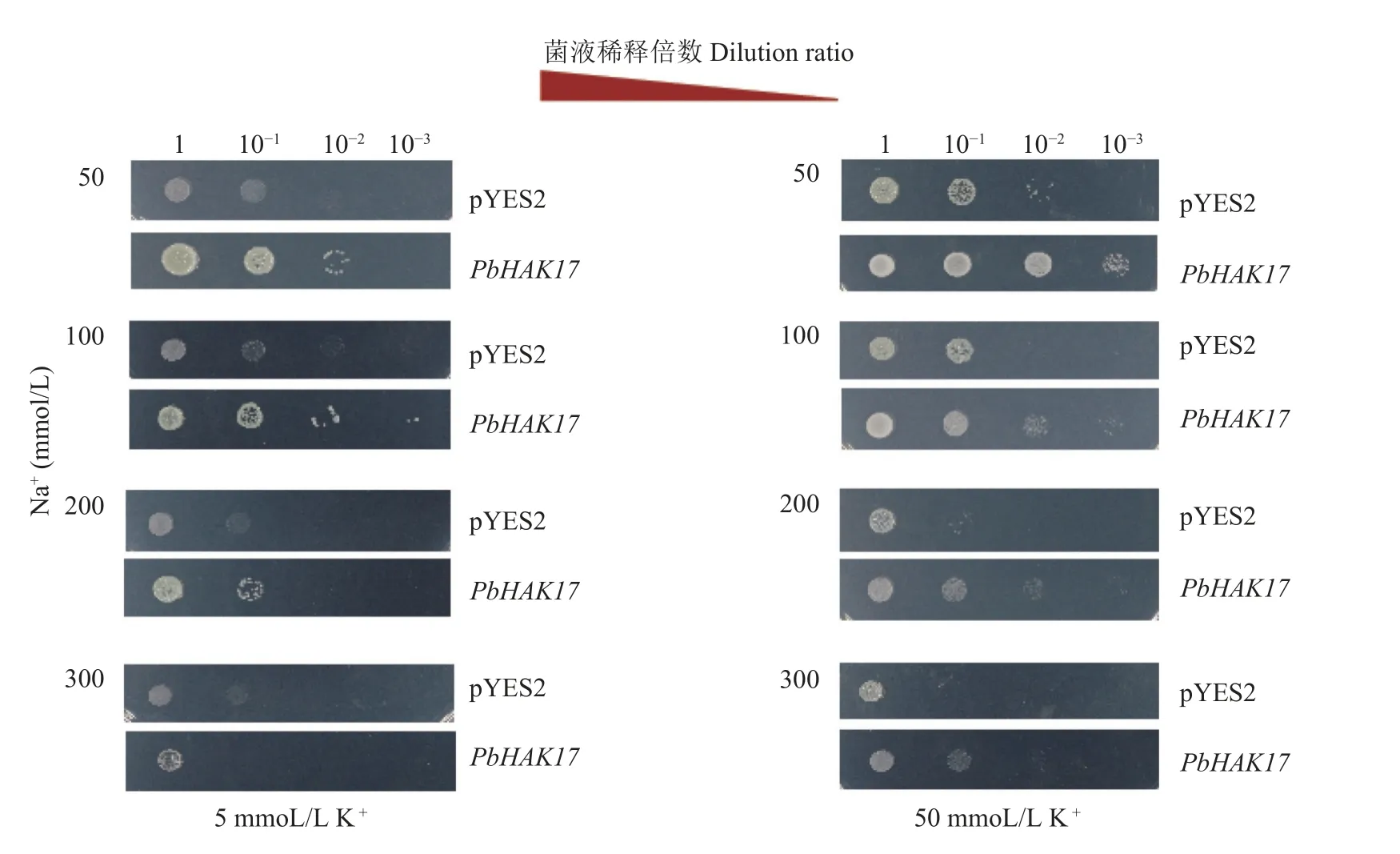
图8 PbHAK17 和pYES2 在不同Na+胁迫浓度下的生长Fig.8 Growth of PbHAK17 and pYES2 under different Na+ stress concentrations
2.7 PbHAK17 阳性植株PCR 鉴定
取T2 代拟南芥叶片提取基因组DNA,以其为模板进行PCR 检测,图9 的DNA 检测结果表明,PbHAK17已经成功转入转基因株系中,可用于下一步功能研究。
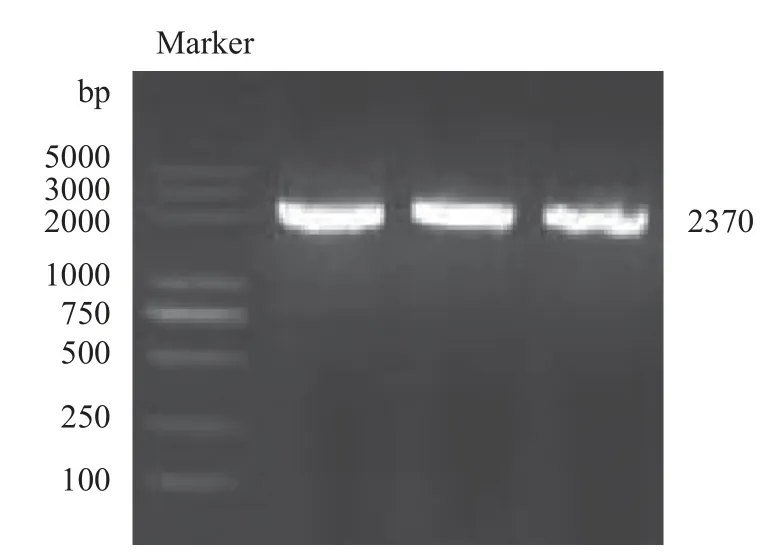
图9 PbHAK17-OE 转基因拟南芥苗DNA 的PCR 检测图Fig.9 PbHAK17-OE detection DNA PCR transgenic Arabidopsis seedlings
2.8 钾钠胁迫对超表达PbHAK17 拟南芥植株生物量的影响
如图10A所示,适钾(+K)和缺钾(-K)处理后,PbHAK17转基因拟南芥株系明显比野生型拟南芥生长更加健壮,莲座叶片大且多,缺钾使野生型拟南芥生长受到抑制。在0、50、200 mmol/L 浓度盐处理后,随着盐浓度的增加,植株生长均逐渐变差,野生型拟南芥在200 mmol/L NaCl 下叶片萎蔫严重且失绿,PbHAK17转基因株系生长虽然受抑制,但仍可正常生长,表明PbHAK17转基因株系对盐胁迫有更强的耐受性。如图10B所示,在适钾供应(3 mmol/L K+)下,随着盐浓度的增加,PbHAK17转基因拟南芥和野生型拟南芥干重均下降,但野生型拟南芥干重下降更明显。
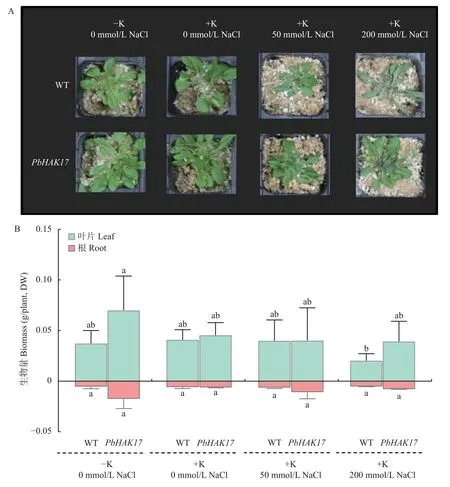
图10 不同钾钠水平下PbHAK17 超表达拟南芥的生长(A)及生物量(B)Fig.10 Growth(A)and biomass(B)of PbHAK17 overexpressing Arabidopsis thalian under different K+ and NaCl concentrations
2.9 钾钠胁迫对PbHAK17 超表达拟南芥植株钾钠积累量和钾钠比的影响
缺钾条件下,相比野生型拟南芥(WT),PbHAK17超表达拟南芥(PbHAK17-OE)叶片、根中K+积累量显著提高9%、24%(图11A,B),说明PbHAK17基因可以调控缺钾胁迫下根对K+的吸收。而适钾水平下,随着盐处理浓度增加,相比野生型拟南芥,PbHAK17-OE 拟南芥叶片中K+积累量分别显著提高0.61、0.42、1.75 倍(图11A),PbHAK17-OE 拟南芥根中K+积累量分别显著提高0.60、0.47、2.39 倍(图11B),表明PbHAK17基因可以提高植株对盐胁迫的耐受性。随着盐浓度的增加,野生型拟南芥和PbHAK17-OE 拟南芥的Na+积累量均提高,在0 mmol/L NaCl 时,野生型拟南芥叶中Na+积累量是PbHAK17-OE 拟南芥的1.88 倍,在200 mmol/L NaCl 时,PbHAK17-OE 拟南芥叶中Na+积累量是野生型拟南芥的1.56 倍(图11C),在50 mmol/L NaCl时,野生型拟南芥根中Na+积累量是PbHAK17-OE拟南芥2.11 倍(图11D)。K+/Na+随盐胁迫的增加而降低,在叶中PbHAK17-OE 拟南芥 K+/Na+分别是野生型的3.06、1.53、1.75 倍,在根中PbHAK17-OE 拟南芥K+/Na+分别是野生型拟南芥的2.85、3.06、2.97倍(图11E,F)。因此,PbHAK17在耐盐胁迫过程中提高了 K+的积累量,提升K+/Na+,使PbHAK17-OE拟南芥具有更强的抗盐能力。
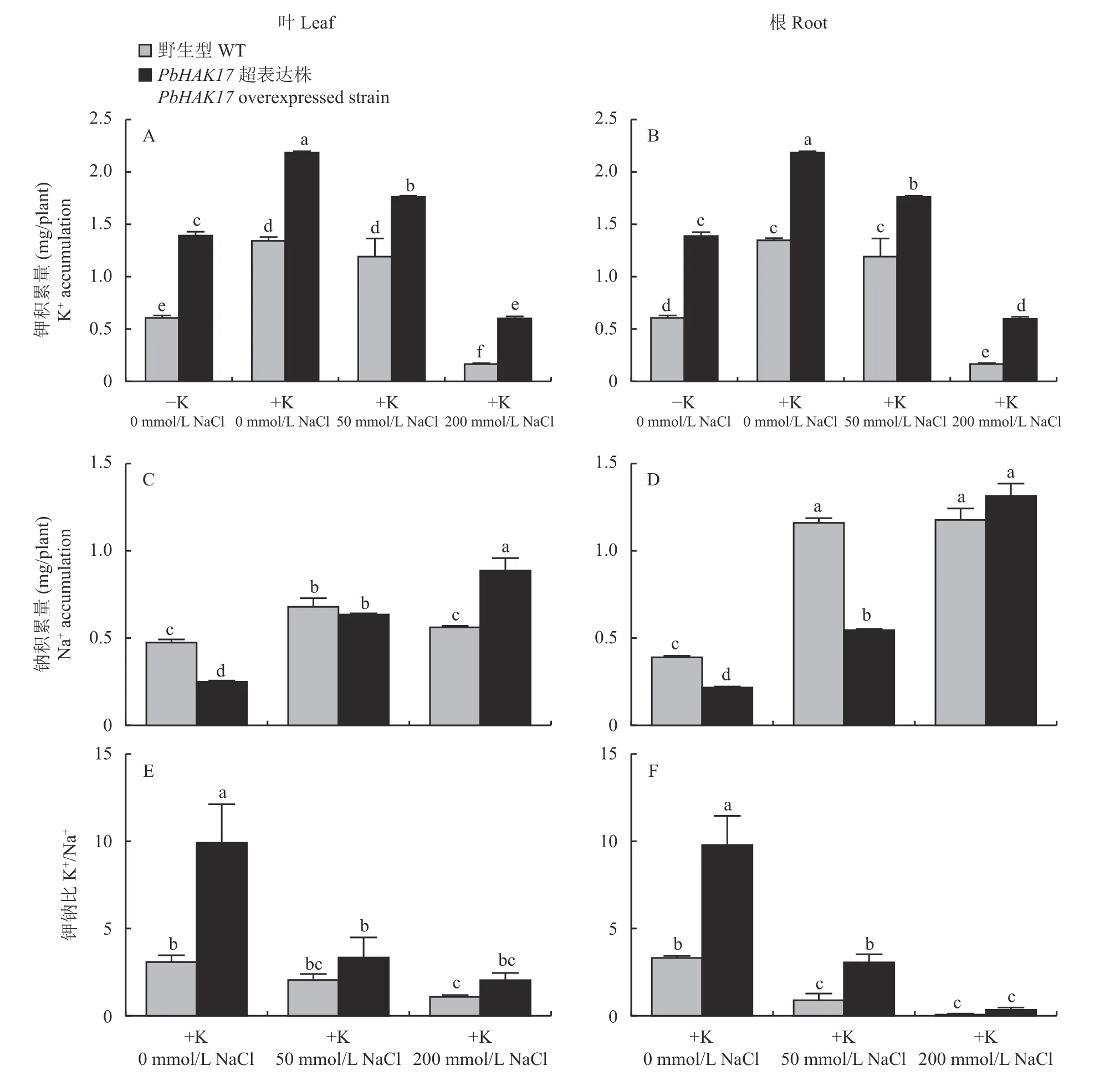
图11 不同钾和盐胁迫水平下PbHAK17 超表达拟南芥叶片和根中的钾钠积累量及钾钠比Fig.11 K and Na accumulation and the K/Na ratio in leaves and roots of PbHAK17 overexpressed Arabidopsis thaliana under different K+ and NaCl stress levels
3 讨论
3.1 PbHAK17 基因具有钾吸收和转运的功能
植物体内钾转运体HAK/KUP/KT 家族在维持细胞内阳离子的平衡中发挥重要作用,可以促进根系对钾的吸收和转运,从而加强植物对逆境胁迫的适应能力[25]。HAK/KUP/KT 家族成员在结构上具有12~13 个跨膜结构域并且在第二和第三跨膜结构域之间具有一个较长的胞质环[26],对PbHAK17基因在线分析跨膜结构域可知,与 HAK/KUP/KT 家族跨膜结构一致。本研究中,钾转运体基因PbHAK17定位于质膜,与 HAK/KUP/KT 家族已有研究结果具有一致性,推测PbHAK17基因在质膜上发挥钾离子的吸收与转运功能。杜梨PbHAK17受缺钾诱导表达,且在根中表达量最高,为高亲和性钾转运体家族成员。R5421酵母缺陷型菌株为钾吸收缺陷型菌株,可根据其独特的生长特性和简单的细胞结构验证目的基因是否具有钾吸收转运的功能。水稻OsHAK1、OsHAK5、OsHAK7、OsHAK10等基因钾吸收和转运功能均在R5421 酵母突变体中得到验证[27-28]。本研究中,PbHAK17酵母转化子在低钾培养基上可恢复钾吸收缺陷型酵母的生长,表明其具有钾素吸收的功能,且PbHAK17对低钾胁迫更敏感。与水稻OsHAK5研究结果相似,在低钾或缺钾下OsHAK5过表达转基因水稻株系能促进钾离子的吸收及向地上部的转运[27],由此推测PbHAK17作为拟南芥和水稻HAK5的同源基因也具有促进钾吸收和利用功能。但是,AtHAK5和OsHAK5对Na+的敏感性具有显著差异[28-29],表明该基因在不同植物的耐盐性方面具有不同的功能。
3.2 PbHAK17 基因具有提高植株耐盐性的功能
植物根系没有针对Na+吸收的专一性的转运蛋白,而Na+进入植物根系细胞一般是通过非选择性离子通道来完成的[26-27]。植物提高耐盐性的重要策略之一是通过增加对钾离子的吸收和减少对钠离子的吸收,维持K+/ Na+稳态[28]。拟南芥中AtHAK5受缺钾调控表达量显著上调,在盐胁迫处理下表达量虽然降低但仍高于适钾处理;突变体athak5植株的生物量显著低于野生型植株,表明AtHAK5在低钾下可以提高拟南芥对盐胁迫的耐受性[29]。水稻在50 mmol/L NaCl 处理下显著抑制了低钾诱导的OsHAK1的上调表达,但仍显著高于正常供钾下的表达量。本研究中缺钾下进行不同程度的盐胁迫导致PbHAK17的表达量在6 h 内均随盐浓度的增加而增加,且高于适钾下的表达量[23],这与水稻的研究结果一致,表明高盐胁迫下,增强钾转运蛋白基因的表达,提高植株钾吸收和积累是提高植株耐盐能力的重要手段[24,30]。本研究中PbHAK17酵母转化子在外源施钾0.05~50 mmol/L 条件下,NaCl 均不能抑制其生长,也表明PbHAK17可提高酵母的耐盐能力。长时间高浓度的NaCl 胁迫不仅导致离子毒害及细胞内离子失衡,从而造成营养缺乏,还可能使植物受到更大程度的渗透胁迫,使叶肉细胞严重失水,气孔关闭[31],而K+在盐碱环境下的特殊调控模式可以增加植物的耐受性[32-33]。OsHAK5基因超表达能够促进水稻在高盐(100 mmol/L NaCl)胁迫下的生长,其机理是通过对 K+的选择性吸收,提高植株地上部 K+/Na+,从而提高抗盐能力。在本研究中,50 和200 mmol/L NaCl 处理下拟南芥随盐胁迫强度增加生长受到抑制,但PbHAK17转基因拟南芥的长势要明显优于野生型拟南芥,PbHAK17-OE 拟南芥 K+积累量高于野生型拟南芥,说明PbHAK17可介导盐胁迫下 K+吸收,在50 mmol/L NaCl 低盐胁迫处理下PbHAK17-OE拟南芥Na+积累量较野生型拟南芥少,在 200 mmol/L NaCl 高盐胁迫处理下PbHAK17-OE 拟南芥Na+积累量反而较野生型拟南芥多,说明PbHAK17在高盐胁迫下不能抑制 Na+吸收,主要是通过吸收并向地上部转移更多的K+,使植株维持较高的K+/Na+以应对盐胁迫。
4 结论
杜梨钾转运体基因PbHAK17定位于细胞质膜上,该基因在适钾和缺钾条件下主要在根中强烈表达,介导根系对钾的吸收。盐胁迫下超表达PbHAK17增强了转基因拟南芥根系的K+/Na+和耐盐性。PbHAK17酵母转化子在低钾和盐胁迫下均可恢复钾吸收缺陷型酵母的生长,证明了该基因同时具有提高植物钾素吸收和耐盐能力的功能。
