有机酸提高土壤植酸生物有效性的机制、影响因素及应用
2023-12-25曹兴圆艾雯妍文思颖杨晓莉
曹兴圆,艾雯妍,文思颖,杨晓莉,刘 雪
(西南林业大学生态与环境学院,云南昆明 650224)
磷是植物必需大量元素,亦是不可再生资源[1-3]。植物生长发育所需磷素90%以上来源于土壤磷库[4-5],因此土壤中磷含量与供给直接影响植物生长和农业生产[6]。土壤中磷包括无机磷和有机磷,其中无机磷主要为铁、铝、钙结合的磷酸盐[4,7],不仅溶解度低、易被土壤固相吸附[8],且经微生物作用后可转化为有机磷,导致溶解性和生物可利用性降低[9],植物全可直接利用的正磷酸盐只占土壤总磷的约1%[10]。有机磷是土壤磷的重要组成部分,占比20%~80%[2],经矿化分解可转化为易被植物吸收利用的无机磷,是植物生长所需磷素的重要来源[11-12]。土壤中有机磷主要以植酸(肌醇六磷酸,C6H18O24P6;myo-inositol hexakisphosphate,IP6)及其盐类形式存在,土壤中植酸占有机磷的50%~80%[13-14],是植物磷素的潜在储备库。然而,植酸由于强吸附和难溶解性,难以被植物直接吸收利用。虽然植酸可被专一性酶—植酸酶(myo-inositol hexakisphate phosphohydrolase)矿化水解,经脱磷酸化过程释放无机磷供植物吸收,但水解反应发生的前提是植酸以有效态形式进入土壤溶液[13]。
为提高土壤中植酸的生物有效性,植物和微生物可分泌有机酸对根际土壤进行酸化、解吸附或络合植酸盐中的金属离子进而溶解植酸盐[15-17],使植酸以有效态形式进入土壤溶液,促进植酸与植酸酶的接触和反应,从而水解植酸释放磷,提高土壤植酸磷的利用效率[9,15]。土壤中有机酸来源于植物根系和微生物分泌物,亦可在土壤动植物残体等有机质降解、转化过程中产生[12,18-20]。为进一步探明土壤中植酸与有机酸的相互作用,本文在总结土壤植酸和有机酸的来源、种类与含量的基础上,重点阐述有机酸对土壤植酸活化作用的影响因素、作用机制及其潜在应用。综述内容为提高土壤内源磷—植酸的生物有效性和利用率提供理论依据和技术参考,对保障农业生产、降低外源磷肥施用及降低磷污染风险具有一定的现实意义。
1 土壤植酸
1.1 土壤植酸的来源、形态与溶解性
1.1.1 土壤中植酸的来源与含量 植酸作为含磷天然有机化合物,广泛存在于种子和根茎中,以种子中含量最高[21]。豆科植物的种子、谷物的麸皮和胚芽(如米糠、油菜籽等)中植酸含量较高,主要以钙镁复盐形式存在[22],禾本科植物特别是水稻(Oryza sativa)和玉米(Zeamays)中植酸磷含量可达总磷的75%~80%[23-24],占有机磷的90%~100%[14,25-27]。
土壤中植酸主要来源于动植物残体分解[4]和土壤中微生物转化[28]。此外,单胃动物如猪、鸡等消化系统中缺乏植酸酶,进食富含植酸的谷物饲料后,植酸不能被消化分解,进而随粪便进入土壤[29-30],故单胃动物粪便亦是土壤植酸的重要来源,特别是大量、频繁施用农家肥的农田土壤[4,25,31]。
土壤有机磷是土壤磷的重要组成部分,约占土壤全磷的20%~80%[32],包括肌醇磷酸、磷脂类、核酸类、磷蛋白、微生物磷和卵磷脂等磷脂化合物[12,14]。其中,肌醇磷酸及其盐的含量最高,约占有机磷的50%[13]。肌醇磷酸的羟基被磷酸基团取代形成6 种肌醇磷酸酯(IP1-6),其中肌醇六磷酸(IP6)含量最高,占比约83%。在肌醇六磷酸的4 个立体异构体(myo-、neo-、scyllo-、D-chiro-IP6)中,植酸(myo-IP6)含量最高,占比约56%~90%[33-34]。例如,智利某区土壤植酸含量为674 mg/kg,占有机磷的42%~67%[35]。
1.1.2 土壤中植酸的形态、稳定性与生物有效性植酸分子因其肌醇环上含有12 个可解离质子和6个磷酸基团而具酸性和强络合能力,导致其易被土壤矿物、有机质吸附或与钙、镁、铁、铝等金属离子形成难溶性或不溶性络合物,亦可与蛋白类物质形成配合物而在土壤中大量积累[25,36]。植酸在中性或碱性土壤中常以钙、镁复盐形式存在[12,15],在酸性土壤中则以铁、铝植酸盐形式存在[12]。此外,土壤对植酸的吸附显著高于无机磷和其他有机磷[37]。Shang等[38]研究发现,成土矿物表面对植酸的吸附率是无机磷的1.6 倍(1983 vs.1235 mg/kg),且矿物对植酸的等温吸附常数(K)表现为三水铝石(11.3)>高岭石(4.0)>针铁矿(2.5)>蒙脱石(2.0)。De Groot 等[39]发现,铁铝氧化物通过表面羟基与植酸中的磷酸基团发生置换[40-42],进而对植酸产生强吸附作用[4,39],其中针铁矿和三水铝石对植酸的饱和吸附量分别可达1818 和294 mg/kg[39],且吸附率随铁铝氧化物含量的升高而升高[43]。
关于植酸盐络合物稳定性的研究前期已有大量报道,但目前尚无统一定论。例如,冯屏等[44]认为土壤中植酸与金属离子形成络合物的稳定性顺序为Co2+(logK=15.27)>Ni2+(logK=14.92)>Cu2+(logK=10.91)>Ca2+(logK=10.87)>Mg2+(logK=10.53),Bretti 等[45]认为Co2+>Mn2+~Fe2+>Ag+,而Cigala 等[46]则认为Cu2+>Ni2+>Co2+>Fe2+>Mn2+。另外,在水溶液中矿物对植酸盐的溶解效率表现为:磷铝石(logKsp=-21.0)>红磷铁矿(logKsp=-26.0)[47]。不同类型土壤中植酸的存在形式及生物有效性存在差异。酸性土壤中植酸被铁/铝氧化物表面吸附,以植酸铁盐或植酸铝盐形式存在[48-49]。土壤pH 为4.5 时,植酸被伊利石和高岭石强烈吸附,吸附量达0.39 μmol/m2[4]。在吸附过程中,植酸分子中的2 个磷酸基团与硅酸盐结合,剩余的4 个磷酸基团可增加矿物表面负电荷。在碱性土壤中,植酸通常被黏土矿物、碳酸钙和有机质吸附[4,50],其中,蛭石、蒙脱石对植酸的吸附较强,吸附量分别达8.8 和10.0 mg/g[51],Ca-P 是碱性土壤中植酸磷被吸附固定后的主要存在形式[52]。
1.2 土壤中植酸生物有效性的影响因素
土壤中植酸的移动性和生物有效性受土壤矿物/金属氧化物类型、吸附方式和土壤性质等因素的影响。植酸被吸附的程度与土壤矿物或金属氧化物类型密切相关。黏土矿物如方解石[53]、伊利石、高岭石、蒙脱石[54]、针铁矿[55-56]、赤铁矿[57]等对植酸的吸附存在差异,其活性铁铝氧化物含量越高、羟基等结合位点越多则吸附作用越强[53-57],如勃姆石(γ-AlOOH)、蒙脱石{(Na,Ca)0.33(Al,Mg)2[Si4O10](OH)2·nH2O}、三水铝石[Al(OH)3,Al2O3占比65.4%]对植酸的吸附量(pH=4 时)分别为12、7、1 mg/g。矿物的晶体结构、比表面积亦影响植酸的吸附量。通常情况下,铁铝氧化物结晶度越低,则表面吸附容量越高[58-61]。弱晶质矿物由于其结晶度较低而比晶质矿物对植酸的吸附能力更强[62]。此外,弱晶质水铁矿对植酸的表面吸附方式随植酸浓度升高而由络合转化为表面沉淀,使植酸的生物有效性进一步降低[63]。矿物对植酸的饱和吸附容量与矿物比表面积呈正相关,勃姆石和赤铁矿的比表面积分别为114.6 和32.6 m2/g,其饱和吸附容量分别为65.3 和19.9 μmol/g[64],植酸除通过表面络合作用在土壤矿物表面形成植酸盐络合物[65],亦可通过铁/铝离子的桥键作用被有机质吸附固定[66],因此,吸附量亦与金属氧化物中铁铝含量有关。
土壤中植酸的生物有效性还受土壤吸附方式(配体交换、桥键作用、表面沉淀等)的影响。研究发现,植酸在无定形氢氧化铝(AAH)表面的吸附量较高,该强吸附可归因于吸附方式由表面络合转化为表面沉淀[64]。该过程中,植酸首先通过配体交换(表面水基和羟基)吸附在AAH 表面,形成内圈络合物,随后诱导AAH 溶解产生Al3+,进一步与植酸的磷酸基团络合形成三元络合物,并逐渐转化为表面沉淀[64]。这种表面络合-沉淀反应强烈影响土壤对植酸的吸附作用及其赋存形态和环境行为,最终影响其移动性和生物有效性[64]。此外,不同粒径铁铝氧化物对植酸的吸附方式差异导致其吸附能力差异。例如,5 nm γ-Al2O3对植酸的表面吸附密度(1.32 μmol/m2)高于35 nm 和70 nm γ-Al2O3( 分别为0.97和0.89 μmol/m2),原因是植酸在较小粒径γ-Al2O3表面的吸附除形成内圈络合物外,亦生成了植酸-Al 表面沉淀[64]。
此外,土壤中植酸盐的生物有效性与其自身的稳定性密切相关。植酸盐稳定性的影响因素包括土壤pH、温度和有机质含量等[4,67]。土壤pH 及温度影响黏土矿物对植酸盐的吸附。通常,酸性土壤的吸附量随pH 升高而降低。一方面,酸性土壤中正电荷数随pH 升高而减少[1,12],导致静电斥力增强,从而对磷酸根的吸附降低。此外,当pH 较高时,土壤中磷的释放以离子交换为主,OH 离子可取代植酸盐,使吸附降低。例如,pH 从3 提高至10 时,针铁矿对植酸的吸附量降低47%[56];pH 由3 提高至5 时,赤铁矿对植酸的饱和吸附浓度由0.95 μmol/m2降至0.67 μmol/m2,pH=10 时降至0.38 μmol/m2[58]。Chen等[68]研究亦发现,pH 从5 提高至8.5 后,水铁矿对植酸的吸附量降低25%~61%。若pH 恒定,温度变化亦导致植酸吸附量的改变。pH=6 时,温度由4℃升至55℃,三水铝石对植酸的吸附量由0.47 μmol/m2提高至0.52 μmol/m2;pH=10 时,吸附量则随着温度的升高(4℃ vs.55℃)而降低(0.41 vs.0.35 μmol/m2)[69]。这是由于较高pH 时吸附以外圈络合吸附方式为主,而在较低pH 时,内圈络合和表面沉淀占主导地位,同时热力学参数表明内圈络合物的形成为吸热过程,而外圈络合物则相反[69]。李修臣[25]研究发现,当温度在一定范围内(5℃~25℃)变动时,3 种土壤(红壤、褐土和灰潮土)对植酸的吸附率均随温度升高呈线性升高,并在25℃达到峰值;而温度过高(>25℃)时,吸附率则随温度升高而降低。此外,温度亦在一定程度上影响植酸的络合能力[70]和铁铝氧化物对植酸的吸附速率。刘西德等[71]研究表明,植酸的络合作用受温度影响较大,一定范围内(20℃~60℃)温度越高则络合能力越强。同时,加热时间对络合作用亦有一定影响。同一温度下,加热时间越长,络合反应进行越充分,则植酸盐产物的稳定性越高,生物可利用性越低。此外,植酸的生物有效性随土壤有机质含量升高而降低。例如,McKercher等[50]研究发现,有机质含量为10%的Melfort 土壤对植酸的吸附量(2.5 mg/g)远高于有机质含量4.5%的Sceptre 土壤(0.9 mg/g),即Melfort土壤植酸的生物有效性低于Sceptre 土壤。
2 土壤有机酸
土壤对植酸盐具有极强亲和力,导致土壤中的植酸盐难以直接被植酸酶分解,不利于植酸盐分解产生磷和肌醇供植物吸收利用[72]。有机酸和酚酸可通过解吸或溶解植酸盐提高其生物有效性和可利用性,其中,有机酸是主要贡献因子[73-74]。
2.1 土壤中有机酸的来源与种类
土壤有机酸主要来源于植物根系和微生物分泌物,或产生于土壤动植物残体等有机质的降解、转化过程[12,20-22]。植物和微生物经长期进化产生了一系列的适应机制提高对土壤磷的获取能力[39,75-77]。植物根系和微生物通过分泌有机酸促进自身对土壤植酸磷等化合物的活化利用[16,78,79],常见有机酸包括甲酸、乙酸、草酸、乳酸、酒石酸、琥珀酸、苹果酸和柠檬酸等[78-80]。植物和微生物分泌有机酸的种类和数量因其种类、遗传特性和环境条件而异,一些植物分泌有机酸的种类见表1[81-92]。例如,无芒隐子草(Cleistogenessongorica)可分泌油酸、邻苯二甲酸和棕榈酸;冷蒿(ArtemisiafrigidaWilld)分泌邻苯二甲酸;银灰旋花(Convolvulusammannii)根系可分泌油酸、邻苯二甲酸、棕榈酸和琥珀酸[86]。辐射松(Pinusradiata)在石灰性土壤中分泌柠檬酸、草酸及马来酸[89]。水稻根系主要分泌酒石酸等,小麦(Triticum aestivum)根系主要分泌草酸、乙酸和丙酸等[82-83]。同一植物在不同营养条件下分泌的有机酸种类及含量亦存在差异。如白羽扇豆(Lupinusalbus)缺磷时排根区分泌的柠檬酸含量是磷充足时的1.9 倍[85]。此外,根系不同部位的功能及作用亦影响分泌有机酸的种类[79]。研究发现,土壤缺磷时白羽扇豆根系分泌的苹果酸主要源于根尖5 mm 的非根毛区,而柠檬酸主要源于逆境形成的簇状排根区[79]。耕作方式亦对植物分泌有机酸产生影响。与单作相比,间作使续断菊(Sonchusasper)根系分泌物中草酸、柠檬酸、乙酸、苹果酸和乳酸含量提高29.3%~260%,使琥珀酸含量降低58.5%~76.4%,且这种改变在土培(有机酸总量增加9.7%~43.3%)与水培条件(有机酸总量增加22.6%~103%)下亦存在差异[87]。镉胁迫下,长白落叶松(Larixolgensis)幼苗根系分泌的有机酸含量和种类均增加,且在一定胁迫程度和胁迫时长内,有机酸总量随胁迫程度提高而增加至最大值后又逐渐降低[88](表1)。黄建凤等[79]研究发现,植物根系分泌的有机酸含量与其所处的土壤条件密切相关,如缺铁土壤中,大豆(Glycinemax)、花生(Arachis hypogaea)等作物根系分泌的柠檬酸含量可达正常状态下的5~10 倍[93]。

表1 部分植物根系分泌物中的有机酸种类与含量Table 1 Organic acid species and concentrations in some plants root exudates
植物根际土壤存在大量可分泌有机酸[94]并溶解难溶性磷[95-97]的真菌和细菌。微生物因种类、遗传特性差异,其分泌的有机酸种类和含量差异显著(表2)[98-108]。如黑曲霉(Aspergillusniger)在含磷培养基中分泌苹果酸的量(182 mg/L)显著高于琥珀酸(4.8 mg/L)[107]。Nahas[109]研究了42 种土壤细菌和真菌溶解磷矿和磷酸钙的能力,发现在特定条件下矿物溶解度与微生物产酸量呈正比,且产酸量和溶磷能力取决于微生物种类和磷酸盐类型,例如,以天然磷矿为磷源时细菌产酸量更高,以磷酸钙为磷源时则芽孢杆菌属(Bacillus)的产酸量更多。但目前关于产酸微生物对植酸盐溶解能力的研究仍较少。按分泌有机酸的种类可将微生物分为醋酸生产菌(如醋酸杆菌属和葡糖酸杆菌属等)、乳酸生产菌(如乳杆菌属和片球菌属等)、柠檬酸生产菌(如青霉属和毛霉属等)等。土壤中可分泌有机酸的细菌主要为变形菌门(Proteobacteria)和放线菌门(Actinobacteria),变形菌门中多为α-变形菌纲(Alphaproteobacteria),少量为β-变形菌纲(Betaproteobacteria)和γ-变形菌纲(Gammaproteobacteria),包括微枝形杆菌属(Microvirga)、假单胞菌属(Pseudomonas)、新鞘脂菌属(Novosphingobium)、链霉菌属(Streptomyces)和鞘脂单胞菌属(Sphingomonas)等29 个属[110]。土壤中可分泌有机酸溶解植酸盐的真菌主要为外生菌根真菌[103,111],如彩色豆马勃(Pisolithustinctorius)、硬皮马勃(Scleroderma)等[102-103],主要分泌的有机酸为草酸[102]。部分微生物分泌或代谢、发酵产生的有机酸种类如表2所示[98-108]。

表2 部分微生物及其有机酸种类与含量Table 2 Organic acids species and concentrations in microbial secretions
2.2 土壤中有机酸种类和含量的影响因素
土壤中有机酸种类和含量受植被类型、土壤类型和土壤理化性质等影响。5 种植被类型土壤中有机酸含量表现为:乔木(0.375 cmol/kg)>灌木(0.2 cmol/kg)>农田(0.18 cmol/kg)≈草本(0.175 cmol/kg)>弃耕地(0.065 cmol/kg)[111]。乔木植被凋落物较多,凋落物分解叠加植物根系和微生物有机酸分泌,因而土壤中有机酸含量较高。农田土壤由于施肥、作物秸秆覆盖等使有机质含量较高,有机质分解产生大量有机酸,而弃耕地土壤裸露,有机质矿化作用较弱,因此农田土壤有机酸含量显著高于弃耕地[111]。不同植被类型土壤中有机酸种类亦存在显著差异,乙酸普遍存在于各类植被土壤中,乔木593 μg/kg、农田558 μg/kg、灌木554 μg/kg、草本378 μg/kg、弃耕地243 μg/kg。除农田土壤外,柠檬酸在其余4 种植被类型土壤中均被检出,酒石酸仅在乔木植被土壤中检出,且苹果酸含量亦较少,可能与植被类型和微生物分解有关[111]。例如,喀斯特地区石灰岩森林植被类型原生林中檵木(Loropetalumchinense)、紫弹树(Celtisbiondii)和青檀(Pteroceltistatarinowii)根际土壤中,草酸含量显著高于灌木林中红背山麻杆(Alchorneatrewioides)、小蜡(Ligustrumsinense)和深紫木蓝(Indigoferaatropurpurea)根际土壤中的草酸含量(204 vs.84.9 μg/kg)[112]。
土壤类型[82-83]及土壤理化性质(土壤有机质含量、pH、土壤通气状况和土壤温度等)均影响土壤有机酸的种类与含量[12,113-114]。研究发现,植物根系分泌有机酸量与土壤有机碳和全氮含量呈正相关[112]。例如,在有机碳(150 vs.128 g/kg)和全氮含量(7.45 vs.5.86 g/kg)更高的土壤中,测得的草酸含量更高(204 vs.84.9 μg/kg)[112]。通过土壤有机质分解产生有机酸的量受有机质全碳含量的直接影响,如大豆秸秆(全碳含量403 g/kg)经腐解产生的乙酸(1.59 g/kg)是玉米秸秆(全碳含量373 g/kg)产生乙酸(0.41 g/kg)的4倍[115]。此外,土壤有机质通过影响微生物生长代谢活力影响其有机酸分泌[116]。通常,土壤有机质C:N质量比为25:1 时微生物活力旺盛,有机酸分泌速度加快。土壤pH 通过影响微生物活力及群落组成影响有机质的分解[117],进而影响有机酸的转化形成。真菌适宜pH=3~6 的酸性环境,大多数细菌适宜中性环境,放线菌则在微碱性条件下活性更高。例如,真菌分泌有机酸的能力与土壤pH 呈显著负相关,而细菌则无显著相关性[118]。土壤温度亦通过影响微生物活性及有机质矿化分解速率,进而影响有机酸的转化形成效率[4]。通常,0℃~35℃范围内,有机质分解速率随温度升高而加快,温度每升高10℃,土壤有机质最大分解速率提高2~3 倍,使土壤有机酸含量升高。土壤微生物活性的最适温度为25℃~35℃,超出该范围,微生物活性受明显抑制,有机酸分泌量降低。
此外,土壤有机酸含量亦受降水量和季节变化的影响。潘复静等[112]研究发现,植物根系分泌的草酸含量在雨季(755 μg/kg)高于旱季(143 μg/kg),苹果酸(1.58 vs.4.82 μg/kg)和乙酸(2.59 vs.13.3 μg/kg)则相反。曹莹菲[115]发现,土壤中乙酸含量随季节变化表现为冬季(1.3 g/kg)>春季(0.89 g/kg)>夏季(0.4 g/kg)>秋季(0.38 g/kg)。
3 有机酸活化土壤植酸的作用机制与影响因素
3.1 有机酸活化植酸机制
植物根系、细菌(假单胞菌、芽孢杆菌等)[119-120]和真菌(青霉菌属、曲霉菌属等)[121-122]分泌的有机酸(葡萄糖酸、草酸、柠檬酸等)[74]含有大量羟基和羧基等多种官能团,可通过配体交换、静电吸附、氢键、桥键作用和范德华力等多种方式[123-125]与土壤黏土矿物及金属氧化物发生反应,通过竞争吸附、络合反应、断裂有机质-金属架桥等过程提高植酸盐的溶解性和生物有效性[48,126](图1)。植酸作为一种磷酸单酯,其固定及释放的过程机制与正磷酸盐相似[13],因此可推测植酸盐的吸附-解吸、溶解-沉淀过程机制。植酸盐通过2 个或4 个磷酸基以内圈表面配合物的形式与土壤中铁氧化物(如针铁矿、铁水合矿)、铝氧化物(如薄水铝石、三水铝石)或黏土矿物的结合位点(如羟基)发生吸附[41-42,57]。
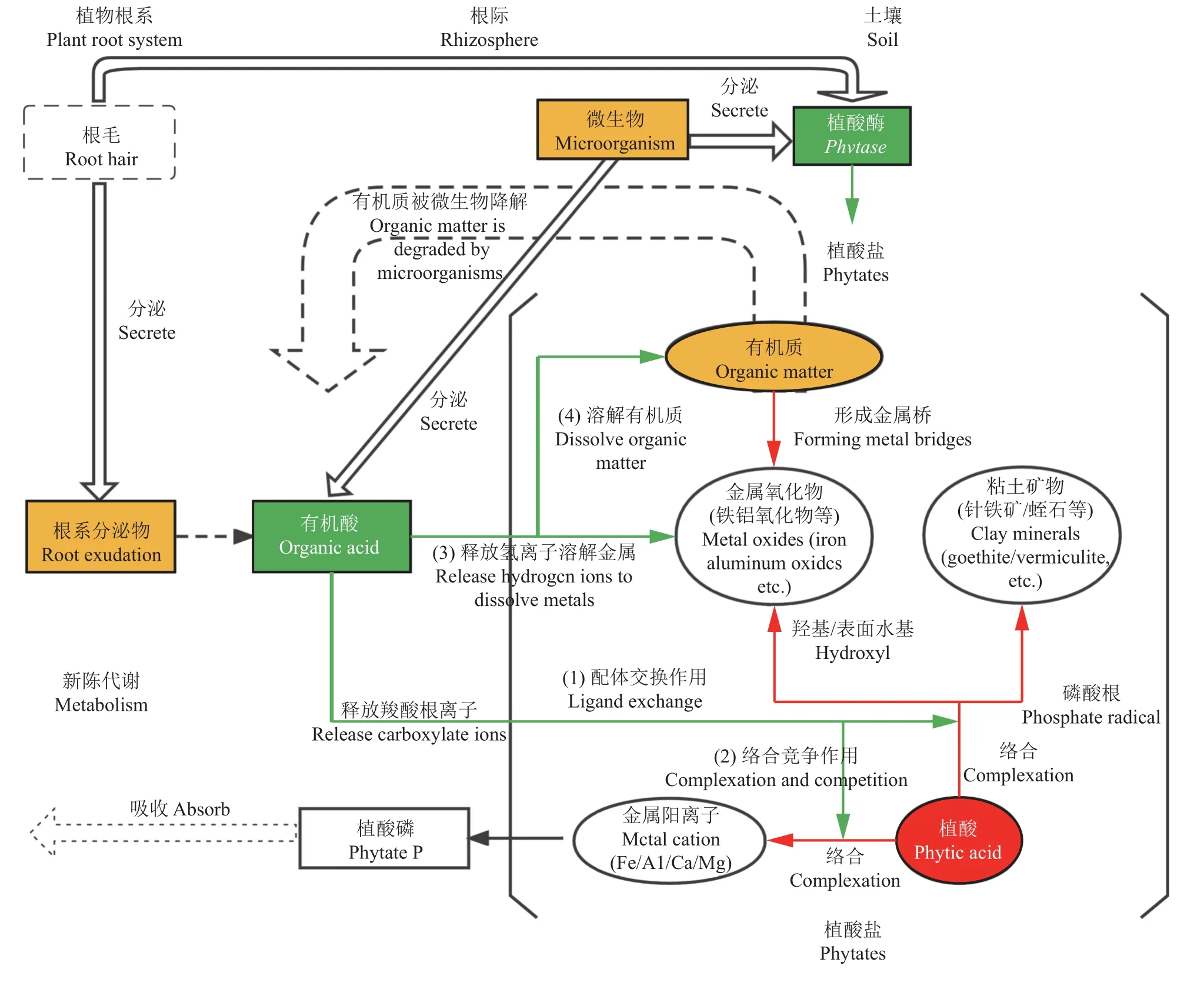
图1 土壤有机酸对植酸的活化机制Fig.1 Mechanism of organic acids-induced phytate mobilization in soils
有机酸对植酸盐的活化则通过竞争黏土和金属氧化物的吸附位点实现[127]。首先,有机酸可通过配体交换,以羧酸根取代土壤吸附的磷酸基团来解吸植酸[66]。Lindegren 等[128]发现,有机配体多重氢键的相互作用比与内圈表面配合物的配体交换作用更强,因此有机酸能与金属离子络合形成更稳定的金属配体复合物,不仅抑制土壤溶液中Al3+或Fe3+与植酸分子发生反应[129],提高植酸的生物有效性,同时有机酸经络合作用形成的金属络合物易被土壤吸附,可防止有机酸被微生物分解,从而促进有机酸对土壤中植酸盐的持续性溶解[130]。研究发现,有机酸如富里酸等通过对金属离子的络合作用,可抑制金属离子与植酸分子结合形成难溶性络合物或不溶性沉淀,进而提高土壤中植酸盐的溶解性和移动性[131]。其次,有机酸可通过氢离子溶解铁和铝,从而破坏其与植酸中磷酸基团的吸附位点,释放植酸分子,提高其活动性[66]。例如,柠檬酸不仅可通过配体交换取代被吸附的植酸分子,亦能使吸附表面负电荷增加[132],同时可促进金属氧化物溶解[133],从而促进植酸盐解吸。再者,有机酸可通过溶解有机质中的金属离子,断裂有机质-金属架桥,促进有机质-金属-植酸复合物的溶解[66],从而提高植酸的溶解性和生物有效性。最后,土壤溶液中的胶体腐殖质-Fe3+-植酸配合物扩散到根表后,Fe3+可被还原为Fe2+,使有机配合物的稳定性降低,从而使植酸从腐殖质中释放,提高植酸的生物有效性[13](图1)。
目前,动物饲料方面的研究发现,饲料中添加有机酸可降低动物消化系统的pH,使植酸酶的活性及利用率提高(数据未给出)[134-135]。由此可推测,土壤中有机酸含量增加导致土壤pH 降低后,亦能使植酸酶活性发生改变。但具体情况需结合土壤pH 的变化与植酸酶最适pH 综合分析。总的来说,根系释放的有机酸可以促进植酸盐活化,增加植酸的溶解度,进而促进植酸酶的水解效率,提高土壤中植酸的生物有效性,但有机酸与植酸酶相互作用的具体机制以及哪种方式活化作用更强仍需进一步探明。
综上,有机酸活化土壤植酸的主要途径包括:1)有机酸通过配体交换与植酸盐竞争结合位点,以羧酸等阴离子取代配体表面的磷酸基团,从而降低土壤矿物对植酸的吸附[12,48,136-137];2)有机酸与铁、铝、钙等金属离子发生络合反应形成复合物[12,48],将Fe-P、Al-P 和Ca-P 中的植酸磷释放,促进植酸盐的溶解[9,12,80,138];3)有机酸不仅可释放氢离子溶解金属氧化物,且在以可变电荷为主的土壤中,有机酸与土壤中的铁铝氧化物、铁铝水化物发生络合反应,使吸附表面负电荷增加,从而降低土壤对植酸盐的吸附[1,12,139];4)有机酸通过增溶有机质,断裂有机质-金属架桥,促进植酸以可溶性复合物形式存在,提高其溶解性(图1)。通常,有机酸对土壤植酸的活化是以上多种途径共同作用的结果[12],且有机酸诱导的植酸活化受植酸盐类型的影响[20]。
3.2 有机酸活化植酸的效率与影响因素
有机酸对土壤植酸的活化效率与土壤对植酸的吸附强度和有机酸的活化能力有关,故主要影响因素包括有机酸种类与浓度、土壤pH、土壤有机质含量、金属氧化物等(表3)[55,57,71,140-141]。
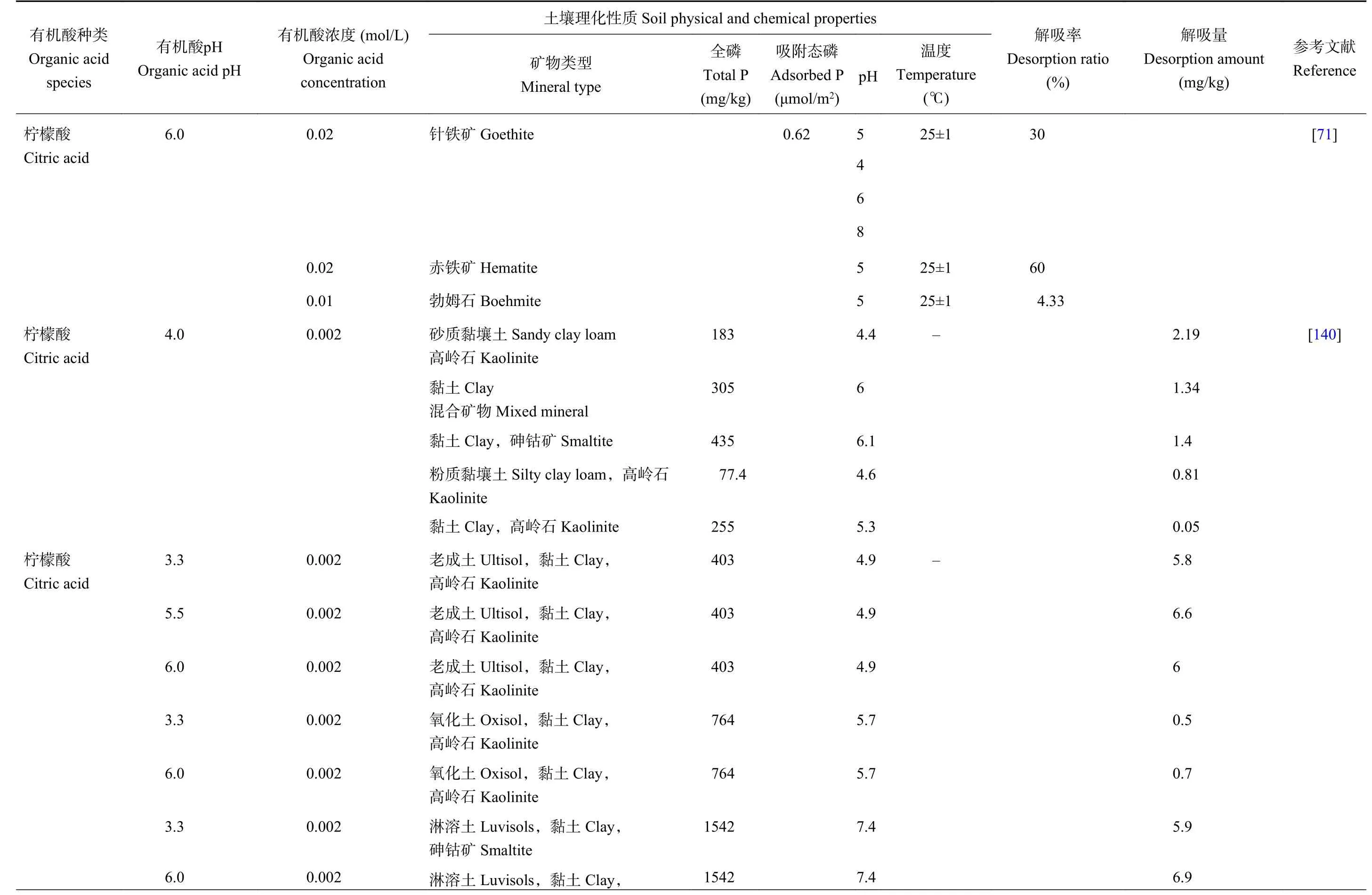
表3 有机酸对不同土壤/矿物中植酸的活化效率Table 3 Mobilization efficiency of phytate by organic acids in different soils or minerals
3.2.1 有机酸种类与浓度的影响 不同植物和微生物分泌的不同种类和数量的有机酸对土壤植酸的活化能力存在差异[74]。一般来说,有机酸对植酸活化作用的强弱顺序表现为三元羧酸>二元羧酸>一元羧酸[20],这与形成的有机酸络合物的稳定性呈正相关,如柠檬酸(logKAl=9.6)>草酸(logKAl=7.3)>乙酸(logKAl=1.5)[130,142]。柠檬酸对铁和铝的络合作用较好,因酸性土壤中植酸主要以铁盐、铝盐形式存在,故柠檬酸对酸性土壤中植酸的活化作用显著。例如,pH=5 时,0.02 mol/L 柠檬酸可活化60%被赤铁矿吸附的植酸[57,64],0.01 mol/L 柠檬酸可活化4.33%被勃姆石吸附的植酸[64]。Bolan 等[143]亦发现,对土壤(pH=5.6)中Ca-P 进行活化时,柠檬酸和草酸的活化率分别为88%和73%。同时,草酸对钙的络合作用较好,因碱性土壤中植酸主要以钙镁复盐形式存在,故草酸对中性和碱性土壤中植酸的活化作用较好[144]。乙酸作为一元羧酸溶解与植酸结合的金属离子而产生的活化效果则相对较弱[145]。对酸性黏土中植酸的活化效率表现为:柠檬酸(2.75 mg/kg)>草酸(0.75 mg/kg)>马来酸(0.33 mg/kg)[140]。
有机酸浓度通过影响配体交换反应速率从而影响对土壤植酸的活化效率[74,113]。植物根系释放的有机酸阴离子通量可影响配体交换反应速率,同时,若无等量阳离子流出或阴离子流入补偿以维持电中性,有机阴离子就无法从根细胞中持续流出[146],导致有机酸对植酸的活化效率降低。通常,有机酸浓度越高则对植酸的活化效率越高。以腐殖酸为例,随着初始浓度由37.5 mg/L 升至75 和150 mg/L,其对勃姆石吸附态植酸的解吸率由10.5%分别提高至17.5%和31.6%[147]。
3.2.2 土壤理化性质的影响
1)土壤pH 的影响 pH 影响土壤中植酸的赋存形态及有机酸与植酸的吸附竞争反应,进而影响有机酸对植酸的活化效率。一般情况下,有机酸对植酸的活化效率随pH 的升高而提高。例如,当柠檬酸溶液pH 由3.3 升至5.5~6.0 时,其对热带森林地区中性或弱碱性(pH=7.4)黏土中植酸的解吸量由5 mg/kg 提高至6.2 mg/kg,使弱酸性(pH=4.9)黏土中植酸的解吸量由5.8 mg/kg 提高至6.0~6.6 mg/kg[140]。类似地,Martin 等[55]发现,pH=4.5 时,柠檬酸对针铁矿表面植酸的解吸率是pH=3.8 时的1.7 倍(2.53%vs.1.47%)。但亦有研究发现,只有在较高的柠檬酸浓度(>1×10-4)和较低的pH(2.5~4.0)条件下,柠檬酸才可通过溶解针铁矿释放被吸附的植酸[62,148]。因此,当pH 由4.0 升至8.0 时,柠檬酸通过配体交换活化针铁矿表面吸附态植酸的速率随pH 升高而降低,解吸速率由0.12 μmol/(m2·h)降至0.05 μmol/(m2·h)[64]。此外,不同pH 条件下,土壤中铁铝氧化物和矿物的存在形态有显著差异,从而影响其对植酸的吸附强度和吸附效率[1,149]。通常,植酸在中性或碱性土壤中易被黏土矿物、碳酸钙和有机质吸附,而在酸性土壤中易与金属离子结合形成络合物[4,52]。不同类型土壤对植酸的吸附能力表现为:红壤(酸性)>褐土(弱碱性)>灰潮土(弱碱性)[25]。
pH 影响有机酸与植酸对吸附位点的竞争吸附,进而影响有机酸对植酸的活化效率[150]。静电作用方面,酸性土壤中矿物表面带正电,与植酸之间的静电引力作用更强,导致植酸的活化效率较低。随土壤pH 升高至超过零点电荷时,矿物表面负电荷增多,植酸和土壤胶体间的斥力增强,植酸与土壤的结合力降低[25],使有机酸更易与矿物表面结合,提高对植酸盐的活化效率。另一方面,植酸盐的P-O 基团可与矿物表面的羟基结合形成氢键而被吸附,这种方式下的吸附作用强度亦受pH 的影响。例如,Persson 等[151]发现,在较高pH 条件下(pH>8),未与Fe3+结合的P-O 基充当氢键受体,质子更靠近配位表面,不利于有机酸发挥解吸的活化作用。最后,pH 降低可提高产酸微生物的活性,提高有机酸的分泌量,进而提高对土壤植酸的活化效率。例如,降低pH 使黑曲霉(Aspergillusniger)产酸量提高,从而促进其对磷酸钙、氟磷灰石等矿物的增溶作用[152]。
2)土壤有机质的影响 磷在土壤剖面中的迁移特性与有机质含量有关[50],由此可推测有机酸对植酸的活化作用亦受有机质含量的影响。首先,有机质通过解离氢离子产生可变电荷[145],如有机质中羧基或羟基官能团中氢离子的解离可使有机质呈现净负电荷,不仅促进金属氧化物溶解,同时通过改变土壤pH 进而影响有机酸对植酸的解吸[153]。其次,土壤有机质带负电荷后可与植酸盐竞争土壤胶体或矿物表面的吸附位点,降低金属阳离子对植酸盐的吸附。
因此,可推测土壤中有机质含量越高,对植酸的吸附越强,有机酸对植酸的活化效率则越低。例如,McKercher 等[50]通过分析有机质含量差异显著的两种土壤对植酸的吸附效率,发现有机质含量为10%的土壤对植酸的吸附量是有机质含量4.5%土壤的2.8 倍(2500 vs.900 μmol/g)。
3)土壤矿物/金属氧化物的影响 金属氧化物表面通常带正电荷,植酸带负电荷,两者通过范德华力、表面配体交换、静电吸附、氢键和表面沉淀等作用方式发生吸附或形成络合物和沉淀。不同金属氧化物对植酸的吸附方式不同,不同作用方式影响有机酸对植酸的活化效率。研究发现,植酸分子的4 个磷酸基与针铁矿发生吸附,剩余2 个磷酸基为自由态,而与水铁矿和赤铁矿的表面吸附只通过2 个磷酸基发生[154-155]。柠檬酸对赤铁矿吸附态植酸的活化效率是针铁矿吸附态的2 倍(60% vs.30%)[64],可能是由于赤铁矿与磷酸根络合形成单齿双核络合物[156],而与针铁矿形成双齿双核络合物[157]。另外,金属氧化物的性质通过决定参与配位交换的磷酸基团数量从而影响吸附作用的强度[158-159]。结合的磷酸基团越多,形成化学键所需能量越高[159],因此吸附亲和力更小,活化效率更高。
金属氧化物的颗粒大小、比表面积及结晶度亦是影响有机酸对植酸活化效率的重要因素[1,160]。通常,矿物颗粒粒径越小,比表面积越大,则矿物与植酸的亲和力越强,越不利于有机酸对植酸的解吸和活化。粒径较大的矿物表面通常以表面络合方式吸附植酸,而粒径较小矿物表面不仅形成内圈络合物,亦可发生表面沉淀反应,导致对植酸的吸附能力提高,不利于有机酸对植酸的活化[64]。铁铝氧化物亦因其比表面积较大,因而比硅氧化物、钙镁氧化物等土壤组分具有更强的吸附能力,对控制植酸在土壤中的赋存形态和生物有效性具有重要作用[161]。因此,通过提高有机酸对铁铝氧化物的溶解作用,可提高对植酸的活化效率。此外,矿物对植酸的最大吸附量通常随矿物结晶度的增加而降低[58-60],即矿物结晶度越高,对植酸的吸附量越低,越利于有机酸对植酸的活化反应,解吸效率表现为晶质矿物>弱晶质矿物。一方面由于弱晶质矿物(如水铁矿和无定形铝)比晶质矿物(如赤铁矿和针铁矿)的羟基和活性吸附位点更多[60]。另一方面,亦与络合方式有关。Yan 等[60]发现,植酸在晶质矿物勃姆石表面主要形成内圈络合物,而在弱晶质的无定形铝表面可发生表面络合-沉淀反应,进一步降低植酸的生物有效性。
3.3 土壤有机酸活化植酸的潜在应用
有机酸被证明可直接用于土壤磷的活化,宋金凤等[162]研究了苹果酸对暗棕壤中磷有效性的影响。同样,土壤有机酸对植酸的活化作用可用于土壤改良,以保障农业可持续发展。有机酸的活化作用可提高植酸在土壤中的活动性和生物有效性,促进植酸与植酸酶的水解反应,催化植酸脱磷酸化速率,释放土壤内源植酸磷供植物吸收,从而减少不可再生磷矿资源的消耗,将对降低外源磷肥的施加以及土壤磷流失的潜在面源和水体污染风险[163],具有十分重要的社会经济和生态环境意义[164]。因此,未来研究可关注土壤中有机酸对植酸活化作用的实际应用效率与影响因素。
在产酸微生物方面,田间试验和温室试验表明,植物根系接种产酸真菌后,不仅可提高土壤中有效态磷含量,增加植物对植酸磷的吸收利用和作物产量,亦能在一定的土壤和气候条件下生产出性能更稳定的产酸真菌[142]。因此,可对产酸真菌进一步筛选,制成植物真菌菌剂,进一步促进作物对土壤植酸磷的利用和作物产量的提高。此外,有机酸可提高植酸酶活性和植物的抗氧化应激能力。Jin 等[165]研究发现,苹果酸使绿豆中植酸酶活性由22 U/g 提高至137 U/g,草酸使植酸酶活性由8.5 U/g 提高至90 U/g,分别是对照组的2.69 和1.58 倍。因此,后续可探究土壤中有机酸对植酸酶活性的影响。此外,真菌分泌的有机酸不仅能活化植酸,同时可作为营养物质供自身吸收。Vassilev 等[166]指出,培养基中黑曲霉(Aspergillusniger)等真菌在营养物质不足时,可利用其分泌的有机酸(如柠檬酸等)维持自身生命活动和产生孢子。
4 展望
植酸是土壤有机磷的主要组分和重要的磷素储存库。充分利用植酸这一磷素资源,尚需加强以下几方面的研究:(1)不同有机酸对不同类型土壤中植酸的活化效率,定量分析有机酸种类和浓度对土壤植酸的解吸量和活化效率;(2)被植酸强吸附的矿物表面在较大pH 范围内具有较高的负电荷,阻碍有机酸的吸附和置换反应,因此需要深入探究提高有机酸活化强吸附态植酸的技术和方法;(3)需监测和评估有机酸活化土壤植酸的长期效应。
