聚集诱导发光型手性烯胺酮的构筑及其手性识别性能研究*
2023-12-24李清阳卫可悦齐春轩
李清阳,白 莹,卫可悦,齐春轩
(宝鸡文理学院 化学化工学院, AIE(聚集诱导发光)研究中心, 陕西省植物化学重点实验室,陕西 宝鸡 721013)
手性是实物与镜像无法完全重合的现象,虽然2种对映异构体理化性质几乎没有差别,但其光学、生化和药理活性却不同[1-5],因此,手性识别与拆分对手性光学材料、药物等领域具有极其重要的作用。基于此,科学家们开发出许多可进行手性识别的方法,其中比较常见的主要有色谱法、核磁法、光谱法等。色谱类方法是目前研究较为成熟的方法,如高效液相色谱法(High-performance Liquid Chromatography, HPLC)[6]。这类方法虽然具有精确度高的分离效果,且可重复利用,但耗时长,仪器成本过高。常用的光谱类方法包括:紫外-可见吸收光谱法[7-8]、圆二色光谱法[9-10]和荧光光谱法等[11-14]。其中荧光光谱法因操作简单、耗时短和灵敏度高等优点被广泛应用[15]。但传统的荧光化合物由于聚集诱导荧光淬灭(Aggregation-caused Quenching, ACQ)效应,限制了手性荧光探针的发展[16]。
聚集诱导发光(Aggregation-induced Emission, AIE)为解决该问题提供了新思路。AIE是我国科学家唐本忠院士2001年首次提出的新概念,该类化合物通常在稀溶液中不发光,而在聚集态有明显的荧光发射[17]。目前被广泛接受的发光机理主要是分子内运动受限,包括分子内旋转受限和分子内振动受限。经过20余年的发展,AIE在生物传感、化学传感、有机光电材料、力敏材料等领域受到广泛关注[18]。特别是在手性识别领域,目前已开发出具有AIE特性的荧光“点亮”型的手性荧光探针[19-25],但该类探针仍处于研究初期,需进一步广泛而深入的研究。
在众多AIE化合物中,四苯乙烯(Tetraphenylethene, TPE)由于易合成、易修饰、光色稳定等特点备受关注。因此,本文主要以TPE为发光源,手性环己二胺为手性源,通过点击反应构筑手性荧光探针,在确认目标化合物后,尝试将其开发为对手性对映异构体具有良好选择性识别的荧光探针。
1 实验部分
1.1 实验仪器与试剂
1.1.1 实验试剂
2-溴-1,1,2-三苯基乙烯(分析纯)由天津希恩思科技有限公司生产;4-醛基苯硼酸(分析纯)、四(三苯基膦)钯(分析纯)、BOC-L-苯丙氨酸(分析纯)、BOC-D-苯丙氨酸(分析纯)、L-二苯甲酰酒石酸(分析纯)、D-二苯甲酰酒石酸(分析纯)、L-苹果酸(分析纯)和D-苹果酸(分析纯)均由上海安耐吉化学有限公司生产;乙炔基溴化镁(分析纯)由北京伊诺凯科技有限公司生产;活性二氧化锰(分析纯)、L-(+)-酒石酸(分析纯)、D-(-)-酒石酸(分析纯)、L-半胱氨酸(分析纯)和D-半胱氨酸(分析纯)均由上海麦克林生化科技有限公司生产;(1R,2R)-(-)-1,2-环己二胺(分析纯)和(1S,2S)-(+)-1,2-环己二胺(分析纯)由北京百灵威科技有限公司生产;L-精氨酸(分析纯)和D-精氨酸(分析纯)由大赛璐药物手性技术有限公司生产。
1.1.2 实验仪器
UV-2550型紫外光谱仪由岛津(香港)公司生产;FluorMax-4稳态-瞬态荧光光谱仪由Horiba公司生产;Agilent-400 MHz核磁共振仪由布鲁克科技有限公司生产;气相色谱质谱联用仪由Thermo公司生产。
1.2 手性荧光探针的构筑及结构表征
1.2.1 四苯乙烯活化端炔的合成及结构表征
4-(1,2,2-triphenylvinyl)benzaldehyde的合成如图1所示。
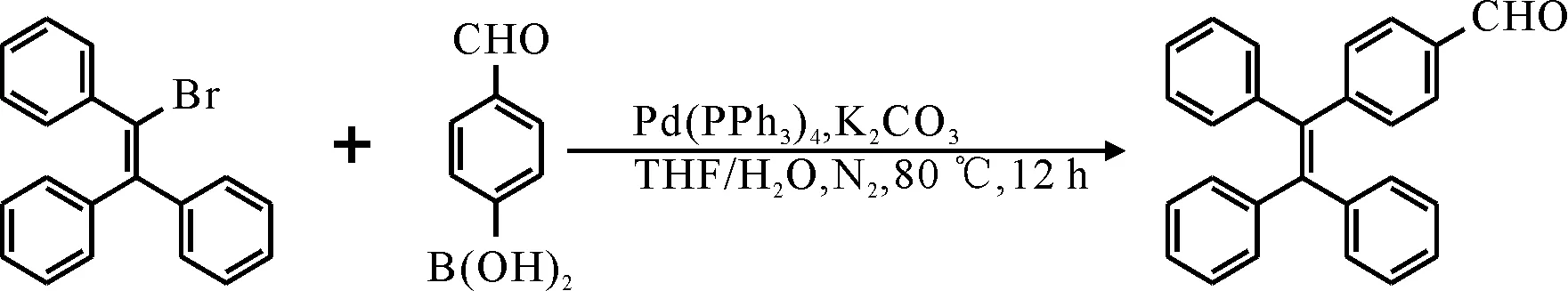
图1 4-(1,2,2-triphenylvinyl) benzaldehyde的合成路线Fig. 1 Synthetic route of 4-(1,2,2-triphenylvinyl) benzaldehyde
在250 mL双口烧瓶中加入磁子、2-溴-1,1,2-三苯基乙烯(3.25 g,9.70 mmol,1.00 equiv.)、4-醛基苯硼酸(2.18 g,14.55 mmol,1.50 equiv.)、四(三苯基膦)钯(0.86 g,0.74 mmol,0.08 equiv.)、无水碳酸钾(2.68 g,19.40 mmol,2.00 equiv.),N2保护;加入四氢呋喃(100 mL)、水(10 mL),80 ℃反应12 h;待反应液冷却至室温后,用饱和NaHCO3溶液(10 mL)、二氯甲烷(20 mL×3)萃取;收集有机相,无水硫酸镁干燥,抽滤,浓缩,柱色谱分离(VPE∶VEA=200∶1)得淡黄色粉末状固体3.07 g,收率为88%。1H NMR(400 MHz,CDCl3)δ9.90(s,1H),7.63~7.60(m,2H),7.20(d,J=8.2 Hz, 2H),7.17~7.07(m,9H),7.07~6.98(m,6H)。13C NMR(100 MHz,CDCl3)δ191.99,150.69,143.20,143.18,143.13,143.03,139.91,134.44,132.07,131.42,131.41,131.36,129.28,128.07,128.05,127.88,127.18,127.02,126.99。
1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-ol的合成如图2所示。

图2 1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-ol的合成路线Fig. 2 Synthetic route of 1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-ol
在100 mL双口烧瓶中加入磁子、4-(1,2,2-三苯基乙烯基)苯甲醛(3.07 g,8.50 mmol,1 equiv.),N2保护;在冰浴中加入乙炔基溴化镁(25.5 mL,12.75 mmol,0.5 M,1.5 equiv.),室温搅拌反应约12 h;加入饱和NH4Cl(10 mL)溶液进行淬灭,乙酸乙酯(20 mL×3)萃取,收集有机相;无水硫酸镁干燥,抽滤,浓缩,柱色谱分离 (VPE∶VEA=10∶1)得淡黄绿色片状固体2.50 g,收率为76%。1H NMR(400 MHz,CDCl3)δ7.29(d,J=8.1 Hz,2H),7.14~7.08(m, 9H),7.07~7.00(m,8H),5.38(s,1H),2.63(d,J=2.2 Hz,1H),2.17(s, 1H)。13C NMR(100 MHz,CDCl3)δ144.24, 143.74, 143.69, 143.65, 141.55,140.44,138.02,131.73,131.46,131.42,127.90,127.82,127.78,126.69,126.63,126.62,126.14,83.56,74.93,64.38。
1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-one的制备如图3所示。

图3 1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-one的合成Fig. 3 Synthetic route of 1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-yn-1-one
在50 mL的茄形瓶中加入磁子、1-(4-(1,2,2-triphenylvinyl)phenyl)prop-2-yn-1-ol (2.50 g,6.5 mmol,1 equiv. )、5 mL DCM以及活性MnO2(12.51 g,143.79 mmol,5 equiv.),室温搅拌反应6 h;抽滤,浓缩,柱色谱分离(VPE∶VEA=100∶1)得黄色粉末状固体1.55 g,收率为62%。1H NMR(400 MHz,CDCl3)δ7.90(d,J=8.6 Hz,2H),7.13(tdd,J=6.1,5.7,2.1 Hz,11H),7.05~6.98(m,6H),3.35(s,1H)。13C NMR(100 MHz,CDCl3)δ176.95,150.85,143.31,143.18,143.09,143.02,139.84,134.23,131.76,131.42,131.37,129.32,128.09,128.07,127.87,127.24,127.04,127.00,80.56,80.51。
1.2.2 目标产物的合成及结构表征
(2Z,2'Z)-3,3'-(((1R,2R)-cyclohexane-1,2-diyl)bis(azanediyl))bis(1-(4-(1,2,2-triphenylvinyl)-phenyl)prop-2-en-1-one)的合成如图4所示。

图4 化合物1的合成路线Fig. 4 Synthetic route of compound 1
在50 mL的茄形瓶中加入磁子、1-(4-(1,2,2-三苯基乙烯基)苯基)丙炔酮(0.82 g,2.30 mmol,2.00 equiv.)、(1R,2R)-(-)-1,2-环己二胺(0.13 g,1.15 mmol,1.00 equiv.)、5 mL DCM,室温搅拌反应6 h;浓缩,柱色谱分离(VPE∶VEA=5∶1)得黄色粉末状固体0.80 g,收率为79%。1H NMR(400 MHz,CDCl3)δ10.26(dd,J=12.3,8.7 Hz,2H),7.56(d,J=8.4 Hz,4H),7.13~7.06(m,18H),7.05~6.97(m,16H),6.79(dd,J=12.4,7.5 Hz,2H),5.54(d,J=7.5 Hz,2H),5.54(d,J=7.5 Hz,2H), 2.84(t,J=9.0 Hz,3H),2.18~2.07(m,2H),1.90~1.78(m,3H),1.52~1.39(m,3H),1.33(dd,J=13.6,6.8 Hz,2H)。13C NMR(100 MHz,CDCl3)δ189.73,153.43,146.76,143.47,143.36,143.32,141.77,140.29,137.29,131.29,131.21,127.73,127.67,127.60,126.63,126.52,90.58,64.56。
(2Z,2'Z)-3,3'-(((1S,2S)-cyclohexane-1,2-diyl) bis (azanediyl)) bis (1-(4-(1,2,2-triphenylvinyl) phenyl) prop-2-en-1-one)的合成如图5所示。

图5 化合物2 的合成路线Fig. 5 Synthetic route of compound 2
在50 mL的茄形瓶中加入磁子、1-(4-(1,2,2-三苯基乙烯基)苯基)炔丙酮(0.47 g,1.31 mmol,2.00 equiv.)、(1S,2S)-(-)-1,2-环己二胺(0.07 g,0.66 mmol,1.00 equiv.)、5 mL DCM,室温搅拌反应6 h,浓缩,柱色谱分离(VPE∶VEA=5∶1)得黄色粉末状固体0.37 g,收率为64%。1H NMR(400 MHz,CDCl3)δ10.26(dd,J=12.0,8.9 Hz,2H),7.56(d,J=8.5 Hz,4H),7.15~7.06(m,18H),7.06~6.95(m,16H),6.79(dd,J=12.4,7.5 Hz,2H),5.54(d,J=7.5 Hz,2H),2.84(s,2H),2.13(d,J=13.0 Hz,2H),1.84(d,J=9.3 Hz,2H),1.49~1.39(m,2H),1.38~1.29(m,2H)。13C NMR(100 MHz,CDCl3)δ189.73,153.43,146.76,143.47,143.36,143.32,141.77,140.29,137.29,131.29,131.26,131.21,127.73,127.67,127.60,126.63,126.52,90.58,64.56。HRMS:m/zcalculated for C64H55N2O2+883.425 8 [M+H]+; Found 883.426 3。
2 结果与讨论
2.1 手性荧光化合物光学性质研究
2.1.1 AIE特性研究
TPE及其衍生物大多具有AIE特性,为研究化合物1和化合物2是否继承了四苯乙烯的AIE性质,我们首先测试了2种化合物的紫外吸收,结果表明在THF溶液中,2种化合物的最大吸收波长均为350 nm。随后以该波长激发化合物进行荧光光谱测试,结果如图6(a,c)所示。2种构型的化合物在纯THF溶液中荧光很微弱,这可能是由于分子内的苯环转动,使激发态能量通过非辐射跃迁至基态,从而导致发光微弱。在加水量的体积分数达到60%前,溶液的发光强度几乎没有变化,这可能由于THF能够完全溶解化合物,致使溶液中没有聚集体产生。而当加水量的体积分数大于60%后,2种化合物的荧光强度随水体积分数的增加逐渐增强,这是由于不良溶剂体积分数增加,溶质不能很好地溶解于混合溶剂中,使溶质分子发生聚集,导致分子内运动受限,使激发态能量再不能通过非辐射跃迁方式回到基态,从而呈现出明显的荧光增强,以上结果说明2种化合物均具有AIE活性。为更加直观地判断2种化合物荧光强度随水含量增加的变化趋势,我们以480 nm处的荧光强度与纯THF溶液的荧光强度比为纵坐标,水体积分数为横坐标作图,结果如图6(b,d)。由图可知,含水量在60%前,荧光几乎没变化;当含水量在80 %前,荧光缓慢增加;而当含水量超过80%,荧光强度出现大幅度增加。因此,2种化合物具有AIE特性。
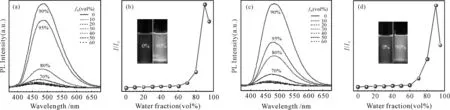
图6 化合物1和2在不同水体积分数下的荧光光谱(a,c)及其在480 nm处的荧光强度(I)与纯THF中的荧光强度(I0)比值(b,d),插图为365 nm紫外光下样品溶于THF和含水量为90 %的照片 (λex=350 nm,slit: 4 nm∶4 nm,浓度:10 μM)Fig. 6 Fluorescence spectra of compounds 1 and 2 at different water volume fractions (a, c) and the ratio of their fluorescence intensity (I) at 480 nm to (I0) in pure THF (b, d) are illustrated with photos of the sample dissolved in THF and water content of 90% under 365 nm UV light (λex=350 nm, slit: 4 nm∶4 nm, concentration: 10 μM)
2.2 手性荧光化合物的手性识别性能研究
为探究所制备化合物是否具有手性识别作用,我们以化合物2为研究对象,用该化合物配制了含水量为50%(1.5 mL THF,1.5 mL H2O)、浓度为5×10-4M的探针分子溶液。手性测试时按照探针分子与手性对映异构体摩尔比1∶1或1∶2将对映异构体分别加到探针分子溶液中,通过荧光测试发现该荧光探针可以选择性地识别6对对映异构体,详细数据如表1所示。

表1 探针分子对不同手性化合物的对映选择性识别aTab. 1 Enantioselective recognition of different chiral compounds by probe moleculesa
在探针分子溶液中分别加入L-二苯甲酰酒石酸和D-二苯甲酰酒石酸,2组溶液均由澄清液变为悬浊液。荧光识别结果如图7(a),相比于D-二苯甲酰酒石酸,加入L-二苯甲酰酒石酸的探针分子溶液荧光淬灭更为明显,2种对映体作用后的荧光强度比为7.1(ID/IL),说明该探针可以在2种对映异构体中选择性识别L-二苯甲酰酒石酸。在探针分子溶液中分别加入L-苹果酸和D-苹果酸后,得到相似的结果(图7(b)),2种对映体作用后的荧光强度比为4.7(IL/ID),因此,该探针可以在2种对映异构体中选择性识别D-苹果酸。在加入BOC-L-苯丙氨酸和BOC-D-苯丙氨酸后,结果同上(图7(c)),其荧光强度比为4.4(IL/ID),因此,该探针可以在2种对映异构体中选择性识别BOC-D-苯丙氨酸。而在探针分子溶液中分别加入L-半胱氨酸和D-半胱氨酸后,2个化合物作用后的荧光均发生增强,其中加入L-半胱氨酸的探针分子溶液荧光增强更明显(图7(d)),其荧光强度比为4.0(IL/ID),该探针可选择性识别L-半胱氨酸;在加入L-精氨酸和D-精氨酸后,2组溶液均为澄清液,荧光光谱测试结果表明,加入D-精氨酸的探针分子溶液荧光增强更明显(图7(e)),其荧光强度比为3.3(ID/IL),所以该探针可以在2种对映异构体中选择性识别出D-精氨酸。在探针分子溶液中分别加入L-酒石酸和D-酒石酸后,观察到2组溶液均由澄清液变为悬浊液。荧光测试结果表明,加入D-酒石酸的探针分子溶液荧光猝灭更明显(图7(f)),其荧光强度比为2.9(IL/ID),因此,该探针可以在2种对映异构体中选择性识别出D-酒石酸。

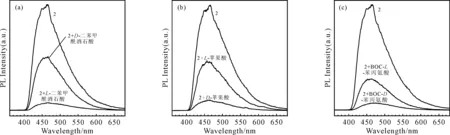
图7 化合物2在加入不同手性化合物后的荧光光谱(a)二苯甲酰酒石酸 VTHF∶VH2O=1∶1, c=5.00 × 10-4 M;(b)苹果酸 VTHF∶VH2O=0.9∶1, c=4.84×10-4 M;(c)BOC-苯丙氨酸 VTHF∶VH2O=1∶1, c=5.00×10-4 M;(d)半胱氨酸 VTHF∶VH2O=0.97∶1, c=4.93×10-4 M;(e)精氨酸 VTHF∶VH2O=1∶1, c=5.00×10-4 M;(f)酒石酸 VTHF∶VH2O=1∶1, c=5.00×10-4 M;(λex=350 nm, slit: 5 nm∶5 nm)Fig. 7 Fluorescence spectra of compound 2 after the addition different chiral compounds(a) dibenzoyl tartaric acid VTHF∶VH2O=1∶1, c=5.00 × 10-4 M; (b) malic acid VTHF∶VH2O=0.9∶1, c=4.84×10-4 M; (c) BOC-phenylalanine VTHF∶VH2O=1∶1, c=5.00×10-4 M; (d) cysteine VTHF∶VH2O=0.97∶1, c=4.93×10-4 M; (e) arginine VTHF∶VH2O=1∶1, c=5.00×10-4 M; (f) tartaric acid VTHF∶VH2O=1∶1, c=5.00×10-4 M; (λex=350 nm, slit: 5 nm∶5 nm)
3 结论
本文以常见的手性化合物环己二胺、AIE型化合物四苯乙烯基活化端炔为原料,常温下通过点击反应设计合成了一种新型的荧光探针。通过核磁、质谱对其结构进行验证后,利用紫外、荧光光谱探究目标化合物的AIE特性。随后在THF与水的混合体系中,测试目标分子对手性化合物的选择性识别能力,结果表明,本文所构筑的手性荧光探针可以实现对6对手性化合物响应,手性对映体及荧光强度比分别是D/L-二苯甲酰酒石酸7.1倍、L/D-苹果酸4.7倍、BOC-L/D-苯丙氨酸4.4倍、L/D-半胱氨酸4.0倍、D/L-精氨酸3.3倍、L/D-酒石酸2.9倍。
