利奈唑胺中对映异构体的测定
2016-05-20周君安琳孙井龙江苏豪森药业集团有限公司连云港222000
周君安 孙 琳孙井龙(江苏豪森药业集团有限公司 连云港222000)
利奈唑胺中对映异构体的测定
周君安孙琳*孙井龙(江苏豪森药业集团有限公司连云港222000)
摘要:目的:对利奈唑胺中的对映异构体进行测定。方法:采用高效液相色谱法,CHIRALPAK AD-H(250mm×4.6mm 5μm);以正己烷-异丙醇-二乙胺(85∶15∶0.2)为流动相;紫外检测器;流速为1.0mL/min;检测波长为254nm;柱温为40℃。结果:利奈唑胺中对映异构体能得到良好的分离,峰面积与浓度在一定的范围内呈良好的线性关系。结论:该方法作为利奈唑胺中对映异构体的检测方法准确、可靠。
关键词:利奈唑胺液相色谱对映异构体
利奈唑胺(linezolid)属噁唑烷酮类抗菌新药。该药对葡萄球菌属、链球菌属、肠球菌属等革兰阳性菌具有良好的抗菌作用,包括多重耐药菌,如MRSA、多重耐药肺炎链球菌、万古霉素耐药肠球菌[1,2,3]。该药于2000年获得美国FDA批准,2007年进入中国市场。根据ICH指导原则及《中国药典》四部通则指导原则要求[4],本实验建立了利奈唑胺中对映异构体的检测方法。
1 仪器与试剂
仪器:电子分析天平,梅特勒XS105;Agilent 1200液相色谱仪,安捷伦色谱工作站;色谱柱:CHIRALPAK AD-H(250mm× 4.6mm 5μm)。试剂:正己烷-异丙醇-二乙胺均为色谱纯,来自MERCK公司;利奈唑胺及利奈唑胺对映异构体均为本公司自制。
2 试验过程与结论
2.1色谱条件:照液相色谱测定法(《中国药典》2015年版通则0512),以正己烷-异丙醇-二乙胺(85∶15∶0.2)为流动相;紫外检测器;流速为1.0mL/min;等度洗脱;检测波长为254nm;柱温为40℃;进样体积10μL。
2.2试验溶液配制:取利奈唑胺适量,精密称定,加适量甲醇溶解,并用流动相稀释制成每1mL中约含0.5mg的溶液,作为供试品溶液;精密量取供试品溶液适量,加流动相稀释制成每1mL中含5μg的溶液,作为对照溶液;取利奈唑胺及利奈唑胺对映异构体对照品适量,加适量甲醇溶解,用流动相稀释制成每1mL中约含0.25mg的溶液,作为系统适用性溶液。
2.3系统适用性试验:量取系统适用性溶液10μL,注入高效液相色谱仪,记录液相图谱。从实验图谱看出,利奈唑胺与对映异构体分离度良好,分离度为5.0,表明该分析方法专属性良好。
2.4定量限和检测限试验:将对照溶液逐步稀释,分别进样至信噪比(峰高/基线噪声)为3±1为检测限,至信噪比为10±2为定量限。结果见下表。
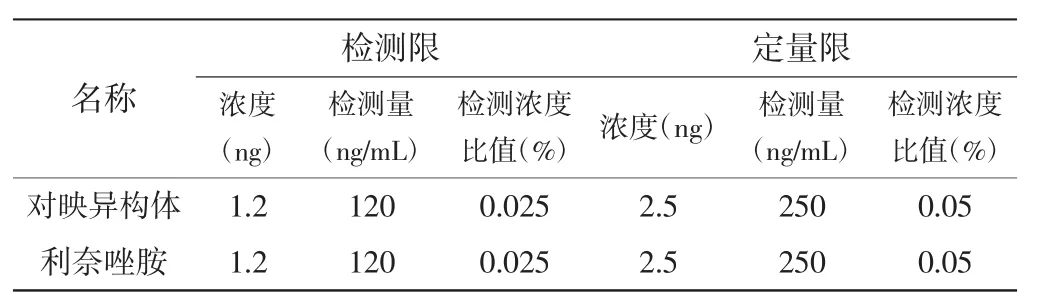
检测限 定量限检测浓度比值(%)对映异构体 1.2 120 0.025 2.5 250 0.05利奈唑胺 1.2 120 0.025 2.5 250 0.05名称 浓度(ng)检测量(ng/mL)检测浓度比值(%)浓度(ng) 检测量(ng/mL)
2.5线性关系试验:按照标准限度配制线性关系试验溶液,利奈唑胺对映异构体在0.25~500μg/mL的范围内,线性相关系数皆大于0.9990,说明线性良好。

名称 回归方程 相关系数利奈唑胺对映异构体 A=29.627×C-0.173 r=0.9998
2.6系统精密度:考察供试品溶液及对照溶液连续六针进样试验结果见下表。

项目对映异构体(%)对映异构体平均值(%) 未检出SD对映异构体(%) / 第1次 第2次 第3次 第4次 第5次 第6次未检出 未检出 未检出 未检出 未检出 未检出
由结果可见,利奈唑胺对映异构体平行测定六次,均未检出,说明本方法系统的精密度符合实验要求。
2.7溶液稳定性:考察供试品溶液及对照溶液在选定稀释液中的稳定性,试验结果下表。

放置时间对映异构体(%)0h 2h 4h 8h 12h 24h 结论未检出 未检出 未检出 未检出 未检出 未检出 无降解
由结果可以看出,利奈唑胺样品在流动相中24h内稳定,无对映异构体降解产生。
2.8回收率:称取利奈唑胺约50mg,置50mL量瓶中,作为回收率基质样品;另精密称取利奈唑胺对映异构体对照品约5mg,置250mL量瓶中,加适量乙腈溶解后,用稀释液稀释定容至刻度,作为储备溶液。以对映异构体限度为基准100%,分别精密量取储备溶液制成含杂质40%、100%和120%的溶液各三份,作为供试品溶液。定量测定的利奈唑胺对映异构体的平均回收率介于95%~104%之间,RSD为5.43%,说明本分析方法对利奈唑胺对映异构体的测定是准确的。
3 讨论
用高效液相色谱法测定利奈唑胺中对映异构体专属性良好;对检测限、定量限进行测定,说明本方法检测灵敏度高,能保证对低限度溶剂的良好检测;另外对线性关系、系统精密度、溶液稳定性、回收率进行测定,发现本方法均能满足上述实验的要求,对利奈唑胺中对映异构体进行准确定量,能满足对利奈唑胺中对映异构体的含量控制。
参考文献
[1]李娉,李庆林,刘丽萍,等.利奈唑胺和万古霉素对耐甲氧西林金黄色葡萄球菌感染疗效的Meta分析[J].安徽医药,2015,19(5):969-973.
[2]毛锐.利奈唑胺治疗医院获得性耐甲氧西林金黄色葡萄球菌肺炎的疗效观察[J].北方药学,2015,12(5):60-61.
[3]刘丽.利奈唑胺治疗老年人革兰阳性菌感染的疗效[J].吉林医学,2015,36(15):3289-3290.
[4]国家药典委员会.中国药典四部通则[S].中国医药科技出版社,2015:59,374.
Determination of enantiomers in linezolid
Zhou Junan Sun Lin*Sun Jinglong(Jiangsu Hansoh Pharmaceutical Co.,Ltd. Lianyungang 222000 China)
Abstract:Objective: To establish a method for detection of enantiomers in linezolid Methods The enantiomers in linezolid was determined by HPLC with CHIRALPAK AD -H(250mm×4.6mm 5μm)column; the mobile phase was in the phase of hexane -isopropanol -diethylamine-(85∶15∶0.2)and with UV detector; The flow rate was 1.0mL/min; detection wavelength was 254nm; column temperature was 40℃; Results The enantiomers could be completely separated,and the calibration curves hand good liner relationship within a certain range Conclusion this method is proved accurate and reliable,it can be used for the determination of enantiomers in linezolid
Key words:Linezolid HPLC Enantiomers
*通讯作者
中图分类号:R917
文献标识码:A
文章编号:1672-8351(2016)04-0001-02
