经皮冠状动脉介入术患者平均血小板体积与冠状动脉病变程度及远期预后的相关性
2023-12-20马琳张晓萍周桂玲牛少辉
马琳,张晓萍,周桂玲,牛少辉
(1.河南省三门峡市中心医院心脏重症监护室,河南 三门峡 472000;2.郑州大学第二附属医院心血管内科,河南 郑州 450014)
经皮冠状动脉介入治疗 (Percutaneous coronary intervention,PCI)是目前有手术指征的冠心病患者常见治疗手段, 同时,PCI 也会增加术后缺血事件的发生风险[1]。 在急性冠脉综合征患者中,血小板在其发病机制中起重要作用, 可产生具有非常多的致密颗粒,具有促进血管舒缩、炎症和止血功能, 可能导致出现主要不良心血管事件(Major adverse cardiovascular events,MACE)[2-3]。 平均血小板体积(Mean platelet volume,MPV)是全血细胞计数中评估血小板活性指数的一部分, 研究证实,MPV 与心血管疾病的发病率和死亡率之间存在相关性[4]。研究表明,高表达MPV、糖尿病、高血压、高胆固醇血症、 吸烟和肥胖等都是心血管疾病的危险因素[5-6]。PCI 术前血小板指数升高与MACE 发生率之间存在相关性, 本研究拟探讨PCI 术后患者平均血小板体积与冠状动脉病变程度及远期预后的相关性。
1 资料与方法
1.1 一般资料 选取2016 年6 月至2018 年9 月在我院就诊住院的冠心病PCI 手术患者患者154例。 纳入标准:(1)至少一支主要冠状动脉血管狭窄程度超50%,均通过冠状动脉造影确诊[7];(2)年龄18 岁以上;(3)出现冠心病相关症状,如胸闷或心绞痛等;(4)所有患者均可以全程配合本次研究进行。 排除标准:(1)非首次行PCI 手术患者;(2)近期有手术或外伤史患者;(3) 有风湿病史患者;(4)恶性肿瘤患者;(5)肾功能不全患者(肌酐≥1.5 mg/dL);(6)PCI 手术成功患者。按照常规方法进行冠状动脉造影及PCI,住院期间无MACE 及最小狭窄低于20%,同时,术后靶病变部位血管腔明显增大,则说明PCI 手术成功。 收集患者的一般资料,包括性别、年龄、体重、吸烟史、饮酒史、高血压病史、 糖尿病史等, 还有血小板分布宽度(PDW)、MPV、血小板大细胞比(P-LCR)。 本研究获得医院医学伦理学委员会批准, 所有研究对象或家属对本研究知情并签署知情同意书。
1.2 方法
1.2.1 PCI 围手术期用药 术前, 患者服用325 mg阿司匹林和300 mg 氯吡格雷;术中,静脉追加0.3 mg/kg 肝素;术后,应口服阿司匹林100~300 mg/d,置入金属裸支架(BMS)者服用1 个月,置入药物洗脱支架(DES)者服用6 个月,之后改为100 mg/d长期服用。 置入DES 的患者PCI 术后连续服用氯吡格雷75 mg/d 12 个月,置入BMS 的患者,服用氯吡格雷75 mg/d 1 个月。
1.2.2 冠状动脉造影及PCI 经桡动脉或股动脉途径进行冠脉造影, 由经验丰富的心脏介入专科医师判定。
1.2.3 指标检测 患者术前入院患者空腹12 h 采集静脉血, 采血前均未使用肝素及血小板Ⅱb/Ⅲa受体拮抗剂, 在室温下用含乙二胺四乙酸的标准管取静脉血标本,2 h 内用Sysmex XN 2000 五分类血细胞分析仪进行检测,血细胞计数包括MPV。同时,EDTA 抗凝管采静脉血2 mL,并于抽血后2 h完成生化指标检测。
1.2.4 研究分组 记录所有患者的MPV 值,根据整个研究对象的中位MPV 值,分为低MPV 组(MPV<9.5 fl)和高MPV 组(MPV≥9.5 fl)。
1.2.5 临床事件定义 心源性死亡为无明确非心源性原因导致的死亡。 MACE 包括血运重建(靶血管或靶病变血运重建)、支架内血栓(IST)、心肌梗死(MI)、脑卒中、死亡、心源性死亡。 MI 诊断标准为具有以下情况之一:(1)心电图改变,ST 段偏移2 mm以上,(2)出现了新的Q 波;(3)肌酸激酶(CK)2 倍升高,且肌酸激酶同工酶(CK-MB)百分相对指数在5%以上;(4)通过超声心动图或血管造影检查证实有新的节段性室壁运动异常。 高血压病史为血压高于140/90 mmHg 和/或服用降压药的人。 糖尿病诊断标准为具有以下标情况之一:(1)糖尿病的典型症状加上血浆葡萄糖浓度>200 mg/dL;(2)空腹血糖≥126 mg/dL;(3)OGTT 2 小时后负荷葡萄糖≥200 mg/dL;(4)服用治疗糖尿病药物。
1.2.6 随访 术后开始规律随访,采用电话、信件以及诊室复查等形式观察患者出院后1 年内MACE的发生情况,包括心源性死亡、再发心肌梗死、靶血管重建及脑卒中、心力衰竭等,本研究主要终点为1 年内心源性死亡, 次要终点包括主要MACE和出血,随访截止日期为2019 年10 月。
1.3 统计学方法 采用SPSS 18.0 统计软件, 计量资料行正态性检验和方差齐性检验,采用均数±标准差(±s),检验两组间比较采用独立样本t检验。计数资料以百分比(%)表示,组间比较采χ2检验。冠心病患者预后的危险因素采用单因素及多元Logistic回归分析,相关性分析采用Pearson相关分析。绘制受试者工作特征曲线(ROC)并计算曲线下面积(AUC),基线MPV 值的敏感性和特异性,以预测1 年随访期间的MACE 发生率。P<0.05 为差异有统计学意义。
2 结果
2.1 临床基线资料比较 154 例冠心病PCI 手术患者中男性98 例,女性56 例,年龄为58.5±11.4 岁,其中有高血压病史者77 例, 有糖尿病病史者24例。 高MPV 组PLT 明显低于低MPV 组,而PDW、P-LCR 均高于低MPV 组,差异有统计学意义(P<0.05)。患者在性别、年龄、BMI、LVEF、既往病史、吸烟史、服药史、其他血液常规指标方面差异无统计学意义(P>0.05),具有可比性。 见表1。
表1 临床基线资料比较(±s)
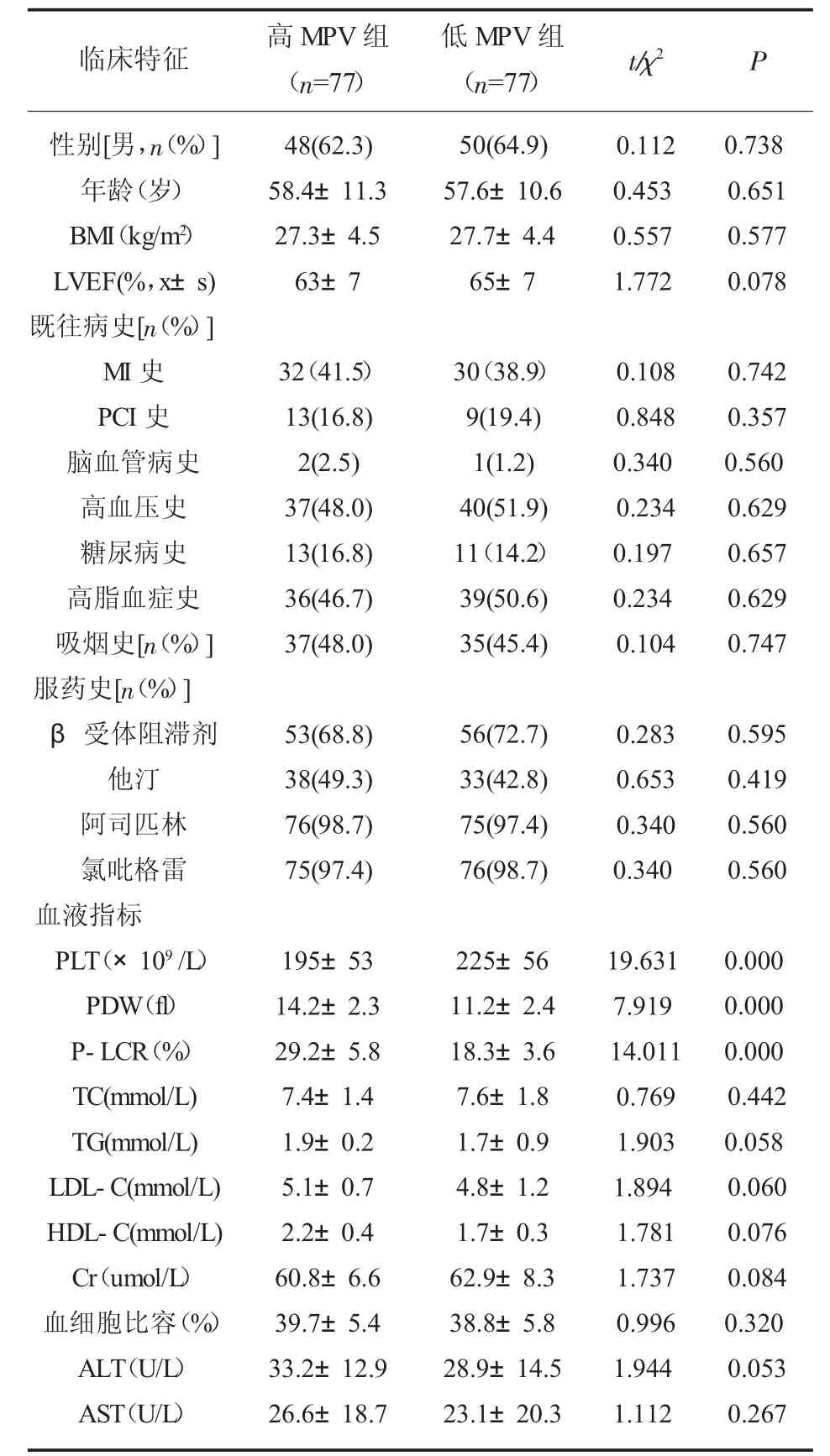
表1 临床基线资料比较(±s)
注: MI 为心肌梗死;PLT 为血小板计数;HDL-C 为高密度脂蛋白胆固醇;LDL-C 为低密度脂蛋白胆固醇;LVEF 为左室射血分数;TC 为总胆固醇;TG 为三酰甘油;BMI 为体重质量指数;ALT 为谷丙转氨酶;AST 为谷草转氨酶。
临床特征 高MPV 组(n=77)性别[男,n(%)]年龄(岁)BMI(kg/m2)LVEF(%,x±s)既往病史[n(%)]MI 史PCI 史脑血管病史高血压史糖尿病史高脂血症史吸烟史[n(%)]服药史[n(%)]β 受体阻滞剂他汀阿司匹林氯吡格雷血液指标PLT(×109/L)PDW(fl)P-LCR(%)TC(mmol/L)TG(mmol/L)LDL-C(mmol/L)HDL-C(mmol/L)Cr(umol/L)血细胞比容(%)ALT(U/L)AST(U/L)低MPV 组(n=77) t/χ2 P 48(62.3)58.4±11.3 27.3±4.5 63±7 50(64.9)57.6±10.6 27.7±4.4 65±7 0.112 0.453 0.557 1.772 0.738 0.651 0.577 0.078 32(41.5)13(16.8)2(2.5)37(48.0)13(16.8)36(46.7)37(48.0)30(38.9)9(19.4)1(1.2)40(51.9)11(14.2)39(50.6)35(45.4)0.108 0.848 0.340 0.234 0.197 0.234 0.104 0.742 0.357 0.560 0.629 0.657 0.629 0.747 53(68.8)38(49.3)76(98.7)75(97.4)56(72.7)33(42.8)75(97.4)76(98.7)0.283 0.653 0.340 0.340 0.595 0.419 0.560 0.560 195±53 14.2±2.3 29.2±5.8 7.4±1.4 1.9±0.2 5.1±0.7 2.2±0.4 60.8±6.6 39.7±5.4 33.2±12.9 26.6±18.7 225±56 11.2±2.4 18.3±3.6 7.6±1.8 1.7±0.9 4.8±1.2 1.7±0.3 62.9±8.3 38.8±5.8 28.9±14.5 23.1±20.3 19.631 7.919 14.011 0.769 1.903 1.894 1.781 1.737 0.996 1.944 1.112 0.000 0.000 0.000 0.442 0.058 0.060 0.076 0.084 0.320 0.053 0.267
2.2 MACE 发生情况比较 术后随访1 年,高MPV组总MACE 发生率、 心源性死亡的发生率明显高于低MPV 组,差异有统计学意义(P<0.05);而心力衰竭、靶血管重建及脑卒中、再发心肌梗死、脑卒中及出血与低MPV 组比较, 差异无统计学意义(P>0.05),见表2。
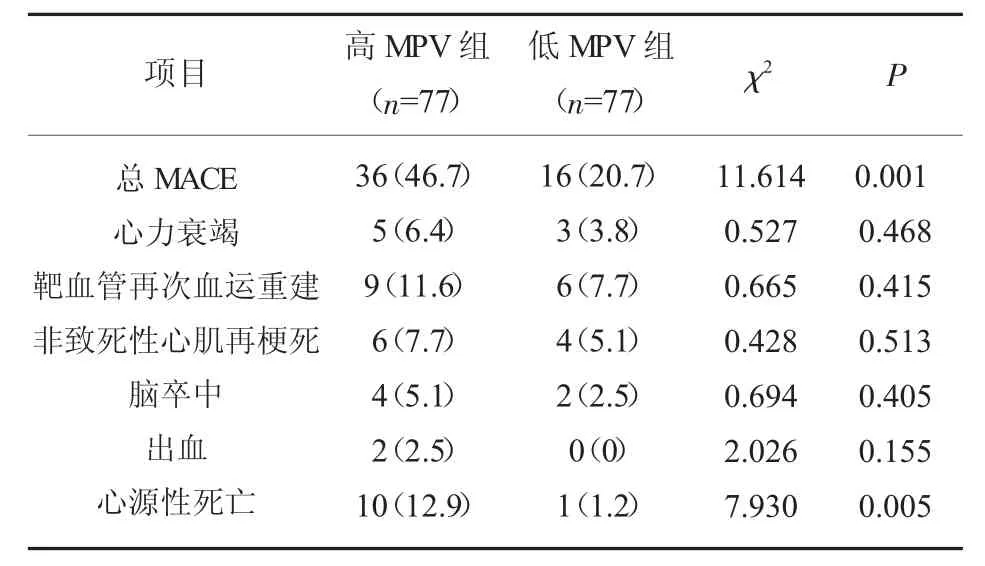
表2 不同组别MACE 发生情况比较[n(%)]
2.3 患者术前MPV 与血液指标的关系 患者术前MPV 与PDW、P-LCR 存在显著正相关关系,与PLT 存在负相关关系,均有统计学意义(P<0.05);MPV 与胆固醇、 甘油三酯、 血细胞比容、 肌酐、ALT、AST、LDL、HDL 均无明显相 (P>0.05)。 见表3。
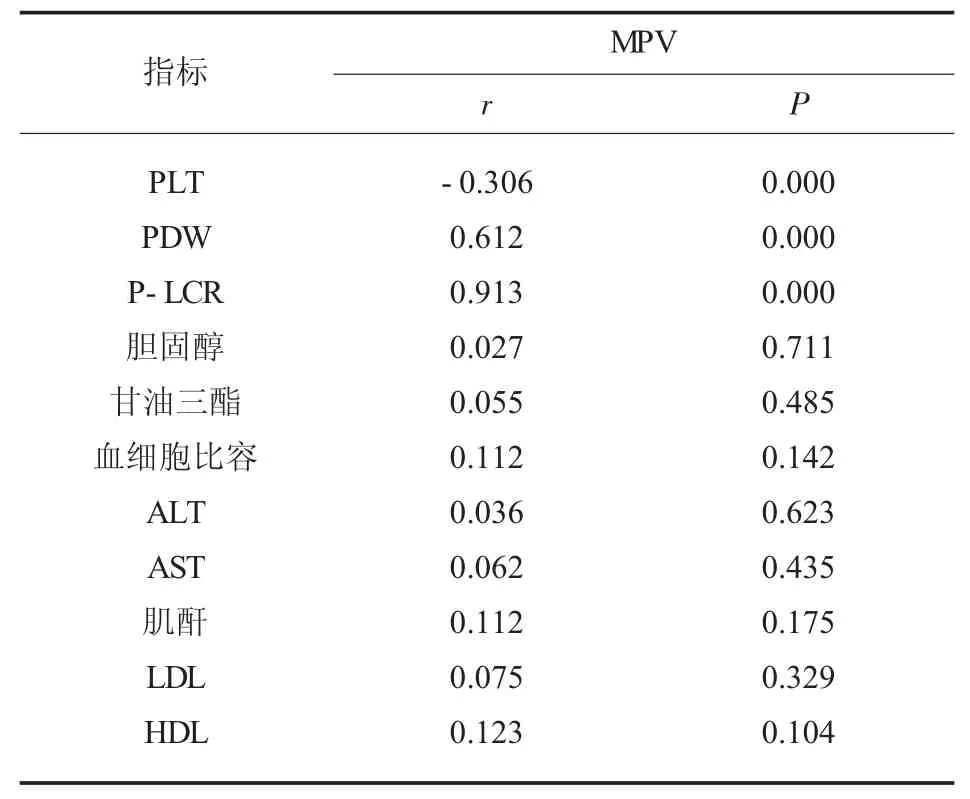
表3 MPV 与血液指标的相关分析
2.4 MPV 的诊断和预后价值 以患者发生MACE为因变量,以年龄、既往病史、服药史、PDW、PLT、P-LCR、MPV 为自变量, 进行多因素Logistic回归分析。 结果显示:发现高MPV 是冠心病PCI 手术患者发生MACE 的独立危险因素,见表4。
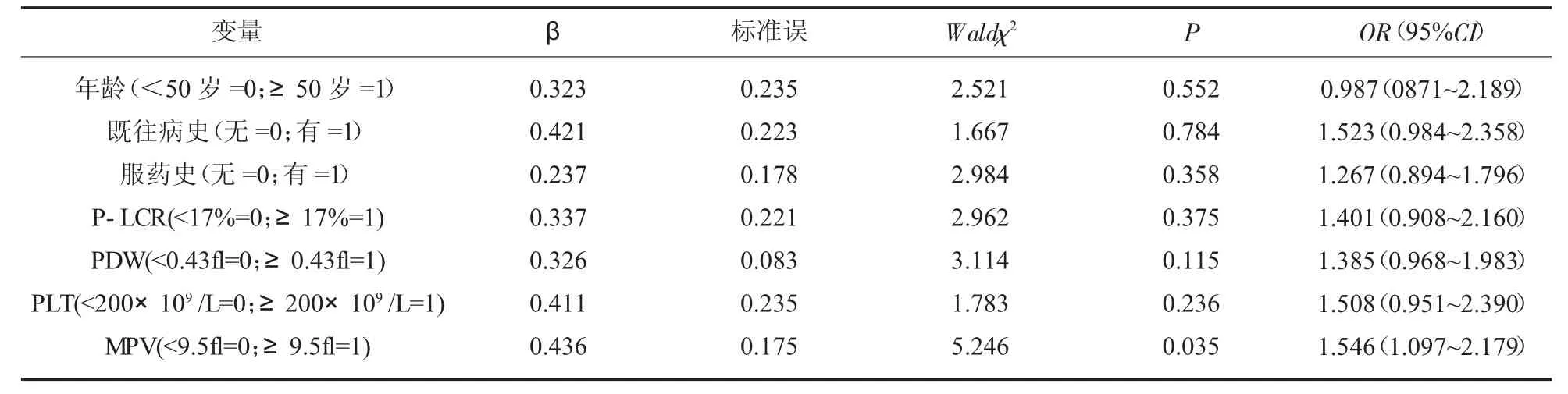
表4 冠心病PCI 手术患者预后多因素Logistic 回归分析
根据两组患者血液中MPV 的变化,绘制ROC曲线。 血浆中MPV 在预测冠心病PCI 手术患者1年内发生MACE 的曲线下面积(AUC)和效能分别为0.755 (95%CI:0.641~0.869;P<0.05), 敏感度为79%,特异度为68%。 见图1。
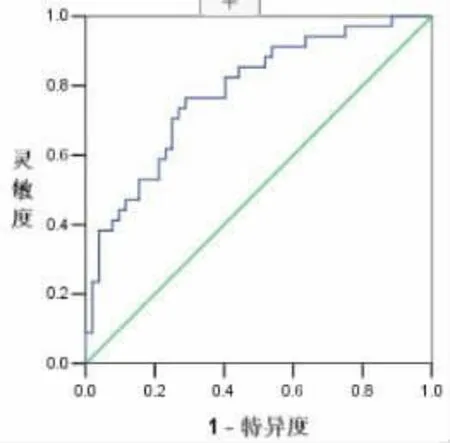
图1 MPV 预测冠心病PCI 手术患者1 年内发生MACE 的ROC 曲线
3 讨论
冠心病严重威胁人类健康, 占全死因死亡疾病的17%左右[8]。 冠心病PCI 治疗不能从根本上消除MACE 的发生,只能改善患者的血管狭窄状况,术后依然会存在不同程度的并发症[9]。 血小板是血栓形成和动脉粥样硬化病变血管破裂中起重要作用的血细胞成分之一,MPV 是一种测试方法简便的血小板活性评估指标, 可用作血小板功能监测标志物[10]。接受PCI 的患者发生斑块破裂和动脉壁受伤的风险较高, 可能导致血小板活化并增加促凝活性和炎症过程。 研究表明,术前MPV 升高与PCI 后发生MACE 和再狭窄有关[11]。 研究证实,MPV 可作为再狭窄预后指标, 被认为是PCI 后再狭窄的一个潜在指标[12]。因此,接受PCI 且术前MPV高的患者可能在冠状动脉介入治疗后需要大剂量抗血小板治疗[13]。此外,合并心血管危险因素(包括吸烟和糖尿病)的患者其MPV 水平较高[14]。
本研究显示, 在接受选择性PCI 手术的冠心病患者中,1 年随访期内高MPV 组心源性死亡发生率显著高于低MPV 组, 提示MPV 可能是冠心病PCI 手术患者未来发生MI 或死亡的预测因素。既往研究显示[15],基线MPV 和PCI 结果之间没有任何相关性,然而,与MPV 无改变或MPV 值降低的患者相比,MPV 升高患者死亡率更高。其他研究也证实[16],在随访期间有不良结局和心源性死亡的患者MPV 高于无不良反应和心脏死亡患者。 高MPV 组患者心源性死亡显著升高的可能机制[17]:(1) 血小板功能异常:2 型糖尿病患者的血小板对一氧化氮的敏感性丧失, 且更容易黏附聚集于血管内皮;(2)血小板高活性的天然拮抗剂胰岛素作用缺陷;(3)血小板活性和聚集增加:有研究发现高MPV 组患者血小板增加,骨髓中巨核细胞生成的新生血小板体积大、 反应性增强且释放增加;(4)P-选择素增加:可溶性P-选择素与血小板正相关,可引发血小板聚集增加,并导致对抗血小板药物的反应不良。 也有研究表明,与没有MPV 改变或MPV 值降低的患者相比,MPV 升高的患者的死亡率更高, 但在他们的分析中MPV 基线数值和PCI 术后结果之间没有任何相关性。
本研究显示,1 年随访期内高MPV 组MACE发生率约为低MPV 组的3 倍,ROC曲线分析显示,血浆中MPV 在预测冠心病PCI 手术患者1 年内发生MACE 的曲线下面积(AUC)为0.755(95%CI:0.641~0.869),敏感度为79%,特异度为68%,结果表明在1 年的随访期内,MPV 值升高对PCI 后MACE 发生率具有独立的预测作用。这一结果与先前的研究结论一致,即MPV 作为一个新型血液参数可用于预测冠心病PCI 手术患者长期预后。 血小板激活后可释放出大量促炎因子IL 和P-选择素,强化白细胞的募集和转运,进而调节白细胞功能,血小板体积与活化后反应程度成正比,大体积血小板数量越占优势对于冠心病PCI 手术患者来说提示血栓形成风险更高[18]。当然本研究也存在一定局限性:本研究为单中心且样本量相对较小,需要进一步扩大样本规模及样本来源单位进行研究;其次,所有患者的血样分析时间都不尽相同,检测延迟可能会导致MPV 值异常。
综上所述, 在接受择期PCI 的冠状动脉病变患者中,MPV 是其1 年随访期MACE 的预测因子,检测MPV 有助于PCI 术前进行风险分层以及辅助制定冠心病患者个体化治疗方案,提高患者预后。
