负载型磷钨酸催化剂催化大豆油环氧化的性能研究
2023-12-18莫斯敏程谦伟韦潇丽孟陆丽
莫斯敏, 程谦伟, 韦潇丽, 孟陆丽, 陈 通, 明 高
(广西科技大学生物与化学工程学院1,柳州 545006)
(柳州工学院机械工程学院2,柳州 545000)
邻苯二甲酸酯类作为传统增塑剂,由于对人体健康和环境有害,因此受到限制使用[1,2]。而环氧植物油具有无毒、挥发性低、稳定性好、耐浸出等优点,可作为绿色增塑剂。此外,因为它们来自可再生资源,易于获取且环保,除可作为增塑剂外,还是重要的有机合成中间体,故受到广泛地关注[3,4]。
目前,工业上主要以甲酸和双氧水为原料,原位生成过氧甲酸,再使大豆油发生环氧化反应合成环氧大豆油[5]。传统工艺大多使用硫酸、磷酸等均相催化剂,合成效率高,但容易造成环境污染且腐蚀设备。因此,开发应用于植物油环氧化反应的新型催化剂是必要的[6]。近年来,固体酸催化剂相较于液体酸,有着对反应设备的腐蚀和对环境污染小,发生副反应少的优点,且其易从产物中分离,可进行回收重复利用,得到了广泛的关注[7,8]。作为相转移催化剂,磷钨杂多酸(PHA)具有高效的H2O2利用率和对环氧化物的高选择性,作为双键环氧化的有效催化剂引起了广泛关注[9]。朱超等[10]以磷钨酸(HPW)为活性物质制备的磷钨杂多酸季铵盐,在无羧酸条件下催化可得到环氧值高达6%的环氧化大豆油。高比表面积的载体可以提高负载活性物质的分散度,加强活性物质和载体之间的相互作用,进而提高催化剂活性和稳定性,ZrO2具有高的比表面积,故常被用作催化剂载体[11,12]。Pasupulety等[13]通过溶胶-凝胶法制备高效钽-锆氧化物催化剂,用于从废弃食用油和动物脂肪生产生物柴油,催化剂在重复使用2次后,生物柴油的产率仍达到80.0%。淳宏等[14]将制备的SnO2-Al2O3作为大豆油甲醇解反应中的催化剂,发现其具有较高的催化活性稳定性。研究不同金属氧化物负载SnO2-ZrO2/HPW型催化剂的制备,并探讨其催化合成环氧大豆油的性能。
1 材料与方法
1.1 实验材料
大豆油(碘值为123.81)。氧氯化锆、四氯化锡、30%过氧化氢、88%甲酸、三氧化钨、二氧化硅、氧化铝、二氧化铈、氧化镧等均为分析纯。
1.2 催化剂的制备
催化剂通过共沉淀法-浸渍法制备[15]。制备过程如下:首先,分别将1 g SnCl4·5H2O、7.2 g ZrOCl2·8H2O分别溶于20 mL蒸馏水中,缓慢滴加28%的氨水溶液调节pH=9~10,将两种溶液混合,以300 r/min的速率搅拌1 h后,静置陈化12 h,将混合液减压抽滤,用蒸馏水反复洗涤滤饼(直至所有Cl-被洗掉),在110 ℃条件下烘干8 h,研磨后将其放入马弗炉中550 ℃煅烧2 h,得到SnO2-ZrO2前驱体。
采用浸渍法制备了系列 MxOy-SnO2-ZrO2/HPW 催化剂(MxOy=Al2O3,SiO2,WO3,CeO2和 La2O3)。首先,取1.25 g HPW 溶于30 mL的蒸馏水中,充分搅拌溶解。再将1.25 g 相应的金属氧化物与5 g SnO2-ZrO2加入到该溶液中,在室温下以300 r/min的转速搅拌2 h,然后将混合物在110 ℃下烘干8 h后,放入马弗炉600 ℃煅烧5 h,即可得到MxOy/HPW固体酸催化剂。
1.3 催化剂的表征
采用Bruker D8A A25型X射线衍射仪表征样品的晶相结构,XRD工作条件为:发生器功率9 kW,扫描步长0.02°,扫描速度0.01(°)/s,扫描范围 2θ=5°~90°。采用KBr压片法,以Frontier型红外光谱仪对样品进行测试,波数范围从3 000~400 cm-1。采用merlin型扫描电子显微镜(SEM)对样品微粒的微观形貌进行检测。
1.4 大豆油环氧化反应
将20 g大豆油加入三口圆底烧瓶中,同时按一定比例加入甲酸和催化剂,启动搅拌装置,以一定搅拌速率搅拌混合物并加热到所需温度,同时逐滴加入过氧化氢。从双氧水滴加完毕开始计时,反应进行3 h。取样离心分离,弃去水层,将油层用3%氢氧化钠溶液、温蒸馏水依次洗涤直至中性,然后进行减压蒸馏,得环氧大豆油。采用GB/T 1677—2008增塑剂环氧值的测定方法分析样品的环氧值[16]。所有实验重复3次,结果以平均值表示。根据式(1)计算环氧值相对转化率(RCO) :
环氧值相对转化率(RCO)=OOexOOth×100
(1)
式中:OOex(g/100 g样品)为实验所得环氧值;OOth为理论最大环氧值,由式(2)得出:
OOth=[(IV0/2Ai)100+(IV0/2Ai)A0]×A0×100
(2)
式中:Ai(126.9)和A0(16.0)分别为碘和氧的相对原子质量;IV0为油样的原始碘值。
2 结果与讨论
2.1 固体酸催化剂的催化性能
采用共沉淀-浸渍法制备了一系列MxOy-SnO2-ZrO2/HPW型催化剂,并在反应温度60 ℃、反应时间3 h、催化剂用量为1.0%(为质量分数,且以大豆油为基准)、n(C=C)∶n(H2O2) ∶n(HCOOH)=1∶2.0∶1.6,搅拌速率为300 r/min的条件下对各催化剂应用于大豆油环氧化中的催化活性进行了筛选,MxOy-SnO2-ZrO2/HPW对大豆油环氧值相对转化率的影响如图1所示。可以看出,负载不同金属金属氧化物的催化效果由强到弱的顺序为:WO3-SnO2-ZrO2/HPW、CeO2-SnO2-ZrO2/HPW、SiO2-SnO2-ZrO2/HPW、La2O3-SnO2-ZrO2/HPW、Al2O3-SnO2-ZrO2/HPW。其中,WO3-SnO2-ZrO2/HPW表现出较好的催化活性,环氧值相对转化率达到82.89%。
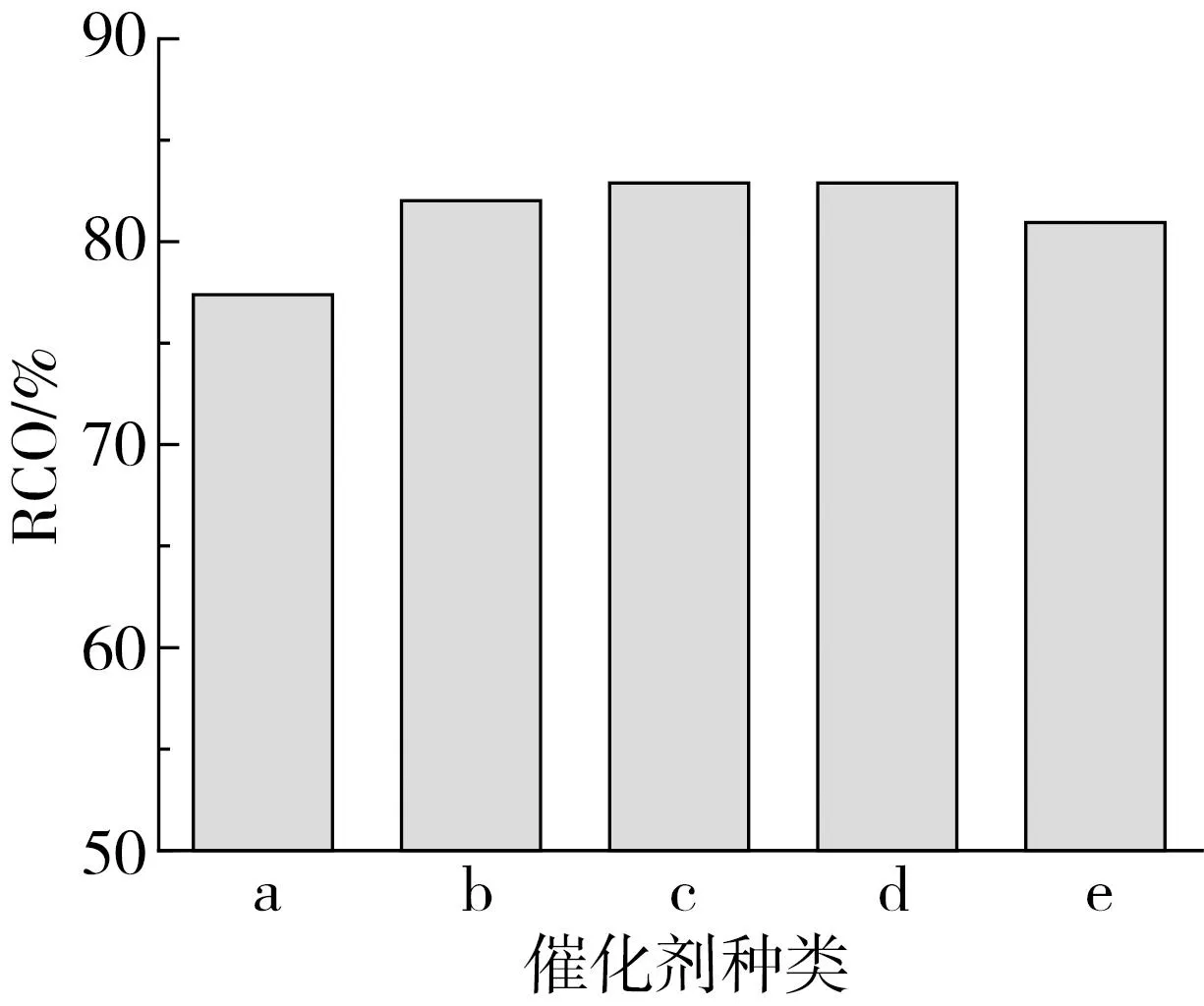
注:MxOy=(a) Al2O3; (b) SiO2; (c) WO3; (d) CeO2; (e) La2O3。
2.2 催化剂表征
2.2.1 XRD表征
负载不同金属氧化物的MxOy-SnO2-ZrO2/HPW催化剂的XRD图如图2所示。可以观察到各谱线中均出现了二氧化锆的特征峰:在24.1°、28.3°、31.1°和34.2°出现的2θ峰属于m-ZrO2(单斜相),50.0°、59.9°出现的2θ峰属于t-ZrO2(四方相)[17,18],但在图2中没有出现明显的SnO2衍射峰,结合图4中EDX元素分析,说明SnO2以无定形状态存在,已均匀分布到ZrO2表面。在SiO2-SnO2-ZrO2/HPW谱线中,分别在2θ=21.0°、26.8°、36.6°、39.2°、50.0°、59.9°和68.0°观察到了SiO2的衍射峰(PDF#46-1045);在WO3-SnO2-ZrO2/HPW谱线中,分别在2θ=23.0°、23.8°、24.0°和34.0°观察到了WO3的衍射峰(PDF#32-1395);在CeO2-SnO2-ZrO2/HPW谱线中,分别在2θ=28.3°、47.5°、56.1°、76.8°和88.2°观察到了CeO2的衍射峰(PDF#34-0394);而La2O3-SnO2-ZrO2/HPW和Al2O3-SnO2-ZrO2/HPW谱线中没有观察到负载的La2O3和Al2O3的衍射峰,但在金属氧化物负载后,原有的SnO2-ZrO2/HPW的峰强度变弱,可能是由于金属氧化物的负载导致样品中SnO2-ZrO2/HPW的相对含量降低[19]。
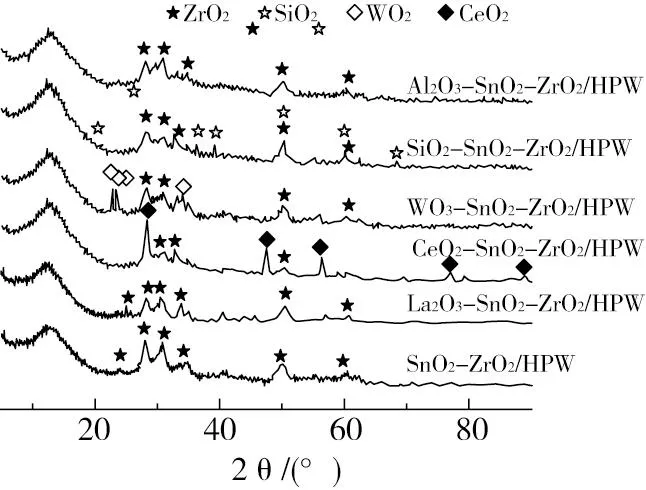
图2 负载不同金属氧化物的MxOy-SnO2-ZrO2/HPW催化剂的XRD图
2.2.2 FT-IR表征
负载不同金属氧化物的MxOy-SnO2-ZrO2/HPW催化剂的FT-IR图如图3所示。可以发现,各催化剂样品都存在着相似的特征峰。在1 630 cm-1附近之间出现了属于吸附水的H—O—H带的弯曲振动峰[20,21]。1 398.96 cm-1出现的谱带与—OH 基团有关,这是金属氧化物的特征[22]。在1 080、890 cm-1附近观察到的特征峰,可对应于磷钨酸P—Oa、WObW的吸收峰[23]。在1 043.2 cm-1处观察到Zr—O—C的伸缩振动吸收峰,在510和589 cm-1处观察到的两个特征峰,均属于Zr—O伸缩振动[24]。而O—Sn—O键的伸缩振动位于601 cm-1附近[24],与Zr—O伸缩振动重叠。对于添加不同金属氧化物的催化剂,分别从谱线图中观察到,Al2O3-SnO2-ZrO2/HPW谱线中Al—O的弯曲振动峰出现在588 cm-1附近[25];SiO2—SnO2—ZrO2/HPW谱线中,1 080 cm-1附近出现的特征峰归属Si—O—Si[26];WO3-SnO2-ZrO2/HPW谱线中,W—O键的振动峰出现在762.5、425 cm-1[27,28];CeO2—SnO2—ZrO2/HPW谱线中,Ce—O的特征峰位于655 cm-1附近[29],在谱线中不明显可能是因为和Sn—O 键的相互作用所致;La2O3—SnO2—ZrO2/HPW谱线中,出现在1 523、1 460 cm、854 cm-1的特征峰归属于La2O3[30]。
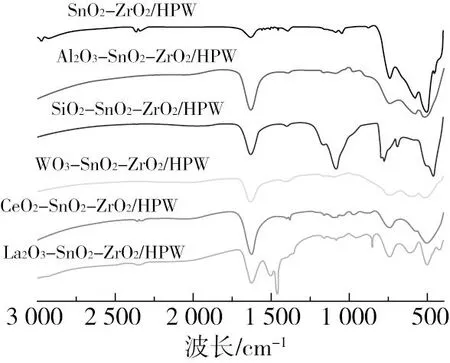
图3 负载不同金属氧化物的MxOy-SnO2-ZrO2/HPW催化剂的FT-IR图
2.2.3 SEM-EDX表征
为了进一步探究催化剂的形貌,对催化性能较好的WO3-SnO2-ZrO2/HPW进行SEM表征,WO3-SnO2-ZrO2/HPW的SEM-EDX图如图4所示。观察到催化剂呈现出0~10 μm左右的不规则块状,结合EDX元素分析,可知大的块状物质主要为Zr,且观察到Sn和W分散在块状结构表面,说明ZrO2作为催化剂的载体,SnO2和WO3等金属氧化物主要为细小颗粒分布在ZrO2块状表面。
2.3 环氧化反应的单因素优化
选用WO3-SnO2-ZrO2/HPW催化剂对环氧化反应的反应条件进行研究。甲酸作为环氧化反应体系中的氧载体,所以研究甲酸和大豆油中双键摩尔比十分关键[31]。甲酸用量对大豆油环氧值相对转化率的影响如图5a所示,RCO值随着甲酸用量的增加,呈现出先增加后下降的趋势。这是因为适量的甲酸可以促进过氧甲酸的生成,从而促进环氧化反应的进行。然而,由于羧酸的存在,反应混合物的酸性同样有利于开环副反应的发生,从而降低环氧油的环氧值相对转化率[32]。

图5 操作条件对大豆油环氧值相对转化率的影响
在环氧化反应中,双氧水作为氧供体,与羧酸共同生成过氧羧酸[33]。双氧水用量对大豆油环氧值相对转化率的影响如图5a所示,可以观察到环氧化效果随着双氧水用量的增加而增加,在n(H2O2)∶n(CC)=1.2∶1到2.0∶1时转化率提高的效果较为明显,继续增加双氧水用量,增加的趋势较为缓慢,在n(H2O2)∶n(CC)=2.8∶1时,转化率最高,达到86.09%。再继续增加双氧水的用量,大豆油的转化率没有继续增加,反而有略微下降的趋势。说明适量的双氧水是必要的,而过量的双氧水可能会导致开环反应的发生,从而降低RCO值[34]。
反应温度对环氧值相对转化率和环氧乙烷环的稳定性具有重要影响。在本研究中,观察反应温度在50、55、60、65、70 ℃变化,以了解该参数如何影响RCO,反应温度对大豆油环氧值相对转化率的影响如图5a所示。提高反应温度会提高环氧值相对转化率,但继续增高温度,RCO值不增反降。因为低温不利于反应物分子与催化剂活性中心充分接触,而随着反应温度的升高,反应物分子间运动速度和碰撞的频率也随之提高,从而加快了反应的速度,环氧值相对转化率随之提高[35]。继续升高温度,转化率又出现降低,这是由于环氧乙烷环是一个非常活泼的三元环,很容易发生开环反应生成不必要的副产物,即环氧化物产物在酸性体系中在高反应温度下不稳定[36,37]。
通过调节搅拌速率在200~400 r/min之间进行实验,观察搅拌速率对RCO的影响,搅拌速率对大豆油环氧值相对转化率的影响如图5b所示。RCO值随着搅拌速率的增加呈现先增加后降低的趋势。在350 r/min的搅拌速度和3 h的反应时间下,RCO最高(87.21%)。说明搅拌速率对RCO有显著影响,即把搅拌速率提高会增加环氧乙烷的形成,但过高的搅拌速率对反应也不利。因为高搅拌速度对于确保所有反应物充分混合具有重要作用,这有助于环氧化过程中的热传递;而过度混合会使溶液不稳定[36]。
催化剂用量对大豆油环氧值相对转化率的影响如图5b所示,催化剂以活性位点的形式对反应起着促进作用[38],增加催化剂的用量,即可增加反应体系中催化剂的活性位数量,使得环氧化反应的转化率提高。但是当催化剂用量增加至1.5%时,环氧大豆油的RCO出现下降趋势,这是因为催化剂量的增加导致反应体系酸性增加,酸性使得环氧键开环,生成副产物[35]。由图5b可知,选用催化剂用量为1.0%较为合适。
在反应体系中,环氧乙烷环会由于酸的存在和高温打开,且这些副反应与环氧化物的形成同时发生,因此,控制环氧化的反应时间也格外的重要[39]。反应时间对大豆油环氧值相对转化率的影响如图5b所示,环氧值相对转化率随着反应时间的增加,先增加后降低。在反应时间为3 h是环氧化效果较好,原因可能是由于反应时间的延长,体系中甲酸和双氧水生成的水逐渐增多,甲酸和双氧水逐渐被消耗,过氧甲酸形成的量及速度减少,从而减缓了环氧化反应的进行;同时水分的增加也促进了开环副反应[40]。
2.4 WO3-SnO2-ZrO2/HPW的重复使用性能
反应结束后,将反应液进行离心分离,所得固体催化剂依次环己烷和蒸馏水洗涤,然后在110 ℃烘箱中烘干8 h后,置于550 ℃马弗炉中煅烧2 h,用于下次反应。催化剂重复性实验均在催化剂用量为1.0%、n(C=C)∶n(H2O2) ∶n(HCOOH)=1∶2.8∶1.2、反应温度为60 ℃、搅拌速率为350 r/min、反应时间为3 h的条件下进行。WO3-SnO2-ZrO2/HPW催化合成环氧大豆油反应的重复使用性能如图6所示。经过5次使用后,环氧大豆油的环氧值相对转化率仅出现了轻微下降。结果表明,WO3-SnO2-ZrO2/HPW对大豆油的环氧化反应具有较好的重复使用性能。

图6 WO3-SnO2-ZrO2/HPW的重复使用性能
3 结论
采用共沉淀-浸渍法制备了一系列负载不同金属氧化物的MxOy-SnO2-ZrO2/HPW 催化剂(MxOy=Al2O3,SiO2,WO3,CeO2和 La2O3)。分别研究了各催化剂催化大豆油环氧化的性能,其中WO3-SnO2-ZrO2/HPW有较好的环氧化催化活性,在反应温度为60 ℃,反应时间为3 h,n(C=C)∶n(H2O2) ∶n(HCOOH)=1∶2.0∶1.6,催化剂用量为1.0%(质量分数),搅拌速率为300 r/min的条件下环氧值相对转化率达到了82.89%。
以WO3-SnO2-ZrO2/HPW为催化剂,考察了甲酸用量、双氧水用量、反应温度、催化剂用量、搅拌速率、反应时间对大豆油环氧化的影响。在催化剂用量为1.0%、n(C=C)∶n(H2O2)∶n(HCOOH)=1∶2.8∶1.2、反应温度为60 ℃、搅拌速率为350 r/min、反应时间为3 h的条件下,大豆油的环氧值相对转化率达到87.21%,表明WO3-SnO2-ZrO2/HPW催化剂可以在一定程度上提高大豆油的环氧化效率。通过考察催化剂的回收性能可知,WO3-SnO2-ZrO2/HPW还具有良好的重复使用性能。
