掺杂锰氧化物的聚乙烯醇基碳包覆复合材料的制备及界面改良优化机制
2023-12-17王雪琪施思齐
王雪琪, 喻 嘉, 施思齐
(上海大学材料科学与工程学院, 上海 200444)
氟化碳基锂(Li/CFx) 电池是一类广泛应用前景的贮备型一次电池. 相比于其他常用的锂一次电池, Li/CFx电池具有比能量高、自放电率低、贮存性能好、搁置时间长、平均年容量损失小于1%等优点[1], 广泛应用于移动电话、笔记本电脑等便携式设备, 心脏起搏器、胶囊内窥镜等医用器材, 无人机、导弹点火装置、潜艇等军用武器装备, 以及航空航天装备、电动汽车、大规模储能技术等领域.
氟化碳(CFx) 材料的氟碳键共价键极强, 导致氟化碳材料的电子电导率较差, 并且氟化碳的表面能极低, 与电解液渗透性差, 容易导致电极极化, 导致Li/CFx的倍率性能受限、电压迟滞、体积膨胀等问题[2], 不能满足高功率放电要求. 为提升锂氟化碳电池倍率性能, 研究者尝试从氟化碳导电性角度入手, 如采用高电导率碳源、表面包覆、复合正极等手段, 其中碳包覆最为常用. 然而, 单一的碳包覆改性方式对电化学性能的改善效果并不突出, 尤其是低电压平台与电压滞后现象制约了倍率性能的提升. 研究者们采用复合的方式对氟化碳进行改性, 将氟化碳与氧化物进行复合, 能够显著改善氟化碳的电化学性能.
二氧化锰(MnO2) 是一种很有前景的电化学活性金属氧化物, 被认为可降低电池电压滞后性. Li 等[3]研究了不同排列组合方式对CFx/MnO2混合正极电化学性能的影响, 发现当CFx和MnO2平行排列时性能最优, 且锂离子的传输速率明显增加, 提升了电池的能量密度和功率密度. Chang 等[4]采用CFx/MnO2作为复合正极材料, 测试分析发现电池的电压平台显著提升、自放电率明显降低, 同时也证明其具有超长的贮存寿命. Guo 等[5]采用化学沉积方法用MnO2涂覆了LiNi1/3Co1/3Mn1/3O2, 氧化锰包覆层可以减少电极与电解液之间的接触面积, 从而减少副反应的发生, 而且在其表面生成了LixMnO2保护层, 可促进电极表面的电荷转移, 提高了复合材料的比容量. Lu 等[6]利用碳包覆层与金属氧化物二氧化锰的协同作用, 用水热法在氟化碳表面包覆了一层三维导电的二氧化锰纳米线, 提高了倍率性能, 也防止类似碳的多孔结构导致电极与电解液发生副反应, 所组装的电池可在6 C 的高倍率进行放电, 能量密度和功率密度均有明显提升. 因此有必要同时引入锰氧化物(MnOx) 进行多组分多机制的协同增效.
本工作提出了掺杂锰氧化物的聚乙烯醇(polyvinyl alcohol, PVA) 基碳包覆CF0.79正极材料的制备方法. 为了更好地提高锂氟化碳电池倍率性能, 引入MnOx和碳包覆进行多组分多机制的协同增效, 并对制备掺杂MnOx的PVA 基碳包覆的CF0.79材料的碳化温度、氧化温度及包覆层厚度进行研究以获得界面改良最佳优化机制. 最后, 采用X 射线衍射(X-ray diffraction, XRD)、扫描电子显微镜(scanning electron microscope, SEM)、X 射线能谱(energy dispersive X-ray spectroscopy, EDX)、X 射线光电子能谱(X-ray photoelectron spectroscopy, XPS) 对改性后的CFx的微观形貌进行表征, 通过电化学性能测试进行电化学表征.
1 实 验
1.1 制备MnOx 的PVA 基碳包覆CFx 复合材料
将1 g 氟化碳加入到滴加了20 µL 分散剂的20 mL 的Mn(NO3)2和PVA 混合溶液中,混合均匀; 采用离心加抽滤法, 得到了表面包覆一层含Mn(NO3)2和PVA 混合溶液的CF0.79材料; 在氩气氛围下进行碳化处理, 选择碳化温度, 升温速率为5◦C/min, 保温时间为6 h,然后自然降温; 在氧气氛围下对碳化处理的CF0.79材料进行高温氧化, 选择氧化温度, 升温速率为5◦C/min, 保温时间为6 h, 然后自然降温, 得到CF0.79@C-MnOx. CF0.79@C-MnOx-X-Y-Z-N表示将包覆有一层PVA 和Mn(NO3)2混合溶液的氟化碳放在管式炉里依次在高温氩气气氛中碳化和氧气气氛中氧化, 其中X表示碳化温度,Y表示氧化温度,Z表示Mn(NO3)2的浓度,N表示PVA 的浓度. 例如: CF0.79@C-MnOx-450◦C 氩气-400◦C 氧气-0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 表示碳化温度450◦C、氧化温度400◦C、Mn(NO3)2浓度0.25 mol/L、PVA 浓度0.25 mol/L 条件下合成的CF0.79@C-MnOx复合材料.
1.2 材料结构与表征
采用Hitachi Regulus-823 公司的场发射SEM 分析材料的微观形貌; 采用PANalytical Empyrean 公司的粉末XRD 分析材料的晶体结构; 采用美国SDT 650 同步热分析仪来分析材料热分解温度; 采用牛津仪器(Oxford Instruments-Ultim Extreme)X 射线能谱仪分析元素分布情况; 采用Nicolet 6700 傅里叶红外光谱仪检测分子反应中各种官能团的相互作用.
1.3 电池组装与电化学性能测试
(1) 电池组装. 首先, 以掺杂锰氧化物聚乙烯醇基碳包覆氟化碳材料w(CF0.79@C-MnOx):w(导电剂乙炔黑)=8∶1 进行手动研磨混合,研磨时间为10 min; 然后, 加入含黏结剂聚偏氟乙烯(polyvinylidenefluoride, PVDF) (质量分数为5%) 的N-甲基吡咯烷酮(NMP) 在脱泡机中进行混合处理(PVDF 的用量与导电剂相等) 30 min, 得到均匀浆料; 接着, 用厚度为100µm的刮刀将浆料均匀涂布至铝箔上, 70◦C 条件下真空干燥3∼4 h, 用裁片机裁剪为圆片极片,100◦C 条件下真空烘10 h 后放入手套箱里; 最后, 以负极壳、弹簧片、不锈钢垫片、锂片, 单层PP/PE 隔膜, 以1 mol/L 六氟磷酸锂溶于n(EC)∶n(EMC)∶n(DMC)=3∶4∶3 的有机溶剂中组成电解液, 正极壳的顺序组成扣式电池(原始氟化碳极片也是如此顺序组装扣式电池), 电解液用量为80 µL.
(2) 电化学性能测试. 用高性能电池测试系统(CT-4008T-5V10mA-164 型) 对装配的电池进行恒流放电测试, 观察电压平台、比容量、倍率性能等. 电池放电截止电压为1.5 V. 用1400A 型电化学综合测试系统对组装的扣式电池进行交流阻抗(electrochemical impedance spectroscopy, EIS) 测试, 交流电压振幅为5 mV.
2 结果与讨论
2.1 电化学性能和热重分析
图1 为CF0.79、高温CF0.79和CF0.79@C-MnOx正极的恒流放电曲线图. C—Mn 基复合材料包覆层有效提高了CF0.79正极的导电性, 因此与CF0.79相比, CF0.79@C-MnOx正极明显提高高倍率下的放电比容量,放电平台也得到了明显提高. 图2 给出了CF0.79和CF0.79@CMnOx的红外谱图. 可以看出, 2 种材料在1 220 cm-1都有C—F 共价键[15-16]的吸收峰区,而在1 100 cm-1附近只有CF0.79@C-MnOx存在C—F 半离子键[17-18]吸收峰区, C—F 键的“半离子” 特性[19]可以被解释为共价键和离子键之间的中间状态. 为了深入研究CF0.79@CMnOx合适的合成温度, 在空气氛围下对氟化碳进行了热重分析(thermogravimetric analysis,TGA)[7]测试(见图3), 可以看出: CF0.79的分解温度为500∼650◦C; 氟化碳分解后生成类似CF4、F2等挥发性氟化碳化合物; 650◦C 后氟化碳不再分解是因为残留的石墨[11]. 综合考虑,本工作中碳化温度上限选择450◦C, 氧化温度上限选择400◦C.
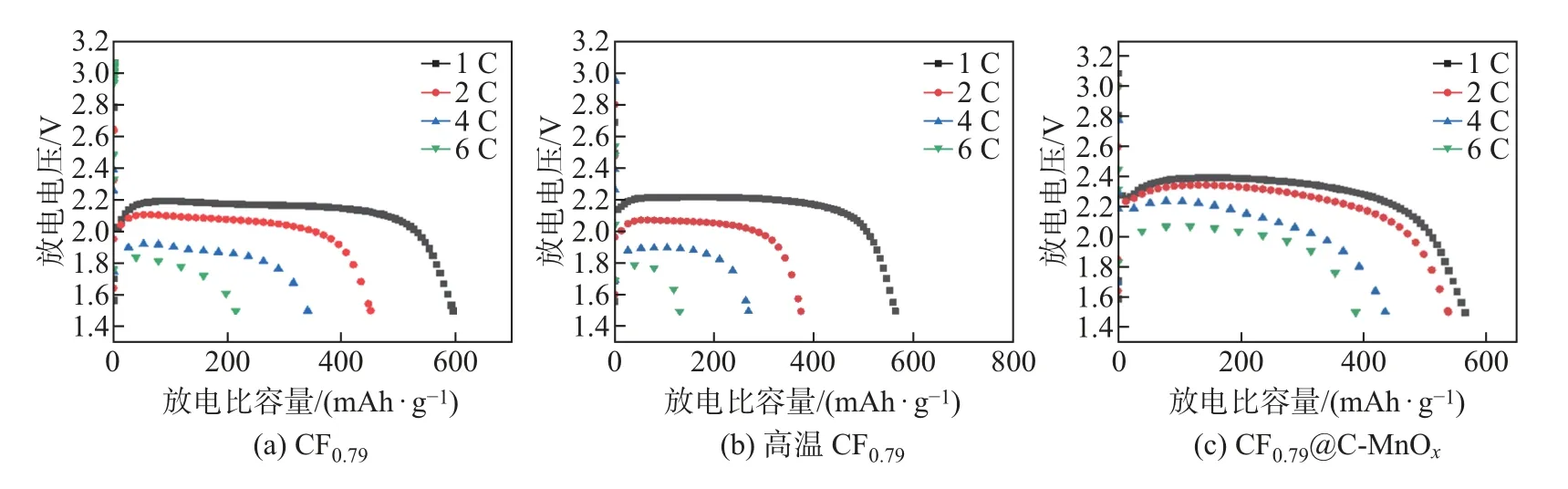
图1 3 种材料正极恒流放电曲线的比较Fig.1 Comparison of galvanostatic discharge curves of three kinds of materials

图2 CF0.79 与CF0.79@C-MnOx 的红外谱图Fig.2 Infrared spectrogram of CF0.79 and CF0.79@C-MnOx

图3 CF0.79 的热重曲线Fig.3 TGA curve of CF0.79
图4 为采用XPS 测定得到的CF0.79和CF0.79@C-MnOx-450◦C 氩气-400◦C 氧气的化学结构和元素价态. 可以看出, CF0.79@MnOx中主要存在C、F、Mn 元素; CF0.79和CF0.79@MnOx的C 1s 和F 1s 光谱分别呈现出不同的碳与氟结合状态. C 1s 光谱中,CF0.79@C-MnOx中半离子C—F 键的结合能小于CF0.79中半离子C—F 键的结合能,而半离子C—F 键的出现有利于提高氟化碳材料导电性. 因此, CF0.79@C-MnOx导电性高于CF0.79.在C 1s 和F 1s 光谱中, CF0.79@C-MnOx共价C—F 键的结合能均低于CF0.79, 这说明与原始氟化碳相比, CF0.79@MnOx中C—F 键含量减少, C—F 键容易断裂, 放电中易与锂离子相结合[20]. 氟化碳本身导电性差也与表面存在的惰性基团C—Fx(x= 2, 3) 有关, 由图4(d)∼(e) 可以看出, 改性后的氟化碳惰性基团C—Fx(x= 2, 3) 结合能(291.4 ev) 低于原始氟化碳惰性基团C—Fx(x= 2, 3) 结合能(291.7 ev)[21-22]. 惰性基团结合能的降低可能与锰氧化物有关, 可能是部分氟与锰氧化物发生了反应. 惰性基团的减少利于放电过程中更多的锂离子扩散到氟化碳正极表面, 使锂氟化碳电池的倍率性能和电压平台都得到了提高.

图4 CF0.79 和CF0.79@C-MnOx 的XPS 图Fig.4 XPS diagram of CF0.79 and CF0.79@C-MnOx
2.2 选择不同的碳化温度
2.2.1 物相与形貌表征
图5 为CF0.79与采用不同碳化温度CF0.79@C-MnOx-X-400◦C 氧气-0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 的SEM 和EDS 图. 可以发现, 原始氟化碳表面成功包覆了碳和锰氧化物, 在碳化温度为300∼325◦C 时, 氟化碳表面掺杂MnOx的碳包覆层出现了很多稀松的孔结构和一些裂缝, 说明碳层的结晶性很差. 碳化温度继续升高到350◦C, 氟化碳表面掺杂MnOx的碳颗粒增加, 均匀地分布在氟化碳层状结构间和氟化碳边缘处; 当碳化温度提高到400◦C, 氟化碳表面掺杂MnOx的碳包覆层出现了很多稀松的孔结构; 继续提高碳化温度到450◦C, 氟化碳表面掺杂MnOx的碳包覆层是光滑的, 没有出现孔洞与裂缝, 但此温度下氟化碳开始出现分解.
图6 为CF0.79与不同碳化温度CF0.79@C-MnOx的XRD 图. 测试结果表明: 不同碳化温度下的CF0.79@C-MnOx晶体结构与原始氟化碳基本一致, 只是CF0.79@C-MnOx的碳衍射峰很强, 说明表面成功包覆了一层碳. 另外, 这也说明用此方法制备复合材料, 碳化温度没有改变CFx的基本结构, 对CFx的晶型结构没影响.

图6 CF0.79 与不同碳化温度CF0.79@C-MnOx 的XRD 谱图Fig.6 XRD patterns of CF0.79 and CF0.79@C-MnOx under different carbonization temperatures
2.2.2 电化学性能测试
图7 为不同倍率下CF0.79和不同碳化温度制备的CF0.79@C-MnOx的恒流放电曲线. 由图可看出: 碳化温度影响复合材料的电化学性能. 当碳化温度为300∼325◦C 时, PVA 碳化后导电性不如纯碳, CF0.79@C-MnOx的倍率性能低于原始氟化碳; 随着温度的提高, 当碳化温度为350◦C 时, 复合材料的倍率性能和电压平台都明显的提高; 进一步提高碳化温度至400◦C 时, 复合材料的放电比容量和电压平台下降; 当碳化温度为425∼450◦C、放电倍率为1 C 时, 复合材料的放电比容量低于原始氟化碳, 说明原始氟化碳开始分解, 高温下氟化碳生成了气体氟化物, 损失了一部分氟含量[12-14].

图7 不同倍率下CF0.79 和CF0.79@C-MnOx 恒流放电曲线的对比Fig.7 Comparison of galvanostatic discharge curves CF0.79 and CF0.79@C-MnOx at different rates
为了更好地确定复合材料最佳的碳化温度, 图8 对比分析了CF0.79与不同碳化温度CF0.79@C-MnOx的放电性能. 可以看出, 碳化温度为350◦C 时, 复合材料的放电比容量是最好的. 在碳化温度425◦C 以上时, 虽然在2、4 和6 C 的电压平台也比其他碳化温度的高一些. 综合考虑, 确定最佳的碳化温度为350◦C.

图8 CF0.79 与不同碳化温度CF0.79@C-MnOx 的恒流放电曲线Fig.8 Galvanostatic discharge curves of CF0.79 and CF0.79@C-MnOx under different carbonization temperatures
2.2.3 交流阻抗测试
锂离子扩散快慢可以从电化学阻抗谱[8]中看出. 阻抗图解释了锂离子在氟化碳正极材料中的3 个扩散过程: 高频区(半圆) 为锂离子在氟化碳正极表面扩散, 中高频区为氟化碳正极和电解液界面电荷传递, 低频区(半圆右侧倾斜的直线) 为锂离子在氟化碳颗粒内部的扩散.图9 是CF0.79与不同碳化温度CF0.79@C-MnOx在放电倍率1 C 条件下的阻抗图. 由图9 可以看出, 碳化温度为350◦C 时CF0.79@C-MnOx的电池反应电阻最小. 颗粒间的接触电阻减小利于氟化碳颗粒间更快的电子传导速率, 同时也加快了电解液中的锂离子在正极表面的输运, 从而加快了电池反应. 这主要归因于适当的碳化温度使导电性良好的MnOx掺杂碳包覆层形成了更好的导电网络. 从电化学阻抗谱中得出, 碳化温度为350◦C 的复合材料具有最佳的电化学性能.

图9 CF0.79 与不同碳化温度CF0.79@C-MnOx 的阻抗图(1 C)Fig.9 Electrochemical impedance spectroscopy of CF0.79 and CF0.79@C-MnOx under different carbonization temperatures (1 C)
考虑物相与形貌表征、电化学性能测试及交流阻抗测试的实验结果, 碳化温度为350◦C的复合材料具有最佳的电化学性能.
2.3 选择不同的氧化温度
2.3.1 物相与形貌表征
图10 为CF0.79与不同氧化温度CF0.79@C-MnOx-350◦C 氩气-Y-0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 的SEM 和对应元素的EDS 分布. 从SEM 图可以看出, 氟化碳表面层状结构不明显, 而从EDS 可以看出, 氟化碳表面成功包覆了Mn. 当氧化温度为300◦C 时, 氟化碳表面零星不均匀分布着白色小颗粒, 这些颗粒应该是MnOx; 当氧化温度为350◦C 时, 氟化碳表面包覆了一层乳白色的包覆层, 不均匀分布着一部分白色的大的颗粒物; 当氧化温度为400◦C 时, 氟化碳表面均匀分布着很多白色小颗粒, 且分布在氟化碳边缘处. 从SEM 对应的EDS 中可以看出, Mn 元素分布均匀.

图10 CF0.79 和不同氧化温度CF0.79@C-MnOx SEM 图以及对应元素的EDS 分布Fig.10 SEM images and corresponding EDS elemental mapping images of CF0.79 and CF0.79@CMnOx under different oxidation temperatures
图11 为CF0.79与不同氧化温度下CF0.79@C-MnOx的XRD 图谱. 从XRD 图可看出,不同氧化温度下的CF0.79@C-MnOx与原始CF0.79的3 个衍射峰基本一致, 其中CF0.79结构中12.6◦与40.8◦对应着氟相[9], 26.8◦出现了一个碳的衍射峰[10]. 不同氧化温度下的CF0.79@C-MnOx晶体结构与原始氟化碳基本一致, 说明用此方法制备的复合材料在不同的氧化温度下没有改变CFx的基本结构, 对CFx的晶型结构没影响.
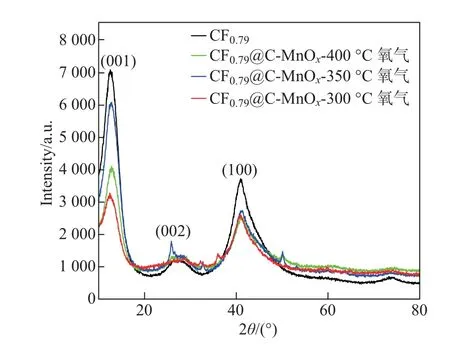
图11 CF0.79 与不同氧化温度下CF0.79@C-MnOx 材料XRD 图谱Fig.11 XRD patterns of CF0.79 and CF0.79@C-MnOx under different oxidation temperatures
2.3.2 电化学性能测试
图12 为CF0.79和不同氧化温度下CF0.79@C-MnOx复合材料的电化学性能. 可以看出:当氧化温度为300∼350◦C 时, CF0.79@C-MnOx复合材料在不同的放电倍率下, 放电比容量均低于原始氟化碳的放电比容, 这可能是MnOx结晶性较差, 导致复合材料的导电性较差; 当氧化温度为400◦C 时, 其放电比容量和电压平台均高于其它氧化温度下的复合材料和原始氟化碳. 图13 是CF0.79@C-MnOx在1、2、4 和6 C 下的恒流放电曲线. 可以看出, 氧化温度为400◦C 时, 放电比容量和电压平台都是最高的.

图12 CF0.79 和CF0.79@C-MnOx 在不同倍率下恒流放电曲线的对比Fig.12 Comparison of galvanostatic discharge curves of CF0.79 and CF0.79@C-MnOx at different rates

图13 CF0.79 与CF0.79@C-MnOx 在不同放电倍率下的恒流放电曲线Fig.13 Galvanostatic discharge curves of CF0.79 and CF0.79@C-MnOx at different rates
2.3.3 交流阻抗测试
图14 是CF0.79与不同氧化温度下CF0.79@C-MnOx在放电倍率为1 C 时的阻抗图. 由阻抗谱可以看出: 在氧化温度为400◦C 时, CF0.79@C-MnOx的正极的阻抗值低于其他氧化温度下CF0.79@C-MnOx和CF0.79的正极的阻抗值; 氧气温度为300◦C 的氟化碳复合材料阻抗值大于纯氟化碳阻抗值, 说明这个温度下锰氧化物可能结晶太差, 不利于锂离子扩散到氟化碳正极上. 氧化温度为350 和400◦C 的复合材料阻抗值均小于纯氟化碳阻抗值, 通过不同氧化温度下的阻抗值的比较, 氧化温度为400◦C 的复合材料材料阻抗值最小, 也说明400◦C时MnOx形貌与结构有利于锂离子扩散, 放电性能也是最好的.

图14 CF0.79 与不同氧化温度下CF0.79@C-MnOx 的阻抗图(1 C)Fig.14 Electrochemical impedance spectroscopy of CF0.79 and CF0.79@C-MnOx under different oxidation temperatures (1 C)
综合考虑物相与形貌表征、电化学性能测试及交流阻抗测试的实验结果, 氧化温度为400◦C 的复合材料具有最佳的电化学性能.
2.4 选择不同的包覆层厚度
2.4.1 物相与形貌表征
改变包覆层厚度即通过改变Mn(NO3)2与PVA 浓度来调控氟化碳材料的包覆层. 图15为不同Mn(NO3)2和PVA 浓度制备的CF0.79@C-MnOx的SEM 和EDS 图. 由图15 可以发现, 氟化碳是片层状结构, 不同浓度的Mn(NO3)2和PVA 包覆的氟化碳形貌是不同的. 当PVA 浓度为0.05 mol/L、Mn(NO3)2浓度为0.05∼0.25 mol/L 时, 氟化碳表面光滑, 层状结构明显, 颗粒物很少附着在其表面, 包覆的碳颗粒少; 而当PVA 浓度为0.25 mol/L、Mn(NO3)2浓度为0.25 mol/L 时, 氟化碳表面掺杂MnOx的碳颗粒增加, 并均匀分布在氟化碳层状结构间和氟化碳边缘处. 由不同Mn(NO3)2/PVA 浓度制备的氟化碳材料的EDS 可以看出, 氟化碳都成功地包覆了Mn. 比较4 种浓度情况下复合正极材料与氟化碳的XRD 图(见图16), 可以看出, 用此方法制备的复合材料没有改变CFx的基本结构.
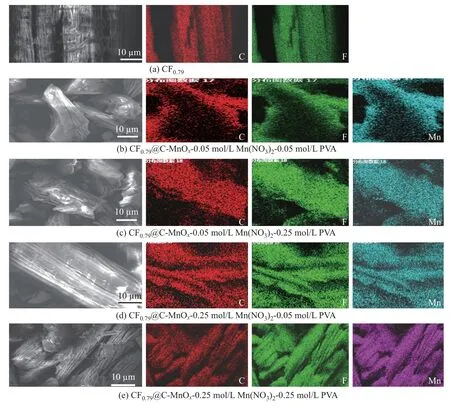
图15 CF0.79 与不同Mn(NO3)2/PVA 浓度制备CF0.79@C-MnOx 的SEM 图以及对应元素的EDS 分布Fig.15 SEM images and corresponding EDS elemental mapping images of CF0.79 and CF0.79@C-MnOx under different concentrations of Mn(NO3)2/PVA

图16 CF0.79 与不同Mn(NO3)2/PVA 制备的CF0.79@C-MnOx 的XRD 图谱Fig.16 XRD patterns of CF0.79 and CF0.79@C-MnOx under different concentrationsof Mn (NO3)2/PVA
2.4.2 电化学性能分析
图17 为CF0.79和Mn(NO3)2/PVA 浓度分别为0.05/0.05 mol/L、0.05/0.25 mol/L、0.25/0.05 mol/L、0.25/0.25 mol/L 制备的CF0.79@C-MnOx复合正极材料的放电曲线图. 由图可以看出, 与CF0.79相比, 不同PVA 和Mn(NO3)2浓度制备复合材料的放电比容量增加, 电压平台提高以及放电初期电压迟滞现象得到了明显改善. 0.25 mol/L PVA 基碳包覆层致密的包裹在氟化碳表面加上无定形碳的多孔结构, 利于更多的电解中的锂离子输运到电极表面, 减小极化. 0.25 mol/L 锰氧化物颗粒均匀的分布在氟化碳层间和边缘处浓度较高的锰氧化物颗粒可以作为孤立的氟化碳颗粒的电子桥进行电子传输.

图17 CF0.79 和不同浓度的Mn(NO3)2/PVA 制备的CF0.79@C-MnOx 恒流放电曲线的对比Fig.17 Comparison of Galvanostatic discharge curves of CF0.79 and CF0.79@C-MnOx under different concentrations of Mn (NO3)2/PVA
图18 为CF0.79@C-MnOx在1、2、4 和6 C 下恒流放电曲线图对比. 可以看出: 不同放电倍率下, 当PVA 和Mn(NO3)2的浓度为0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 时, 放电比容量和电压平台均是最高的; 从图18(a) 可以更清晰地看出, 在1 C 放电倍率下, 不同浓度的PVA 与Mn(NO3)2包覆的CF0.79@C-MnOx放电比容量都在700 mAh/g 以上, 远高于CF0.79的放电比容量(568 mAh/g), 进一步说明包覆是有效的.
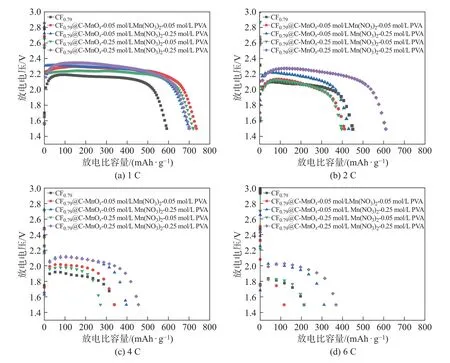
图18 CF0.79 和不同Mn(NO3)2/PVA 浓度制备的CF0.79@C-MnOx 恒流放电曲线图的对比Fig.18 Comparison of galvanostatic discharge curves of CF0.79 and CF0.79@C-MnOx under different concentrations of Mn(NO3)2/PVA
2.4.3 交流阻抗测试
图19 是CF0.79与不同Mn(NO3)2/PVA 浓度制备的CF0.79@C-MnOx在放电倍率为2 C条件下的阻抗图. 从阻抗谱发现, CF0.79@C-MnOx-0.25 mol/L Mn(NO3)2-0.25 mol/L PVA正极的阻抗值都低于其他浓度情况下的氟化碳材料. 这也说明应适当地提高Mn(NO3)2/PVA的浓度. 高浓度下的Mn(NO3)2和PVA 溶液包覆在氟化碳表面, 经高温碳化和氧化烧结后的导电包覆层为氟化碳表面提供了更多的电子路径, 有利于锂离子的扩散, 阻抗值最低, 电化学性能最好.
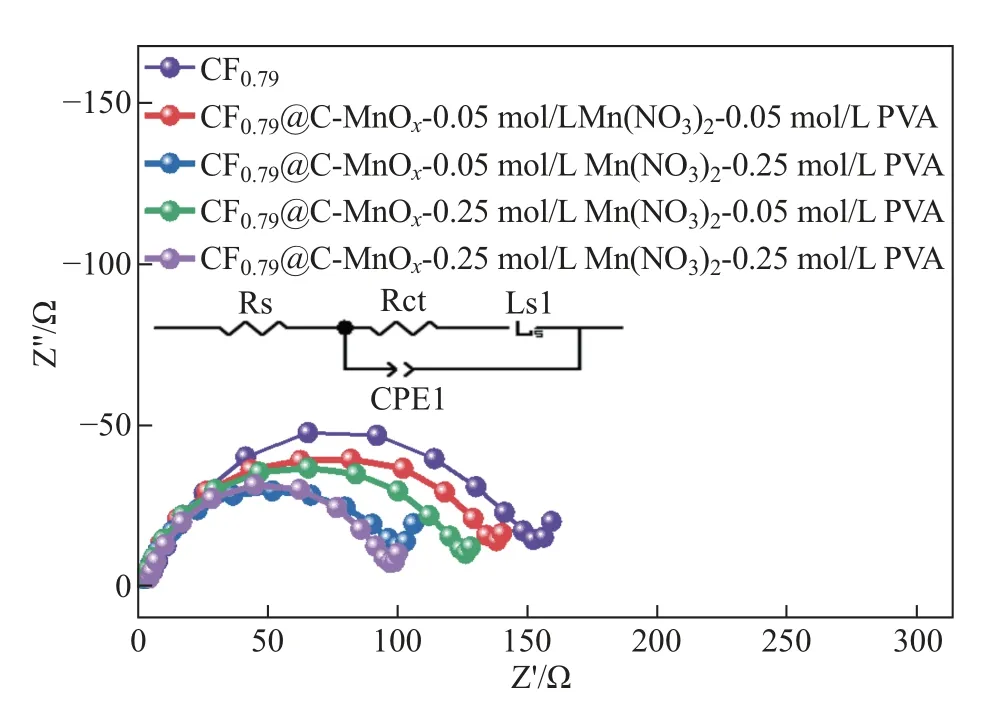
图19 CF0.79 与不同Mn(NO3)2/PVA 浓度制备的CF0.79@C-MnOx 的阻抗图(2 C)Fig.19 Electrochemical impedance spectroscopy of CF0.79 and CF0.79@C-MnOx under different concentrations of Mn(NO3)2/PVA (2 C)
综合上述物相与形貌表征、电化学性能测试及交流阻抗测试的实验结果, 0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 制备的复合材料具有最佳的电化学性能.
3 结 论
本工作采用简单的抽滤法在氟化碳表面包覆一层掺杂锰氧化物的有机碳源聚合物包覆层,再分别通过氩气和氧气氛围下的煅烧制备了掺杂MnOx的聚乙烯醇基碳包覆CF0.79正极材料. 为了改善氟化碳的界面, 进一步研究了制备掺杂锰氧化物的聚乙烯醇基碳包覆的氟化碳材料的不同碳化温度、氧化温度及包覆层厚度对复合材料性能的影响, 通过物相与形貌表征、电化学性能及交流阻抗测试的实验, 得出如下结论:
(1) 选择抽滤法与高温烧结相结合的方法制备的掺杂MnOx的聚乙烯醇基碳包覆CF0.79正极材料, 在氟化碳表面确实成功了包覆了一层掺杂锰氧化物的碳壳, 且与原始氟化碳相比,放电比容量增加, 电压平台提高, 放电初期电压迟滞现象得到了明显改善.
(2) 425◦C 以上时, 氟化碳可能在氩气气氛中出现轻微分解, 碳化温度350◦C 时复合材料可获得导电性较好的碳层, 在放电比容量和电压平台方面优于其他碳化温度. 当氧化温度较低时, MnOx可能结晶性较差, 复合材料的导电性较差, 导致CF0.79@C-MnOx在不同的放电倍率下, 放电比容量均低于原始氟化碳的放电比容量; 当氧化温度为400◦C 时,复合材料的放电比容量和电压平台均高于其他氧化温度下的复合材料和原始氟化碳. 通过改变Mn(NO3)2/PVA 的浓度调控氟化碳材料的包覆层, 以改善氟化碳的界面, 一般当Mn(NO3)2/PVA 浓度为0.25/0.25 mol/L 时制得的复合材料的放电比容量和电压平台是最高的. 综上所述, CF0.79@C-MnOx-350◦C 氩气-400◦C 氧气-0.25 mol/L Mn(NO3)2-0.25 mol/L PVA 的复合材料具有较佳的电化学性能.
(3) 通过XRD、SEM 和EDS 测试证明氟化碳表面确实成功包覆了掺杂MnOx的聚乙烯醇基碳层. 通过TG 得出氟化碳合成材料较适合的碳化和氧化温度. 通过XPS 解释了改性后的氟化碳电化学性能高的原因. 此外, 红外测试与XPS 也测出了改性后较低结合能的半离子C—F 键以及结晶度较低的LiF, 这也能解释改性后的氟化碳电子/离子电导率高的原因. 通过EIS 的数据发现, 改性后的氟化碳有较小的电荷转移阻抗, 这也说明电解液中的锂离子更容易扩散到氟化碳正极上. 从而在电化学性能上得到了充分体现.
