Hippo-YAP通路参与NaAsO2对PC12细胞周期及细胞凋亡的影响
2023-12-12张小龙康文润王宏健王东艳潘际刚
吴 松,顾 丹,张小龙,康文润,刘 宇,李 成,王宏健,王东艳,潘际刚
( 贵州医科大学基础医学院1.生理学教研室、2.机能实验室,贵州 贵阳 550025)
砷是一种在自然界中广泛存在的非金属元素,人群常通过水、食物和空气等途径接触砷而导致人体砷中毒[1]。我国是砷污染较为严重的国家,其中贵州是我国一个典型的燃煤污染型地方性砷中毒病区[2]。经过流行病学调查,发现砷可造成包括心血管系统、呼吸系统、神经系统、内分泌系统和皮肤在内的许多人体系统和器官的毒性损伤[3]。砷可诱发中枢和周围神经病变,导致多发性神经炎和神经衰弱等疾病[4]。但是,砷引起神经损伤的具体机制至今仍不十分明确。Hippo-YAP信号通路的核心部分是由3个激酶组成的级联反应构成,分别是哺乳动物STE20样蛋白激酶1/2(mammalian STE20-like protein kinase 1/2,MST1/2),大肿瘤抑制因子1/2 (large tumor suppressor 1/2,LATS1/2) 和最终效应因子Yes 相关蛋白(Yes-associated protein,YAP)[5]。此通路在调节细胞周期、控制细胞增殖与凋亡方面有重要作用,并且在进化上高度保守[6]。本课题组前期研究已经证明,NaAsO2能激活Hippo-YAP通路,诱导PC12细胞凋亡,促进细胞S期阻滞[7],而且Hippo-YAP通路参与NaAsO2影响PC12细胞活力、形态及突触后致密蛋白95(post synaptic density protein,PSD95)、突触素蛋白(synaptophysin,SYN)表达[8]。那么,Hippo-YAP信号通路是否参与NaAsO2对PC12细胞周期及细胞凋亡的影响,本实验将在前期研究基础上对这些问题进行探讨。
1 材料与方法
1.1 材料
1.1.1细胞系 PC12细胞株,从中科院昆明细胞库购买。
1.1.2试剂 亚砷酸钠(S7400)购于美国Sigma 公司。青霉素 - 链霉素(15140163)、高糖DMEM培养基(8120293)和胰蛋白酶(25200056)均购自Gibco公司。胎牛血清(10099141C)于BioInd 公司购买。XMU-MP-1(HY-100526)购自MCE公司。一抗抗体LATS1(17049-1-AP)、MST1(22245-1-AP)、YAP1(13584-1-AP)、BAX(50599-2-Ig)、p53(10442-1-AP)和BCL-2(12789-1-AP)均在 ProteintechGroup公司购买。Phospho-MST1(49332S)和Phospho-LATS1(9157S)购自Cell Signaling Technology。Phospho-YAP1(ab76252)订购自Abcam。内参抗体Tubulin(11224-1-AP)、Histone-H3(17168-1-AP)和GAPDH(10494-1-AP)于ProteintechGroup公司订购。抗兔 IgG-HRP二抗(ZB-2305)从北京中衫金桥订购。细胞周期检测试剂盒(KGA512)及细胞凋亡检测试剂盒Annexin V-FITC /PI( KGA1012)于凯基生物购买。核蛋白提取试剂盒(R0050)从索莱宝购买。
1.1.3仪器 流式细胞仪FACSCalibur(美国BD公司),细胞超净工作台(苏州净化),凝胶全自动成像仪(美国 SynGene公司),全波长多功能酶标仪(美国 BioTek 公司),恒温二氧化碳细胞培养箱Model 310(美国ThermoFisher公司),激光共聚焦显微镜(日本Nikon公司)。
1.2 方法
1.2.1细胞培养 PC12细胞置于饱和湿度、37 ℃和5% CO2的培养箱中,用含10% FBS和1%青霉素-链霉素的高糖DMEM全培养基进行培养。培养基两天更换一次,细胞融合度达到80%时,进行传代或冻存。
1.2.2细胞处理及分组 免疫荧光实验将细胞分为control组和NaAsO2(40 μmol·L-1)组,其余实验将细胞分为control组、NaAsO2(40 μmol·L-1)组、NaAsO2+XMU-MP-1(3 μmol·L-1)组、XMU-MP-1组。
1.2.3细胞周期检测 PC12细胞以5×108L-1的密度铺于6孔板中培养过夜。以含3 μmol·L-1XMU-MP-1的高糖DMEM培养基对NaAsO2+XMU-MP-1组及XMU-MP-1组细胞预处理4 h。之后分别用含40 μmol·L-1NaAsO2、40 μmol·L-1NaAsO2+3 μmol·L-1XMU-MP-1、3 μmol·L-1XMU-MP-1的高糖培养基处理细胞,空白对照组以高糖培养基培养。细胞处理24 h,无EDTA胰酶消化并收集。使用PBS进行清洗,然后以1 100 r·min-1的速度离心5 min,这个步骤重复2次,并且丢弃上清液。接着,使用70%的乙醇在4 ℃下固定30 min,固定完成后以1 100 r·min-1的速度离心5 min并丢弃固定液。再次使用PBS清洗2次,加入300 μL的PI/RNase,避光在室温下孵育60 min。最后,使用流式细胞仪对细胞样品进行检测。
1.2.4流式细胞仪检测PC12细胞凋亡 本实验分组以及细胞收集、固定步骤同“1.2.3”。接着PBS洗2次,1 100 r·min-1离心弃上清。加500 μL PBS吹打得细胞悬液。然后加入5 μL Annexin V-FITC和10 μL PI振荡混匀,避光冰上静置20 min ,用流式细胞仪检测。
1.2.5核质分离 在处理完所有细胞组后,移除培养液并用PBS进行一次清洗。然后,使用细胞刮刀收集细胞,以2 000 r·min-1的速度离心2 min,丢弃上清液。接着,加入200 μL的浆蛋白提取试剂,摇匀后在冰浴中放置10 min。然后进行高速振荡,4 ℃下以1.2×104r·min-1的速度离心10 min,取上清液(即细胞浆蛋白)备用。细胞核为沉淀物,加入50~100 μL的核蛋白提取试剂,高速涡旋15 s以确保充分分散,然后在冰浴中放置10 min。再次进行高速涡旋,4 ℃下以1.2×104r·min-1的速度离心10 min,取上清液(即细胞核蛋白)。
1.2.6Western blot检测经过药物处理的各组细胞,使用200 μL含有PMSF的RIPA裂解液在冰上裂解细胞10 min,然后以1.2×104r·min-1离心15 min。使用BCA法测量上清液的浓度。然后使用双蒸水和5×上样缓冲液将各组蛋白调至相同浓度,以100 ℃变性8 min。使用恒压电泳将蛋白质分离,然后转移到PVDF膜上。在室温下使用5%脱脂牛奶封闭2 h,然后在4 ℃下孵育一夜使用一抗(根据抗体说明书稀释)或内参(GAPDH、Tubulin、Histone-H3)。使用TBST洗膜5 min,重复3次,然后在室温下孵育兔二抗(1 ∶10 000稀释)2 h。再次使用TBST洗膜3次,使用化学发光方法,全自动凝胶成像仪进行检测,并用ImageJ软件进行蛋白条带的分析和处理。

2 结果
2.1 NaAsO2对PC12细胞中YAP蛋白核质分布的影响核质分离,检测YAP蛋白核质分布,如Fig 1A所示,与control组相比,40 μmol·L-1NaAsO2组中YAP总蛋白的表达无变化,细胞质内的YAP蛋白表达明显升高(P<0.05),而细胞核内YAP蛋白的表达明显减少(P<0.01)。利用免疫荧光对YAP蛋白染色,如Fig 1B所示,control组的细胞核显示较强的红色荧光,胞质内荧光强度较弱;而NaAsO2处理后,细胞核中的红色荧光减弱,胞质内荧光增强。

Fig 1 Effect of NaAsO2 on YAP protein in cytoplasmic and nucleus of PC12 cells detected by Western blot (A) and immunofluorescence (B)
2.2 XMU-MP-1抑制NaAsO2激活Hippo-YAP通路如Fig 2所示,与control组相比,40 μmol·L-1NaAsO2处理PC12细胞24 h后,Hippo-YAP信号通路中的p-MST1、p-LATS1、p-YAP蛋白表达以及p-LATS1/LATS1、p-YAP/YAP比值增加(P<0.01)。而经过XMU-MP-1(MST1/2抑制剂)预处理后,p-MST1、p-LATS1、p-YAP蛋白表达以及p-LATS1/LATS1、p-YAP/YAP比值相比于NaAsO2组均有所下调(P<0.05)。
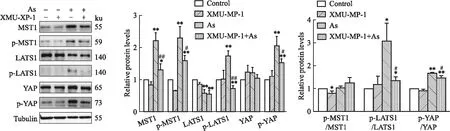
Fig 2 Effect of NaAsO2 and XMU-MP-1 on expression of proteins associated with Hippo-YAP signaling pathway in PC12 cells
2.3 Hippo-YAP通路参与NaAsO2对PC12细胞周期的影响通过流式细胞仪检测各组细胞周期的变化,如Tab 1和Fig 3所示,与control组相比,XMU-MP-1对PC12细胞周期无影响。NaAsO2组G0/G1期细胞比例由control组的(63.80±0.69)%下降到(59.83±1.02)%(P<0.01),S期比例由control组的(17.25±1.09)%上升到(19.29±0.63)%(P<0.05),提示细胞周期被阻滞在S期。而XMU-MP-1预处理后,G0/G1期细胞比例由NaAsO2组的(59.83±1.02)%上升到(64.62±0.56)%(P<0.01),S期比例由NaAsO2组的(19.29±0.63)%下调到(16.71±0.31)%(P<0.01),可逆转NaAsO2对S期的影响。
Tab 1 Effect of NaAsO2 and XMU-MP-1 on cell cycles
2.4 Hippo-YAP通路参与NaAsO2对PC12细胞凋亡的诱导利用流式细胞仪检测各组细胞凋亡率,如Fig 4所示, PC12细胞经NaAsO2处理24 h后,凋亡率由control组的3.83% 上升至11.00%(P<0.01),而XMU-MP-1预处理后,凋亡率由NaAsO2组的11.00%下降到6.88%(P<0.05)。然后,再利用Western blot检测凋亡相关蛋白,如Fig 5所示,与control组相比,NaAsO2处理24 h后明显下调BCL-2蛋白表达,上调BAX、P53蛋白表达(P<0.01)。而与NaAsO2组相比,XMU-MP-1预处理可以上调BCL-2蛋白表达,下调P53、BAX蛋白表达(P<0.05)。两部分结果都表明,XMU-MP-1预处理可以部分逆转NaAsO2诱导的细胞凋亡。

Fig 3 Effect of NaAsO2 and XMU-MP-1 on cell cycles of PC12 cells

Fig 4 Effect of NaAsO2 and XMU-MP-1 on apoptosis rates of PC12 cells
3 讨论
研究显示,砷暴露严重影响学习记忆、认知能力以及神经系统的发育[9]。课题组前期研究证明NaAsO2可抑制PC12细胞生长[10],促进细胞凋亡,并且干扰细胞周期,激活Hippo-YAP信号通路[7]。

Fig 5 Effect of NaAsO2 and XMU-MP-1 on expression of apoptosis-related proteins in PC12 cells
Hippo-YAP信号通路是一条高度保守的信号通路,可以对细胞增殖与凋亡进行调控。文献报道,Hippo-YAP通路激活时,首先是MST1/2被磷酸化激活,然后MST1/2磷酸化LATS1/2,最终导致YAP蛋白磷酸化阻止其入核;而Hippo-YAP通路失活时,未磷酸化的YAP蛋白转移至细胞核,然后与转录因子TEAD结合以诱导细胞生长和增殖相关的基因表达[5]。而用XMU-MP-1抑制MST1/2的活性可逆转NaAsO2对Hippo-YAP通路的激活及对PC12细胞活力、形态及神经突触相关蛋白的影响[8]。本次实验还发现,NaAsO2激活Hippo-YAP通路后可抑制YAP蛋白入核,这可能是Hippo-YAP通路参与NaAsO2对PC12细胞生长的依据。
细胞周期分四个不同阶段,DNA合成前期(G1期)、DNA合成期(S期)、DNA合成后期(G2期)和有丝分裂期(M期)。毒性损伤会导致细胞周期检查点的异常,使细胞周期停留在某一阶段[11]。研究表明YAP蛋白可以促进B-MYB和FOXM1表达,并且诱导B-MYB与MuvB复合物在S期结合形成MMB亚复合物。MMB亚复合物招募FOXM1,在S/G2过渡期形成MMB:FOXM1复合物。进入G2期后,B-MYB被降解,FOXM1磷酸化激活促进G2/M期基因表达,使细胞进入M期[12]。研究发现,利用siRNA敲低YAP表达将导致WB-F344细胞(大鼠肝上皮样干细胞)停滞在G0/G1期[13]。本课题组前期研究发现NaAsO2处理PC12细胞24 h后p-YAP表达和S期细胞比例均明显增加,细胞阻滞在S期[7]。而用XMU-MP-1阻断Hippo-YAP通路则逆转NaAsO2诱导的S期阻滞,表明Hippo-YAP通路参与NaAsO2对细胞周期的影响。
BCL-2可抑制细胞凋亡,而BAX则促进凋亡的发生,当BAX/BCL-2的比例增加时,可促进细胞凋亡[14]。P53是肿瘤抑制基因,其编码的P53蛋白可促进肿瘤细胞凋亡,抑制肿瘤发生[15]。Jin等[16]发现,YAP通过与TEAD相互作用并结合到BCL-2启动子区域来上调BCL-2转录。前期研究发现NaAsO2能增加PC12细胞凋亡及P53、BAX蛋白表达而下调BCL-2的表达,提示NaAsO2可能通过促进YAP磷酸化阻碍其入核,来抑制BCL-2表达,从而促进PC12细胞凋亡。利用XMU-MP-1阻断Hippo-YAP通路则逆转NaAsO2对细胞凋亡、P53、BCL-2和BAX表达的调控,表明Hippo-YAP通路参与NaAsO2对细胞凋亡的影响。
综上所述,本研究发现NaAsO2激活Hippo-YAP通路可改变YAP蛋白核质分布,而NaAsO2诱导细胞S期阻滞和促进细胞凋亡的内在机制可能涉及Hippo-YAP通路。然而,YAP如何进一步调控细胞周期,是否通过结合启动子来调控凋亡相关蛋白表达,仍需要进一步实验加以验证。
