维奈克拉联合阿扎胞苷加供者淋巴细胞输注治疗髓系肿瘤异基因造血干细胞移植后复发的临床疗效及安全性分析
2023-12-11施玲玲吴梅青刘练金刘倍材赖永榕赵卫华刘振芳陈英华章忠明
施玲玲, 吴梅青, 刘练金, 刘倍材, 赖永榕, 赵卫华, 刘振芳, 陈英华, 章忠明
异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)是治愈急性髓系白血病(acute myeloid leukemia,AML)及高危骨髓增生异常综合征(myelodysplastic syndrome,MDS)的重要方法。然而,30%~40%的患者在allo-HSCT后出现复发。一旦复发,患者的2年总生存率只有20%~30%[1],移植后6个月内复发的患者3年总生存率<10%[2]。移植后复发的处理十分棘手,传统治疗通常给予细胞毒药物化疗加供者淋巴细胞输注(donor lymphocyte infusion,DLI),但效果通常不尽如人意。只有不到15%的患者能够获得重新缓解[3]。维奈克拉(venetoclax,VEN)是一种抗凋亡蛋白B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)的选择性抑制剂。Bcl-2是抗凋亡蛋白亚家族中的一员,可抑制细胞凋亡。AML细胞中Bcl-2过表达,介导肿瘤存活,VEN直接与Bcl-2结合启动凋亡级联反应,导致白血病细胞凋亡[4]。阿扎胞苷(azacitidine,AZA)是一种DNA甲基转移酶抑制剂,是目前证实可以延长AML患者总生存时间的去甲基化药物。AZA治疗老年AML可显著减少输血依赖,改善生活质量,非血液学不良反应发生率低[5]。研究结果表明,AZA可以降低抗凋亡蛋白髓样细胞白血病-1(myeloid cell leukemia-1,MCL-1)的水平,联合VEN起到协同抗白血病的作用[4]。DLI是一种过继性细胞免疫疗法,将正常供者来源的外周血淋巴细胞输注到患者体内以诱导移植物抗白血病(graft-versus-leukemia,GVL)效应,达到清除患者体内白血病细胞治疗复发的目的。DLI治疗移植后复发取得了肯定的疗效,但存在导致输注相关移植物抗宿主病(graft-versus-host disease,GVHD)、骨髓造血功能障碍等问题[6]。粒细胞集落刺激因子(granulocyte colony-stimulating factor,G-CSF)动员的外周血干细胞采集物输注在保留淋巴细胞免疫活性的同时降低了治疗相关死亡率,大大改善了DLI的临床疗效。北京大学血液病研究所输注G-CSF动员后的外周血造血干细胞单个核细胞数(mononuclear cell,MNC)为1×108/kg,治疗性DLI后短期应用免疫抑制剂可预防重度GVHD发生[7]。本研究回顾性分析VEN与AZA联合DLI治疗8例allo-HSCT后复发的髓系肿瘤患者的临床资料,并探索其临床疗效及安全性。现报道如下。
1 资料与方法
1.1临床资料 回顾性分析2018年9月至2022年6月在广西医科大学第一附属医院接受allo-HSCT后复发,并接受VEN+AZA+DLI挽救性治疗的8例AML和MDS患者的临床资料。所有患者为血液学复发,骨髓细胞学涂片原始细胞均超过5%[中位数24.25%(5.5%~42.5%)],根据2018版《中国白血病异基因造血干细胞移植后复发的监测、治疗和预防共识》[7],allo-HSCT后血液学复发需要尽早干预治疗。本研究获广西医科大学第一附属医院伦理委员会批准[(医伦)快审2017第(011)号]。
1.2VEN+AZA+DLI治疗方法 维奈克拉片(100 mg/片,28片/盒,生产企业AbbVie Ireland NLB.V,批号:1139747)100 mg/d1、200 mg/d2、400 mg/d3~28,口服;AZA(100 mg/支,生产企业:Baxter Oncology GmbH,批号:HJ20170238)75 mg/m2,使用中位剂量为123.5(100~147)mg,d1~7,皮下注射。每28 d为1个治疗周期。视白细胞情况调整维奈克拉片剂量,每个疗程VEN至少用14 d。7例患者在第1疗程VEN+AZA治疗结束后接受DLI,1例患者因病情进展未能进行DLI。DLI后常规给予环孢素[3~5 mg/(kg·d)]预防DLI相关GVHD。本研究中DLI均为G-CSF动员后的供者外周血淋巴细胞,回输MNC为1×108/kg。
1.3观察指标 (1)治疗过程中通过每月评估骨髓细胞学、流式细胞学微小残留病变(mininal residual disease,MRD)等来评估治疗效果。根据指南定义,完全缓解(complete remission,CR):临床无白血病浸润所致的症状和体征;血象:血红蛋白男性≥100 g/L,女性≥90 g/L,中性粒细胞≥1.5×109/L,血小板≥100×109/L;骨髓象:原粒细胞或原始单核细胞+幼稚单核细胞≤5%。血细胞计数未完全恢复的完全缓解(complete remission with incomplete count recovery,CRi):满足CR的标准和不依赖输血,但是伴有持续的中性粒细胞减少(≤1.0×109/L),或持续的血小板减少(≤100×109/L)。部分缓解(partial remission,PR):化疗后骨髓原始细胞比例至少减少50%,且下降到5%~25%,外周血细胞计数正常。未缓解(non-remission,NR):临床、血常规及骨髓象3项均未达到CR的标准,骨髓白血病细胞>20%,包括治疗无效者。复发(relapse):获CR后,外周血中又出现白血病细胞,骨髓原始细胞≥5%;髓外出现白血病细胞浸润;已经达到遗传学或分子学缓解的患者又出现AML相关的染色体异常或基因异常[8]。总体反应率(overall response rate,ORR)定义为患者在治疗后达到CR、CRi的比例。(2)血细胞减少分级参照文献[9-10]。
1.4随访方法 通过电话或查阅门诊、住院病历的方式进行随访。总生存时间的计算从患者接受VEN+AZA治疗开始至随访截止或患者死亡的时间。随访截止时间为2023年10月10日。
1.5统计学方法 应用SPSS22.0统计软件进行数据处理。计量资料采用中位数(最小值~最大值)来描述。计数资料采用频数及百分率来描述。采用Kaplan-Meier(K-M)法绘制生存曲线图。
2 结果
2.18例患者的临床特征 8例患者中男女各4例,中位年龄为31(15~64)岁,AML 5例,MDS 3例。AML患者中,移植前CR 3例,PR 1例,NR 1例。MDS患者3例均为MDS伴原始细胞增多1型,诊断后桥接移植,移植前均为NR。8例患者均接受allo-HSCT,同胞全相合供者3例,非亲缘全相合供者1例,亲缘单倍体供者4例。移植后1个月评价均为CR,嵌合率为99.51%(95.00%~100.00%)。见表1。

表1 8例患者的临床特征
2.2allo-HSCT后复发治疗及疗效评价 allo-HSCT后复发的中位时间为316(77~1 099)d,均为血液学复发。复发时骨髓原始细胞比例中位数为24.25%(5.50%~42.50%)。复发后接受VEN+AZA挽救性治疗的中位时间为10(4~25)d,中位疗程为3.5(1~6)个,1例AML患者联合吉瑞替尼治疗,1例AML患者因白血病未能控制,在第2、3疗程联合达雷妥尤单抗治疗。VEN+AZA用药后10(4~25)d给予DLI,本研究中7例患者接受1次DLI,1例MDS患者在首次DLI后3个月序贯第2次DLI。本研究中DLI均为G-CSF动员后的供者外周血淋巴细胞,回输MNC均为1×108/kg。DLI后常规使用环孢素预防GVHD,1个月后逐渐停用。1例患者因病情进展,未进行DLI。5例患者接受第1次VEN+AZA+DLI治疗后达到CR/CRi,1例患者在第2疗程联合达雷妥尤单抗治疗后获得CR,ORR为75.00%。2例患者接受首次治疗后仍为NR。1例患者在治疗5周期后再次血液学复发。在获得ORR的患者中,CR/CRi持续时间为481(216~746)d。见表2。

表2 8例患者复发后治疗及转归
2.3并发症发生情况 8例患者均出现血细胞减少。3~4级中性粒细胞减少5例,3~4级血小板减少3例,3级贫血3例。视情况调整VEN剂量100~400 mg/d,每个疗程至少使用14 d。DLI后2例患者出现皮肤Ⅱ度GVHD,抗GVHD治疗后好转。2例患者出现闭塞性细支气管炎(bronchiolitis obliterans,BO)合并肺真菌病,其中1例存活,1例合并带状疱疹,最终因呼吸衰竭死亡。1例患者出现肺结核感染,最终因白血病复发死亡。1例患者出现突发性耳聋,不能排除为疾病本身进展导致,因疾病进展死亡。1例患者在治疗5个疗程后再次血液学复发,最终死亡。见表2。
2.4随访及生存状态 本研究中位随访时间为429(40~746)d。截至随访结束,8例患者中4例存活(均为首次治疗后即获得并持续CR/CRi的患者),4例死亡,其中3例因疾病进展死亡[2例为AML,1例为治疗相关性骨髓增生异常综合征(therapy-related myelodysplastic syndrome,t-MDS)],1例AML患者因肺部感染导致呼吸衰竭死亡。见表2。中位生存时间为429(40~746)d,预计2年总生存率为41.67%。见图1。
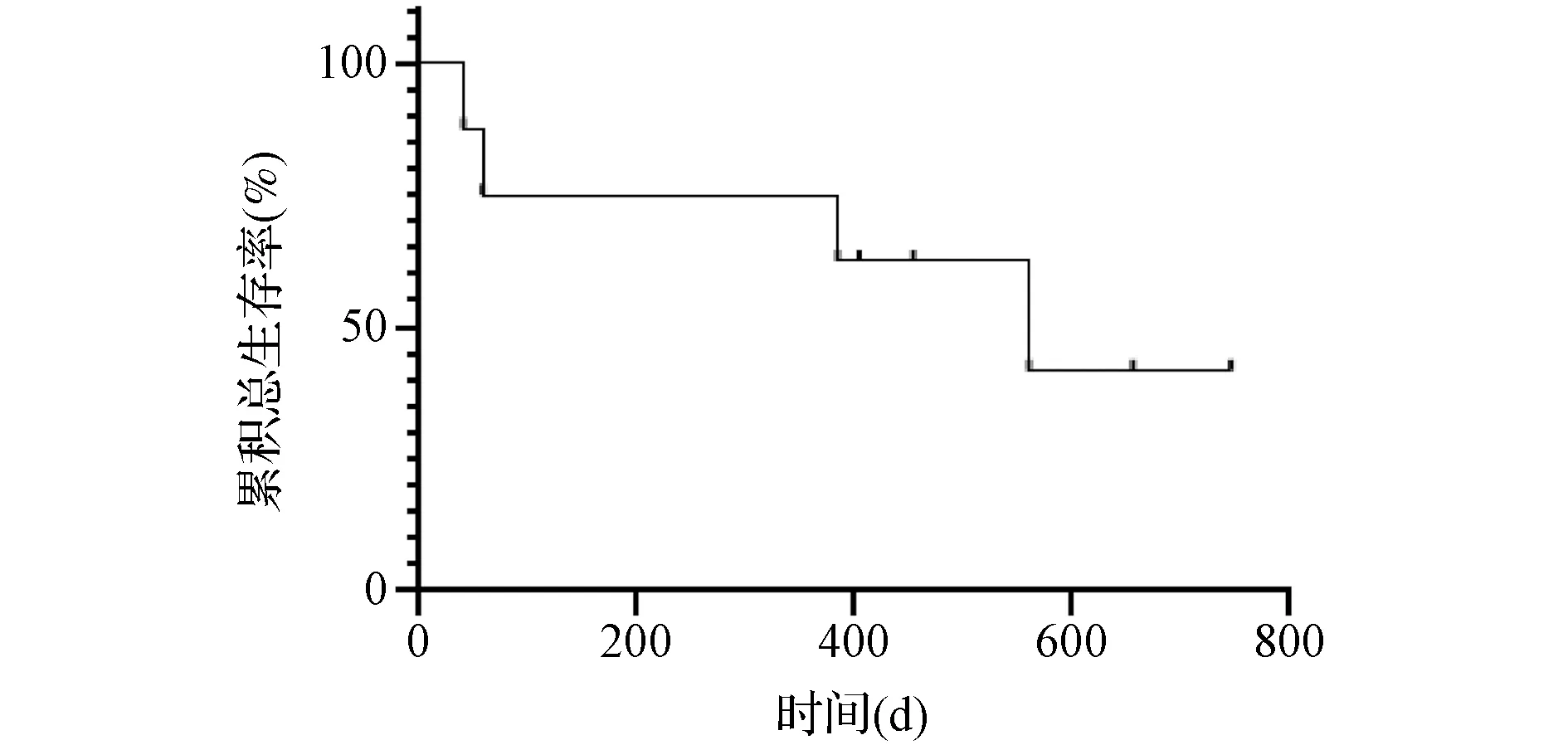
图1 8例患者接受VEN+AZA+DLI治疗后生存曲线图
3 讨论
3.1髓系肿瘤移植后复发是导致移植失败的主要原因之一,约50%AML患者面临着移植后复发的风险。移植后复发与疾病危险度分层、预处理方案等密切相关。髓系肿瘤移植后一旦复发,2年总生存率低于20%[11]。如何处理髓系肿瘤移植后复发是亟待解决的重要问题。本研究回顾性分析了8例AML/MDS患者,allo-HSCT后复发并接受VEN联合AZA挽救性治疗,绝大部分患者接受DLI。尽管病例数少,仍能得到一些启示:首先,移植后复发的8例患者使用VEN联合AZA加DLI,有6例患者获得ORR,ORR持续时间为481(216~746)d。首次治疗CR/CRi率可达到62.50%(5/8),其中4例患者能够获得持续CR/CRi,预计2年总生存率为41.67%。其次,绝大部分患者能耐受VEN联合AZA加DLI,中位疗程为3.5(1~6)个,治疗后仅1例因并发症死亡,其余3例均因疾病进展死亡。
3.2近年来,随着恶性血液肿瘤的免疫和分子靶向药物研究的进展,对于移植后复发的治疗方案也层出不穷。主要分为以药物治疗为基础的VEN、去甲基化药物(demethylation drugs,HMAs)和异柠檬酸脱氢酶(lsocitrate dehydrogenase,IDH)抑制剂;以细胞治疗为基础的DLI、二次移植;还有针对髓系肿瘤的嵌合抗原受体T细胞免疫疗法(chimeric antigen receptor T-cell immunotherapy,Car-T)临床研究[11]。2020年VEN被我国批准与AZA联合应用治疗75岁以上或不能耐受强化疗的初诊AML。VEN与HMAs联合使用,在老年AML患者中,无论是作为一线治疗还是复发治疗,都具有良好的耐受性和反应[12-13]。在复发难治AML的治疗探索中,VEN+AZA+西达本胺方案、VEN+高三尖杉酯碱+HMAs方案具有较高的反应率,CR/CRi分别达56.3%和63.8%[14]。近年来,VEN联合HMAs用于allo-HSCT后复发的挽救治疗也有报道,疗效不低于传统化疗,并且不良反应较少[15]。
3.3由于VEN在治疗老年AML患者及不能耐受强化疗患者中表现出良好的疗效及耐受性[16],许多学者尝试在移植后复发的患者中使用VEN为基础的方案进行挽救性治疗。Zucenka等[17]在移植后髓系肿瘤复发的患者中,分别使用VEN和小剂量阿糖胞苷为基础的挽救治疗和FLAG方案(氟达拉滨+大剂量阿糖胞苷+G-CSF)联合IDA强化疗,ORR分别为75%和66%(P=0.542)。尽管ORR差异无统计学意义,但VEN组治疗相关死亡率为0%,而强化疗组高达34%。因此,以VEN为基础的挽救性治疗具有与强化疗相同的抗白血病效应,并且毒性更小。
3.4AZA可以通过增加人白细胞抗原DR-1和其他肿瘤相关抗原的表达来增强移植后GVL效应,从而更好地控制白血病。除了通过DNA去甲基化抗白血病活性外,AZA还具有免疫调节活性,通过增强调节性T细胞和细胞毒性T细胞的活性调节GVHD,同时维持GVL效应[18]。Chen等[15]回顾性比较了VEN+HMAs[AZA/地西他滨(decitabine,DAC)]或强化疗分别联合DLI,治疗移植后髓系肿瘤复发的患者。VEN+HMAs组和强化疗组之间的总体缓解率无显著差异(60.1% vs 64.3%,P=0.785),肺部感染(17.4% vs 50.0%,P=0.010)、血小板减少(73.9% vs 95.2%,P=0.035)、aGVHD(13.0% vs 50.0%,P=0.003)发生率在强化疗组发生率更高。Zhao等[19]使用VEN+AZA+DLI治疗allo-HSCT后AML复发,总体有效率达到61.5%,无事件生存(event-free survival,EFS)和总生存时间分别为120 d和284.5 d。本研究结果与文献报道一致。
3.5本研究中,1例患者接受VEN+AZA+DLI 1个疗程后未能缓解,第2疗程加达雷妥尤单抗后达到CR。有1例患者接受VEN+AZA+DLI联合吉瑞替尼治疗。2例患者均获得持续CR,但使用达雷妥尤单抗患者因出现BO及肺部真菌感染,最后因呼吸衰竭死亡。Yang等[20]报道达雷妥尤单抗和VEN方案治疗allo-HSCT后复发的恶性血液肿瘤患者,中位年龄为26(5~49)岁。经过1个周期诱导治疗后,5例患者获得CR,1例患者获得PR,6例患者NR。达到CR的中位时间为26(18~42)d。CR患者的中位无病生存期为10个月。中位随访时间为144(46~244)d,12例患者中有8例存活。提示达雷妥尤单抗可能为allo-HSCT后恶性血液肿瘤复发、肿瘤细胞表达CD38的患者提供新的治疗选择。
3.6欧洲骨髓移植协会和白血病工作组(European Bone Marrow Transplantation Association and Leukemia Working Group,EBMT-ALWP)早期进行的一项研究提出,年轻和allo-HSCT后5个月以上的晚期复发是DLI后总生存获益的独立影响因素。此外,较低的肿瘤负担(骨髓中<35%的原始细胞)、疾病缓解和有利的细胞遗传学也与总生存相关[21]。另一项研究提出对复发后一线治疗有反应的患者能从DLI获益[22]。本研究中4例患者获得持续CR/CRi,其中3例为晚期复发,均为首次VEN+AZA+DLI即获得CR,与文献报道一致。因此,在DLI之前使用VEN、HMAs和(或)其他治疗方法减轻肿瘤负荷是非常重要的。DLI最常见的并发症是GVHD,可能危及生命。DLI的剂量与GVHD的风险相关,输注>1×108/kg的T细胞的风险高达50%,而<1×107/kg的风险低至10%[23]。本研究中DLI的MNC控制在1×108/kg,并给予环孢素预防GVHD,有1例患者出现皮肤GVHD,2例患者出现BO,其中1例因BO合并感染导致呼吸衰竭死亡。如何更好地控制DLI后GVHD风险,仍需要进一步研究。
综上所述,VEN+AZA+DLI作为髓系肿瘤allo-HSCT后复发的挽救性治疗具有较好的疗效,且患者耐受性良好,为髓系肿瘤allo-HSCT后复发的治疗开拓了新的治疗思路,值得在临床工作中进一步探索。但此治疗方案也存在不足之处,VEN极易导致血细胞尤其是中性粒细胞减少,增加了机会性感染及治疗中断的风险,有可能导致患者无法接受连续有效的药物治疗。另外,DLI后出现GVHD必须引起高度重视。如何预防严重GVHD的发生,仍然需要深入研究。总之,髓系肿瘤allo-HSCT后复发的处理具有进一步探索和研究的价值。
