自体造血干细胞移植治疗急性髓系白血病的疗效及安全性单中心回顾性研究
2023-12-11姜文娜刘焕平陈璐璐
张 敏, 刘 玲, 姜文娜, 刘焕平, 陈璐璐, 张 颢
据世界卫生组织报道,急性髓系白血病(acute myeloid leukemia,AML)的发病率为2.5/105~3/105[1-2]。一项来自瑞典的大型研究表明,AML的发病率随着年龄的增长而增加[3]。以阿糖胞苷(cytosine arabinoside,Ara-C)和蒽环类药物组成的“3+7”方案是AML适合强化疗患者的标准疗法,能使50%~60%患者在治疗后完全缓解(complete remission,CR)[4]。地西他滨联合维奈克拉方案对不适合接受强化疗的老年初治AML患者也可使73%患者治疗后CR[5]。但未接受额外巩固治疗的AML患者生存期仅4~8个月,因此缓解后的巩固治疗非常重要[6]。传统化疗、自体造血干细胞移植及异基因造血干细胞移植是AML最常用的巩固治疗方案[7-8]。自体造血干细胞移植与传统化疗相比,能降低复发率,改善患者的总生存期,是有前景的巩固治疗方案[9-10]。异基因造血干细胞移植能降低患者的复发率,但其非复发相关的死亡率高于自体造血干细胞移植,二者在总生存期上无显著差异[11-12]。自体造血干细胞移植毒性低,成为低中危AML、不适合异基因造血干细胞移植及缺乏人类白细胞抗原(human leukocyte antigen,HLA)相合供者巩固治疗的首要选择。本研究回顾性分析济宁医学院附属医院血液内科采用自体造血干细胞移植治疗18例AML患者的临床资料,探讨自体造血干细胞移植治疗AML的临床疗效和安全性。现报道如下。
1 资料与方法
1.1一般资料 回顾性分析2017年3月至2022年10月于济宁医学院附属医院血液内科行自体造血干细胞移植治疗的18例AML患者的临床资料,其中男6例,女12例,中位年龄50.5岁(16~68岁)。按照法、英、美分型系统(French-American-British classification systems,FAB)分型,M2型3例,M4型9例,M5型6例。根据2023年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南[13],低危6例,其中2例染色体t(8;21),3例染色体核型正常伴有单个核仁磷酸蛋白基因(NPM1)突变,1例染色体核型正常伴有单纯双等位基因CEBPA双突变;中危8例,其中5例染色体核型正常,1例染色体t(9;11),1例染色体核型+8,1例染色体del(16)伴TET2突变;高危4例,其中1例正常细胞遗传学伴FLT3-ITD突变,1例染色体48,XY,+4,+6,/idem,+10,+13,1例染色体-X,t(8;21,19)伴JAK2突变,1例TP53突变。11例患者为移植前第1次完全缓解(the first complete remission,CR1),7例患者为移植前第2次完全缓解(the second complete remission,CR2)。所有患者的美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力状态评分≤2分。流式细胞术检测白血病微小残留病灶(minimal residual disease,MRD),移植前MRD转阴13例,未转阴5例。18例AML的临床资料见表1。本研究获济宁医学院附属医院伦理委员会批准(批号:2021B040)。
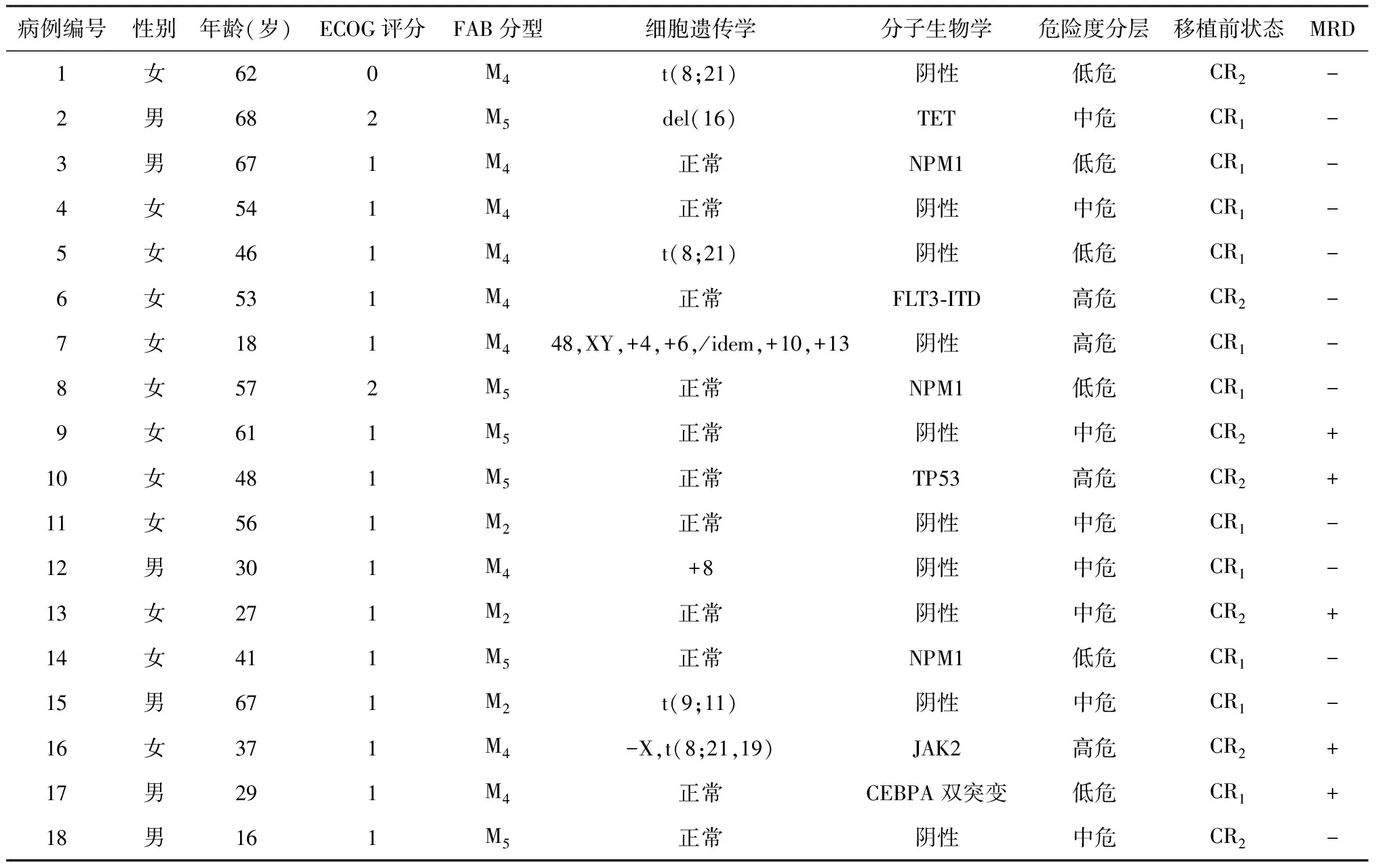
表1 18例AML患者自体造血干细胞移植治疗的临床资料
1.2自体造血干细胞移植前治疗 15例患者诱导缓解采用标准“3+7”方案:结合患者自身耐受性及既往临床经验,给予减量的柔红霉素,柔红霉素45 mg/(m2·d),第1~3天或去甲氧柔红霉素10 mg/(m2·d),第1~3天,Ara-C 100~200 mg/(m2·d),第1~7天。2例患者采用HAG方案,具体为高三尖杉酯碱(homoharringtonine,HHT)2.5 mg/(m2·d),第1~7天,Ara-C 100~200 mg/(m2·d),第1~7天,粒细胞集落刺激因子(granulocyte colony-stimulating factor,G-CSF)5 μg/kg,第0~5天或直至中性粒细胞计数>1×109/L。1例采用CAG方案,Ara-C 10 mg/(m2·d),第1~14天,阿克拉霉素20 mg,第1~4天,G-CSF 5 μg/kg,第0~5天或直至中性粒细胞计数>1×109/L。依据患者耐受性,18例患者缓解后采用Ara-C 2~3 g/m2巩固化疗2个疗程。化疗期间给予腰椎穿刺及鞘内注药(Ara-C、甲氨蝶呤及地塞米松)预防中枢神经系统白血病。
1.3自体造血干细胞移植动员及采集 18例患者动员方案为化疗药物+G-CSF,化疗药物:依托泊苷1.5 g/m2,第1~3天;大剂量阿糖胞苷(high-dose cytosine arabinoside,HD-Ara-C)3 g/m2,第1~2天。动员期间每日监测患者血常规,当白细胞计数开始回升时,给予G-CSF[10 μg/(kg·d)]动员。病例15及病例18因第1次采集CD34+数量不足,第2次采用普乐沙福方案动员,G-CSF 10 μg/(kg·d),第1~4天,普乐沙福0.24 mg/(kg·d),第4~5天。采集造血干细胞的时机为外周血中淋巴细胞计数+单核细胞计数≥2.5×109/L。用Com.TEC(德国费森尤斯公司)及COBS-Spectra(美国Terumobct公司)分离机分离外周血造血干细胞。
1.4移植前预处理方案及移植后维持治疗 6例患者采用BuCy预处理方案:白消安[3.2 mg/(kg·d)]-8~-6 d,环磷酰胺[40 mg/(kg·d)]-3~-2 d,Ara-C[2 g/(m2·d)]-5~-4 d,地西他滨(50 mg/d)-5~-4 d,司莫司汀[250 mg/(m2·d)]-5~-4 d。5例采用BuMel+西达苯胺预处理方案:白消安[3.2 mg/(kg·d)]-5 d,氟达拉滨[30 mg/(m2·d)]-5 d,Ara-C[2 g/(m2·d)]-5~-2 d,西达苯胺(10 mg/d)-6~-2 d,美法仑(140 mg/m2)-2 d。3例采用BuMel预处理方案:白消安[3.2 mg/(kg·d)]-3~-2 d,氟达拉滨[50 mg/(m2·d)]-3~-2 d,Ara-C[2 g/(m2·d)]-3~-2 d,马法兰(Mel)[140 mg/(m2·d)]-2 d。5例老年患者中,4例老年患者耐受性差,采用Bu预处理方案:白消安[3.2 mg/(kg·d)]-8~-6 d,氟达拉滨[30 mg/(m2·d)]-5 d,Ara-C[2 g/(m2·d)]-5~-4 d,司莫司汀[250 mg/(m2·d)]-5~-4 d,地西他滨(50 mg/d)-5~-4 d。1例耐受性好的老年患者给予BuCy预处理方案,其余4例老年患者给予去除环磷酰胺。18例患者移植后采用阿扎胞苷32 mg/(m2·d),第1~5天维持,1次/月,维持2年。
1.5疗效评价 疗效评价采用NCCN指南标准[11],分为CR、部分缓解(partial remission,PR)、稳定和进展。安全性评价根据美国国家癌症研究所(National Cancer Institute,NCI)常见毒性标准(Common Toxicity Criteria,CTC)分级(V5.0)[14],主要包括新陈代谢及营养不良(厌食、脱水、胆红素、高胆固醇血症、高血糖症等),消化道反应(口腔黏膜炎、恶心、呕吐、腹泻、消化道出血等),肾脏、泌尿系统损伤,呼吸道异常,心脏/心血管反应等。
1.6随访 移植后1、2、3、6、9、12、18、24个月进行随访监测,以后每年随访监测1次至移植后3年。随访内容包括血常规、骨髓涂片、流式细胞学及融合基因定量。数据统计包括总生存期(从造血干细胞输注日期到死亡或末次随访日期)、无白血病生存期(从造血干细胞输注日期至复发、死亡或末次随访日期)、复发时间[从造血干细胞输注到微小残留病灶阳性和(或)出现髓外白血病的时间]以及移植相关死亡。
1.7统计学方法 应用SPSS22.0统计软件进行数据分析。计量资料用中位数表示,计数资料以例数(百分率)[n(%)]表示。Kaplan-Meier法绘制自体造血干细胞移植患者的生存曲线,计算术后1年和3年患者的总生存率(overall survival rate,OS)及无白血病生存率(leukemia-free survival rate,LFS)。
2 结果
2.118例AML患者自体造血干细胞移植治疗及预后情况 18例患者输注CD34+计数中位数为4.05×106/kg(1.87×106~27.40×106/kg),单个核细胞计数中位数为14.48×108/kg(4.07×108~24.74×108/kg)。所有患者获得造血重建,中性粒细胞植入的中位时间为10(9~13)d,血小板植入的中位时间为15(10~19)d。见表2。
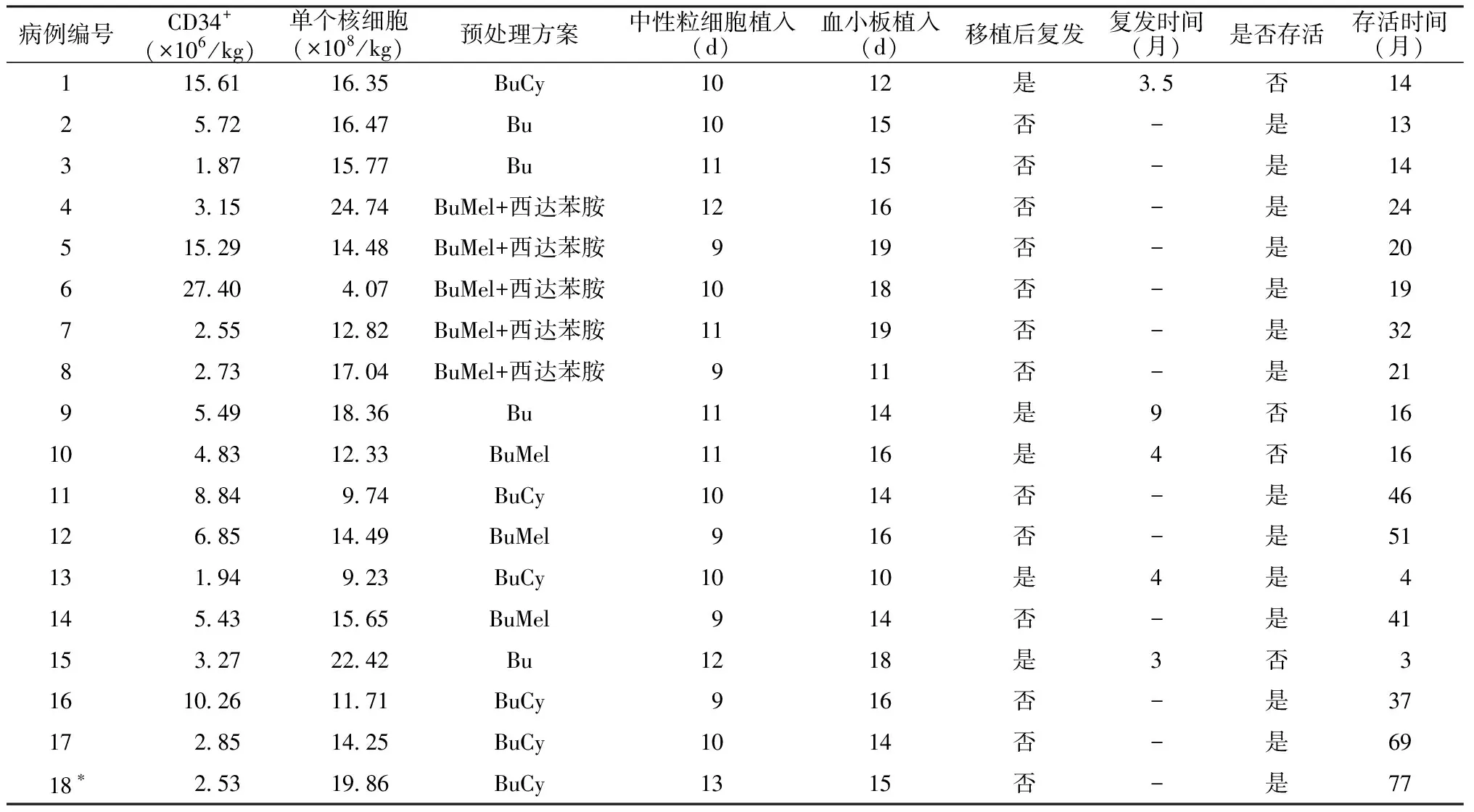
表2 18例AML患者自体造血干细胞移植治疗及预后情况
2.2移植后生存分析 18例患者中无移植相关的死亡,至随访结束,5例患者在移植后3~9个月出现AML复发。2例(33.33%,2/6)BuCy预处理方案患者疾病复发,1例(12.50%,1/8)含BuMel预处理方案患者疾病复发。3年的LFS为72.00%(见图1ⓐ)。18例患者中,4例死亡且均为复发相关死亡,患者移植后1年的OS为94.00%,3年的OS为73.00%(见图1ⓑ)。

图1 18例AML患者自体造血干细胞移植治疗后生存曲线图
2.3预处理的毒性和移植相关并发症 预处理期间18例患者出现不同程度的恶心、呕吐,给予止吐、保护胃黏膜等对症治疗后症状均治愈。11例患者发热,血培养均未培养出致病菌,经验性抗感染治疗后体温均恢复正常。11例发热患者中,1例合并新型冠状病毒感染,给予来瑞特韦片抗病毒治疗后复查病毒转阴。6例以BuCy为预处理方案的患者中,出现Ⅰ~Ⅱ度腹泻5例,Ⅰ~Ⅱ度口腔溃疡4例,心慌、胸闷不适3例,2度的转氨酶升高2例,1度低钾血症1例,给予对症治疗后均好转。1例患者移植后出现植入综合征,给予糖皮质激素对症处理,症状好转。8例以含BuMel为基础的预处理方案患者中,出现Ⅰ~Ⅱ度口腔溃疡3例,1度低钾血症1例。18例患者无移植相关死亡。
3 讨论
3.1AML完全缓解后的巩固治疗目前仍存在争议,其治疗方案的选择取决于风险分层、年龄、是否有HLA匹配的供者[15-17]。多项随机研究已经表明自体造血干细胞移植作为AML缓解的巩固治疗方案,其LFS明显优于化疗[8,18]。欧洲学者回顾性分析809例自体造血干细胞移植治疗AML患者病例资料,结果表明2年的LFS及OS分别为51%及65%,非复发死亡率(non-relapse mortality,NRM)仅为3.7%[19]。一项纳入1 122例的随机对照研究中,547例接受自体造血干细胞移植,575例接受单倍体相合造血干细胞移植,结果表明单倍体相合造血干细胞移植有更低的复发率,但NRM更高,二者LFS(65.9% vs 63.8%)及OS(73.2% vs 80.6%)基本相当[9]。任瑞瑞等[20]比较自体造血干细胞移植与同胞全相合异基因造血干细胞移植治疗CR1期AML的疗效,结果表明二者3年的LFS(75% vs 69.5%)及OS(70.6% vs 82.4%)差异无统计学意义。为探索自体造血干细胞移植的疗效,本研究回顾性分析了18例自体造血干细胞移植治疗AML患者的临床资料,结果显示患者3年的LFS为72.00%。患者移植后1年的OS为94.00%,3年的OS为73.00%。表明自体造血干细胞移植是一种有效的AML缓解后巩固治疗方案。
3.2BuCy是自体造血干细胞移植治疗AML的标准预处理方案。近年来,研究者尝试用抗白血病效应更强、血液学毒性更低的Mel替代Cy,组成新的BuMel预处理方案。BuMel预处理方案在一项129例CR1期AML患者的自体造血干细胞移植研究中首次被报道,这些患者8年的OS及LFS分别为62%和56%。最常见的血液系统外疾病为黏膜炎,未见肝、肾、肺等器官损害报道[21],与本研究结果相似,Nagler等[22]回顾性比较BuCy、BuMel、Bu及依托泊苷、Bu及去甲氧柔红霉素预处理方案对自体造血干细胞移植治疗AML临床结果的影响,结果表明,与其他预处理方案相比,BuMel方案有更好的OS。一项来自日本的研究数据表明,BuMel方案比以BuCy及TBI为基础的方案有更好的抗白血病效果,有更高的LFS、OS及更低的NRM[23]。在本研究中,6例以BuCy预处理方案的患者中2例(33.33%)患者复发,8例以BuMel为基础的预处理患者中仅1例(12.50%)患者复发。在预处理的不良反应方面,采用BuCy预处理方案的患者较采用BuMel预处理方案的患者表现出更多的不良反应,包括腹泻、心慌、胸闷不适、转氨酶升高、植入综合征。以上结果表明,与BuCy预处理方案相比,BuMel预处理方案有更低的复发率及更好的耐受性。
综上所述,自体造血干细胞移植是AML患者缓解后安全、有效的巩固治疗选择。BuMel预处理方案有更轻的不良反应及更低的复发率,可作为AML患者自体造血干细胞移植预处理的首要选择。本研究因样本量限制,未进行影响预后的因素分析,下一步可进一步通过多中心研究扩大样本量,深度探索自体造血干细胞移植在AML治疗的效果与安全性。
