杀菌剂终点体积分数的测定
2023-12-10高欣
高 欣
(湖北轻工职业技术学院 中德啤酒学院,湖北 武汉 430070)
啤酒厂杀菌剂终点体积分数,是指在保证杀灭卫生学指示菌的基础上,规定杀菌时间内杀灭啤酒有害菌所需的最低杀菌剂与水的体积之比[1]。生产中使用杀菌剂一般都采用供应商提供的指导体积分数,该体积分数往往是以医学上有重要意义的微生物如埃希氏大肠杆菌Escherichiacoli8099(简称E.coli8099)作为研究对象而得出的结论[2],使用该指导体积分数是否能有效杀灭啤酒有害菌,还须各啤酒生产企业单独确认。在啤酒厂中如果发生污染事故,按照污染概率,大约60%由嗜温性乳酸杆菌Lactobacilluslindneri(简称L.lindneri)引起,30%由四联球菌Pediococcusdamnosus引起,而常见的嗜温性乳酸杆菌属中林德奈氏乳酸杆菌L.lindneri危害最大,生存能力强于其他的啤酒有害菌[3-5]。啤酒生产企业需以L.lindneri和E.coli8099作为待实验菌,至少每年做1次杀菌剂终点实验,以验证本公司杀菌剂最低的使用体积分数[6]。
目前,国内外对杀菌剂终点体积分数实验的测定一般常用星实验、菌悬液实验两种方法。星实验又称为琼脂扩散实验,在互不渗透的5个星角尖分别注入0.1 mL不同体积分数的杀菌剂溶液,如果杀菌剂体积分数适当,那么实验时对应星角尖区域就没有实验菌生长。星实验对氧化型杀菌剂和有特定pH要求的杀菌剂无效,该实验结果亦不能准确地反映出杀菌剂是抑菌作用还是杀菌作用;而菌悬液实验则采用定量杀灭法,如所使用的某杀菌剂体积分数为0.2%~0.5%,杀菌时间为20 min,则菌悬液实验选择杀菌剂体积分数为0.2%,设定实验时间分别为10,20,30 min,杀菌温度为生产车间温度,以验证该杀菌剂最低使用体积分数的有效性。本次实验采用菌悬液结合杀菌剂体积分数梯度法,杀菌剂以0.05%递减,在有机干扰物存在的情况下将目标菌液L.lindneri和E.coli8099接种到不同体积分数的杀菌剂中,通过目标菌液的菌落生长情况判断杀菌剂终点体积分数[7-9]。与星实验及菌悬液定量杀灭法相比,该实验方法能准确测定杀灭啤酒有害菌所需的最低体积分数,在生产现场更具有实践指导意义。
1 材料与方法
1.1 材料与试剂
悬菌液1:L.lindneri林德奈氏乳酸杆菌(TUM实验室纯菌种,第3代,NBB-B培养基新鲜培养物),用无菌吸管吸取10 mL,接入90 mL无菌生理盐水中制成悬菌液1;悬菌液2:埃希氏大肠杆菌E.coli8099(TUM实验室纯菌种,第4代,肉汤蛋白胨培养基24 h新鲜培养物[10]),用无菌吸管吸取10 mL,接入90 mL无菌生理盐水中制成悬菌液2;杀菌剂过氧乙酸:艺康牌通用型过氧乙酸消毒液(UN3109),批号2021060438,有效成分过氧乙酸质量分数为15%,上海艺康;中和剂无菌0.5%的Na2S2O3溶液;有机干扰物自产无菌除气啤酒;无菌酿造用水;蒸馏水;0.85%无菌生理盐水;NBB-A培养基(德国DöHLER公司NBB-P,自配);营养琼脂:青岛海博生物。
1.2 仪器与设备
HS-840-U超净工作台,苏州安泰净化医疗器材厂;LDZX-75KBS灭菌锅,上海申安净化医疗器材厂;无菌膜过滤器及0.2 μm无菌过滤膜:北京德之杰啤酒技术有限责任公司;厌氧培养罐:北京德之杰啤酒技术有限责任公司;无菌刻度吸管、涂布棒、接种环、酒精灯、底皿直径90 mm的无菌培养皿、无菌三角瓶、0.1~1 mL及1~10 mL无菌移液枪,苏州安泰;XT5204-BS40恒温水浴锅,杭州雪中碳技术有限公司。
1.3 实验方法
1.3.1 检测依据
中华人民共和国卫生部《消毒技术规范》(2002版)中2.1.1.5.5节中的中和剂鉴定实验及2.1.1.7.4节中的细菌定量杀灭实验[2]。
1.3.2 过氧乙酸杀菌剂的配制
本批次艺康牌过氧乙酸杀菌剂按商品说明书其过氧乙酸质量分数为15%,实验中所述杀菌剂体积分数均以过氧乙酸质量分数为15%的杀菌剂原液作为溶质配制[11],比如0.35%的体积分数配制时为每10 L无菌酿造用水中添加杀菌剂原液0.035 L(折算后过氧乙酸质量浓度为525 mg/L),0.2%的体积分数配制时为每10 L无菌酿造用水中添加杀菌剂原液0.02 L(折算后过氧乙酸质量浓度为300 mg/L[12]),依此类推。
1.3.3 目标菌液的配制
分别配制L.lindneri和E.coli8099的目标菌液:取L.lindneri和E.coli8099悬菌液各100 mL,分别与体积分数为3%的无菌除气啤酒100 mL混合配制成目标菌液置(20±1) ℃水浴中待用,菌质量浓度以用肉眼刚刚能识别出轻微混浊为宜。
1.3.4 目标菌液定量杀菌实验
酿造用水将艺康牌过氧乙酸原液配制成体积分数分别为0.50%,0.45%,0.40%,0.35%,0.30%,0.25%,0.20%的梯度及空白对照(用0.85%无菌生理盐水),各取10 mL并按顺序编号分成A(A1,A2,A3,A4,A5,A6,A7,空白CA)、B(B1,B2,B3,B4,B5,B6,B7,空白CB)2组,置(20±1) ℃水浴中5 min备用。A组对应接种1 mL目标菌液L.lindneri,B组对应接种1 mL目标菌液E.coli8099,接种后混匀,作用时间为10 min,后吸取1 mL经杀菌处理后的各梯度样至9 mL 0.5%无菌Na2S2O3溶液试管中进行中和处理,得中和后各梯度样品,用无菌生理盐水10倍系列稀释后,选取适宜稀释度,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基进行活菌培养计数,活菌计数时,稀释度控制标准在平板菌落生长数为30~300[13]。其中目标菌液L.lindneri林德奈氏乳酸杆菌使用的培养基为NBB-A平板,温度为27 ℃,厌氧培养5 d[14];目标菌液埃希氏大肠杆菌E.coli8099使用的培养基为营养琼脂平板,温度为37 ℃,好氧培养1 d;实验重复3次。
1.3.5 目标菌液中和剂鉴定实验
根据实验分组,准备足量试管和平皿,依次进行编号。待1.3.4节目标菌液定量杀菌实验完成后,根据所测定的杀菌剂终点体积分数再进行目标菌悬液中和剂鉴定实验。目标菌悬液按1.3.3节制备备用。目标菌液L.lindneri及E.coli8099活菌计数使用的培养基及稀释度控制同1.3.4节,实验重复3次[15]。
1) 过氧乙酸加菌悬液作用后混合培养实验
观察过氧乙酸对目标菌液有无杀灭或抑制能力。吸取1 mL目标菌悬液于试管内,置(20±1) ℃水浴中5 min后,加入10 mL过氧乙酸于试管内混匀,作用10 min,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基活菌培养计数。
2) 过氧乙酸加菌悬液作用后中和剂培养实验
观察残留过氧乙酸被中和后受到过氧乙酸杀灭作用后的实验菌是否能恢复生长。吸取1 mL目标菌悬液于试管内,置(20±1) ℃水浴中5 min 后,加入10 mL过氧乙酸于试管内混匀,作用10 min,然后加入Na2S2O3体积分数为0.5%的溶液90 mL,混匀中和处理10 min,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基活菌培养计数。
3) 中和剂加菌悬液作用后培养实验
观察Na2S2O3体积分数为0.5%的溶液是否抑菌。吸取1 mL目标菌悬液于试管内,置(20±1) ℃水浴中5 min后,加入无菌Na2S2O3体积分数为0.5%的溶液10 mL,作用10 min,用无菌Na2S2O3体积分数为0.5%的溶液10倍系列稀释后,选取适宜稀释度,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基活菌培养计数。
4) 过氧乙酸加中和剂作用后菌悬液培养实验
观察中和产物或未被完全中和的残留过氧乙酸对目标菌液的生长繁殖是否有影响,中和产物溶液由过氧乙酸溶液10 mL加无菌Na2S2O3体积分数为0.5%的溶液90 mL均匀混合后作用10 min配制而成。吸取1 mL目标菌悬液于试管内,置(20±1) ℃水浴中5 min后,加入中和产物溶液10 mL于试管内,混匀,作用10 min,用中和产物溶液10倍系列稀释后,选取适宜稀释度,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基活菌培养计数。
5) 稀释液加菌悬液培养实验
吸取目标菌悬液1 mL于试管内,置(20±1) ℃水浴中5 min后,加入无菌生理盐水稀释液10 mL,作用10 min,用无菌生理盐水10倍系列稀释后,选取适宜稀释度,再分别吸取1 mL稀释样至2个无菌平皿中,加入固体培养基进行活菌培养计数。该实验可作为阳性菌落数对照。
6) 稀释液加中和剂加培养基培养实验
分别吸取无菌生理盐水稀释液、中和剂体积分数为0.5%的无菌Na2S2O3溶液和无菌酿造用水各1 mL于同一无菌平皿内,倒入上述实验同批次的培养基25 mL,培养观察。如出现细菌生长,则会提示实验材料或操作过程中就有污染,应重新进行上述实验。该实验可作为阴性对照。
7) 中和剂合格评价
实验结果符合以下全部条件,所测中和剂可判为合格。即第1,2组均无实验菌或仅有极少数实验菌菌落生长;中和剂鉴定实验第3,4,5组有相似量实验菌生长,菌悬液实验为1×107~5×107cfu/mL,且组间菌落数误差率要求不超过15%。组间菌落数误差率计算式为
式中:A为3组间菌落平均数;B为各组菌落平均数。
2 结果与分析
2.1 L.lindneri定量杀菌实验
吸取1 mL目标菌悬液L.lindneri于试管内,置(20±1) ℃水浴中5 min后,按1.3.4节所述方法,加入10 mL过氧乙酸于试管内混匀,作用10 min,后经0.5%无菌Na2S2O3溶液中和处理,用无菌生理盐水10倍系列稀释后,使用NBB-A平板培养基进行活菌培养计数,27 ℃厌氧培养5 d,对应中和剂、稀释液和培养基同时作阴性对照,实验结果如表1所示。

表1 L.lindneri不同杀菌剂体积分数终点实验结果
由表1可知:在3%除气啤酒干扰物存在的情况下,当L.lindneri菌悬液采用过氧乙酸体积分数梯度法进行定量杀灭实验10 min(酿造车间灭菌作用时间20 min的0.5倍),杀灭对数>5时,所需质量分数为15%的艺康牌过氧乙酸杀菌剂最低体积分数为0.35%,即在模拟啤酒酿造车间生产环境,按使用说明书作用20 min时杀灭啤酒有害菌所需该过氧乙酸的终点体积分数为0.35%。
2.2 L.lindneri中和剂鉴定实验
如上所述,确认过氧乙酸杀菌剂杀灭目标菌液L.lindneri的终点体积分数为0.35%后,再按1.3.5节所述方法,利用L.lindneri菌悬液进行中和剂鉴定实验,鉴定使用的培养基为NBB-A固体平板,27 ℃厌氧培养5 d,实验结果如表2所示。

表2 L.lindneri中和剂鉴定实验结果
由表2可知:L.lindneri中和剂鉴定实验中第1组平均生长菌落数为0 cfu/mL,第2组平均生长菌落数为0 cfu/mL,第6组平均生长菌落数为0 cfu/mL,第3,4,5组菌悬液为4.1×107~4.2×107cfu/mL,满足菌悬液为1.0×107~5.0×107cfu/mL的实验条件,且其组间菌落数误差率为1.6%,未超过15%,说明0.5%的Na2S2O3溶液作为中和剂时,0.35%过氧乙酸对L.lindneri的杀灭作用被完全抵消了,且0.5%的Na2S2O3溶液及其中和产物对NBB-A培养基及L.lindneri的生长无明显影响,实验菌在NBB-A中生长良好。
2.3 E.coli 8099定量杀菌实验
如1.3.4节所述方法,吸取1 mL目标菌液埃希氏大肠杆菌E.coli8099于试管内,置(20±1) ℃水浴中5 min后,加入10 mL过氧乙酸于试管内混匀,作用10 min,后经0.5%无菌Na2S2O3溶液中和处理,用无菌生理盐水10倍系列稀释后,使用营养琼脂平板培养基进行活菌培养计数,37 ℃好氧培养1 d,对应中和剂、稀释液和培养基同时作阴性对照,实验结果如表3所示。

表3 E.coli 8099不同杀菌剂体积分数终点实验结果
由表3可知:在3%除气啤酒干扰物存在的情况下,当E.coli8099菌悬液采用过氧乙酸体积分数梯度法进行定量杀灭实验10 min(酿造车间灭菌作用时间20 min的0.5倍),过氧乙酸体积分数≥0.2%时,营养琼脂培养基上生长菌落数均为0,其杀灭对数值>5,即在啤酒厂使用体积分数为0.2%~0.5%的过氧乙酸杀菌剂可以完全杀灭卫生学指示菌E.coli8099。因此,食品加工设备、管道、食品罐装容器和设备等的杀菌,推荐作用时间一般为10~20 min,过氧乙酸质量浓度为300~750 mg/L,对应杀菌剂体积分数为0.2%~0.5%。
2.4 E.coli 8099中和剂鉴定实验
在验证体积分数为0.2%的过氧乙酸杀菌剂可有效杀灭卫生学指示菌E.coli8099后,按1.3.5节所述方法,利用菌悬液E.coli8099进行中和剂鉴定实验,鉴定使用的培养基为营养琼脂固体平板,37 ℃好氧培养1 d,实验结果如表4所示。
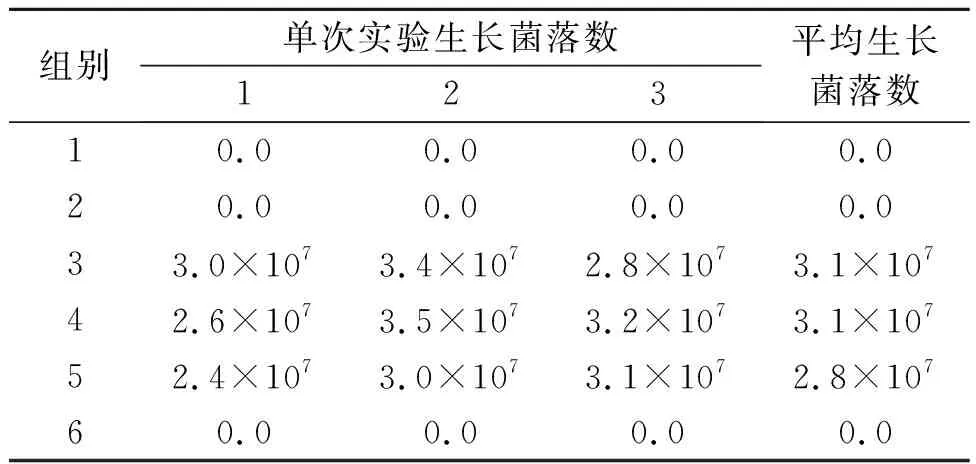
表4 E.coli 8099中和剂鉴定实验结果
由表4可知:E.coli8099中和剂鉴定实验中第3,4,5组间菌落数误差率为4.4%,未超过15%,第1组平均生长菌落数为0 cfu/mL,第2组平均生长菌落数为0 cfu/mL,第6组平均生长菌落数为0 cfu/mL,且第3,4,5组菌悬液生长菌落数为2.8×107~3.1×107cfu/mL,满足菌悬液生长菌落数为1×107~5×107cfu/mL的实验条件。研究结果表明:使用Na2S2O3体积分数为0.5%的溶液作为中和剂,过氧乙酸体积分数为0.2%对埃希氏大肠杆菌E.coli8099的杀灭作用被完全抵消了,且Na2S2O3体积分数为0.5%的溶液及其中和产物对营养琼脂培养基及E.coli8099生长无明显影响,实验菌在营养琼脂培养基中生长良好。
综上所述,以湖北轻工职业技术学院教学啤酒厂为例,酿造车间使用含过氧乙酸质量分数为15%的杀菌剂其终点体积分数测定结果为0.35%。使用实验测定的过氧乙酸终点体积分数指导啤酒生产企业湖北汇鼎酒业有限公司及湖北蜗牛角啤酒酿造有限公司的清洗灭菌操作,最终啤酒产品送样到第三方检测机构检测,啤酒微生物指标沙门氏菌及金黄色葡萄球菌均合乎食品安全国标要求[16-17]。
3 结 论
以湖北轻工职业技术学院教学啤酒厂为例,啤酒厂酿造车间使用含过氧乙酸质量分数为15%的杀菌剂杀菌时间为20 min时,在使用说明书体积分数为0.2%~0.5%的指导下,当其使用体积分数≥0.35%时,既可杀灭以L.lindneri为典型代表的啤酒有害菌,也可杀灭以埃希氏大肠杆菌E.coli8099为代表的卫生学指示菌;当体积分数<0.35%时,则只可杀灭E.coli8099,不能杀灭以L.lindneri为典型代表的啤酒有害菌。因此,湖北轻工职业技术学院教学啤酒厂酿造车间使用过氧乙酸杀灭啤酒有害菌所需的终点体积分数测定结果为0.35%,使用该体积分数的过氧乙酸杀菌剂既可满足生产灭菌需求,又能尽可能地节约清洗灭菌费用,减少设备内杀菌剂残留,利于食品安全,避免不利氧化及其他质量方面的负面影响。
