PD-1抑制剂联合化疗治疗复发膀胱小细胞癌1例报告并文献复习
2023-12-08张又红王桂华
张又红 王桂华
1.湖南中医药大学研究生院,湖南长沙 410000;2.长沙市中心医院肿瘤科,湖南长沙 410000
原发性膀胱小细胞癌(small cell carcinoma of the bladder,SCCB)是一种起源于尿路上皮的恶性神经内分泌肿瘤,临床上罕见[1],目前治疗方案暂未明确。近年来化疗联合免疫治疗在膀胱尿路上皮癌(urothelial carcinoma,UC)中取得不错进展,然而,其在治疗SCCB 方面,少有报道。长沙市中心医院于2021 年收治1 例SCCB 患者,在局部治疗过程中出现膀胱外转移,随后使用了化疗联合免疫治疗。现报道如下。
1 病例资料
患者男性,57 岁,因“无痛性肉眼血尿4 月余,加重5 天”入院。入院查体无明显阳性体征,行尿常规示白细胞1 ~3/HP,红细胞50 ~75/HP,隐血阳性;腹部计算机断层扫描(computed tomography,CT)平扫+增强:膀胱占位病变(图1),于2021 年10 月19 日行经尿道膀胱肿瘤电切术(transurethral resection of bladder tumor,TURBT),病理活检(图2)及免疫组化(图3)确诊为混合型高级别浸润性尿路上皮癌-小细胞神经内分泌癌,CK7(+),34βE12(+),CD56(+),嗜铬素A(chromograninA,CgA)(-),突触素(synaptophysin,Syn)(+),P53(+),Ki67(80%),cT3bN0M0。予以吉西他滨(江苏豪森药业,国药准字 H20030105,规格:0.2 g/ 支)2.0 g/次膀胱内化疗(术后即刻、术后2 个月内1 次/周,2 个月后1 次/月)+术后辅助放疗。术后5 个月,患者诉胸痛不适,未见咳嗽咳痰、胸闷、咯血、痰中带血等。复查胸部CT,见双上肺新发实性结节(图4A、图4C),左侧第5 肋头新发骨质破坏伴软组织肿块(图5A),考虑转移,患者局部行肋骨立体定向放疗(40 Gy/10次),全身行GC 方案静脉化疗[吉西他滨1.8 g 第1、8 天+顺铂(齐鲁制药,国药准字 H37021358,规格:10 mg/ 支)120 mg 第1 天],于第2 周期加用替雷利珠单抗(Tislelizumab,百济神州,国药准字S20190045,规格:10 ml ∶100 mg)200 mg 免疫治疗,患者因出现Ⅳ度骨髓抑制(白细胞0.42×109/L),第3 周期时未足量完成吉西他滨治疗。1 个月过后,患者复查CT 发现,患者肺部原转移灶消退(图4B、图4D)、肋旁软组织肿块明显缩小(图5B),但该肋后段出现病理骨折(图5B),左下叶新发转移(图4E),患者出现进展且难以耐受原治疗方案,换用EP 方案治疗[顺铂45 mg 第1 ~3 天+依托泊苷50 mg(日本化药株式会社,注册证号 H20160613,规格:25 mg×40 粒/ 盒)连服21 天+Tislelizumab 200 mg 第1 天]。第2 周期化疗时,患者肺部左下叶病灶消失(图4F),肋骨头骨折处骨痂形成,其旁软组织肿块进一步缩小(图5C)。4 周期化疗结束后,采用实体肿瘤疗效评估标准1.1(response evaluation criteria in solid tumors,RECIST1.1)进行评估,根据RECIST 最新标准,原转移灶达到部分缓解(partial response,PR)(图5D),未见明显进展。随后予以Tislelizumab 200 mg 免疫维持治疗,截至2023 年4 月,患者仍病情稳定。上述全身化疗和免疫治疗21 d 为1 个疗程。因治疗或预防骨髓抑制,放化疗过程中均酌情使用地榆升白片(成都地奥,国药准字 Z20026497,规格:0.1 g×40 片/盒)、人粒细胞刺激因子(齐鲁制药,国药准字S19990049,规格:100 μg/支)、聚乙二醇重组人粒细胞刺激因子(齐鲁制药,国药准字 S20150013,规格:1 mg ∶3 mg×1 支)升白药物升高白细胞。

图1 腹部CT(膀胱内不规则软组织密度影,较大者约50 mm×33 mm,周围脂肪间隙模糊)
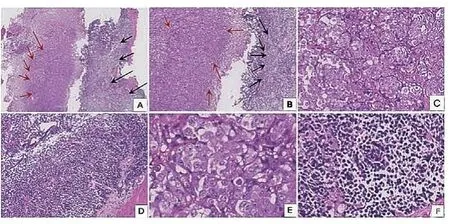
图2 膀胱癌病理常规

图3 CK7(+)、34βE12(+)提示上皮肿瘤,CD56(+)、Syn提示小细胞神经内分泌肿瘤,P53、Ki67(+)(免疫组化100×)
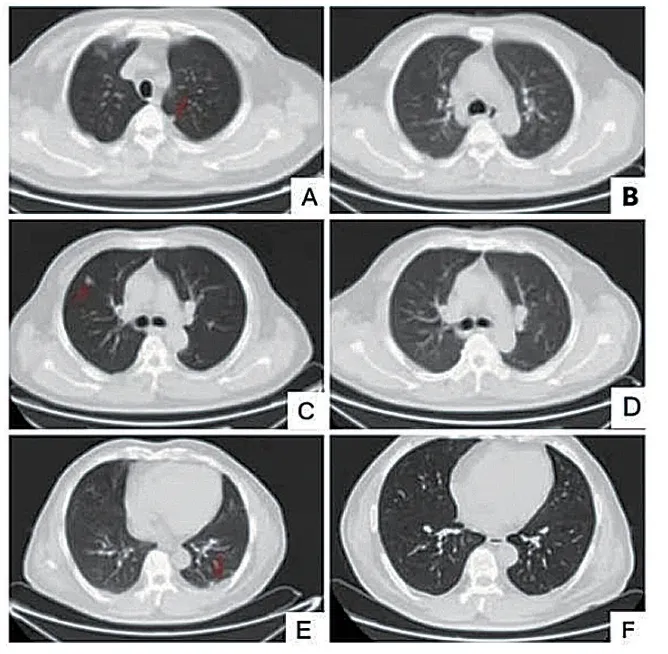
图4 胸部CT
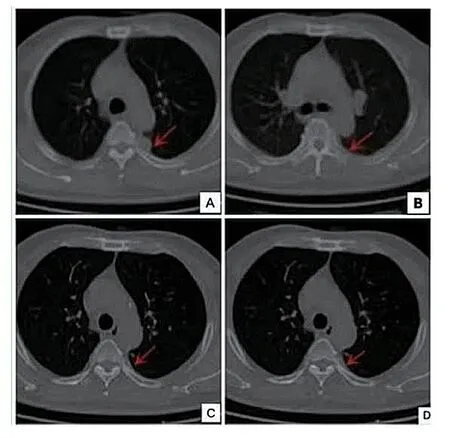
图5 胸部CT
2 讨论
膀胱癌是泌尿系统最常见的恶性肿瘤,位居全球恶性肿瘤第十位[2]。小细胞癌(small cell carcinoma,SCC)多发于肺,泌尿生殖道少见,SCCB 好发于老年男性,男女比例为2.33 ∶1,中位患病年龄为72.5 岁,吸烟是该病发病的主要危险因素[3]。与大部分相关报道相比,该病例发病年龄较早。
在病理类型上,膀胱小细胞癌通常表现为混合型(40%~70%),混杂成分以尿路上皮癌多见(57%)[4],此外还有腺癌、鳞癌等。目前SCCB 的发病机制尚未明确,主要有以下三种假说:①膀胱组织中神经内分泌细胞的恶变;②高分化尿路上皮细胞的化生;③多潜能尿路上皮干细胞特定转化,这解释了SCCB 表达不同细胞标志物且常与其他类型恶性肿瘤并存的现象。
SCCB 目前无标准的治疗方案,因其与小细胞肺癌(small cell lung cancer,SCLC)相似的病理特征,目前治疗主要参考于SCLC 指南和回顾性研究[5]。局限期SCCB 患者,可在行同步放化疗或在行新辅助治疗后行根治手术治疗;而广泛期SCCB 患者,则可行单独化疗[6]。对于保留膀胱意愿强烈,可考虑接受TURBT 术,并术后予以膀胱内化疗+辅助放疗等治疗手段以提高局部控制率。SCCB 具有浸润性强、恶性度高、多有微转移等特性,单纯手术等局部治疗并不能阻止肿瘤发展,多需全身辅助化疗[7-8]。Mackey 等[9]发现以铂类为基础的化疗是影响患者预后的独立因素。然而使用含铂方案化疗,转移性SCCB 的中位总生存期也仅为7.6 个月[10]。程序性死亡受体(programmed cell death-1,PD-1)在许多免疫细胞表面表达,PD-1与程序性死亡受体配体1(programmed deathligand 1,PD-L1)结合,可以抑制T 细胞对癌症的免疫应答。Tislelizumab 是一种新型人源化单抗PD-1 抑制剂。GC 方案化疗联合Tislelizumab 相较于单纯GC 化疗治疗局部晚期或者转移性膀胱癌,具有更好的疗效[11]。Tislelizumab 用于既往含铂治疗的转移性膀胱癌可在临床获益并安全性可控[12]。化疗联合Tislelizumab 可作为混合病理变异的SCCB 患者的有效治疗选择。与小细胞肺癌类似,EP 方案主要用于局限期或广泛期SCCB 治疗方案[13]。有研究[14]报道,Tislelizumab 联合EP 化疗作为全身疗法相比于单纯化疗治疗广泛期SLCL更有效,也有研究表明Tislelizumab 在食管癌等常见进展期实体肿瘤中取得不错疗效,但在SCC 尤其是SCCB 中鲜有报道。因此,本病例可能为复发性SCCB 使用化疗联合免疫治疗时提供一种新的思路。
SCCB 预后非常差,5 年平均生存率为19%[15]。有文献指出纯SCCB 和混合SCCB 均以p53 过表达和高PD-L1 表型为特征[16],尽管p53、PD-L1 是膀胱上皮癌的预后指标,但在SCCB 中无预测价值[17-19]。相关研究表明混合型SCCB 预后更好[20]。Choong 等[8]发现相较于Ⅱ期,Ⅲ、Ⅳ期SCCB 患者预后明显更差,5 年存活率只有15.4%和10.5%。总体来说,由于SCCB 病例较少,目前对于其预后因素仍需进一步探究。
综上所述,SCCB 临床罕见,目前尚无标准的治疗方案。本病例行局部治疗后出现远处转移,使用化疗联合替雷利珠单抗疗效显著。对于极易发生复发和转移的SCCB,该方案可能是一种有用的治疗的选择。然而,还需相关研究来评估这种治疗方案在人群水平上的有效性和安全性,并建立更多的SCCB 治疗策略。
