凝胶渗透色谱-激光光散射联用法检测医用壳聚糖类产品稳定性
2023-12-07刘叶彭健郭利娟孟晓依陈仿如高川
刘叶,彭健,郭利娟,孟晓依,陈仿如,高川
(山东省医疗器械和药品包装检验研究院,国家药品监督管理局生物材料器械安全性评价重点实验室,国家药品监督管理局医用卫生材料及生物防护器械质量评价重点实验室,济南 250101)
壳聚糖及其衍生物为天然高分子多糖,具有选择性促进表皮细胞生长的独特生物活性、生物相容性、生物可降解性且降解产物安全无毒等特点,除此之外,亦具有广泛的抗菌、止血、止痛作用,是理想的医用生物材料。壳聚糖及其衍生物具有优异的生物学特性,被广泛应用于医疗器械领域,如壳聚糖凝胶、壳聚糖敷料、壳聚糖止血粉等[1-3]。研究表明,医用壳聚糖类产品的作用机理与分子量大小及其分布、浓度、脱乙酰度、金属离子、菌株、晶型等因素相关[4-7]。董谦等[8]建议使用分子量作为壳聚糖类产品的属性界定依据。综上所述,分子量及其分布是评价壳聚糖类医疗器械产品安全性、有效性的重要指标之一。
医用壳聚糖类产品按风险管理分类属于ⅠⅠ、ⅠⅠⅠ类医疗器械,临床使用时与人体直接接触,存在潜在的安全风险,需对其安全性和有效性进行控制。医用壳聚糖产品的稳定性是反映其安全性和有效性的重要方面,而其相对分子质量及其分布的变化是表征其稳定性的重要参数。现行有效的与医用壳聚糖类产品相关的指南或行业标准有YY/T 0953—2020、YY/T 1699—2020 及ASTM F2602-18[9-11],以上标准或指南中虽然规定了相关医用壳聚糖产品相对分子质量及其分布的测试方法,但未涉及其货架有效期内稳定性的研究。目前,有关壳聚糖及其衍生物稳定性的研究多集中于其抑菌性能[12-14],如吕志华等[15]曾利用加速试验并采用高效凝胶渗透色谱法、明胶比浊法、氧瓶燃烧法考察几丁糖酯原料药的稳定性,但鲜有通过自然存放条件下相对分子量及其分布研究医用壳聚糖类产品在货架存放有效期内稳定性的报道。
笔者利用凝胶渗透色谱-激光光散射联用法检测外科手术用防粘连冲洗液、医用几丁糖、医用防粘连改性壳聚糖(膜)以及壳聚糖基可吸收止血非织布4种样品状态与预期目的具有代表性的医用壳聚糖产品在货架存放有效期内的相对分子质量及其分布的变化,以评价4 种产品在货架存放有效期内的稳定性。该研究结果可为相关审评部门提供技术支撑,为生产企业的产品质量控制及其在货架存放有效期内的稳定性提供参考。
1 实验部分
1.1 主要仪器与试剂
凝胶渗透色谱-激光光散射联用仪:Agilent 1260Ⅰnfinity型,美国安捷伦科技有限公司。
示差检测器:Optilab T-rEX 型,美国怀雅特技术公司。
18 角度激光光散射检测器:DAWN HELEOS-Ⅱ型,美国怀雅特技术公司。
电子天平:XS204 型,感量为0.1 mg,瑞士梅特勒-托利多公司。
纯水/超纯水一体化系统:Millipore Advantage A10型,美国密理博公司。
硝酸钠、乙酸、乙酸钠:分析纯,国药集团化学试剂有限公司。
叠氮化钠(NaN3):分析纯,北京化学试剂公司。
医用几丁糖样品:1 mL,上海其胜制剂有限公司。
壳聚糖基可吸收止血非织布样品:30 mm×30 mm,青岛博益特生物材料股份有限公司。
外科手术用防粘连冲洗液:250 mL,杭州协合医疗用品有限公司。
医用防粘连改性壳聚糖(膜)样品:100×50×0.06 mm,北京百利康生化有限公司。
10 种葡聚糖相对分子质量标准品:编号、相对分子质量、来源见表1。
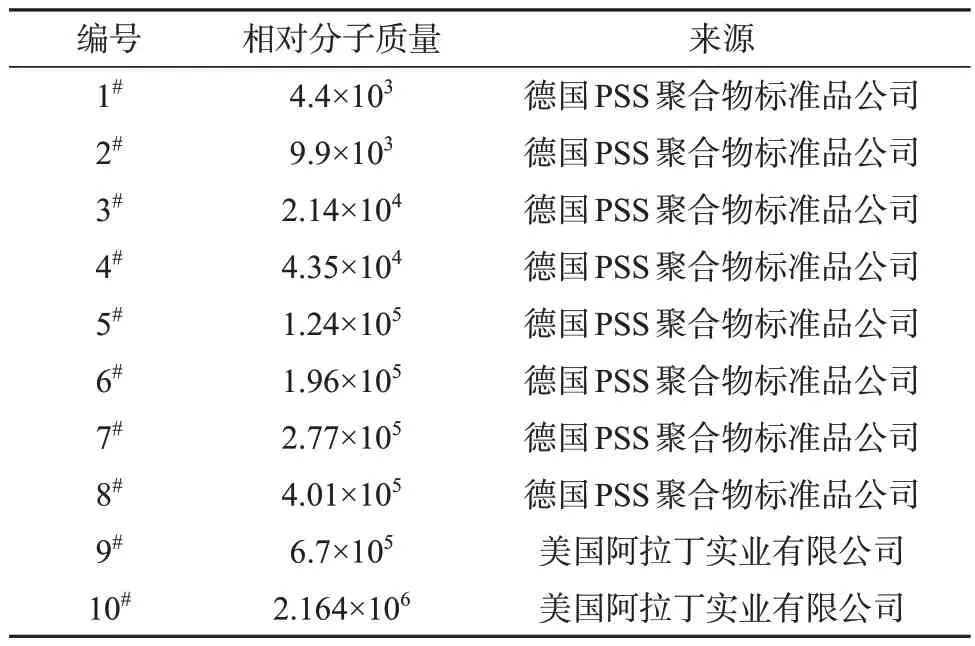
表1 10种葡聚糖相对分子质量标准品信息
1.2 色谱条件
色谱柱:OHpak SB-803 HQ(8.0 mm×300 mm,6 μm,日本昭和电工株式会社)、OHpak SB805 HQ(8.0 mm×300 mm,13 μm,日本昭和电工株式会社)、OHpak SB-806 HQ(8.0 mm×300 mm,13 μm,日本昭和电工株式会社)及OHpak SB-G 6B(6.0 mm×50 mm,13 μm,日本昭和电工株式会社);柱温:35 ℃;流动相:A 为0.1 mol/L 硝酸钠溶液(含质量分数为2×10-4的NaN3)、B 为0.25 mol/L 乙酸-乙酸钠缓冲液(含质量分数为2×10-4的NaN3,并用乙酸调节pH 为4.5);流动相流量:1.0 mL/min;进样体积:900 μL。
1.3 样品选择
选取作为Ш类医疗器械管理的4种医用壳聚糖类产品,样品名称及货架存放有效期见表2。

表2 样品统计表
1.4 溶液配制
1.4.1 葡聚糖相对分子质量系列混合标准品溶液
分别称取1#葡聚糖标准品11.7 mg、6#葡聚糖标准品10.1 mg,用流动相溶解并定容至10 mL,作为混合标准溶液1;分别称取2#葡聚糖标准品14.2 mg、7#葡聚糖标准品13.3 mg,用流动相溶解并定容至10 mL,作为混合标准溶液2;分别称取3#葡聚糖标准品12.8 mg、8#葡聚糖标准品13.0 mg,用流动相溶解并定容至10 mL,作为混合标准溶液3;分别称取4#葡聚糖标准品13.4 mg、9#葡聚糖标准品16.5 mg,用流动相溶解并定容至10 mL,作为混合标准溶液4;分别称取5#葡聚糖标准品11.8 mg、10号葡聚糖标准品12.7 mg,用流动相溶解并定容至10 mL,作为混合标准溶液5。
1.4.2 样品溶液
样品溶液1:5 mg/mL,称取医用几丁糖约100 mg,分别加入流动相A、流动相B 稀释至20 mL,静置12 h。
样品溶液2:1 mg/mL,称取约20 mg 壳聚糖基可吸收止血非织布,分别加入流动相A、流动相B稀释至20 mL,静置12 h。
样品溶液3:取外科手术用防粘连冲洗液直接测定。
样品溶液4:1 mg/mL,称取约20 mg 医用防粘连改性壳聚糖(膜),分别加入流动相A、流动相B稀释至20 mL,静置12 h。
1.5 实验方法
取1.4.2 配制的样品溶液,按照1.2 色谱条件分别在流动相A 和流动相B体系下进行检测;取1.4.1配制的葡聚糖相对分子质量标准品溶液按照1.2 色谱条件分别在流动相A 体系下进行检测;取初始时4种样品和自然条件下存放一年后的4种样品,分别按照1.4.2方法配制样品溶液按照1.2色谱条件在流动相A 体系下进行检测,通过怀雅特Astra 6.1 软件积分拟合计算得到不同时间点样品溶液的重均相对分子质量、数均相对分子质量以及相对分子质量分布,通过比较相对分子质量来判断样品稳定性。
2 结果与讨论
2.1 流动相的选择
对比了两种流动相对4 种样品的溶解性,分别称取医用几丁糖、壳聚糖基可吸收止血非织布、外科手术用防粘连冲洗液、医用防粘连改性壳聚糖(膜)各10 mg 于玻璃瓶中,平行取样,分为两组,第1 组分别加入10 mL流动相A,第2组分别加入10 mL流动相B。30 min 后,第1 组中4 种样品均完全溶解,第2 组中外科手术用防粘连冲洗液、医用几丁糖完全溶解,而医用防粘连改性壳聚糖(膜)、壳聚糖基可吸收止血非织布未完全溶解。
同时分别以流动相A 和B 进行试验,对比了1.4.2 配制的四种样品溶液,色谱图见图1。结果表明,在流动相B 中样品带来的基线噪音大于流动相A,另外由于部分样品未完全溶解于流动相B,影响检验结果的准确性。综合考虑基线噪声和溶解性能,选择0.1 mol/L 硝酸钠(含质量分数为2×10-4的NaN3)为样品稳定性试验流动相。

图1 分别使用流动相A和流动相B时的样品色谱图
2.2 色谱柱的选择
选择Shodex SB803、SB805、SB806 及保护柱四柱串联,分别对1.4.1 配制的5种葡聚糖相对分子质量系列混合标准品溶液进行分析,色谱图见图2。结果表明,四柱串联能实现良好的分离效果。
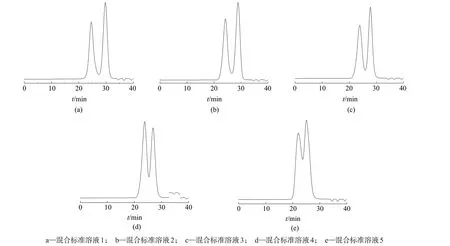
图2 不同相对分子质量葡聚糖标准品分离色谱图
2.3 样品稳定性试验
在1.2色谱条件下,选择表2列举的4种样品,分别于初始放置于货架时及自然条件下存放一年后取样,按照1.4.2方法配制样品溶液,对两个时间点的4种样品分别进行检测。用软件计算出样品的重均相对分子质量、数均相对分子质量以及相对分子质量分布结果,对初始值和一年后的检验数据进行比对计算,结果见表3。4种样品稳定性试验相对分子质量色谱图见图3。
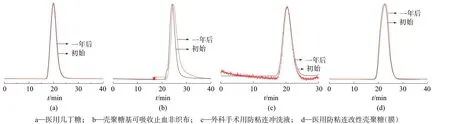
图3 4种样品稳定性试验相对分子质量色谱图
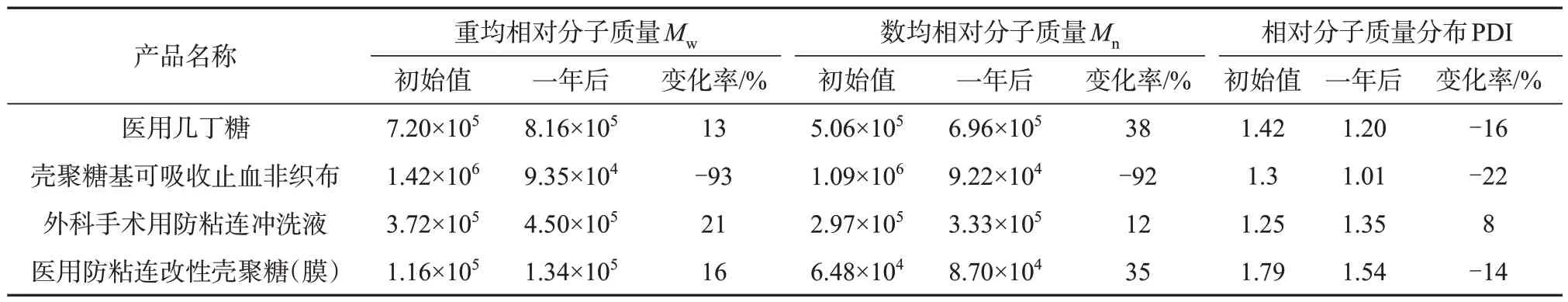
表3 4种样品稳定性试验结果
壳聚糖类产品的相对分子质量大小及分布与该类产品使用时的作用机理有关[16],相对分子质量也被认为是影响壳聚糖抗菌性能的主要因素,有研究者[17-19]选取不同相对分子质量大小的壳聚糖产品在对常见的黄色葡糖糖球菌、大肠杆菌等菌种进行抑菌性能实验时,均发现在抗菌作用的表现中壳聚糖产品相对分子质量大时能有效阻隔细菌,而小分子的壳聚糖会渗透至细菌中破坏细菌结构起到杀菌效果。结合以上作用机理,董谦等[8]建议使用相对分子质量作为壳聚糖类产品的属性界定依据,当相对分子质量为1.0×105及以上时,壳聚糖利用物理阻隔作用达到抗菌目的,可认为是医疗器械作用;当相对分子质量为1.0×104及以下时,壳聚糖利用渗透细菌细胞干扰细胞新陈代谢活动达到抗菌目的,可认为是药理作用;当相对分子质量为1.0×104至1.0×105时,对不同类型的壳聚糖产品其抑菌功效机理需要进一步考察界定。
几丁糖类产品作为粘弹性补充物质直接恢复关节滑液的流变性特性(弹性和粘性),起到关节润滑作用,通过大分子自身的三维网络结构,形成物理屏障,保护关节软骨,减少相互之间的摩擦,作为眼科粘弹剂在手术过程中可以维持前房的深度,同时保护眼角膜内皮,防止角膜内皮损伤,并能起到润滑作用[20-21]。对于防粘连产品来说,作用机理主要为物理阻隔,部分产品能够具有选择性的促进上皮细胞以及内皮细胞生长而抑制成纤维细胞生长的生物学特性,从而促进组织生理性修复,抑制疤痕形成,减少组织粘连,并具有局部止血作用及抑制血纤维蛋白束形成,从而减少了因血肿机化而造成的组织粘连,还能起到润滑及生物屏障作用,能有效防止粘连发生[22-23]。表3 结果表明,医用几丁糖、外科手术用防粘连冲洗液、医用防粘连改性壳聚糖(膜)产品的重均相对分子质量、数均相对分子质量及其分布变化均小于38%,并且重均相对分子质量均保持在1.0×105及以上,表明该类产品具有良好的稳定性,在使用过程中能起到优良的润滑及生物屏障作用,有效防止粘连发生,并可在应用部位保持足够的时间,达到预期目的,可认为属于医疗器械作用。
壳聚糖基可吸收止血非织布与创面血液或者渗出液接触后,能在接触面形成高粘性凝胶,迅速与创面紧密贴附,有效封闭创面和血管断端,达到快速止血的目的,同时也能使创面血液的红细胞聚集,辅助凝血块的形成,从而在局部控制出血中发挥辅助止血作用,置入人体后缓慢降解,最终降解物为氨基葡萄糖单体,可被肌体吸收[24-25]。此次实验发现壳聚糖基可吸收止血非织布产品初始相对分子质量是4类产品中最大的,重均相对分子质量和数均相对分子质量均达到了1.0×106以上,同时也是相对分子质量及其分布变化最大的,重均相对分子质量从初始的1.42×106降低到9.35×104,减少93%;数均相对分子质量从1.09×106减少到9.22×104,减少约92%;相对分子质量分布从1.30减少到1.01。说明样品在储藏过程中发生了降解,其功能由原始的物理阻隔抑菌向其渗透抑菌发生了转变,抑菌效果没有发生改变,但是对于其是否能达到快速止血的功效需要进一步考察。
3 结语
通过激光散射-凝胶渗透色谱联用法跟踪了医用几丁糖、壳聚糖基可吸收止血非织布、外科手术用防粘连冲洗液、医用防粘连改性壳聚糖(膜)4种医用壳聚糖类产品在货架有效期内的相对分子质量及其分布的变化。医用几丁糖、外科手术用防粘连冲洗液、医用防粘连改性壳聚糖(膜)3种产品在货架有效期内的相对分子质量及其分布变化在可接受范围内,仍保持其产品原本作用机理。壳聚糖基可吸收止血非织布临期时的相对分子质量及其分布较临期1 年时急剧下降,表明该产品在货架有效期内发生了明显降解,其临床使用时的安全性和有效性需进一步评估。研究结果表明,需要关注医用壳聚糖类产品在货架有效期内的稳定性,以保证其临床使用时的安全有效性。
