基于小鼠子宫平滑肌收缩活性测定的桂枝茯苓胶囊质量评价研究
2023-11-27金祎敏王东帆章晨峰王振中吕耀中
金祎敏,谢 燕,王东帆,章晨峰,曹 亮,谢 雪,肖 伟, ,王振中, *,吕耀中*
基于小鼠子宫平滑肌收缩活性测定的桂枝茯苓胶囊质量评价研究
金祎敏1,谢 燕1,王东帆2, 3,章晨峰2, 3,曹 亮2, 3,谢 雪2, 3,肖 伟1, 2, 3,王振中1, 2, 3*,吕耀中2, 3*
1. 南京中医药大学,江苏 南京 210023 2. 中药制药过程控制与智能制造技术全国重点实验室,江苏 连云港 222001 3. 江苏康缘药业股份有限公司,江苏 连云港 222001
从桂枝茯苓胶囊(Guizhi Fuling Capsules,GZFLC)临床用于治疗痛经的功效出发,探索建立基于子宫平滑肌收缩活性测定的GZFLC质量生物活性评价方法。通过注射雌激素增加小鼠子宫敏感性,建立缩宫素诱导的小鼠离体子宫平滑肌收缩模型,采集给药前后小鼠子宫平滑肌的收缩频率、幅值和峰面积,以收缩峰面积为指标进行统计并对药效进行归一化处理。考察小鼠离体子宫平滑肌收缩模型的主要影响因素如雌激素注射方式与天数、缩宫素浓度、动物周龄和GZFLC前处理方法。建立GZFLC质量生物活性评价方法并进行方法学考察,测定10个批次GZFLC合格样品及2个GZFLC高温破坏样品的生物活性。连续3 d ip雌激素10 mg/(kg·d)后小鼠子宫平滑肌收缩峰面积较高且收缩节律较好;最适缩宫素造模质量浓度为0.050 μg/mL;将GZFLC配制成质量浓度为0.125 g/mL的药液并超声溶解60 min有利于药效发挥;重复性考察RSD为11.298%,日内精密度RSD为12.452%,日间精密度RSD为10.438%;10批次GZFLC半数抑制浓度(half inhibitory concentration,IC50)为1.526~1.631 mg/mL,高温破坏后GZFLC的IC50明显增大。基于子宫平滑肌收缩活性测定的GZFLC质量评价方法重复性和精密度较好,为后续GZFLC的综合质量评价标准建立提供了科学依据。
桂枝茯苓胶囊;离体子宫;平滑肌收缩活性;生物活性测定;质量评价
痛经是最常见的妇科疾病之一[1-2]。临床上根据病因可分为原发性痛经和继发性痛经2种类型[3-4]。其中原发性痛经指由于子宫过度收缩引起的、无盆腔器质性病变的痛经,其主要临床表现为经期前后或月经期出现下腹部坠胀和痉挛性疼痛,发病率高达34%~94%[5-6]。中医治法多以调理冲任气血为主,具体方法为补益气血、疏肝理气、温经散寒等[7]。桂枝茯苓胶囊源自东汉张仲景《金匮要略》中的桂枝茯苓丸,由其经过剂型改革而来,主要成分包括桂枝、茯苓、桃仁、丹皮、白芍[8],具有活血、化瘀、消癥等功效[9],临床上常用于原发性痛经[10]、慢性盆腔炎[11]、子宫肌瘤[12]、子宫内膜异位症[13]等疾病。
质量稳定可控是中药有效性和安全性的重要前提[14]。现行的中药质量控制模式主要包括形态学鉴定、化学定性鉴别和指标性成分测定[15]。但中药药效是多种成分、多个环节、多个靶点协同作用的结果,从而表现出整合性的特征。因此,不能用单一活性成分来衡量中药整体质量[16]。目前桂枝茯苓胶囊的生产质控过程已进行了优化,其抗痛经等药效显著增强,且产品均一性显著提升[17-19],但现有质量控制成分尚不能完全反映药物的整体临床疗效。
中药生物活性测定是一种基于药物的生物效应,利用生物统计方法,通过特定的实验设计评价中药的有效性,从而保证中药质量的方法[17]。该方法可以反映中药的整体效应和协同作用,为中药的质量控制提供科学依据。本研究考察了小鼠离体子宫收缩模型关键影响因素及桂枝茯苓胶囊前处理方法,利用维拉帕米进行了模型的方法学考察,初步建立基于抑制子宫平滑肌收缩活性的桂枝茯苓胶囊质量生物活性评价方法。在此基础上,检测了10个批次桂枝茯苓胶囊合格样品及经高温破坏后样品的生物活性,为进一步优化桂枝茯苓胶囊产品质量标准提供参考。
1 材料
1.1 动物
SPF级雌性C57BL/6小鼠,体质量16~23 g(6周龄15.8~16.4 g、8周龄17.3~18.1 g、10周龄18.5~19.0 g、12周龄20.6~22.7 g),购自斯贝福(北京)生物技术有限公司,许可证号SCXK(京)2019-0010,合格证号No.110324221106926117、No.110324221106450846、No.110324221107297012,小鼠统一放置于动物屏障房内适应性饲养,12 h黑暗与光照循环,自由饮食。动物实验经江苏康缘药业股份有限公司动物伦理委员会批准(批准号2022103102、2022101804、2022111702)。
1.2 药品与试剂
桂枝茯苓胶囊(国药准字Z10950005,批号210311、210312、220305、220702、230213、230214、230215、230301、230302、230303),由江苏省康缘药业股份有限公司提供;盐酸维拉帕米(批号SLBH9660V)购自上海阿拉丁生化科技股份有限公司;雌激素注射液(批号C2209262)购自宁波第二激素厂;缩宫素(批号I221BA0012)购自生工生物工程(上海)股份有限公司;氯化钠注射液(批号B21120704)购自浙江国镜药业有限公司;其余试剂均为分析纯。
1.3 仪器
LE01086型八通道离体组织灌流系统、PowerLab 8/35多通道信号采集系统(AD Instruments公司);Milli-Q reference超纯水制备系统(美国Millipore公司);FE20型pH计、ME104E型电子天平(梅特勒-托利多仪器上海有限公司)。
2 方法
2.1 小鼠离体子宫平滑肌制备及收缩检测
将小鼠断颈处死,迅速剪开下腹部,暴露双侧子宫,先仔细分离子宫周边结缔组织,左右同时各取约1 cm长的子宫平滑肌,用细线进行两端结扎,将子宫条取出后置于持续通O2混合气(含5% CO2)的4 ℃乐氏液(NaCl 9.2 g、KCl 0.42 g、CaCl20.24 g、NaHCO30.15 g、葡萄糖1.0 g溶解于1 L重蒸水中,pH 7.4)中备用。在各浴槽中加入20 mL乐氏液,待水温37 ℃恒定后,将制备的子宫组织下端在浴槽中固定,上端悬挂于张力换能器上,同时通入O2混合气(含5% CO2),使平滑肌保持松弛状态。待肌条适应20 min后,调节旋钮使子宫收缩基线的张力为0.5 g,并开始记录子宫收缩曲线。待子宫平滑肌出现平稳的自主收缩节律后,在浴槽中加入缩宫素,子宫平滑肌随之出现短时间强直收缩,待收缩节律稳定后记录10 min收缩曲线。随后每隔10 min由低到高依次累积加入不同浓度的药物溶液,同时采集收缩频率、幅度和峰面积等数据。
2.2 造模条件考察
2.2.1 缩宫素浓度考察 取成年未孕雌性小鼠连续3 d ip雌激素[10 mg/(kg·d)]。实验当天分别在不同子宫浴槽中加入不同质量浓度(终质量浓度5、10、20、50、100、200、500 ng/mL)的缩宫素。考察不同质量浓度缩宫素对离体子宫收缩频率、幅度和峰面积的影响。
2.2.2 雌激素注射方式考察 考察不同雌激素注射方式下离体子宫自发性收缩及加入缩宫素诱导后收缩频率、幅值、峰面积的变化。
2.2.3 动物周龄 考察不同周龄C57BL/6小鼠子宫自发性收缩及缩宫素诱导后收缩频率、幅值和峰面积的变化。
2.3 指标选择及累加给药法药物抑制效应的归一化处理
离体子宫收缩情况考察指标有收缩频率、收缩幅值、收缩峰面积等[20]。收缩峰面积为子宫收缩曲线下面积,体现子宫张力的总体变化情况。在各指标中收缩峰面积变化最为明显,且组内差异较小,故本实验均采用收缩峰面积为指标进行统计。
维拉帕米是-型钙通道阻断剂,实验结束时加入终浓度为1×10−5mol/L的维拉帕米完全抑制子宫收缩,从而得到离体子宫收缩基线。将加入缩宫素后子宫的收缩状态作为0%抑制效应,将加入阻断剂后子宫的收缩状态作为100%抑制效应[21]。对于每个药物浓度计算抑制率。采用抑制率数值描绘量效曲线,计算半数抑制浓度(half inhibitory concentration,IC50)值。
抑制率=(FD-DX)/(FD-LD)
FD为给药前AUC值;DX为加入抑制剂后在X浓度下AUC值;LD为实验结束时加入-型钙通道阻断剂后AUC值
2.4 离体子宫收缩模型方法学考察
2.4.1 重复性考察 取同一份维拉帕米粉末配制相同浓度的维拉帕米供试品溶液6份,按上述方法测定,计算维拉帕米对离体子宫平滑肌收缩活力的平均IC50和RSD。
2.4.2 日内精密度考察 取同一份相同浓度的维拉帕米溶液,按上述方法测定,于同一天不同时间内,检测6次其对离体子宫平滑肌的抑制作用,计算维拉帕米对离体子宫平滑肌收缩活力的平均IC50和RSD。
2.4.3 日间精密度考察 取同一份相同浓度的维拉帕米溶液,按上述方法测定,分6 d检测其对离体子宫平滑肌的抑制作用,计算维拉帕米对离体子宫平滑肌收缩活力的平均IC50和RSD。
2.5 桂枝茯苓胶囊前处理条件的优化
2.5.1 配制浓度 以乐氏液为溶媒将同一批次桂枝茯苓胶囊分别配制成0.062 5、0.125 0、0.250 0、0.500 0 g/mL的药物溶液,超声60 min后备用。将以上每个质量浓度的桂枝茯苓胶囊分别进行累加给药,同时采集反应体系中药物最终质量浓度为0.5、1.0、2.0、4.0、8.0 mg/mL时的离体子宫收缩峰面积,比较不同配制质量浓度桂枝茯苓胶囊的IC50。
2.5.2 超声时间 以乐氏液为溶媒将同一批次桂枝茯苓胶囊配制成0.125 g/mL的药物溶液,分别进行15、30、60、120 min超声处理。比较不同超声时间桂枝茯苓胶囊的IC50。
2.6 桂枝茯苓胶囊对子宫平滑肌活力的抑制作用
在建立桂枝茯苓胶囊生物评价方法基础上考察10个批次桂枝茯苓胶囊对离体子宫收缩抑制作用的IC50。
2.7 高温破坏后桂枝茯苓胶囊对子宫平滑肌活力的抑制作用
200 ℃高温加热桂枝茯苓胶囊5、10 min,测定高温破坏后桂枝茯苓胶囊的IC50。
3 结果
3.1 造模条件考察
3.1.1 缩宫素浓度考察 如图1所示,缩宫素质量浓度为0.050 μg/mL时,小鼠子宫平滑肌收缩节律性较好,随时间变化峰面积衰减幅度较小,说明离体子宫的稳定性较好,选择此质量浓度进行后续实验。
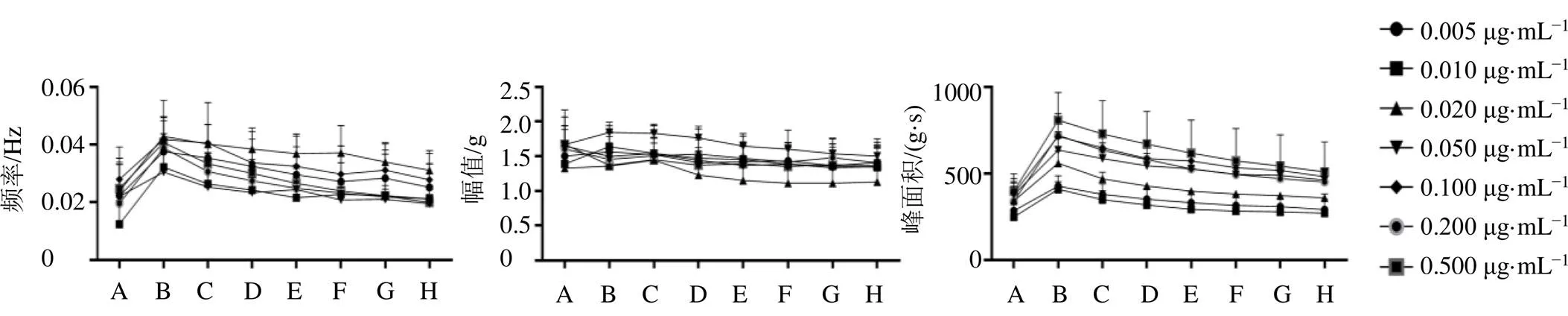
A-给药前 B-缩宫素 C-0~10 min D-10~20 min E-20~30 min F-30~40 min G-40~50 min H-50~60 min,图2、3同
3.1.2 雌激素注射方式考察 如图2所示,连续3 d ip 10 mg/(kg·d)雌激素时,小鼠子宫平滑肌收缩峰面积最大,说明在此条件下,子宫平滑肌对缩宫素的敏感性较好,易于后续实验统计。
3.1.3 动物周龄考察 考察不同周龄C57BL/6小鼠子宫自发性收缩及缩宫素诱导后收缩频率、幅值和峰面积的变化,结果见图3,不同周龄小鼠子宫平滑肌收缩峰面积差异较小。
3.2 离体子宫收缩模型方法学考察
3.2.1 重复性考察 重复性实验结果显示维拉帕米对离体子宫平滑肌收缩活力的IC50为1.09×10−7mol/L,RSD为11.298%(图4-A)。
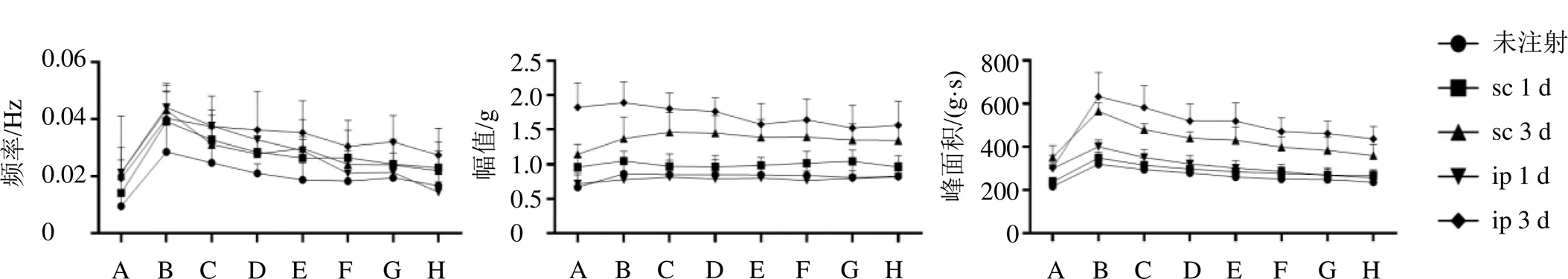
图2 不同雌激素注射方式下小鼠子宫平滑肌收缩频率、幅值、峰面积的变化(, n = 6)
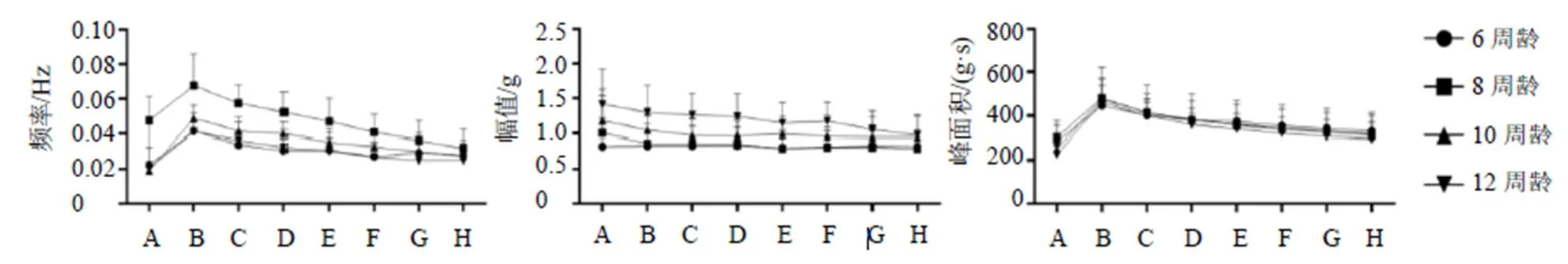
图3 不同周龄小鼠子宫平滑肌收缩频率、幅值、峰面积的变化(, n = 8)
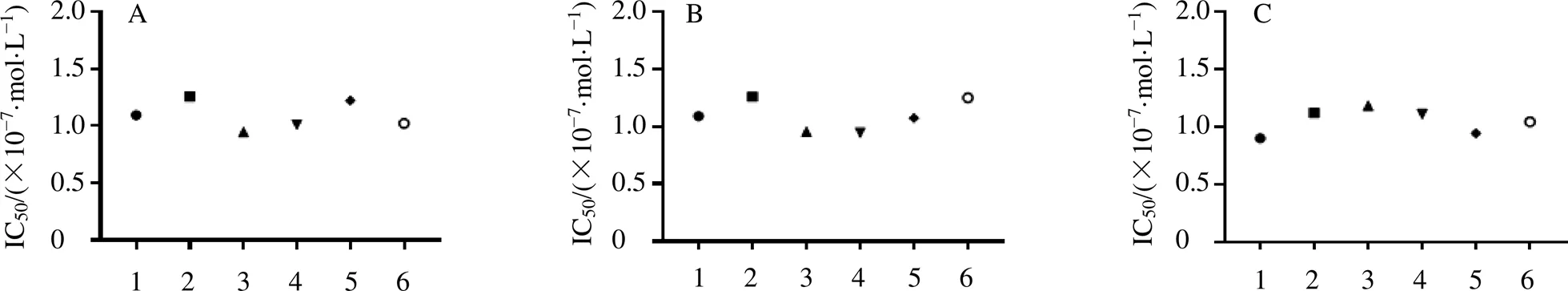
A-重复性考察 B-日内精密度考察 C-日间精密度考察
3.2.2 日内精密度考察 日内精密度实验结果显示维拉帕米对离体子宫平滑肌收缩活力的IC50为1.10×10−7mol/L,RSD为12.452%(图4-B)。
3.2.3 日间精密度考察 日间精密度实验结果显示维拉帕米对离体子宫平滑肌收缩活力的IC50为1.05×10−7mol/L,RSD为10.438%(图4-C)。
3.3 桂枝茯苓胶囊前处理条件的优化
3.3.1 质量浓度 比较不同质量浓度桂枝茯苓胶囊的IC50(表1),结果显示药物浓度增大,其IC50值反而有所升高,不利于药物溶解及发挥药效。当药液质量浓度为0.125 g/mL时,桂枝茯苓胶囊对子宫平滑肌收缩抑制作用的IC50值最小,因此选择为最佳质量浓度。
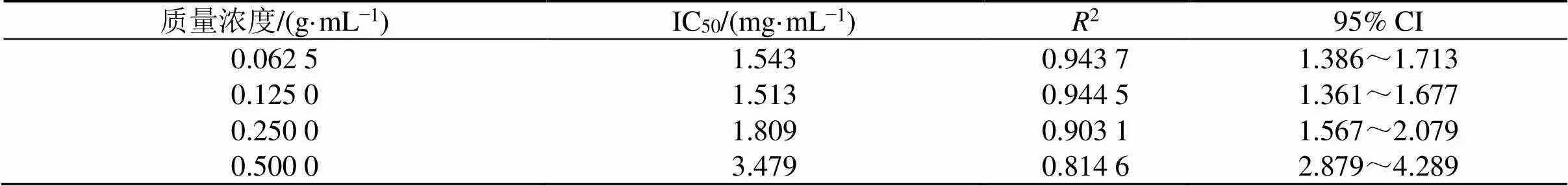
表1 不同质量浓度桂枝茯苓胶囊的IC50 (n = 6)
3.3.2 超声时间 比较不同超声时间桂枝茯苓胶囊的IC50(表2),当超声时间为60 min时,桂枝茯苓胶囊对子宫平滑肌收缩抑制作用的IC50值较小,结果说明超声前处理可能通过促进桂枝茯苓胶囊药物溶解从而利于药效发挥,但时间过长也可能引起药效减低。因此,选择最佳超声时间为60 min。

表2 不同超声时间桂枝茯苓胶囊的IC50(n = 6)
3.4 桂枝茯苓胶囊对子宫平滑肌活力的抑制作用
考察不同批次桂枝茯苓胶囊对离体子宫收缩抑制作用的IC50,结果见表3,10批次桂枝茯苓胶囊的IC50为1.526~1.631 mg/mL,RSD为2.344%。
3.5 高温破坏后桂枝茯苓胶囊对子宫平滑肌活力的抑制作用
高温破坏后样品IC50与正常样品相比明显提高,且高温破坏10 min样品IC50高于高温破坏5 min样品(表4)。说明高温破坏样品对离体子宫收缩的抑制作用明显降低。
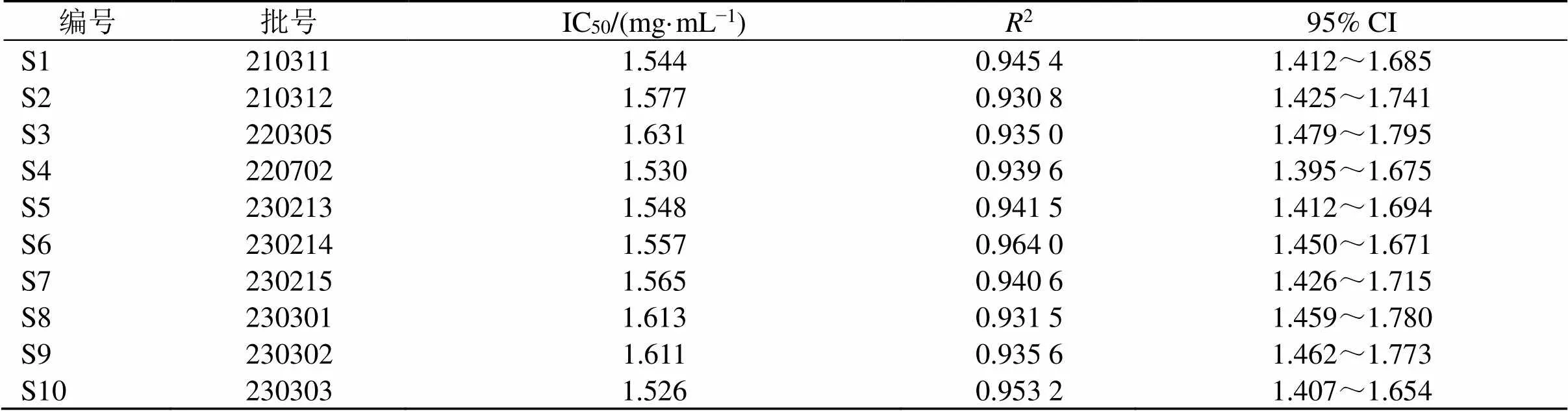
表3 不同批次桂枝茯苓胶囊的IC50(n = 8)
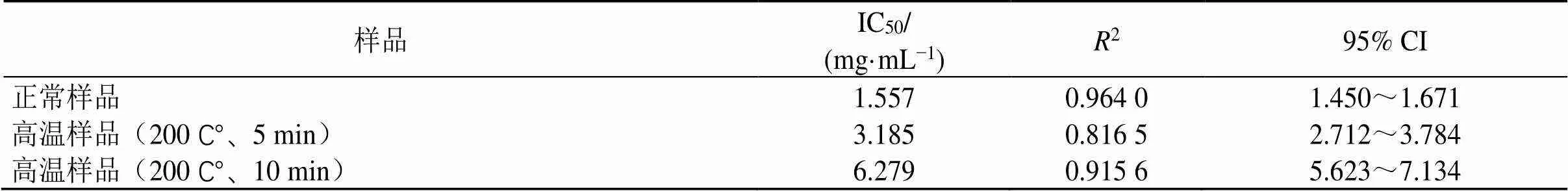
表4 正常样品与高温破坏样品的IC50 (n = 8)
4 讨论
生物活性测定作为一种用于评价药物质量的方法,主要通过使用细胞、离体组织、器官、整体动物等生物材料,测定药物的疗效或毒性[22]。它能够有效地反映中药的临床疗效和安全性[23],也可以与现行的质量控制体系相互补充[24]。
近年来不少学者,基于生物活性建立了反映中药功效与毒性、中药制剂的一致性等的评价方法,如李寒冰等[25]基于神经氨酸酶活性检测,建立了板蓝根品质的生物评价方法;张海珠等[26]进行了基于活血生物效价和化学指纹图谱的大黄品质评价研究;樊华等[27]研究了血塞通注射液活化部分凝血活酶时间(activated partial thromboplastin time,APTT)生物活性检测方法。但目前尚未见基于生物活性测定的桂枝茯苓胶囊质量评价研究。现代医学发现,原发性痛经的发病机制主要与子宫收缩异常有关。当子宫收缩过度时,子宫肌层的血液供应不足,导致缺氧和代谢产物堆积,刺激疼痛感受器,产生疼痛信号[28]。本研究基于桂枝茯苓胶囊临床治疗痛经的功效出发[29],从其抑制子宫平滑肌收缩生物活性的角度进行质量评价研究。
首先,本研究对离体子宫收缩模型的主要影响因素进行优化,通过实验确定适宜的缩宫素浓度、雌激素注射方式及注射天数、动物周龄等条件。实验结果显示,加入不同浓度的缩宫素后小鼠离体子宫收缩反应性不同,最佳质量浓度为0.050 μg/mL。当加入缩宫素浓度较低时,小鼠子宫平滑肌所受刺激较小,其峰面积较小不易统计;而浓度过高时,小鼠子宫平滑肌持续长时间痉挛性收缩,收缩节律性不佳,峰面积易下降,难以完全反映药物对子宫平滑肌的抑制作用。其次,本研究对雌激素的注射方式与注射天数进行考察,结果显示连续3 d ip雌激素后小鼠子宫平滑肌收缩峰面积较高且在1 h内收缩节律性较好。另外,不同周龄小鼠子宫平滑肌之间收缩频率与收缩幅值有所差异,但峰面积组间差异较小。为了保证实验结果的科学性,统一使用8~10周龄小鼠进行实验。
本研究利用维拉帕米对优化后的模型进行了方法学考察,结果显示该方法重复性、日内精密度和日间精密度均较好。在此基础上,还对桂枝茯苓胶囊配制浓度和超声时间等前处理条件进行优化。当桂枝茯苓胶囊配制浓度较大时其抑制子宫收缩效应不佳,可能由于药物溶解度偏低,在浴槽中加入药物后不易扩散,药效起效时间长;而配制浓度较低时,需在浴槽中加入的药液体积过多,也会影响子宫的稳定性。不同超声时间也对桂枝茯苓胶囊的药效有影响,时间过短容易造成药物溶解不充分,而时间过长可能引起药效降低。因此,本研究最终选择桂枝茯苓胶囊在0.125 g/mL质量浓度下超声60 min溶解后进行实验。
离体子宫收缩主要考察指标一般有收缩频率、收缩幅值、收缩峰面积等。在各指标中收缩峰面积变化最为明显,且组内差异较小,故本实验均采用收缩峰面积为指标进行统计。将加入缩宫素后子宫的收缩状态作为0%抑制效应,将加入阻断剂后子宫的收缩状态作为100%抑制效应,从而进行药效的归一化处理,计算桂枝茯苓胶囊抑制小鼠离体子宫收缩的IC50,作为其生物活性测定的量化指标。
根据本研究建立的离体子宫生物活性测定方法,对10个批次桂枝茯苓胶囊进行了生物活性测定,考察本方法作为桂枝茯苓胶囊质量控制标准的可行性。结果表明,10个批次桂枝茯苓胶囊的组间差异较小。而与合格批次相比,高温破坏样品对离体子宫平滑肌收缩抑制的IC50明显增大,也说明其药效和质量明显降低。综上,本研究建立了一种基于离体子宫收缩测定的生物活性评价方法,为后续桂枝茯苓胶囊的综合质量评价标准建立提供了科学依据。
利益冲突 所有作者均声明不存在利益冲突
[1] Rafique N, Al-Sheikh M H. Prevalence of menstrual problems and their association with psychological stress in young female students studying health sciences [J]., 2018, 39(1): 67-73.
[2] Wu X, Gan L, Zhang Y,. Moxibustion for primary dysmenorrhea: Protocol for a systematic review of randomized controlled trials [J]., 2020, 99(1): e18547.
[3] Ju H, Jones M, Mishra G. The prevalence and risk factors of dysmenorrhea [J]., 2014, 36: 104-113.
[4] de Sanctis V, Soliman A, Bernasconi S,. Primary dysmenorrhea in adolescents: Prevalence, impact and recent knowledge [J]., 2015, 13(2): 512-520.
[5] Woo H L, Ji H R, Pak Y K,. The efficacy and safety of acupuncture in women with primary dysmenorrhea: A systematic review and meta-analysis [J]., 2018, 97(23): e11007.
[6] Tuo L, Tang S M, Li S Y,. Murine models and research progress on dysmenorrhea [J]., 2023, 30(8): 2362-2372.
[7] 袁仁智. 基于中医传承辅助系统研究治疗原发性痛经的组方规律 [J]. 西部中医药, 2016, 29(6): 57-60.
[8] Gao J, Yang J M, Lu Z Y,. The multiple pharmacologic functions and mechanisms of action of Guizhi Fuling formulation [J]., 2022, 2022: 6813421.
[9] Wang X, Shi Y X, Xu L,. Traditional Chinese medicine prescription Guizhi Fuling Pills in the treatment of endometriosis [J]., 2021, 18(11): 2401-2408.
[10] Zhao Q L, Cheng J X, Bian X K,. Pharmacokinetics-derived absorbed components responsible for Guizhi-Fuling Capsule target PI3K/Akt-Erk to exert an anti-dysmenorrhea effect [J]., 2022, 297: 115525.
[11] 张新庄, 萧伟, 徐筱杰, 等. 基于网络药理学的桂枝茯苓胶囊治疗痛经、子宫肌瘤和盆腔炎的分子作用机制研究 [J]. 中草药, 2016, 47(1): 81-94.
[12] Chen L W, Chen H L, Yang Q W,. Guizhi Fuling Capsule inhibits uterine fibroids growth by modulating Med12-mediated Wnt/β-Catenin signaling pathway [J]., 2022, 290: 115115.
[13] Gao Y, Ji W J, Lu M,. Systemic pharmacological verification of Guizhi Fuling Decoction in treating endometriosis-associated pain [J]., 2022, 297: 115540.
[14] 王伽伯, 李会芳, 肖小河, 等. 生物检定方法控制中药质量的思考 [J]. 世界科学技术—中医药现代化, 2007, 9(6): 36-39.
[15] Jiang Y, David B, Tu P F,. Recent analytical approaches in quality control of traditional Chinese medicines: A review [J]., 2010, 657(1): 9-18.
[16] 娄天宇, 马贝贝, 王子健, 等. 活血化瘀类中药生物活性测定模型研究进展 [A] // 中国药理学会药检药理专业委员会第十六届 (2019年) 学术年会论文集[C]. 深圳: 中国药理学会药检药理专业委员会, 2019: 208-215.
[17] 李家春, 王金玲, 伍静玲, 等. 过程控制技术对桂枝茯苓胶囊质量的影响 [J]. 中国中药杂志, 2015, 40(6): 1017-1022.
[18] 王玉琴, 徐芳芳, 张欣, 等. 基于中红外光谱技术桂枝茯苓胶囊浓缩过程快速检测方法研究 [J]. 中草药, 2022, 53(16): 5026-5033.
[19] 丁玥, 曹泽彧, 柯志鹏, 等. 桂枝茯苓胶囊质量标准提升对制剂主要药效影响的研究 [J]. 中国中药杂志, 2015, 40(19): 3786-3793.
[20] 张恺, 李嵩, 邓昊, 等. 元胡止痛口服液对缩宫素致小鼠离体子宫痉挛性收缩的影响 [J]. 中成药, 2019, 41(12): 2893-2897.
[21] 华永庆, 段金廒, 王言才, 等. 小鼠离体子宫收缩模型定量药理学研究 [J]. 中国药理学通报, 2009, 25(11): 1527-1530.
[22] 马文苑, 谢媛媛, 王义明, 等. 基于生物测定方法的中药质量标准控制技术发展现状与展望 [J]. 中药与临床, 2018, 9(4): 56-62.
[23] 张萌, 封亮, 贾晓斌. 基于生物活性与效应基准的中药质量评价技术发展现状与展望 [J]. 世界中医药, 2020, 15(15): 2234-2239.
[24] 肖小河, 王伽伯, 鄢丹. 生物评价在中药质量标准化中的研究与应用 [J]. 世界科学技术—中医药现代化, 2014, 16(3): 514-518.
[25] 李寒冰, 鄢丹, 王伽伯, 等. 基于神经氨酸酶活性检测的板蓝根品质的生物评价 [J]. 药学学报, 2009, 44(2): 162-166.
[26] 张海珠, 谭鹏, 刘振杰, 等. 基于活血生物效价和化学指纹图谱的大黄品质评价研究 [J]. 药学学报, 2017, 52(3): 436-442.
[27] 樊华, 章颖慧, 康强, 等. 血塞通注射液APTT生物活性检测方法探索研究 [J]. 中国药理学通报, 2020, 36(5): 650-654.
[28] 孙兰, 李家春, 刘莉娜, 等. 散结镇痛胶囊对小鼠子宫平滑肌收缩的影响及其机制研究 [J]. 世界科学技术—中医药现代化, 2020, 22(6): 1828-1835.
[29] 段昆, 高霞, 耿婷, 等. 基于血清代谢组学技术探讨桂枝茯苓胶囊及其主要成分治疗原发性痛经的作用机制 [J]. 中国新药杂志, 2020, 29(18): 2066-2074.
Quality evaluation of Guizhi Fuling Capsules based on contractile activity assay of mouse uterine smooth muscle
JIN Yi-min1, XIE Yan1, WANG Dong-fan2, 3, ZHANG Chen-feng2, 3, CAO Liang2, 3, XIE Xue2, 3, XIAO Wei1, 2, 3, WANG Zhen-zhong1,2,3, LYU Yao-zhong2, 3
1. Nanjing University of Chinese Medicine, Nanjing 210023, China 2. National Key Laboratory on Technologies for Chinese Medicine Pharmaceutical Process Control and Intelligent Manufacture, Lianyungang 222001, China 3. Jiangsu Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China
To explore a method to evaluate the quality of Guizhi Fuling Capsules (桂枝茯苓胶囊, GZFLC) through its biological activity, which inhibits the contractile activity of uterine smooth muscle based on clinical anti-dysmenorrhea effect of GZFLC.Uterine sensitivity in mice was increased by estrogen injection, and a contraction model ofuterine smooth muscle contraction in mice induced by oxytocin was established. The contraction frequency, amplitude and peak area of uterine smooth muscle before and after administration were recorded. Peak area was used as an indicator for normalized efficacy. The main influencing factors of the contraction model such as estrogen injection method and injection days, oxytocin concentration, animal age and GZFLC pretreatment methods were investigated. After the biological activity evaluation method of GZFLC was established, the methodology was investigated. A total of 10 batches of GZFLC qualified samples and two GZFLC high-temperature destruction samples were detected for biological activity.After ip 10 mg/(kg·d) estrogen for three consecutive days, the contraction peak area of smooth muscle was higher and the contraction rhythm was better; The optimal induction concentration of oxytocin was 0.050 μg/mL; The GZFLC was configured to a concentration of 0.125 g/mL and then dissolved ultrasonically for 60 min, which was conducive to the efficacy; The repeatability RSD was 11.298%, the intraday precision RSD was 12.452%, and the interday precision RSD was 10.438%; The half inhibitory concentration (IC50) of 10 batches of GZFLC was 1.526—1.631 mg/mL, and the IC50of GZFLC was significantly increased after high temperature destruction.The quality evaluation method of GZFLC based on anti-contractive activity of uterine smooth muscle is reproducible and precise, which provides a scientific basis for the establishment of comprehensive quality evaluation criteria for GZFLC.
Guizhi Fuling Capsules; isolated uterus; smooth muscle contraction activity; bioactivity assays; quality evaluation
R285.5
A
0253 - 2670(2023)22 - 7482 - 07
10.7501/j.issn.0253-2670.2023.22.025
2023-07-24
2021年国家中医药管理局岐黄学者项目(国中医药人教函[2022]6号)
金祎敏,硕士研究生。E-mail: jinyimin1031@163.com
通信作者:王振中,研究员,硕士生导师,研究方向为中药新药研发及应用。E-mail: kyyywzz@163.com
吕耀中,高级工程师,研究方向为中药及天然药物药理毒理学。E-mail: yaozhonglv@sina.com
[责任编辑 李亚楠]