玉米芯木质素低聚物超声波辅助制备及其表征
2023-11-25刘婧伊王春鹏储富祥许玉芝
刘婧伊, 马 林, 王春鹏, 储富祥, 许玉芝
(1.中国林业科学研究院 林产化学工业研究所;江苏省生物质能源与材料重点实验室;国家林业和草原局林产化学工程重点实验室;林木生物质低碳高效利用国家工程研究中心,江苏 南京 210042;2.南京林业大学 江苏省林业资源高效加工利用协同创新中心,江苏 南京 210037)
木质素是一类具有复杂、无规则、三维网状结构的酚类聚合物。随着国家“双碳”目标的进一步明确,木质素作为天然芳香化合物的最大可再生来源,因具有易于获取、高碳含量、高热稳定性[1]等特性而逐渐成为科研工作者关注的重点。在世界上一些木材资源不那么丰富的地方,秸秆、甘蔗和竹子等非木材植物材料的利用已变得越来越重要[2],其中玉米芯作为一种价格低廉、来源广泛的农业副产物,其木质素成分在现代工业中常常得不到有效利用,造成资源浪费甚至污染环境。目前,对玉米芯-木质素研究越来越多[3-4]。天然木质素具有数均相对分子质量大[5]的特点,导致了其较大的空间位阻并降低了反应活性。同时,相对分子质量分布宽导致其均一性差,难以作为工业原料加以利用。解聚是一种高效利用木质素的重要手段,多种方法[6]均可导致木质素中较低键能的化学键断裂从而得到更易利用的低相对分子质量产物。超声波辅助解聚作为一种物理解聚方法具有绿色环保、实验条件温和、能耗低、产物选择性较高等诸多优点[7-8],其空化引起的机械性断键作用被认为是超声波解聚大分子物质的主要机理之一[9-10]。此外,超声空化效应分解溶剂体系产生羟基自由基和氢自由基[11]也同样影响木质素的解聚过程及效果。常见的超声波辅助解聚通常是在高温下直接将木质素解聚为单体[12-13]。Du等[14]在310 ℃、磷钨酸(PTA)/MCM-41做催化剂的条件下,使用超声波成功将木质素解聚为小分子的液体燃料。然而这些方法依旧需要较高的温度,能耗较高且处理价格高昂,这与将木质素这一廉价原料进行高值化利用的目的相悖。目前,常温条件下将木质素解聚为低聚物的研究还未见报道。因此,本研究将玉米芯木质素在常温溶剂体系中用超声波辅助解聚,探讨木质素常温超声波辅助解聚的较优工艺以及超声波对木质素结构的影响,以期为玉米芯木质素的高效利用提供研究基础。
1 实 验
1.1 材料与仪器
玉米芯木质素,山东圣泉有限公司,烘干至质量恒定备用,数均相对分子质量(Mn)3 000,多分散指数(PDI)2.62;氢氧化钠、硫酸、盐酸、甲醇、无水乙醇等均为分析纯,国药集团化学试剂有限公司;色谱级四氢呋喃(THF)、 2-氯-4,4,5,5-四甲基-1,3,2-二噁磷杂环(TMDP)、环己醇、乙酰丙酮铬,上海麦克林生化科技有限公司。
液晶单频超声波清洗仪(40 kHz,0~240 W),深圳市洁盟清洗设备有限公司;超声细胞粉碎仪(20 kHz,20~1 200 W),宁波新芝生物科技股份有限公司;Nicolet is10型傅里叶变换红外光谱(FT-IR)仪,美国Thermo Fisher Scientific公司;Waters 1525型凝胶渗透色谱(GPC)仪,美国Waters公司; Bruker DRX 500核磁共振波谱(NMR)仪,德国Bruker公司。
1.2 木质素的超声波辅助解聚
取玉米芯木质素10 g、溶剂100 mL,在超声波作用下反应2 h。实验中考察了6种不同的溶剂:甲醇(MeOH)、乙醇(EtOH)、甲醇-水(4∶1,体积比)、乙醇-水(4∶1,体积比)、甲醇-NaOH(4∶1,NaOH溶液中含有NaOH 2%)、甲醇-H2SO4(4∶1,H2SO4溶液中含有H2SO42%)。超声波处理结束后,溶剂中含NaOH或H2SO4的样品用稀盐酸或NaOH调节pH值为7,减压过滤后透析48 h后干燥,其他样品直接减压过滤后干燥。实验选定甲醇-水作为提取溶剂,考察了在该体系中超声波功率(60、 150、 240 W)及频率(20,40 kHz)对产物的影响,然后分别考察了溶剂中甲醇与水的体积比(9∶1、 8∶2、 7∶3、 6∶4),反应时间(1、 2、 3、 4 h),以及木质素与溶剂的固液比值(100、 200、 300、 400,g∶L)对木质素解聚结果的影响。
1.3 产物表征
1.3.1GPC分析 利用色谱纯THF将样品配制成5 g/L溶液,经0.22 μm孔隙过滤器过滤。流动相为THF溶液,流速为1 mL/min,色谱柱型号为GeneralMixed Org(300 mm×7.8 mm,5 μm),柱温30 ℃,检测系统为示差折光检测器。样品的相对分子质量根据聚苯乙烯标准物的标准曲线计算。
1.3.2FT-IR分析 利用傅里叶变换红外光谱仪以衰减全反射法对样品进行扫描,检测产物的官能团。扫描范围600~4 000 cm-1,分辨率4 cm-1,扫描次数32次。
1.3.32D-HSQC NMR测定 称取40 mg木质素溶解在0.5 mL DMSO-d6中,在核磁共振波谱仪上进行测定,温度25 ℃,测试条件:1H和13C维度的谱宽分别为5 000和20 000 Hz,扫描次数分别7 500和30 000次,1H采集点为1 024个,弛豫时间为1.5 s[15]。
1.3.431P NMR测定 称取20 mg左右的木质素试样记录质量,加入100 μL内标溶液(环己醇),随后加入氘代吡啶-氘代氯仿混合液(两者体积比1.6∶1)500 μL,充分溶解后,加入100 μL松弛剂,充分混合后,加入100 μL磷化试剂TMDP,15 min后测定[16]。
2 结果与分析
2.1 溶剂体系的选择
溶剂体系的选择是提高木质素低聚物的产率及有效分离不同相对分子质量木质素的重要因素[17],木质素低聚物的相对分子质量用GPC进行表征,结果如表1所示。甲醇溶剂体系中添加碱,样品数均相对分子质量(Mn)为4 200,不但高于纯甲醇溶剂的样品(Mn=1 200),还高于未解聚的木质素(Mn=3 000),这是因为木质素在碱作用下发生了缩合反应[18]。甲醇体系中添加酸,样品Mn=2 600,比未解聚木质素低,但比纯甲醇溶剂的样品高出一倍多,这可能是因为部分低相对分子质量的低聚木质素在酸性条件下无法溶解。在乙醇体系中加入水,木质素低聚物的产率从22.1%显著提高到69%,然而产物的多分散指数(PDI)也同时升高到3.88,均一性变差。在甲醇体系中加入水,所得木质素低聚物的Mn由1 200降低到600,同时PDI从2.71下降到1.62,提高了木质素低聚物的均一性。因此,选择甲醇-水作为后续工艺优化实验的溶剂体系。

表1 不同溶剂体系对木质素解聚的影响Table 1 Effects of different solvents on lignin depolymerization
2.2 不同超声波辅助提取条件对木质素解聚的影响
物质的质点在超声波中具有极高的运动加速度,在介质中随着波动的高速振动和剪切力的作用而降解[9]。为了探究超声波作用条件是否对木质素低聚物的产率及相对分子质量有影响,实验考察了10 g玉米芯木质素在MeOH-H2O体系中解聚时超声波功率及频率对产物的影响,结果如表2所示。在超声波频率均为40 kHz时,超声波功率从60 W增加至240 W,木质素低聚物产率从26.9%上升到34.7%,Mn从900下降到600,分布均一性增强。这是因为功率的增加导致介质获得的能量增加,更多的键在剪切力的作用下断裂。在同样的超声波功率下超声波频率由40 kHz降为20 kHz,木质素的产率略微下降,这是因为降低超声波频率后其能量虽然升高[12],但反应介质在高能量下温度急剧上升,造成溶剂的挥发。根据结果,40 kHz、 240 W为最优的超声波作用条件,后续实验均在该条件下进行。
2.3 不同反应条件对超声波解聚木质素的影响
2.3.1甲醇与水的体积比 甲醇与水的比例通过影响溶剂的极性来影响木质素低聚物的溶解度[17],进而影响低聚木质素的产率和效果,因此甲醇在溶剂体系的含量是影响木质素解聚的重要因素。甲醇与水的体积比对木质素解聚的影响见表3。由表可知,溶剂体系中甲醇比例越高,木质素低聚物产量越高,Mn和重均相对分子质量(Mw)与分散性也同时升高。这是因为高分子木质素组分在纯甲醇中溶解度高于混合溶剂。然而在V(甲醇)/V(水)由8∶2变为9∶1时,产率仅提升0.6个百分点,Mn升高22.5%,PDI升高18.0%。因此,综合比较,V(甲醇)/V(水)8∶2更适于木质素的超声波辅助解聚。

表3 不同工艺条件对木质素解聚的影响Table 3 Effects of different reaction conditions on lignin depolymerization
2.3.2超声波处理时间 过短的超声波处理时间使木质素不能充分解聚致使产率下降,过长的超声波处理时间则会造成能量的浪费,因此超声波处理时间在木质素解聚反应中同样重要。其他条件相同时,与超声波处理1 h相比,超声波处理2 h产率从25.7%提高到了34.7%,而超声波处理3 h与4 h的产率仅差5.8%,说明处理时间为3 h时,大部分木质素已解聚完成,为了减少能量浪费,选择3 h作为最合适的反应时间。
2.3.3木质素固液比 木质素的固液比同样影响解聚效率,反应体系中木质素固液比过高时,由于溶解度的限制,部分木质素低聚物不能充分溶解,造成了木质素的浪费,木质素质量分数过低时会造成试剂浪费,提取成本增加。由表3可知,将木质素固液比值(g∶L)从100提高到400会导致木质素产率先上升后下降,在200时达到最高产率40.2%。产率的上升可能是因为固液比低时解聚产生的小分子物质更多[5],再聚合生成了无法溶解的大分子,木质素固液比继续增大,但产率下降是因为产生的可溶木质素低聚物在溶剂中的浓度达到了可溶解的上限。综合比较,选择木质素固液比值200为最佳的木质素固液比。
综上,选择的工艺条件为V(甲醇)/V(水)4∶1,木质素固液比值200(g∶L),反应时间3 h,此条件下,木质素低聚物的产率为40.2%,Mn为710,PDI为1.62。
2.4 解聚产物分析

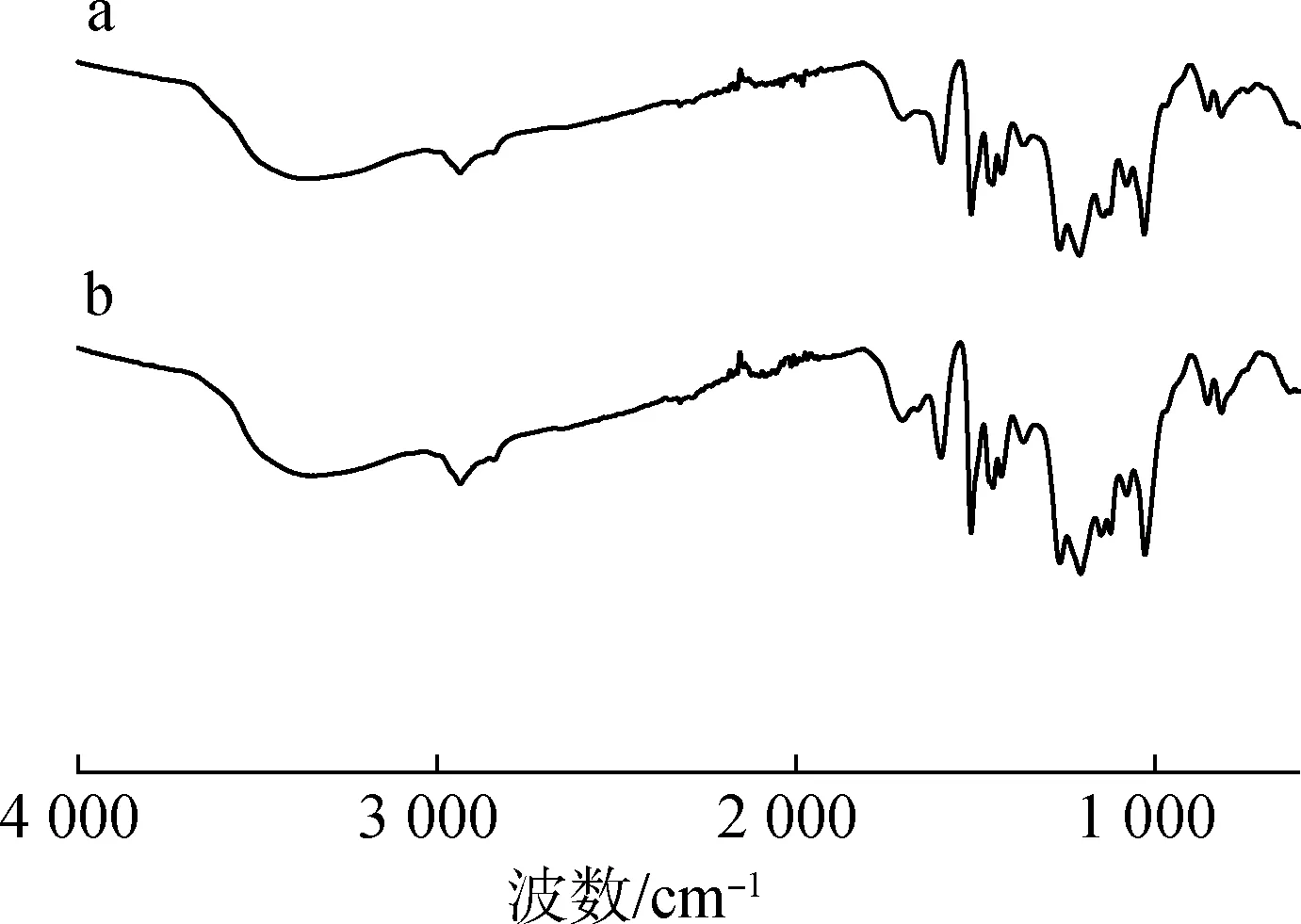
a.玉米芯木质素corn cob lignin;b.木质素低聚物lignin oligomer图1 玉米芯木质素解聚前后的红外光谱Fig.1 FT-IR spectra of corn cob lignin before and after depolymerization
2.4.22D-HSQC NMR分析 为进一步分析玉米芯木质素解聚前后的结构特点和结构单元间连接键,本研究对解聚前后的木质素进行了2D-HSQC核磁分析,其侧链区和芳香环区图谱见图2。图中主要信号的归属参考文献[15]。由侧链区谱图可观察到β-芳基醚(β-O-4)、苯香豆素(β-5)和树脂醇(β-β)键的普遍存在。解聚后δC/δH84.6/4.35位置的β-O-4信号强度降低,证明了小分子产物的增加是由于超声波作用下木质素大分子中醚键的断裂引起的。
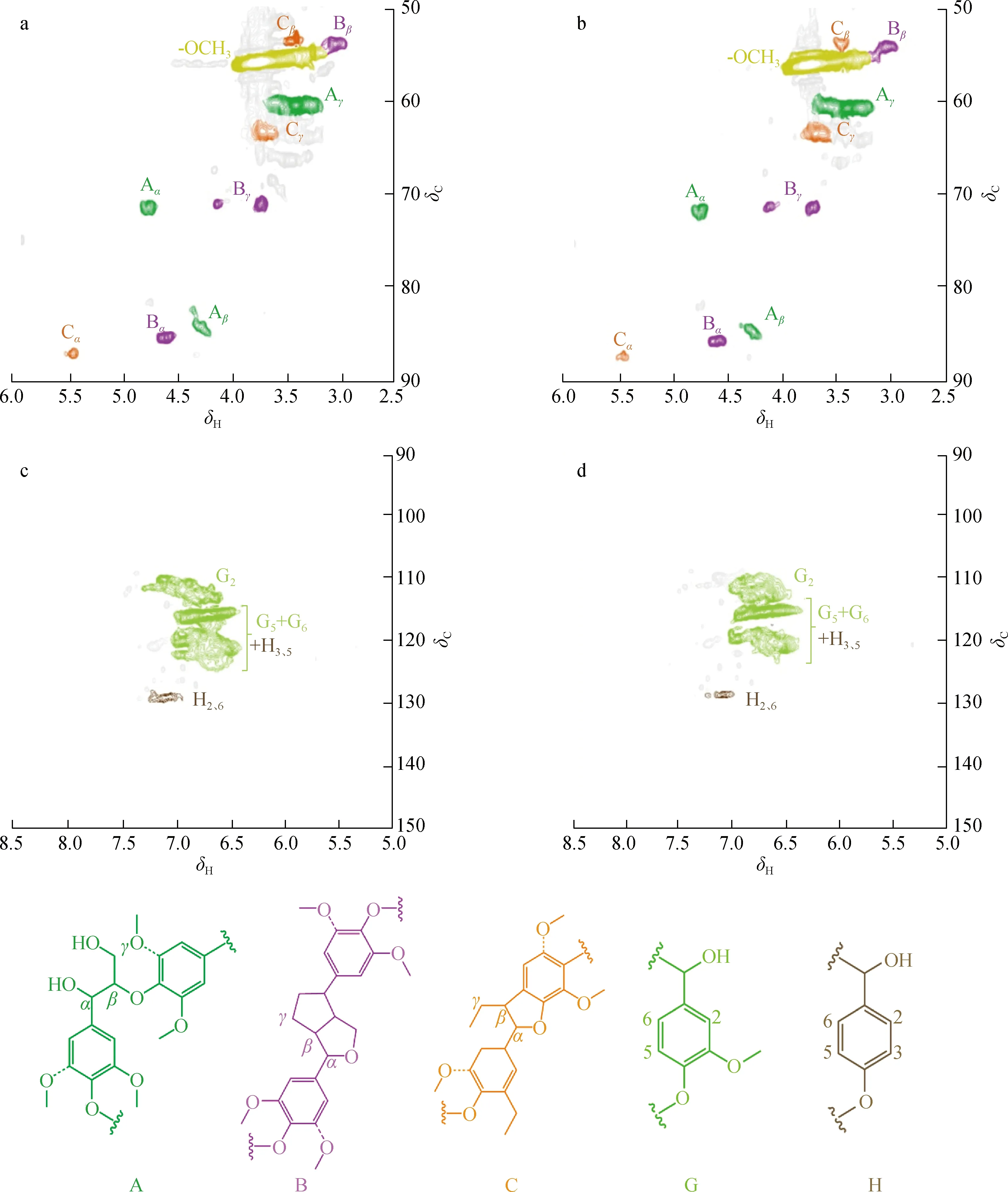
a.木质素侧链区side-chain region of lignin;b.木质素低聚物侧链区 side-chain region of oligomeric lignin;c.木质素芳香区aromatic region of lignin;d.木质素低聚物芳香区aromatic region of lignin图2 木质素解聚前后2D-HSQC图谱Fig.2 2D-HSQC spectra of corn cob lignin before and after depolymerization
在芳香区的二维谱图可观察到愈创木基(G)和对羟基苯基(H)2种结构单元信号,但木质素紫丁香基(S)结构单元的相关信号并未出现,G型结构单元2、 5、 6位的相关信号在δC/δH110.0/6.76、 115.4/6.63和120.6/6.76位置;H型结构单元3、 5位的相关信号与G型结构单元5、 6位的相关信号重合,2、 6位的相关信号在δC/δH128.0/7.01位置出现,说明玉米芯木质素中含有愈创木基及对羟基苯基结构,紫丁香基结构未检出。木质素低聚物芳香区相关信号峰与解聚前基本一致,说明常温超声波辅助解聚木质素可以有效保留木质素的基本结构。
2.4.331P NMR分析 近年来,定量核磁共振31P谱已经成为测量木质素羟基最有效的方法,可以直接测定木质素中脂肪族羟基、酚羟基等的含量[20]。用核磁磷谱分析超声波辅助解聚前后玉米芯木质素的羟基含量,结果如图3和表4所示。δ145为内标环己醇的信号峰,以其积分作为羟基定量分析的基准。δ139.5~137和144.3~139.5分别为非缩合型和缩合型酚羟基信号峰,δ148~145为脂肪族羟基信号峰[20-21], 不同羟基及其总羟基的计算结果见表4。结果表明:超声波辅助解聚产物的脂肪族羟基由解聚前的2.01 mmol/g提高到4.00 mmol/g,缩合型酚羟基由1.72 mmol/g提高到2.54 mmol/g,木质素低聚物的总羟基含量明显高于解聚前的总羟基含量,增加了36.9%,说明在超声波辅助解聚的过程中发生了部分醚键的断裂。

a.木质素lignin;b.木质素低聚物lignin oligomer图3 木质素解聚前后31P NMR图谱Fig.3 31P NMR spectra of corn cob lignin before and after depolymerization
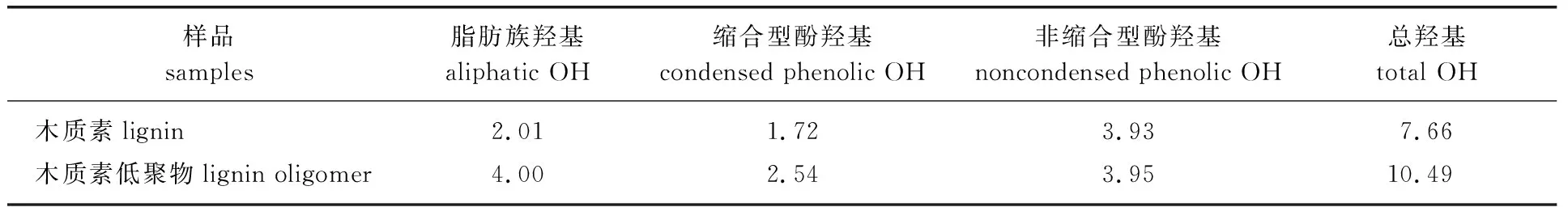
表4 解聚前后木质素中的羟基Table 4 Hydroxyl contents of corn cob lignin before and after depolymerization mmol/g
3 结 论
以玉米芯木质素为原料,采用超声波辅助解聚制备了相对分子质量较为均一的木质素低聚物,制备条件:10 g玉米芯木质素,甲醇/水(4∶1,体积比)体系,木质素与溶剂固液比200∶1(g∶L),超声波频率40 kHz, 超声波功率240 W处理3 h,所得木质素低聚物的产率达到40.2%。GPC分析表明:超声波可以促使木质素解聚,较优条件下制得木质素低聚物的数均相对分子质量(Mn) 为710,多分散指数(PDI)为1.62。FT-IR与2D-HSQC NMR的谱图显示:木质素低聚物较好保留了木质素的主要分子结构单元和官能团;31P NMR定量分析结果表明:木质素解聚后其含总羟基量增加了36.9%。
