扶正口服液联合安罗替尼治疗晚期非小细胞肺癌临床观察*
2023-11-23邓平浩
邓平浩 刘 华
中国恶性肿瘤中,肺癌发病率及其病死率明显增高,目前已经居于首位[1]。根据肺癌的分化程度、形态特征和生物学特点,目前将肺癌分为小细胞肺癌与非小细胞肺癌,其中非小细胞肺癌发生率明显高于小细胞肺癌,为80%~85%[2],多数患者确诊时已发生肺内或远处转移,不能单纯依靠手术切除等手段,需要多学科综合治疗。2个世纪以来,科学家对肺癌的探索从未停止,肺癌的治疗手段在不断增多,尽管早中期肺癌患者生存率及生活质量都显著提升,但晚期非小细胞肺癌患者的5年生存率仅15%[3]。西医治疗肺癌主要包括手术、化疗、放疗、免疫治疗及分子靶向治疗,而针对III~IV期非小细胞肺癌的分子靶向治疗,其有效率在近年来得到显著提高。在治疗III~IV期非小细胞肺癌的靶向药中,安罗替尼具有抗肿瘤血管生成和抑制肿瘤生长的作用,对于III-IV期非小细胞肺癌有值得肯定的疗效。临床试验已表明,安罗替尼可显著延长晚期非小细胞肺癌患者的无进展生存期(Progress Free Survival,PFS)和总生存期(Overall Survival,OS)[4]。扶正口服液是湖南中医药大学第一附属医院院内制剂,在改善肺癌患者症状、减轻放化疗不良反应、改善癌症恶病质等方面具有一定的客观效果,该文就扶正口服液联合安罗替尼治疗60例晚期非小细胞肺癌患者临床观察作一报道。
1 资料与方法
1.1 一般资料选择2020年1月—2022年1月湖南中医药大学第一附属医院门诊部和住院部III~IV期非小细胞肺癌患者60例。采用随机数字表法分为治疗组30例,对照组30例。其中治疗组男性13例,女性17例;年龄35~70岁,平均(54±12)岁;腺癌26例,鳞癌3例,混合型1例;驱动基因阳性者23例,驱动基因阴性者7例。对照组男性16例,女性14例;年龄42~68岁,平均(56±11)岁;腺癌25例,鳞癌3例,混合型2例;驱动基因阳性者22例,驱动基因阴性者8例。将2组患者性别、年龄、病理类型及既往治疗情况等比较,P>0.05,差异无统计学意义,具有可比性。
1.2 诊断标准经细胞学或病理学明确诊断为非小细胞肺癌,以美国癌症联合委员会(American Joint Committee on Cancer,AJCC)制定的《非小细胞肺癌TNM分期(第八版)》为依据[5],分期为III~Ⅳ期。
1.3 纳入标准①卡氏功能状态评分评分[6](Karnofsky Performance Status,KPS)大于60分;②年龄18~80岁;③无其他恶性肿瘤病史;④肝肾功能、凝血功能正常;⑤患者自愿同意参加本观察并签署知情同意书。
1.4 排除标准①妊娠期或者哺乳期妇女;②对试验用药过敏;③合并有心肺功能障碍、颅内高压、高血压病II级及以上、极度衰竭状态等疾病;④伴有精神、意识障碍,不能合作评价者;⑤存在其他安罗替尼禁忌证者。
1.5 治疗方法对照组患者给予盐酸安罗替尼胶囊(正大天晴药业集团股份有限公司国药准字H20180004,12 mg/粒)每日1次,每次1粒,晨起空腹口服。连续口服14 d,停药7 d,21 d为1个治疗周期,服用4个周期。
治疗组在对照组的基础上加用扶正口服液治疗。方药:黄芪30 g,西洋参20 g,枸杞子15 g,熟地黄15 g,何首乌15 g,白术15 g,麦冬15 g,女贞子20 g,山萸肉15 g,当归15 g,鸡血藤15 g,大枣10 g,甘草6 g。由湖南中医药大学第一附属医院药剂科制成口服液(批准文号:湘药制字Z20080456, 规格:250 ml/瓶), 每次30 ml,每天3次,安罗替尼服用间期仍继续服用。
1.6 观察指标观察安罗替尼常见不良反应如高血压病、骨髓抑制、皮疹等情况;非小细胞肺癌常见中医证候如咳嗽、咯血、胸痛、胸闷、乏力等情况。
1.7 疗效判定标准根据世界卫生组织实体瘤疗效评价标准[7],评估患者治疗后临床疗效,分为完全缓解(Complete response, CR)、部分缓解(Partial response, PR)、疾病稳定(Stable disease,SD)、疾病进展(Progressive disease, PD)。疾病控制率(Disease control rate, DCR)=(CR+PR+SD)例数/总例数×100%。生活质量评价:比较2组治疗前后KPS评分变化情况。不良反应监测:患者每日监测血压,每隔1周期复查一次血常规,观察皮疹情况。中医证候疗效评价:根据《中药新药临床研究指导原则(试行)》[8]进行系统评分,按症状的轻重程度分级,轻度为1分,中度2分,重度3分,证候积分为所有症状积分总和。
1.8 统计学方法采用SPSS 25.0软件进行处理。疾病控制率以率(%)表示,采用秩和检验;不良反应发生率以率(%)表示,采用Mann-WhitneyU检验;KPS评分采用t检验进行处理。P<0.05表示差异有统计学意义。
2 结果
2.1 2组患者临床疗效比较治疗4个周期后,治疗组临床疗效疾病控制率优于对照组,差异具有统计学意义(P<0.05)。见表1。

表1 2组患者临床疗效比较 (例,%)
2.2 2组患者KPS评分比较治疗前,2组KPS评分差异无统计学意义(P>0.05);治疗4个周期后,2组KPS评分均显著高于治疗前(P<0.05);治疗后,2组KPS评分比较,差异无统计学意义(P>0.05)。见表2。

表2 2组患者KPS评分比较 (分,
2.3 2组患者不良反应程度比较2组治疗后中性粒细胞减少程度、贫血程度优于治疗前差异具有统计学意义,治疗组较对照组而言,中性粒细胞减少、贫血程度轻,高血压病、手足皮肤反应程度比较差异无统计学意义。见表3。

表3 2组患者不良反应程度比较 (例,%)
2.4 2组患者中医证候评分比较治疗后,2组中医证候评分与治疗前比较,差异具有统计学意义,且治疗组在改善中医证候评分方面较对照组有优势。见表4。
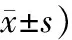
表4 2组患者中医证候评分比较 (分,
3 讨论
晚期非小细胞肺癌的治疗手段十分有限,且治疗中的不良作用让部分患者难以接受。多数患者经过了多次治疗,使得患者身心健康等方面均难以再次接受放化疗,而安罗替尼解决了这一方面的部分难题。安罗替尼是一种多靶点酪氨酸酶抑制剂,不仅对驱动基因阳性患者有肯定的疗效,对于二线治疗中基因突变阴性的晚期非小细胞肺癌也具有良好的抑制效果,且其不良反应在可控范围内[9]。同时安罗替尼也被国家卫生健康委办公厅推荐为非小细胞肺癌的三线推荐使用药物[10]。安罗替尼治疗接受过放化疗但进展后的晚期小细胞肺癌患者,可提高患者生活质量,降低肿瘤标记物水平,提升疗效,延长生存时间[11]。但是安罗替尼在临床实践中的主要问题是存在乏力、高血压病、手足皮肤反应等不良反应,以及耐药问题。
中医认为“正气存内,邪不可干”,肿瘤的发生或体内气血不足,或阴阳亏虚,以致气行受阻,或血行不畅,或寒凝经脉,或虚火内生;外有寒湿、火热、癌毒等侵袭,以致经络阻滞,津液不化,痰实凝结,日久化形,形成肿瘤;复加情志不畅、饮食不洁等因素相互影响而成。而癌症中后期患者机体多为本虚标实,中医治疗以扶正抗瘤为主。安罗替尼治疗肿瘤既攻癌毒,亦损正气,使中晚期患者正气更虚,更易出现不良反应。扶正口服液是扶正固本的补益之剂,其中药组成多为健脾补肾、益气养阴之品。晚期非小细胞肺癌患者,往往气血阴阳皆虚,故补脾以生气血,益肾以实阴阳。既往临床研究表明,扶正口服液能改善晚期肺癌患者的生活质量[12],减轻放化疗不良反应等作用[13]。本研究利用扶正口服液联合安罗替尼治疗晚期非小细胞肺癌,结果显示其能提高安罗替尼的疾病控制率,并减轻安罗替尼相关的不良反应。
本研究结果表明扶正口服液能够提高安罗替尼的疾病控制率,减轻相关不良反应,提高患者的生活质量。然而安罗替尼应用的另一大难题是耐药问题。后续值得深入研究的是扶正口服液是否可以改善安罗替尼的耐药问题,可以设计相关临床研究对此进行深入的探讨。
