实验室不符合工作与风险识别控制
2023-11-22闫顺华夏依拉·艾尼古力尼格尔·玉散江
闫顺华 夏依拉·艾尼 古力尼格尔·玉散江
摘 要:本文阐明了“实验室运行过程中发生的不符合工作即是实验室存在的风险”的观点。通过统计汇总2016年至2021年实验室发生不符合项的数量及分布情况,深入分析CNAS-CL01:2018的25个要素中的风险点,研究不符合项的分布、数量、整改措施与风险点、风险发生的概率、风险的预防之间的关系,探索降低、减小实验室风险的方法和思路,为实验室安全运行提供借鉴和参考。
关键词:实验室,不符合工作,风险识别,风险控制
DOI编码:10.3969/j.issn.1002-5944.2023.21.033
基金项目:本文受新疆维吾尔自治区食品药品监督管理局科研项目〔项目编号:新药监20220002(科)〕资助。
Non-conformity Work in Laboratory and Risk Identifi cation Control
YAN Shun-hua SHAYIRA·Aini GULINIGEER·Yusanjiang
(Institute for Drug Control of Xinjiang Uygur Autonomous Region)
Abstract: This paper elaborates the argument that the non-conformity work that occurs during the operation of the laboratory is the risk that exists in the laboratory. Through the statistical summary of the number and distribution of nonconformity occurring in the laboratory from 2016 to 2021, the paper thoroughly analyzes the risk points in the 25 elements of CNAS-CL01:2018, studies the relationship between distribution, number, corrective measures and the risk points, the probability of risk occurrence, and the prevention of risk of non-conformity items, to explore methods and ideas to reduce and avoid laboratory risks, and to provide reference for safe operation of laboratories.
Keywords: laboratory, non-conformity work, risk identifi cation, risk control
風险是指在某一特定时间段内,某种损失发生的可能性[1]。风险识别是指风险没有发生时,对潜在风险准确识别[2]。CNAS-CL01:2018《检测和校准实验室能力认可准则》[3]规定实验室应策划应对风险的措施。RB/T 214-2017《检验检测机构资质认定能力评价 检验检测机构通用要求》[4]规定检验检测机构应考虑与检验检测活动有关的风险,并策划应对这些风险的措施。通过内部审核、外部审核和日常监督检查发现检验检测工作中的不符合工作(以下称为不符合项)实际上就是实验室存在的风险点,不符合项的严重程度反映了风险的大小。
本文依据GB/T 24353-2022《风险管理 指南》[5],根据管理体系关键要素中的风险源,识别实验室运行关键要素中可能存在的风险,结合实验室运行过程中发现的不符合项及其整改过程,对风险进行有效控制,为实验室安全发展提供借鉴。
1 2016年至2021年不符合项统计分析
2016-2021年,实验室在内、外部审核和各项监督检查中发现的年度不符合项统计情况如表1所示。
1.1 不符合项数量分析
从表1可以看出,2018年发生的不符合项数量有50项,在6年之中居于首位。年度不符合项数量的多少取决于以下几方面的原因:一是与实验室运行管理的规范程度及检验任务量有关,检品数量少,检测人员的质量意识强,检验检测过程越规范,不符合项数量就会越少;检验工作量越大,实验室投入质量管理的时间相对会减少,发生不符合工作的数量可能会增加。二是与年度内、外部审核及监督检查的次数有关。每年实验室内部审核和日常监督检查的次数基本上是固定的,如果当年还有资质认定复评审、实验室认可复评审和飞行检查,实验室通常还会进行附加审核。随着内外部审核次数的增加,实验室年度不符项的数量会大大增加,表1中2018年产生的不符合项数量最多,反映的就是这种情况,因为这一年实验室分别进行了资质认定复评审、实验室认可复评审,国家对食品领域进行了飞行检查。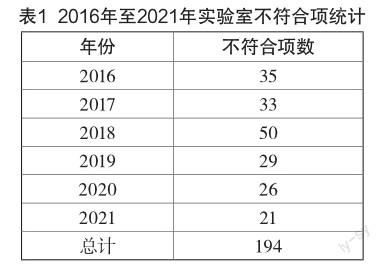
1.2 不符合项产生的趋势
从表1可以看出,除了2018年,其他年度不符合项的数量基本呈下降趋势,说明通过不断发现检验过程中的不符合项,及时采取纠正和纠正措施,实验室的管理体系得到了持续改进,不符合项的数量也越来越少。
1.3 不符合项分布
按照CNAS-CL01:2018的架构和内容要求,2016年至2021年实验室不符合项的分布情况如表2所示。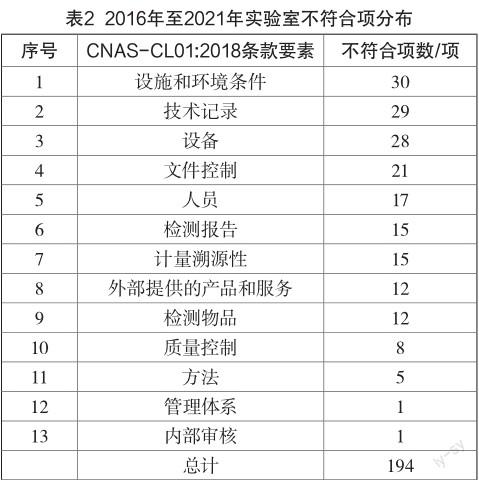
通过表2中的数据可以看出,6年来产生的不符合项主要分布在13个要素中,其中设施和环境条件、技术记录和设备发生不符合项的数量依次占到前三位,说明实验室在日常工作中要加强对这三方面工作的监督和管理;管理体系和内部审核两个条款发生不符合项的数量居于未位。
2 实验室运行过程中的风险识别
以下从CNAS-CL01:2018涵盖的6大要求、25个要素[6]系统识别实验室运行过程中可能存在的风险。
2.1 通用要求
2.1.1 公正性
实验室未要求从业人员签订公正性声明;检验人员未回避存在利益关系的活动。
2.1.2 保密性
实验室人员未签订保密协议;检测过程中客户提供的样品信息或检测结果泄露;未对大型仪器连接的检验用计算机进行加权、加密、加备管理。
2.2 结构要求
实验室组织机构框图(外部和内部)与现有职能不一致。
2.3 资源要求
2.3.1 人员
人员数量与工作量不匹配;未对授权签字人等关键岗位人员进行授权;人员监督计划内容不全面,对新上岗人员、转岗人员等未安排质量监督;未对检验检测人员的持续能力进行评价;人员技术档案缺少资格确认、专业培训等方面的材料且未及时进行更新完善。
2.3.2 设施和环境条件
未按要求对实验室的环境条件实施监控和记录;实验室未配备沙箱、灭火器等应急装置;实验用气瓶缺少安全防护措施;相互有影响的工作区域没有有效隔离[6];实验环境缺少安全警示标识和措施。
2.3.3 设备
仪器设备不按期检定/校准;检定/校准证书未进行计量确认、修正因子未能得到更新应用;仪器设备未做期间核查或维护保养;仪器设备无使用记录或记录不规范;仪器设备档案信息不全,资料不完整,未动态更新;气路未定期进行防泄漏安全检查。
2.3.4 计量溯源性
使用无证标准物质,或有证标准物质已过期;标准物质没有进行期间核查;无标准溶液的配制和标定记录;标准物质和菌种未按照说明书的要求分类贮存;未对标准物质的存储环境进行监控;校准证书中的校准点没有覆盖标准要求的使用范围。
2.3.5 外部提供的产品和服务
未建立合格供应商、服务商名录,未对二者提供的产品和服务进行评价;缺少关键试剂、耗材的符合性验收记录;试剂未进行分类、分柜存放。
2.4 过程要求
2.4.1 合同评审
检验委托书缺少委托单位、样品状态描述、检测项目、是否做符合性声明等内容;与客户沟通重要事项或关键环节未做记录;偏离、分包、删减项目未经客户同意。
2.4.2 方法
未对资质认定或实验室认可范围内的检测标准进行定期查新;未对新扩项标准或变更方法进行验证,或方法验证的内容不全面;未制定仪器设备操作规程、样品制备作业指导书等;检测方法长期偏离。
2.4.3 抽样
未按照抽样计划和抽样方法进行抽样,样品采集的代表性不强;抽样数量不足造成无法复检;抽样单信息填写不准确;封样时封条张条位置不合适,无防拆封措施;未采取适当措施保证样品运输、储藏符合标准或样品标示要求;包装运输过程防护不到位,造成损坏。
2.4.4 检测物品
没有制定样品管理作业指导书,未任命样品保管人;对于有时效性样品未及时进行检验;未对样品储存的环境条件进行监控;未对进入样品储存区的人员进行控制;检测样品无唯一性标识和检测过程中的状态标识;未规定留样样品的保存期限;未提供过期样品的处置记录。
2.4.5 技术记录
检验委托书无接收样品时的样品状态和数量;原始记录信息不充分,缺少仪器设备、标准物质、检测标准、环境条件等溯源信息;原始记录数据计算错误、数值修约不规范、更改不符合规定要求;电子数据未按要求定期备份。
2.4.6 测量不确定度
测量不确定度评定没有覆盖实验室新扩项目及参数;未对临界值进行不确定度的评估导致错误的结论。
2.4.7 质量控制
质量监控计划缺少结果判定依据及超限时采取的措施;日常检验检测工作中,未采取相应的内部质量控制措施;未对超标结果进行OOS分析;能力验证活动未覆盖资质认定或实验室认可范围的所有领域;参加能力验证活动的频次不满足要求;对能力验证的不满意结果或离群结果没有措施记录。
2.4.8 检测报告
检测报告超范围加盖CMA或CNAS章;授权签字人超范围签发报告;结果未检出,报告未提供检出限;含分包项目的检验报告缺少分包方的的名称和资质认定许可编号;检驗报告缺少免责声明。
2.4.9 投诉
缺少客户满意度调查;未对客户的反馈意见进行统计分析,并提出改进措施;处理客户投诉未采取回避措施。
2.4.10 不符合工作
对不符合工作事实的描述不具体,无法进行整改;不符合报告未对不符合项产生的原因、严重性和可接受性进行分析。
2.5 管理体系要求
2.5.1 体系文件
质量方针缺少持续改进管理体系有效性的承诺[7];管理体系文件没有涵盖CNAS的最新要求,或引用的文件不是最新版本。
2.5.2 文件控制
实验室未对体系文件进行定期审核和修订,未能体现文件当前修订状态和修订内容;受控文件管理不规范,存在使用作废无效版本情况;未能提供分类明确、内容完整的内、外部受控文件目录;未对检测标准实施标识、发放、查新等有效控制;未对需要保留的作废文件作适当的标记。
2.5.3 内部审核
未制定年度内部审核计划;内审计划审核内容不具体、未覆盖管理体系的所有要素和部门;对内审中发现的不符合项采取的纠正措施未经验证;
2.5.4 管理评审
管理评审输入与输出内容不全面,对工作状况分析不到位,无评审结论;未对管理体系的适宜性、有效性等做出评价和决定[8];提出的改进措施缺少落实计划、实施记录和验证记录。
2.6 其他要求
实验室发生重大变化不及时通知CNAS[9], 如法人、组织机构、地址、关键技术人员等变动时未提交书面变更申请;超范围使用认可标识,涉及的报告数量较大等。
3 内、外审不符合项与实验室风险识别分析
3.1 不符合项的发现、整改与风险的识别、控制
从表2可以看出,通用要求、结构要求和其他要求均没有发生不符合工作,说明这3个要求中的要素不易产生风险。管理体系要求的4个要素中有3个要素发生了23项不符合工作,资源要求中的5个要素全部发生了不符合工作,总计有102项,过程要求的10个要素中有5个要素发生了不符合项,总计有54项。说明资源要求、过程要求和管理体系要求中的要素容易发生风险。
通过分析,可以看出CNAS-CL01:2018中的25個关键要素都存在风险(即不符合项),但在内、外部审核和各种监督检查中,经常发现的不符合项,即风险,只占到了其中的13个要素,说明这13个要素是风险的高发点,在日常工作中要注重加强监督管理和检查。对没有发现不符合工作的另外12个要素,没有开具不符合项,一方面是有些要素实验室确实做的比较到位,如日常检验检测工作中的质量控制、测量不确定度评定、实验室的公正性和保密性等不存在明显的问题;另一方面是有些要素的不符合工作不易被发现,如抽样。通过对25个要素易出现风险的识别,能够对实验室可能产生的不符合项(即风险)进行全面把控,在内、外部审核和监督检查中对其进行重点关注;通过对不符合项产生的原因进行分析并采取纠正措施进行改正,又能够对实验室的风险进行有效管理,使风险消除或降低至可控范围内,二者相辅相成。
实验室每年对本年度内发现的不符合项进行汇总,分析各不符合项发生的原因、已经采取的纠正措施、整改完成情况及跟踪验证结果,形成实验室年度风险评估报告。
3.2 不符合项的严重程度与风险的大小
根据不符合项对实验室能力和管理体系运作的影响,不符合项又分为严重不符合项和一般不符合项[10]。2016年至2021年实验室发生的194项不符合工作均为一般不符合项,通过分析原因,及时采取纠正措施,全部完成了整改并通过验证。一般不符合项产生的风险是可接受的,可以通过不断采取纠正和纠正措施得到持续改正,对不符合项进行整改的过程就是对实验室的风险进行控制的过程。
严重不符合项产生的风险会影响实验室的运行甚至可能造成停止运行,如存在出具不实检验检测报告或虚假报告的实验室,会有被撤销、吊销、取消其检验检测资质证书[11]的风险;又如实验人员操作不当,发生安全事故,造成人员伤害、设备设施损坏,导致实验室无法运行等。对于严重不符合项可能造成的的重大风险,实验室应进行重点分析、评估,并采取有针对性的风险控制预防措施,防止风险的发生。
3.3 预防措施与风险的防控
实验室应识别潜在不符合工作的原因和所需的改进,并采取预防措施,以减少不符合情况的发生。预防措施是事先主动识别风险的过程,而不是对已发现问题的反应。如实验室定期对标准进行查新并及时下发标准查新清单,预防检验人员使用作废标准;监督检查中发现实验室化学试剂较多,存在潜在安全隐患,采取增加沙箱、灭火器、灭火毯数量的预防措施等。
对大多数实验室来说,内部审核一般一年1次,外部审核不是每年都有,质量监督检查的频率可由实验室自己制定。实验室在运行过程中,执行院(所)级和科室两级监督检查,院(所)级质量监督由质量管理部门组织实施,每月至少组织实施1次,重点检查实验室水暖电气的使用与安全、试剂耗材验收、人员健康防护、实验操作、仪器设备使用、标签标识、内务情况等,对检查中发现的问题责成相关科室进行整改,并对整改情况进行跟踪检查。科室监督检查由科室质量监督员对检验的全过程进行监督,并重点加强对新上岗人员、转岗人员、新扩实验项目、能力验证活动等实验过程的监督。通过加强质量监督检查,对发现的问题及时进行改进[12],可有效预防风险的发生。
4 结 语
本文统计汇总了2016年至2021年实验室发生不符合项的数量及分布情况,深入分析了CNASCL01:2018的25个要素中的风险点,阐明了实验室运行过程中发生的不符合工作(不符合项)即是实验室存在的风险的论点,研究了不符合项的发现、整改与风险的识别控制、不符合项的严重程度与风险的大小、预防措施与风险的防控之间的关系,探索降低、减小实验室风险的方法和思路,为实验室安全运行提供借鉴和参考。
参考文献
[1]刘莉.第三方检测实验室质量风险管理研究[J].质量安全与检验检测,2020,30(5):94-96.
[2]王辉,张全军,罗季阳.海关实验室的风险识别与控制对策研究[J].口岸卫生控制,2022,27(1):48-50.
[3]苑艳飞,刘广文.药品检验检测机构开展能力验证的质量控制要点[J].质量安全与检验检测,2021,31(4):94-96.
[4]检测和校准实验室能力认可准则: CNAS-CL01:2018[S].
[5]检验检测机构资质认定能力评价检验检测机构通用要求:RB/T 214-2017[S].
[6]风险管理 指南:GB/T 24353-2022[S].
[7]邵先涛,沈鹏,张建生.环境检测实验室风险管理的探讨[J].能源环境保护,2021,35(4):92-95.
[8]徐雪梅,续艳丽,周斌,等.基于检验过程管理的食品药品检测实验室风险评估和控制[J].食品安全质量检测学报,2020,21(11):8079-8085.
[9]王正,赵榕,罗仁才,等.疾控机构食品理化检验实验室安全和质量风险识别与控制[J].首都公共卫生,2021,15(2):108-110.
[10]曾文珊,韩莹.药品检验所差错报告书情况分析及风险控制的探讨[J].中国药事,2017,31(11):1285-1288.
[11]黄瑛,徐永安,何晟煜.以风险思维管理食品检测实验室[J].食品安全质量检测学报,2020,11(18):6303-6310.
[12]闫顺华,马国明,王秀霞,等.2013-2019年实验室能力验证结果不满意OOS分析[J].中国药事,2020,34(10):1158-1164.
作者简介
闫顺华, 硕士,高级工程师,主要从事食品药品检验检测技术研究工作。
(责任编辑:张瑞洋)
