3, 5-二氯硝基苯在乙腈溶液中电化学还原机制研究
2023-11-20金葆康
刘 岩,金葆康
(安徽大学 化学化工学院,安徽 合肥 230601)
目前,全世界CO2的排放量每年约为400亿吨,在未来仍将有所增长.然而,只有一小部分CO2被捕获和利用,导致大气中CO2浓度不断增加,威胁着环境安全和人们健康[1-2].减少化石燃料的使用,降低CO2排放,开发绿色可持续的方法来减少大气中CO2的浓度成为研究热点.
而3,5-二氯硝基苯(3,5-DCNB)是一种对皮肤和黏膜有显著刺激作用,能引起人体血液中毒和损伤肝脏、肾脏,同时损害神经以致发生神经痛、神经炎等的有毒化合物,具有寿命长、化学稳定性好、不可生物降解等特点,多年来已成为严重的环境问题[3-4].这类化合物自然形成极其罕见,它们在环境中的存在是由于大规模的工业生产造成的.因此,如何快速可靠地消除这类物质已经成为越来越多研究者们关注的问题.现有的去除这类物质的方法可分为3大类:物理、化学和生物方法[5-7].其中,最常用的方法是物理吸附法,它通常被认为是去除有机污染物最有效、低成本和更方便的方法[8-10].有机电化学采用电子作为“清洁”试剂,可以大大减少废物的产生,并可以避免有害试剂的使用,被认为是一种绿色和可行的工具.
1 实验部分
1.1 试 剂
3,5-二氯硝基苯(3,5-DCNB 98%),购自阿拉丁上海发展有限公司;四乙基四氟硼酸铵(TEABF4)纯度为97%,购自毕得医药科技股份有限公司.高纯度的CO2和N2(99.999%)购自南京特种气体有限公司,直接用于电化学反应.
1.2 循环伏安实验
循环伏安实验的工作电极为直径2 mm的Au圆盘电极,每次使用前在抛光布上抛光,然后在超声波清洗器中用去离子水冲洗,最后用N2吹干.准参比电极为Ag/AgCl,辅助电极为铂丝.实验时,将3,5-二氯硝基苯溶解在含有0.2 mol·L-1TEABF4的乙腈(AN)中,然后将溶液平均分成两部分,其中一部分用高纯度N2匀速通气60 min得到除去残留O2和CO2的N2饱和溶液,另一部分先用高纯度N2通气30 min,然后用高纯度CO2匀速通气30 min得到饱和CO2溶液.
1.3 原位FT-IR光谱电化学实验
采用自制的薄层光谱电化学池,以直径4 mm的Ag圆盘为工作电极,Pt丝为辅助电极,Ag/AgCl为准参比电极,进行所有的原位FT-IR光谱实验.在循环伏安(CV)实验中,每张红外光谱采集32张干涉图,采样间隔为1.45 s,在计时安培(CA)实验中,每张红外光谱采集8张干涉图,采样间隔为0.21 s,红外光谱的分辨率为16 cm-1.最后,利用Grams/3D软件对实验结果进行处理.
1.4 整体电解
电解实验以金(10 mm×10 mm×0.2 mm)、铂(10 mm×10 mm×0.2 mm)片和Ag+/Ag(0.1 mol·L-1)电极作为工作、辅助和参比电极.在-1.6V的电解电位下持续电解16 h,电解全程持续不断通入CO2.电解结束后,将电解池静置,随后阴极室逐渐析出黄色固体.将阴极室溶液转移至蒸馏烧瓶中旋转蒸发以除去AN,然后向蒸馏烧瓶中加水,产生黄色沉淀(3,3′,5,5′-四氯偶氮苯),过滤将沉淀与溶液分离开来,并将沉淀溶于有机溶剂二氯甲烷中.采用纯石油醚作为洗脱剂进行柱色谱实验,分离并收集黄色物质(3,3′,5,5′-四氯偶氮苯).
1.5 化合物的结构测定方法
通过旋转蒸发和在11 000 r·min-1离心5 min得到粗品.沉淀物用过量的石油醚洗涤,并通过离心法收集.室温下在纯石油醚溶液中结晶,3 d后得到适合X射线分析的黄色单晶结构.在Stoe Stadivari衍射仪上进行单晶X射线衍射数据采集.
2 结果与讨论
2.1 3,5-DCNB在AN溶液中的电化学行为
图1为 2 mmol·L-13,5-DCNB在0.2 mol·L-1TEABF4的AN中的CV曲线,扫描的电位范围为-0.4~-1.2 V,扫速为10 mV·s-1.其中红色线是3,5-DCNB在饱和CO2溶液中的CV曲线,蓝色线是饱和N2条件下的CV;黑色线是在不含反应物3,5-DCNB情况下饱和CO2的CV曲线.

图1 2 mmol·L-1 3,5-DCNB在0.2 mol·L-1 TEABF4的AN中的CV曲线,扫速为10 mV·s-1
从图1可以看出,在-0.85 V附近仍可以观察到1个小的还原峰,这可能是电解质阳离子的还原[11].图1还显示,3,5-DCNB在N2条件下有1对明显的氧化还原峰,可当通入CO2后,还原峰峰电流显著增加,且氧化峰消失,表明当质子惰性溶剂AN中引入CO2时,CO2可能参与了3,5-DCNB的电化学还原反应.
2.2 3,5-DCNB在N2条件下的电化学研究
图2(a)为在-0.4 V至-1.2 V电位范围内10 mmol·L-13,5-DCNB在AN溶液中进行的CV扫描,扫速为10 mV·s-1.在此范围内,可以观察到一对峰形良好的氧化还原峰,还原峰电位为-0.95 V,氧化峰电位为-0.80 V.图2(b)为相对应的3D现场红外光谱图,图中的红外吸收峰可分为两大类:负向峰(1 540 cm-1和1 348 cm-1)和正向峰(1 325 cm-1和1 256 cm-1).其中负向峰1 540 cm-1和1 348 cm-1分别归属于3,5-DCNB的-NO2的不对称伸缩振动和对称伸缩振动[12],用来追踪反应物3,5-DCNB浓度的变化;正向峰1 325 cm-1和1 256 cm-1分别归属于 3,5-DCNB·-苯环的伸缩振动和 C—N 伸缩振动[13],可以用来代表反应过程中3,5-DCNB·-的浓度变化.3,5-DCNB在电化学过程中的各红外吸收峰归属汇总在表1.

表1 电化学还原过程中的红外吸收峰的分布情况
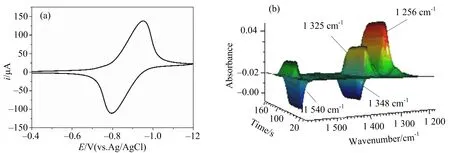
图2 10 mmol·L-1 3,5-DCNB在0.2 mol·L-1 TEABF4的AN溶液中的薄层CV曲线(a) 及相对应的 3D 红外光谱图(b),扫速10 mV·s-1
为了更加清晰地了解3,5-DCNB的电化学还原机制,对3D红外图中红外吸收峰进行处理得到了相对应的循环伏吸(CVA)图(图3(a)).分别用1 540 cm-1和1 325 cm-1表示电化学过程中3,5-DCNB和3,5-DCNB·-的浓度变化.

图3 在N2条件下,3,5-DCNB在1 325 cm-1和1 540 cm-1处的吸收峰对应的CVA(a)和DCVA(b)
图3(b)是将图3(a)中指定物质波数的吸光度值进行一阶求导所得到的导数循环伏吸图(DCVA).
由图3(a)可知,在还原过程中,1 540 cm-1处的负向峰呈现先减小后增大的趋势,在约40 s时开始下降,约70 s时至最低点;1 325 cm-1处的正向特征吸收峰则呈现先增大后减小的趋势,在约40 s时逐渐升高,约70 s时达到最高点.2个物种的特征吸收峰变化趋势同步,表明3,5-DCNB得电子被还原为3,5-DCNB·-.而在氧化过程中,2个红外特征吸收峰变化正好与还原过程相反.当电位回到初始值-0.4 V时,特征吸收峰吸光度值恢复到初始值,表明3,5-DCNB·-失电子且全部被氧化为3,5-DCNB.以上结果表明, N2条件下,3,5-DCNB的电化学还原反应是可逆的一步单电子转移过程.从图3(b)中可以看出,1 325 cm-1和1 540 cm-1的DCVA曲线形状表现为1对氧化还原峰,这与电化学的CV曲线一致,进一步说明3,5-DCNB为可逆的一步单电子转移过程.
在N2存在下,不同扫速的循环伏安扫描结果如图4(a)所示.图4(b)为不同扫速下还原峰峰值电流与扫描速率的关系曲线.
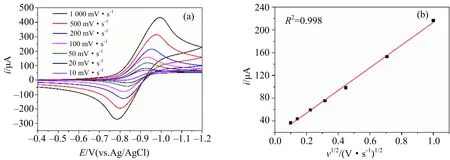
图4 5 mmol·L-1 3,5-DCNB在0.2 mol·L-1 TEABF4的AN中,不同扫速下的CV(a);在N2条件下还原峰峰值电流与扫速的关系(b)
由图4(a)可知,随着扫速的不断增大,峰电位基本保持不变,峰电流逐渐增大.图4(b)中Ipc值与υ1/2呈现良好的线性关系,这是典型的可逆反应的特征,说明3,5-DCNB从溶液到电极表面的扩散控制在阴极还原过程中起主导作用.
此外,考察了10 mmol·L-13,5-DCNB在AN中3个连续循环的循环伏安扫描,得到了相应的3D光谱(图5(a))和CVA曲线(图5(b)).采用25 μm直径Au电极做工作电极得到了LSV曲线,如图5(c)所示.
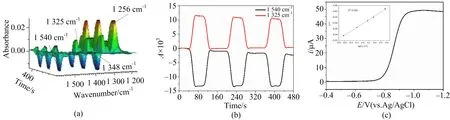
图5 10 mmol·L-1 3,5-DCNB在含有0.2 mol·L-1 TEABF4的AN中的3个连续循环薄层CV图(扫描速率10 mV·s-1)(a),相对应的CVA图(b),在25 μm Au圆盘工作电极上的LSV(c)以及E和lg[(id-i)/i]的关系图(c中插图)
从图5(a)~(b)可以看出,第1个循环和CVA曲线的形状与第2和第3个循环基本一致,表明在AN中3,5-DCNB的电化学行为是化学可逆的.由图5(c)的LSV曲线得到了E与lg[(id-i)/i]的线性关系,其线性方程为y=-0.86+0.056*x,通过斜率可知,其电子转移数为1.由此可确定,3,5-DCNB在AN溶液中的电化学行为为一步单电子转移机制,即3,5-DCNB +e3,5-DCNB·-.
2.3 3,5-DCNB在CO2条件下的电化学研究
图6(a)为-0.4 V到-1.2 V的电位范围内10 mmol·L-13,5-DCNB在AN溶液中的CV图,图6(b)是相应的3D红外图,图6(c)为图6(b)对应的CVA图.
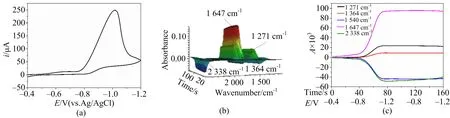
图6 10 mmol·L-1 3,5-DCNB在CO2存在下的0.2 mol·L-1 TEABF4的AN溶液中的薄层池CV(a)及相对应的3D红外光谱图(b),扫速为10 mV·s-1;3,5-DCNB在1 271,1 364,1 540,1 647,2 338 cm-1处的CVA(c)


为了确定3,5-DCNB的电化学过程电子转移数,对3,5-DCNB在N2和CO2条件下的CV扫描中的还原过程进行了电量积分.如前所述,N2条件下为单电子转移过程,CO2条件下转移的电子数Z可以根据法拉第公式(1)进行计算
Q=nFZ=it,
(1)
其中:Q为电量,单位C;n为反应物的物质的量;i为电流,单位A;t为反应进行的时间,单位s;F为法拉第常数(96 500 C·mol-1).
N2和CO2条件下的电量积分结果如表2所示.
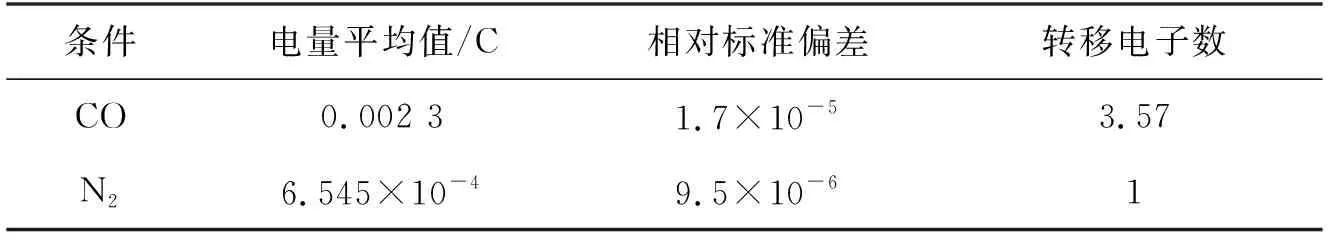
表2 反应过程的电量及电子转移数(n=3)
由表2的电量积分结果可知,N2条件下,3,5-DCNB在AN中的反应是1电子可逆过程,在CO2条件下相同浓度的3,5-DCNB的电化学过程近似为1个4电子过程.
为了进一步探究CO2存在下3,5-DCNB电化学还原机制,开展了CA(图7(a))及3D红外光谱快速扫描(图7(b))实验.在图7(b)中同样观察到5个特征吸收峰:1 271,1 364,1 540,1 647,2 338 cm-1.图7(c)和图7(d)分别为图7(b)相应的CAA图和DCAA图.
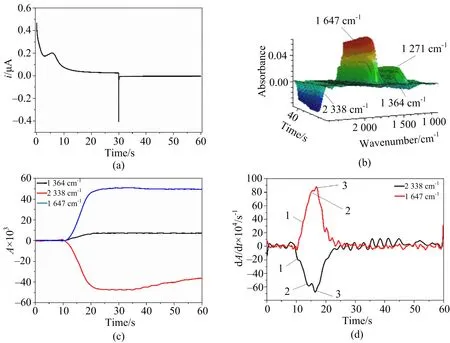
图7 10 mmol·L-1 3,5-DCNB在含0.2 mol·L-1 TEABF4的AN中的薄层CA(a),双电位阶跃从-0.4到-1.2 V及相应的3D红外光谱图(b),扫描速率10 mV·s-1,3,5-DCNB在1 647, 1 364, 2 338 cm-1的CAA(c)和DCAA(d)图
由图7(c)可以看出,不同波数特征吸收峰随时间的变化趋势与之前的CV所对应的CVA曲线一致.图7(d)显示,CO2的特征吸收峰2 338 cm-1呈现出3次变化,表明在CO2的存在下3,5-DCNB电还原过程中,CO2参与了3个步骤的反应.从图7(c)可以看出,不同波数特征吸收峰随时间的变化趋势与之前的CV所对应的CVA曲线一致.图7(d)显示,CO2的特征吸收峰2 338 cm-1呈现出3次变化,表明在CO2的存在下3,5-DCNB电还原过程中,CO2参与了3个步骤的反应.
此外,在CO2的存在下,对50 mL的10 mmol·L-13,5-DCNB在-1.6 V vs.Ag/Ag+进行了整体电解研究,得到lgi(t)与t的曲线,如图8所示.通过用公式(2)~(3)计算的理论法拉第电解效率,得出3,5-DCNB的法拉第效率为78.5%.

图8 在CO2存在下,50 mL 10 mmol·L-1 3,5-DCNB在-1.6 V vs. Ag/Ag+下的恒电位电解过程中lgi(t)和t的关系
(2)
(3)
其中:i(t)为电解电流(A);i0为初始电流(A);p=m0A/V,m0为传质系数(cm·s-1),A为电极面积(cm2),V为溶液总体积(cm3);Q(t)为电量(C);t为反应时间(s).
2.4 3,5-DCNB在CO2存在下的电化学还原产物的结构分析
将电解产物溶解在纯石油醚中,缓慢挥发3 d,最后得到黄色的晶体.然后用X射线单晶衍射仪(Stoe Stadivari)测定了该产物的单晶结构(图9),所得晶体学数据列于表3.NMR的分析也与相应的最终产品相同.C12H6Cl4N2:1H NMR (400 MHz, chloroform-d)δ7.25~7.12 (m,2H), 7.00~6.98 (m,4H), 6.82~6.81 (m, 2H);13C NMR (400 MHz, chloroform-d)δ155.58, 129.71,128.18,127.12, 126.77,118.80.

表3 化合物3,3′,5,5′-四氯偶氮苯的晶体学数据
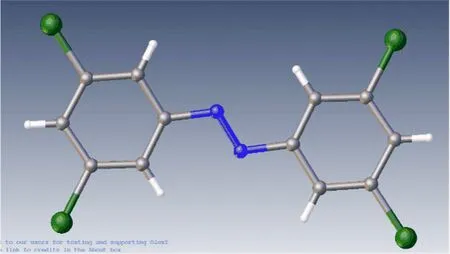
图9 3,3′,5,5′-四氯偶氮苯的X射线单晶衍射结构

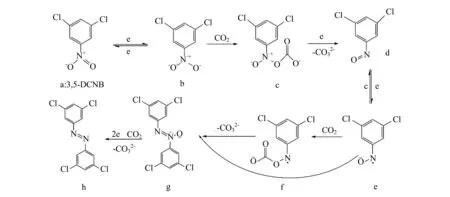
方案1 3,5-DCNB在含有CO2的AN中的电化学还原过程
3 结束语

