CEUS联合MRI增强扫描早期评价射频消融治疗原发性肝癌患者疗效研究*
2023-11-18刘思宏谢琉嘉周志明许亚春
刘思宏,谢琉嘉,周志明,许亚春
由于原发性肝癌(PLC)发病隐匿,大多患者诊断时病情已发展为晚期,手术不可切除,综合治疗效果差[1]。射频消融(RFA)是通过等离子震荡产生热量,对肝癌细胞造成不可逆的生物学损害,从而达到治疗的目的[2,3]。然而,RFA治疗后仍有病灶残留的可能,残存病灶仍有侵袭和转移的风险,因此在RFA治疗后早期对残存病灶进行筛查和评估具有重要的意义。目前,评价RFA疗效的方法较多,如血管造影、CT增强扫描、超声造影(contrast enhanced ultrasound,CEUS)、磁共振成像(magnetic resonance imaging,MRI)等[4,5]。CEUS具有经济、操作便捷、无辐射等优势,在评价肝癌治疗后的疗效方面越来越受到重视[6]。目前,已有研究探讨了采用CEUS和MRI增强评估治疗PLC的效果。本研究采用RFA治疗PLC患者,探讨了CEUS联合MRI增强扫描评价治疗效果的价值,现报道如下。
1 资料与方法
1.1 一般资料 2019年1月~2022年1月我院诊治的PLC患者81例,男性54例,女性27例;年龄为33~71岁,平均年龄为(53.6±7.9)岁。诊断参照《原发性肝癌规范化病理诊断指南》[7]。纳入患者均为肝内单发病灶,Child A/B级。排除标准:(1)合并心脑血管疾病;(2)合并肝性脑病或顽固性腹水;(3)治疗前已发生肝外肿瘤转移。患者及其家属签署知情同意书,本研究经我院医学伦理委员会批准(伦理批号:2019-06号)。
1.2 RFA治疗 使用德国西门子公司生产的SOMATOM Definition AS+64排128层4D螺旋CT、美国通用电气公司生产的LOGIQE E9型彩色多普勒超声诊断仪和SC6U-1探头和上海寰熙医疗器械有限公司提供的LDRF-120S多极射频消融仪。术前,行血常规、肝功能和凝血功能检查。全身麻醉,患者取仰卧位,经超声实时引导,明确肿瘤大小、回声和周围重要的解剖结构。经超声引导确定进针入路并选择穿刺点,常规消毒、铺巾。在超声引导下向肿瘤组织内刺入消融针,调整方向并确认无误,确保有效消融体积可覆盖至肿瘤边缘1 cm,之后进行热消融。根据病灶位置和大小,确定射频消融次数,保证总体覆盖范围满意。在射频消融后,行影像学检查,对消融边缘仍有异常强化灶者,则补充消融治疗。在手术过程中,全程监测心电图,密切关注生命体征变化。
1.3 影像学检查 使用彩色多普勒超声诊断仪进行CEUS检查,探头频率为3~5 MHz。首先,常规超声检查病灶形态、大小和位置。选择最佳扫描位置切面,进行CEUS检查。将探头固定,注射造影剂(声诺维,国药准字J20080052)后,观察病灶血流分布和造影剂灌注情况,记录5~7 min造影图像并将其储存于超声工作站;使用美国通用电气公司生产的Discovery 750 MR扫描系统,先行常规扫描,之后给予钆喷酸葡胺(北京北陆药业股份有限公司,国药准字H10960045)0. 2 ml.kg-1静脉注射,进行MR增强扫描。
1.4 疗效评价方法 经CEUS检查,3期均无对比剂填充提示肿瘤被灭活,肿瘤存活为动脉期和门静脉期显示病灶内出现等回声、高回声,或肝实质期病灶呈现为低回声;经MRI增强扫描检查,3期内病灶均无强化效应,DWI信号降低,提示肿瘤灭活。若动脉期存在病灶强化,门静脉期或延迟期显示强化效应降低,DWI显示高信号,提示肿瘤残存;经CEUS和MRI增强扫描检查,任何一种检查判定为残存病灶时,则为阳性病灶残存,两种检查方法都判定为病灶被完全灭活时,判定为阴性。以DSA检查为金标准,应用Kappa分析CEUS联合MRI增强扫描评价RFA治疗效果的效能。

2 结果
2.1 CEUS与DSA评价RFA治疗效果的一致性情况 在治疗后1个月,经CEUS检查并与DSA检查行一致性分析,其判定病灶残存或完全灭活的效能较高(表1、表2和图1)。
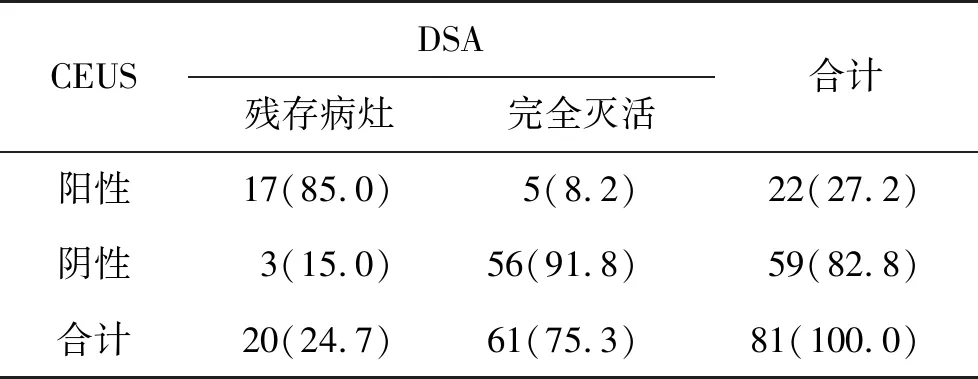
表1 CEUS与DSA评价RFA治疗效果一致性情况
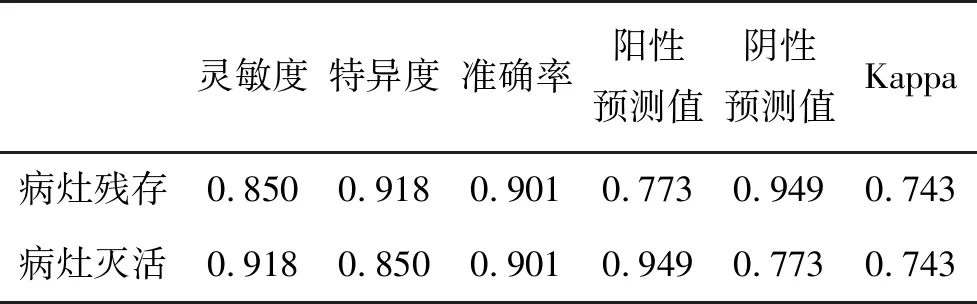
表2 CEUS评估RFA治疗效果的效能
2.2 MRI增强扫描与DSA评价RFA治疗PLC病灶效果的一致性情况 经MRI增强扫描显示,其评价RFA治疗疗效的效能与DSA评价具有较高的一致性(表3、表4、图2)。
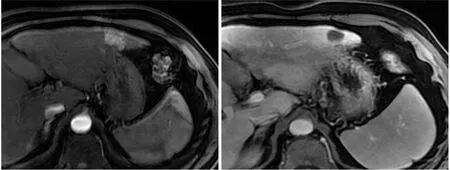
图2 PLC患者腹部MRI增强扫描表现 在RFA治疗后,MRI增强扫描动脉期(左)和门静脉期(右)显示病灶被灭活
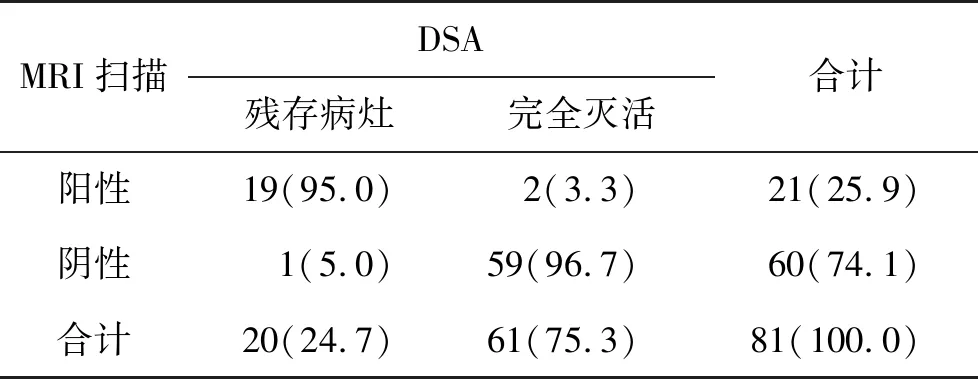
表3 MRI增强扫描与DSA评价RFA治疗效果的一致性情况

表4 MRI增强扫描评估RFA治疗效果的效能
2.3 CEUS联合MRI增强扫描与DSA评价RFA治疗效果的一致性 CEUS联合MRI增强扫描与DSA评价RFA治疗PLC患者的疗效具有更高的一致性(表5、表6)。

表5 CEUS联合MRI增强扫描与DSA评价RFA治疗效果的一致性
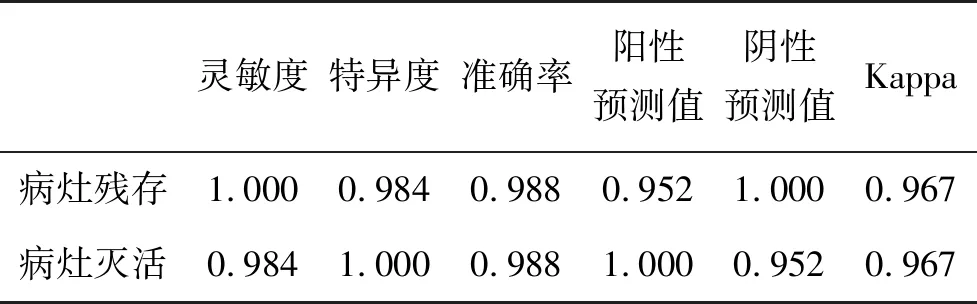
表6 CEUS联合MRI增强扫描评估RFA治疗效果的效能
3 讨论
RFA治疗是在影像学指引下,从皮肤穿刺到肝癌病灶,向病灶插入射频针,释放射频波,使病灶局部温度升高,造成肿瘤细胞变性坏死,使周围血管闭塞,阻断病灶血供,达到治疗目的,并降低肿瘤转移风险[8,9]。早期对RFA治疗的疗效进行评估有利于及早筛查出灭活不全的病灶,及时对残存病灶进行再次RFA治疗,防止病灶转移或复发[10]。既往对RFA疗效评价的方法较多,如血清学指标和影像学方法[11,12]。本研究旨在探究CEUS联合MRI增强扫描早期评价RFA治疗原发性肝癌患者的效果。
健康肝脏主要由门静脉供血,而肝动脉可为肝癌病灶供血,因此CEUS检查肝癌病灶时,动脉期呈现高回声,门静脉期呈现等回声或低回声,延迟期呈现出低回声[13]。经RFA治疗后,完全灭活的肝癌病灶呈现出黑洞征,无造影剂填充,与周围组织表现出明显的差异,而在残存病灶中,动脉期或整体表现为明显强化,其原因为RFA术后病灶动脉供血已经被切断,但门静脉仍在为病灶供血,病灶继续得到营养物质和氧,因此残存病灶在动脉期呈现出等回声,门静脉期则呈现出相对低回声[14,15]。CEUS可以直接反映人体病变器官、肿瘤病灶血流动力学变化。研究显示[16,17],病灶血液供应的阻断程度可反映治疗效果,因此许多研究者将其作为评估肝癌治疗效果的依据。对比剂在靶器官中的留存情况是一个动态的变化过程,CEUS可据此反映出血流动力学的动态变化,也可反映出器官功能变化。CEUS使用的对比剂六氟化硫是一种惰性气体,不会向细胞间隙弥散,其作用稳定,不通过肝肾排出,并且无毒、无辐射,安全性较高,有利于多次反复检查[18]。此外,CEUS仍然存在常规超声检查的不足,其应用也可能受到一定的限制,如病灶位置过深易导致显示效果差、患者呼吸或肥胖或操作者经验和手法可能影响CEUS的检查效果。另外,对于多病灶患者,实时超声造影可能难以在同一时相内兼顾多个病灶[19],因此本研究仅纳入单病灶患者。
MRI的检查效果与多种因素有关,如呼吸移动、扫描层厚等,受到这些因素的影响可能导致图像出现伪影,从而增加判断病灶的难度。与其他影像学方法相比,MRI可以获得与软组织背景优越的高分辨率图像,还能利用不同序列采集多项参数,从肝脏的功能和形态等多方面进行评估[20]。由于血管瘤或肝癌中可能存在正常肝组织,对ADC值造成影响,因此DWI单独用于诊断肝脏恶性肿瘤时可能出现误诊或漏诊,但采用动态增强扫描可显著提高诊断率,减少误诊或漏诊。增强MRI在肝癌诊断方面应用广泛,钆对比剂可明显提高MRI增强扫描筛查残存病灶的优势。
本研究显示,CEUS或MRI增强扫描单独评估残存病灶的灵敏度、特异度、准确率稍低,而两者联合判断的灵敏度、特异度和准确率都达到了新高,提示CEUS联合MRI增强扫描有利于提高对RFA治疗疗效的评估,指导临床的价值更高。
综上所述,采用CEUS或MRI增强扫描评价RFA治疗PLC患者的疗效均有较高的价值,而两者联合应用时,有利于提高评估的灵敏度、特异度和准确性。
