恩替卡韦联合α-干扰素治疗慢性乙型肝炎患者疗效研究*
2023-11-18党子龙孙珺珺
宋 涛,徐 敏,党子龙,孙珺珺
慢性乙型肝炎(chronic hepatitis B,CHB)是我国常见和多发慢性传染病之一,严重威胁公众生命安全[1]。据WHO统计数据显示[2],全球乙型肝炎病毒(hepatitis B virus,HBV)感染人群已超3.5亿。对于CHB患者来说,治疗的关键在于有效抑制HBV复制,减轻肝组织炎症和纤维化,防止疾病进一步发展,减少疾病相关并发症的发生。同时,联合应用免疫调节药物以达到个体化长期治疗的目的[3]。临床上,抗HBV治疗药物包括α-干扰素(IFN-α)类和核苷(酸)类药物。恩替卡韦属于核苷酸类似物[4],是一种抗病毒作用效果较强的鸟嘌呤核苷类似物,可有效阻碍HBV聚合酶的启动、反转录和病毒DNA链的合成,干扰HBV的复制,实现抗病毒的治疗目的,其耐药性相对较低,适用于长期抗病毒治疗[5,6]。IFN-α为抗病毒治疗的一线药物,具有抗病毒和免疫调节双重作用,可通过调节机体免疫功能抑制病毒复制或清除病毒感染[7]。本研究应用恩替卡韦联合IFN-α治疗CHB患者,观察了疗效情况,现报道如下。
1 资料与方法
1.1 病例来源 2019年5月~2022年3月我院收治的CHB患者69例,男43例,女26例;年龄为32~66岁,平均年龄为(40.7±5.3)岁。符合《慢性乙型肝炎防治指南》的诊断标准[8]。排除标准:合并恶性肿瘤;合并其他严重的器质性疾病;合并自身免疫性疾病;存在血液系统疾病;伴有肺结核等其他传染性疾病;近期应用过免疫抑制剂;重叠其他肝炎病毒或人类免疫缺陷病毒感染;妊娠或哺乳期妇女。入组对象签署知情同意书,本研究经我院医学伦理委员会批准。
1.2 治疗方法 采用随机数字表法将患者分为A组35例和B组34例。给予A组恩替卡韦(中美上海施贵宝,国药准字H20052237)0.5 mg口服,1次/d,IFNα-2b(北京凯因科技,国药准字S20030032)300万单位皮下注射,1次/隔日;给予B组恩替卡韦治疗,用法同上。两组均连续治疗观察12个月。
1.3 指标检测 采用ELISA法检测血清HBeAg和HBeAb(广州中山生物);采用荧光定量PCR 法检测血清HBV DNA(上海克隆生物,最低检测下限为 1.0×103copies/ml);采用放射免疫分析法检测血清层粘连蛋白(laminin,LN)、透明质酸(hyaluronan,HA)、III型前胶原(procollagen III,PIIIP)和IV型胶原(collagen IV,CIV)水平(天津博奥赛斯生物);采用ELISA法检测血清人尾肢同源蛋白2(human pygopus homolog 2,Pygo2)水平(美国Bio Rad公司);采用ELISA法检测血清核转录因子κB ( nuclear transcription factorκB,NF-κB)、转化生长因子-β(transforming growth factor,TGF-β)、肿瘤坏死因子-α(tumour necrosis factor-α, TNF-α) 和白介素-6(interleukin-6,IL-6) 水平(上海尚宝生物科技)。

2 结果
2.1 两组疗效比较 在治疗6个月和12个月末,两组HBeAg转阴率无显著性差异(P>0.05),但A组血清ALT复常率显著高于B组(P<0.05,表1)。

表1 两组疗效(%)比较
2.2 两组肝功能指标比较 在治疗12个月末,A组血清ALT和AST水平显著低于B组(P<0.05,表2)。
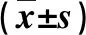
表2 两组肝功能指标比较
2.3 两组血清肝纤维化指标水平比较 在治疗12个月末,A组血清HA和PC-Ⅲ水平显著低于对照组(P<0.05,表3)。

表3 两组血清肝纤维化指标比较
2.4 两组血清细胞因子水平比较 在治疗12个月末,A组血清NF-kB、TGF-β和Pygo2水平显著低于对照组(P<0.05,表4)。
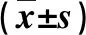
表4 两组血清细胞因子水平比较
3 讨论
在感染HBV后,CHB患者机体出现异常免疫反应。HBV高复制诱发免疫损伤,不断损伤患者肝细胞。CHB是肝硬化、肝衰竭和肝细胞癌主要的致病因素之一[9]。有效抑制HBV复制,改善机体免疫反应,对抑制CHB患者肝纤维化的发生发展和保护肝细胞功能具有重要的意义[10]。
α-干扰素为目前临床公认有效的抗病毒药物,具有抗病毒和免疫调节作用,应用于CHB患者的治疗可获得较高的血清和免疫学应答[11]。2005年,恩替卡韦于美国被批准上市,并应用于HBV感染的治疗,在体内磷酸化后成为三磷酸盐,又通过与三磷酸脱氧鸟嘌呤核苷竞争,高选择性地抑制病毒复制过程。与此同时,恩替卡韦对HBV DNA 多聚酶的抑制力相较于其对正常细胞DNA的作用力明显较高,安全性较佳[12]。过去应用的阿德福韦经两步磷酸化转变为二磷酸阿德福韦,与脱氧腺苷三磷酸竞争,终止病毒链延长,发挥抗病毒效应[13]。α-干扰素与恩替卡韦联合抗病毒作用的靶点和机制不同,不存在相互竞争抑制,为进一步提高临床疗效,本研究分别以恩替卡韦联合α-干扰素或单纯应用恩替卡韦治疗,以控制HBV感染,改善CHB患者的疾病进程。
体外研究结果表明[14],恩替卡韦抗HBV能力是阿德福韦酯的数倍。血清HBV DNA载量越高代表体内病毒复制能力越强,传染性越强[15]。本研究两组血清HBV DNA转阴率类似,表明恩替卡韦的抗病毒作用较强,但联合α-干扰素能较好地改善肝功能指标,效果优于单纯应用恩替卡韦。恩替卡韦在降低病毒活性,抑制其复制过程方面的效果较佳,一方面可能与恩替卡韦对病毒高效抑制机制有关,另一方面可能与其易于吸收,用药后1 h,即可达血药峰值,血药分布容积到达全身[16]。此外,本研究显示A组血清ALT复常率显著高于B组,肝功能指标如ALT和AST水平显著低于B组,表明恩替卡韦联合α-干扰素在患者肝功能改善方面效果优于单用恩替卡韦。恩替卡韦降低肝组织HBV DNA载量,有助于抑制肝组织炎症,减轻病毒诱发的肝损伤[17]。有效抑制HBV 复制对抑制CHB患者肝纤维化和保护肝细胞功能具有积极的意义。本研究治疗后A组血清肝纤维化指标改善效果优于B组。恩替卡韦联合α-干扰素治疗更有利于减轻患者肝纤维化。恩替卡韦发挥较强的抗病毒活性,有利于肝纤维化的有效控制。相关研究显示[18],Pygo2为重要的肝脏病变标志物,肝脏病变时呈现其血清水平异常,CHB患者血清Pygo2水平呈现升高。本研究两组患者治疗后血清Pygo2水平均较治疗前降低,且A组显著低于B组,进一步说明恩替卡韦联合α-干扰素治疗在改善细胞因子作用方面效果更佳。
CHB患者感染HBV诱导巨噬细胞和淋巴细胞激活,促使机体炎症反应。在疾病发生发展过程中,激活NF-κB,启动 IL-6和TNF-α等炎性细胞因子高表达,引起肝组织白细胞浸润,加重肝损伤[19]。本研究治疗后两组血清炎性指标如NF-kB、TGF-β、TNF-α和IL-6水平均明显下降,且A组显著低于B组。恩替卡韦联合α-干扰素能减轻CHB患者机体炎症反应,其效果显著优于恩替卡韦治疗。恩替卡韦发挥积极的抗HBV复制作用,使机体血清HBV DNA保持持续的低水平,减轻了患者肝组织炎症反应。外周血T细胞亚群能有效反映机体免疫状态。T淋巴细胞免疫参与体内清除HBV活动。CD4+细胞是人体重要的免疫细胞,可抑制病毒复制,降低血清病毒载量,减轻免疫损伤。CD8+为细胞毒性T细胞亚群,可引起细胞免疫紊乱[20]。有研究结果显示,在抗病毒治疗后,外周血CD4+细胞百分比和CD4+/CD8+细胞比值紊乱被显著改善,表现为CD8+细胞百分比显著下降。恩替卡韦联合α-干扰素治疗能有效抑制HBV复制,调节机体紊乱的免疫反应,为疾病康复提供良好的内部条件。两种药物联合的作用被加强,可能是由于恩替卡韦本身不具备免疫调节作用,发挥机体免疫调节功效的主要药物在于α-干扰素,因此,联合治疗的短期效果更好。
综上所述,临床应用恩替卡韦联合α-干扰素治疗CHB患者更有利于抑制HBV复制,减轻肝功能损伤和肝纤维化,降低机体炎性反应。由于短效α-干扰素的作用可能不持久,在停药后可能出现病毒学反弹或肝功能损伤复发。因此,探讨合适的患者对象和用药疗程,对于改善抗病毒治疗的长期效果非常重要。