左心耳封堵术后装置不完全内皮化的危险因素及临床影响
2023-11-15丁树生宁彬
丁树生 宁彬
心房颤动(房颤)是临床上常见的一种心律失常,其缺血性脑卒中风险是非房颤患者的4~5倍,是致残和致死的重要原因,临床常用抗凝药预防缺血性脑卒中,然而抗凝治疗客观上存在出血风险[1]。研究发现,房颤导致的血栓栓塞事件源于左心房内形成的血栓脱落,90%以上房颤患者的血栓来源于左心耳[2-3]。左心耳封堵术(left atrial appendage closure,LAAC)的理论基础是通过手术将左心耳隔绝于循环之外,近年来逐渐应用于临床,尤其适用于存在抗凝禁忌及脑卒中高风险患者的预防,多项研究已证实其临床疗效及安全性[4]。LAAC后面临的主要问题是装置相关血栓(device-related thrombosis,DRT)的发生,PROTECT研究[5]显示LAAC后装置相关血栓发生率为4.2%,且与再发性缺血性脑卒中密切相关。DRT形成多见于封堵器中心螺钉处,与这一特殊凸起部位较难完成内皮覆盖相关[6-7]。目前对于装置不完全内皮化和DRT形成相关的研究较少,本研究旨在探讨LAAC后装置不完全内皮化的危险因素及临床影响。
1 对象与方法
1.1 研究对象
收集2021年1—12月就诊于阜阳市人民医院接受LAAC联合房颤射频消融术治疗并具有完整随访资料的非瓣膜性房颤患者60例。其中置入Watchman封堵器患者26例,置入LACbes患者34例。纳入标准:(1)非瓣膜性房颤患者;(2)房颤患者脑卒中风险评估CHA2DS2-VASc≥2分;(3)存在口服抗凝药物禁忌或不愿意接受长期口服抗凝药物治疗者。排除标准:(1)术前经食管超声心动图提示左心房内有血栓者;(2)瓣膜性房颤患者;(3)左心室射血分数<30%者;(4)严重肾功能不全[肾小球滤过率(glomerular filtration rate,GFR)<30 ml/min]者;(5)1个月内新发缺血性脑卒中者;(6)严重凝血功能异常存在抗凝禁忌者;(7)未控制的纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅳ级患者。本研究经阜阳市人民医院医学伦理委员会批准(2020)9号,所有患者术前均已签署知情同意书。
1.2 资料收集
(1)收集患者的一般资料,包括年龄、性别、身体质量指数、吸烟史、房颤类型(阵发性或持续性)、CHA2DS2-VASc评分、HAS-BLED评分,实验室指标[血红蛋白、谷丙转氨酶、谷草转氨酶、血肌酐、脑钠肽(brain natriuretic peptide,BNP)、空腹血糖],左心耳直径、左心耳深度、左心房大小(指左心房大小测量根据左心房前后径)、左心室射血分数(left ventricular ejection fraction,LVEF)、二尖瓣反流情况,冠心病、高血压病、心力衰竭、糖尿病、脑卒中、出血事件等病史等;(2)记录患者术中左心耳形态、封堵器类型、封堵器型号、装置位置、残余分流、手术时间、对比剂剂量;(3)记录术后3个月口服抗凝药物类型;(4)术后3个月及6个月行心脏CT血管造影(CT angiography,CTA)检查,观察装置内皮化、装置周围残余分流、DRT等情况,随访不良心脑血管事件[出血事件、脑卒中、短暂性脑缺血发作(transient ischemic attack,TIA)]发生情况。
1.3 LAAC联合房颤射频消融及抗凝方案
患者仰卧,在CARTO3D导航系统下行环肺静脉前庭电隔离(circumferential pulmonary vein isolation,CPVI),终点为肺静脉内与左心房传导双向阻滞,应用标测或消融导管记录肺静脉电位或起搏验证,额外消融线根据患者情况决定,通过消融术或者电复律恢复窦性心律;行LAAC,在X线透视及心电监测下,经房间隔穿刺并将输送系统引入左心耳后给予静脉内肝素,一般在左心耳最大开口直径的基础上加4~6 mm作为封堵器的选择标准。在经食管超声心动图(transesophageal echocardiography,TEE)及数字减影血管造影(digital subtraction angiography,DSA)引导下,将封堵器送至左心耳,评估封堵效果后释放封堵器。术后抗凝方案,对于HAS-BLED评分<3分患者,采用非维生素K拮抗剂口服抗凝药(non-vitamin K antagonist oral anticoagulant,NOAC)或华法林+氯吡格雷或阿司匹林联合治疗3个月;HAS-BLED评分≥3分者,术后单独使用常规剂量的NOAC或华法林治疗3个月;3个月时复查心脏CTA,如果排除DRT和大于5 mm的残余分流,改用阿司匹林+氯吡格雷双联抗血小板治疗3个月。术后6个月时复查心脏CTA,如排除DRT和大于5 mm的残余分流,予阿司匹林长期维持治疗(如阿司匹林不耐受,可用氯吡格雷替代)[8]。血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)或血管紧张素Ⅱ受体拮抗剂(angiotensin Ⅱ receptor blocker,ARB)、β受体阻滞剂、钙离子通道阻滞剂及他汀类药物等的选择根据患者特征及指南推荐[9-10]。
1.4 术后随访
采用Philips256层螺旋CT行冠状动脉CTA检查,患者仰卧位,采用回顾性心电门控技术,单次呼气末屏气扫描,扫描范围自气管隆嵴处1 cm至心脏膈面。采用3D重建技术进行数字后处理和重建,评估LAAC装置周围渗漏的位置,左心房及左心耳[11]。对于封堵器周围血流直径≥3 mm, 定义为装置周围残余分流(peri-device leak,PDL,图1)。在无PDL存在的情况下,左心房与左心耳的CT值差值>50(hounsfield unit,HU)定义为装置完全内皮化(图2);若差值≤50 HU,则定义为装置不完全内皮化(图3)。封堵器周围见增强缺损定义为DRT。

图2 心房颤动患者 女,75 岁,Watchman 封堵装置皮化完全覆盖,左心房与左心耳的CT 值差值>50 HUFigure 2 A 75-year-old patient with atrial fibrillation,with Watchman closure device dermatization completely covered,and the difference between the CT values of the left atrium and LAA was >50 HU
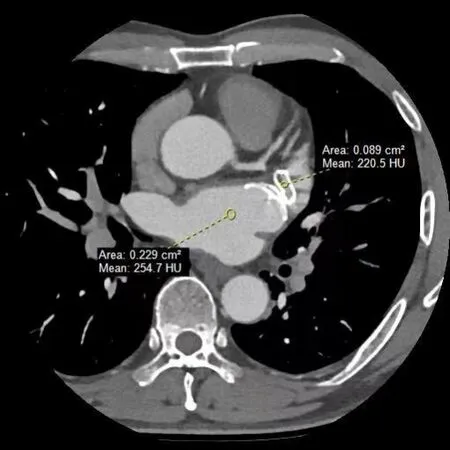
图3 心房颤动患者 男,53 岁,LACbes 封堵装置内皮化覆盖不全,左心房与左心耳的CT 值差值≤50 HUFigure 3 A patient with atrial fibrillation,a 53-year-old male,has inadequate endothelial coverage of the LACbes closure device,and the difference between the CT value of the left atrium and LAA is ≤50 HU
1.5 统计学分析
采用SPSS 26.0统计分析软件进行统计学分析。计量资料符合正态分布用均数±标准差表示,非正态分布用中位数(四分位数间距)表示,计数资料用频数(%)表示。计量资料正态分布数据组间比较使用独立样本t检验;计量资料偏态分布使用非参数秩和检验;计数资料使用χ2检验或Fisher确切概率法。使用二元Logistic回归分析封堵器术后内皮化不完全的独立危险因素。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较
纳入60例患者术后3个月中位时间随访,心脏CTA检查发现装置完全内皮化患者19例,不完全内皮化患者37例,存在PDL患者4例,所有患者均无不良血管事件。术后6个月中位时间随访检查,发现装置不完全内皮化患者中仍有34例(装置不完全内皮化组)存在内皮化不全,其中有1例装置不完全内皮化患者术后6个月内并发脑卒中,完全内皮化患者22例(装置完全内皮化组),术后6个月4例患者PDL仍然存在。两组患者年龄、性别、身体质量指数、吸烟史、CHA2DS2-VASc评分、HAS-BLED评分、既往病史、术中数据、术后抗凝药物、PDL、DRT、不良心脑血管事件比较,差异均无统计学意义(均P>0.05);房颤类型和二尖瓣反流比较,差异均有统计学意义(P=0.011,P=0.029,表1)。
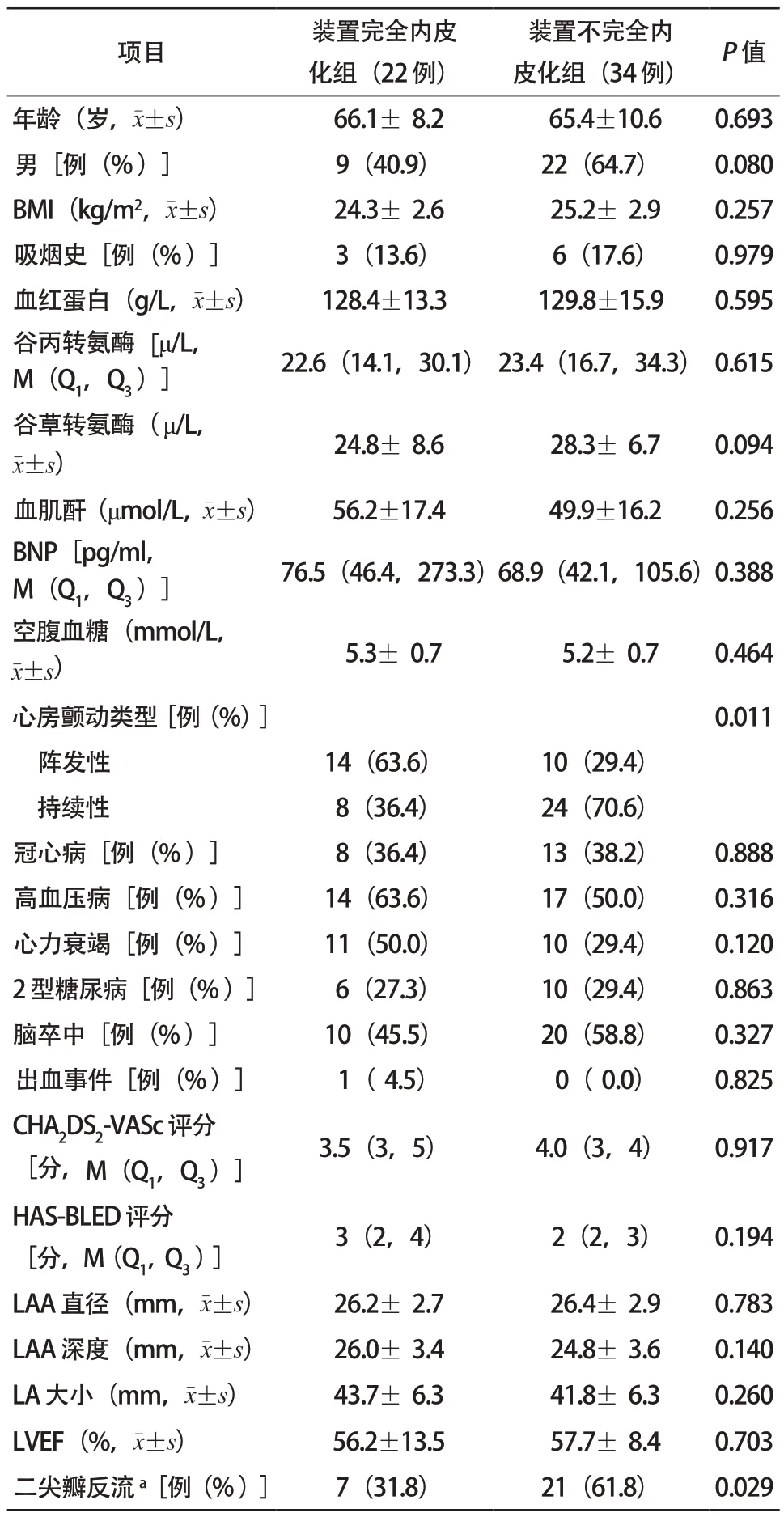
表1 LAAC 术后 6 个月装置完全内皮化与不完全内皮化 一般资料比较Table1 Comparison of general information on complete endothelialization and incomplete endothelialization of devices at 6 months after LAAC
2.2 两组患者术中资料及6个月不良心脑血管事件比较
置入Watchman封堵器患者26例,置入LACbes患者34例,存在PDL4例,其中2例置入Watchman封堵器,另2例置入LACbes封堵器。两组患者Watchman例数、LACbes例数及尺寸、术后即刻PDL、装置位置、残余分流(mm)、手术时间(min)、对比剂剂量(ml)、左心耳形态、抗凝药物种类及术后DRT、出血事件、脑卒中、TIA比较,差异均无统计学意义(均P>0.05,表2)

表2 LAAC 术中数据及6 个月不良心脑血管事件情况Table 2 LAAC intraoperative data and adverse cardiovascular events at 6 months
2.3 LAAC后装置不完全内皮化的Logistic回归分析
以持续性房颤和二尖瓣反流为自变量,装置是否完全内皮化为因变量行二元Logistic回归分析,结果显示持续性房颤(OR4.378,95%CI1.316~14.565,P=0.016)和二尖瓣反流(OR3.629,95%CI1.081~12.184,P=0.037)为影响左心耳封堵装置不完全内皮化的独立危险因素。
3 讨论
在犬类模型中,装置完全内皮化在LAAC后45~90 d内完成[12],但在人体上似乎并非如此,手术6个月或更晚时间经常会遇到装置不完全内皮化[13]。本研究随访发现有34例(60.7%)患者术后6个月心脏CTA检查存在装置不完全内皮化,这一结果与既往研究相比发生率较高。既往研究报告了在LAAC后6个月的中位随访时间,装置不完全内皮化的发生率为56%[14]。LAAC后装置不完全内皮化发生率不同的原因是多方面的,可能与装置不完全内皮化的定义、封堵器类型以及心脏成像技术有关。理论上,两种封堵器表面积差异不同,其装置内皮化不完全发生率可能不同。一项对比Watchman与LACbes封堵器临床有效性及安全性研究发现,术后3个月装置内皮化不完全的发生率分别为27.5%及41.9%,DRT发生率差异无统计学意义[15]。本研究对比2种封堵器装置不完全内皮化发生率相近,可能的原因与装置不完全内皮化的定义尚无统一标准定义及随访时间不同有关。最近,由于心脏CTA具有卓越的空间分辨率、3D评估,并且受操作者影响较小,与TEE相比,其已被证明可以更敏感地检测到左心耳的装置不完全内皮化。通过心脏CTA检查,可以测量左心耳内的线性衰减系数,在无PDL存在的情况下,左心房与左心耳的CT值差值≤50 HU,则定义为装置不完全内皮化。这可能部分解释了本研究中装置不完全内皮化发生率较高的原因。
LAAC后装置不完全内皮化危险因素仍不完全清楚。本研究结果显示,二尖瓣反流是装置不完全内皮化的独立危险因素,轻度及以上的二尖瓣反流可能引起装置不完全内皮化,而长时间的装置不完全内皮化可能增加装置表面血栓形成风险。Sharma等[16]报道了1例患有严重二尖瓣关闭不全的70岁女性,在Watchman手术1.5年后出现装置不完全内皮化。既往研究发现血管狭窄区域的高剪切应力会影响细胞黏附并对内皮细胞造成有害影响;同样,高速反流引起的血液湍流会引起细胞时间及空间的紊乱,从而阻碍正常内皮代偿性重新排列[17]。因此,认为其可能的原因是偏心的二尖瓣反流射流在装置上引起了剪切应力,并阻碍了正常的内皮化,轻度及以下的二尖瓣反流对内皮化影响较小,轻度及以上的二尖瓣反流可增加装置不完全内皮化的风险。
此外,本研究发现,持续性房颤是装置不完全内皮化的另一独立危险因素,持续性房颤抑制装置内皮化进程。Granier等[18]发现存在装置不完全内皮化的患者更有可能患有糖尿病、永久性房颤和置入更大的装置。一项单中心研究发现,装置周围残余分流的存在会增加DRT的风险,在存在残余血流的患者中,左心耳装置间隙导致左心耳残留血液流速减低,这可能会使左心耳内血液形成湍流,进而引起封堵器内皮化延迟或抑制内皮化,同时也使得封堵器表面易形成血栓[19-20]。因此,认为其可能的原因是持续性房颤引起封堵器周围的血液流动紊乱,在左心耳内血液形成湍流,进而影响装置内皮化进程,尽管其确切的机制仍然未知。
临床上经常会遇到装置不完全内皮化,了解装置不完全内皮化的危险因素及临床影响,对LAAC后患者的随访及指导个体化药物抗栓方案具有重要价值。理论上,装置不完全内皮化会导致左心耳平均血液流速减低并形成湍流,其可能会触发左心耳封堵装置上形成血栓。最近的研究发现,LAAC联合射频消融组早期不良事件的发生率高于射频消融组,可能与LAAC术后左心房功能一过性的下降有关[21]。一项单中心研究结果显示,在LAAC后较晚发生的装置不完全内皮化会增加DRT及随后的血栓栓塞事件发生率[22]。另有研究指出,肺静脉嵴覆盖可能与LAAC后DRT发生率较低有关[23]。本研究在6个月中位心脏CTA随访检查中,均未发现TIA、DRT、出血事件等,仅1例患者因LAAC后4个月出现脑卒中于神经内科住院治疗,对该患者复查心脏CTA检查发现存在装置不完全内皮化,考虑该患者为非心原性脑卒中。其可能的原因:(1)本研究中LAAC患者选择封堵器的型号较左心耳最大开口直径稍大,减少肺静脉嵴部区域大小,部分完成了肺静脉嵴覆盖,进而减少DRT的发生;(2)对于术后3个月心脏CTA检查发现存在装置不完全内皮化的患者适当延长抗凝治疗。因此,装置不完全内皮化在短期可能不会增加DRT及不良心脑血管事件风险,未来需要大型多中心前瞻性随访研究进一步明确装置不完全内皮化的临床影响。
本研究的局限性:(1)研究中纳入的患者数量有限,可能存在选择偏倚,研究得出的结论可能不足;(2)作为一项单中心研究,纳入患者的治疗方案可能无法反映LAAC治疗的一般状况;(3)6个月的临床随访时间较短,无法预测装置不完全内皮化患者的远期结果,以及该人群中适合的抗血栓治疗方案。
综上所述,本研究结果初步表明,在LAAC后6个月的随访中装置不完全内皮化并不少见,尤其是在持续性房颤、二尖瓣反流患者中。装置不完全内皮化在短期可能不会增加DRT及不良心脑血管事件风险,未来仍需要大型的前瞻性长期随访研究探讨装置不完全内皮化的临床影响,以指导个体化药物抗栓方案。
利益冲突 所有作者均声明不存在利益冲突
