FOX-7热分解特性及V2O5对其热分解的影响①
2023-11-14吕亭川占明明鲁国林
吕亭川,占明明,鲁国林
(1.航天化学动力技术重点实验室,襄阳 441003;2.湖北航天化学技术研究所,襄阳 441003)
0 引言
FOX-7(1,1-二氨基-2,2-二硝基乙烯)是一种新型的高能钝感炸药,分子式为C2H4N4O4,与RDX(环三亚甲基三硝胺)相比,FOX-7能量水平接近RDX,但是感度明显低于RDX,耐热性好,有望在固体推进剂及火炸药相关领域得到应用。作为一种新型含能物质,对FOX-7热分解特性进行了解是十分必要的。
FOX-7问世后,其热分解研究也随之开展。付秋菠等[1-3]采用热裂解色谱-质谱、DSC和IR等实验研究了FOX-7热分解,认为其首先发生“脱硝”反应,产物首先检测出NO;金朋刚等[4-5]通过非等温热红外动力学处理技术计算FOX-7各官能团断裂所需活化能,认为热分解起始方式为C—NO2键的重排反应,并提出了FOX-7两步热分解机理。宗和厚等[6]采用量子化学计算FOX-7的热分解机理,认为其热分解起始方式为C—NO2键断裂,生成NO2,并且NO2的存在能够加速FOX-7的分解。ZHAO等[7]制备了球形FOX-7,并采用DSC、TG和ARC法分析了其在非等温绝热条件下的热行为,结果表明,与原始FOX-7相比,球形FOX-7释放能量更快,释放的能量更多。KUKJIA等[8]采用密度泛函理论对FOX-7进行计算,发现C—NO2断键所需能量最低,得出FOX-7分子的分解是从C—NO2开始的结论。HELEN等[9]通过量子化学计算研究FOX-7热分解过程,发现其分子在加热后分子层氢键破坏,分子不断撞击下C—NO2键发生断裂。INDRA FUHR等[10]计算了FOX-7分子分解时所需要的能量,发现C—NO2见所需能量最低而C—NH2断键所需能量较高。综上可知,关于FOX-7热分解起始机理存在两种意见,一种认为FOX-7中的—NO2首先发生重排,生成NO气体;另一种认为FOX-7中首先发生C—NO2键断裂,直接生成NO2气体。
燃速催化剂能有效改善推进剂的燃烧在固体推进剂中,金属氧化物在提高燃速和降低压强指数方面有明显的作用[11-13]。通过寻找改变FOX-7热分解特性的催化剂可以为FOX-7在固体推进剂中的应用奠定基础。侯亚琴等[14]实验证明V2O5在低温下能选择性催化NO与NH3的反应(6NO+4NH3→5N2+6H2O)。FOX-7分子中含有氨基和硝基,热分解过程中可能会生成NO和NH3,因此V2O5催化剂有可能影响FOX-7的热分解特性。
本文通过TG-DSC、热重-红外光谱实验研究FOX-7热分解历程和热分解产物,并通过Gaussian 09W计算得到FOX-7的一种热分解途径及其在该途径下的热分解产物,研究其热分解机理。此外,本文选取V2O5催化剂,将其与FOX-7混合,并通过TG-DSC、红外光谱等实验研究V2O5对FOX-7热分解活化能、特性及热分解产物的影响。
1 实验
1.1 实验样品
FOX-7,分析纯,黄色颗粒,d50=106 μm,湖北航天化学技术研究所;V2O5,分析纯,褐色粉末,武汉吉业升化工有限公司。
将V2O5和FOX-7按质量比1∶9均匀混合。
1.2 仪器和实验条件
(1)TG-DSC实验
采用德国耐弛公司的热重-差示扫描量热仪测试FOX-7及其混合物的热分解特性。试样质量为1.5 mg,无特殊说明升温速率为10 ℃/min,温度范围为50~350 ℃,N2流速为20 ml/min。
(2)DSC实验
DSC实验为TG-DSC实验中仅选取DSC的实验结果进行分析。
(3)TG-IR实验
采用傅叶变换红外光谱仪测试FOX-7及其混合物的热分解产物,试样质量为1.5 mg,红外光谱范围为400~4000 cm-1,升温速率为10 ℃/min,温度范围为30~350 ℃。
(4)量子化学计算
采用Gaussian 09W、Gaussview程序计算FOX-7热分解化学反应路径。本文通过计算原子间的化学键键能,对FOX-7的热分解进行解释。采用Density Functional Theory(DFT)理论B3LYP方法,基组为6-31g(d,p)对FOX-7进行优化,对其热分解过程中产生的过渡态(TS)和中间体(M)进行结构优化,得到FOX-7一种可能发生的热分解途径。
2 结果与讨论
2.1 FOX-7热分解特性的研究
2.1.1 FOX-7的热分解特性
FOX-7的TG-DSC曲线如图1所示。
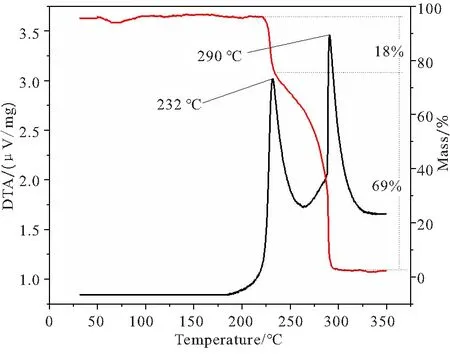
图1 FOX-7的TG-DSC曲线Fig.1 TG-DSC curves of FOX-7
从图1可以看出,FOX-7的热分解分为2个放热阶段:第一阶段热分解在200~250 ℃发生,最大放热峰值温度(峰温)为232.2 ℃,质量损失为29.4%;第二阶段热分解在250~310 ℃发生,最大放热峰温是290.6 ℃,质量损失为64.9%。2个阶段受热分解质量总共减少94.3%,与RDX(RDX热分解只有1个阶段,在200~280 ℃发生[15])相比,FOX-7的 2个阶段热分解峰比较陡峭,热失重曲线下降较快,说明在该研究条件下FOX-7热分解过程比较迅速。
2.1.2 V2O5对FOX-7热分解特性的影响
将FOX-7与金属氧化物V2O5混合后进行DSC热分解实验,得到的结果如图2所示。

图2 含V2O5的FOX-7热分解DSC曲线Fig.2 Thermal decomposition DSC curves of FOX-7 with V2O5
从图2中读取有无催化剂FOX-7的2个阶段起始温度、峰温数值,对2个峰进行积分得到峰面积,具体结果如表1所示。通过图2和表1可以得到:
(1)不添加催化剂的FOX-7第一阶段起始放热温度和峰值放热温度分别为224.5 ℃和235.5 ℃,第二阶段起始温度和峰值放热温度分别为264.6 ℃和290.6 ℃;添加催化剂后FOX-7热分解两个阶段的起始温度基本不变,峰温有所提前,并且V2O5第二阶段峰温提前比较明显。
(2)计算2个峰峰面积的相对大小,峰面积可以反应热分解过程中放热量的大小,无催化剂FOX-7的2个阶段放热峰面积之和的相对值为50.43;添加催化剂后峰面积之和增加到61.85;此外,添加催化剂后FOX-7第二阶段放热量超过第一阶段,使得FOX-7热分解更加充分。
2.1.3 V2O5催化剂对FOX-7分解活化能的影响
为了研究催化剂对FOX-7的热分解活化能的影响,需要进行计算动力学参数(活化能Ea,指前因子A),热分解动力学参数计算公式:
式中β为升温速率,K/min;T为分解峰峰温,K;Ea为活化能,kJ/mol;A为指前因子;R为通用气体常数,R=8.314 J/(mol·K)。
升温速率分别为2、5、10、20 K/min,记录DSC曲线2个放热峰峰温,将峰温T看作升温速率β的函数,以lnβ对1/T作图,通过拟合直线斜率和截距可计算热分解反应的活化能及指前因子。计算结果见表2。

表1 含V2O5FOX-7的DSC数据Table 1 DSC data of FOX-7 with V2O5

表2 含V2O5催化剂FOX-7的热分解动力学参数Table 2 Kinetic parameters of thermal decomposition of FOX-7 containing catalyst V2O5
数据表明,添加V2O5催化剂后,一阶段热分解活化能从179 kJ/mol降低至158 kJ/mol,二阶段热分解活化能从340 kJ/mol降低至272 kJ/mol活化能降低。因此,V2O5能降低FOX-7热分解活化能,促进FOX-7的热分解。
2.2 FOX-7热分解气相产物的研究
2.2.1 FOX-7热分解气相产物
FOX-7热分解在230 ℃和292 ℃下气相产物的红外光谱图如图3所示。

(a)230 ℃
在红外图中可以看到,波数在1400~2000 cm-1以及3500 cm-1以上范围波段较为复杂,这是由于FOX-7热分解的时候有较多氮氧化物生成,包括但不限于N2O、N2O4、N2O5、NO等,其中能观察到较为明显的峰有2360、1630、2283、1906 cm-1四个点,标准红外图谱查得,2360 cm-1处为CO2,2283 cm-1处为HNCO,1906 cm-1处为NO,1630 cm-1处为NO2,FOX-7热分解主要气相产物的红外光谱图在这四个点都有较为明显的特征峰,故FOX-7热分解有CO2、NO、NO2、HNCO气体的生成。FOX-7热分解主要气相产物吸光度随温度变化曲线见图4。
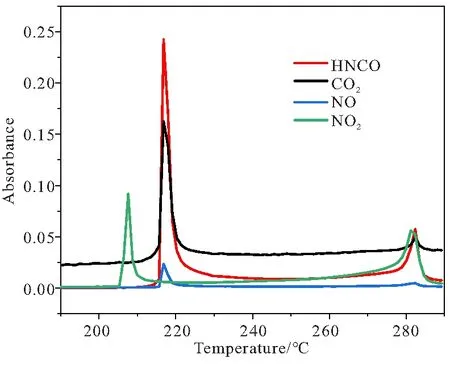
图4 主要气相产物吸光度随温度变化图Fig.4 Absorbance of main gas phase productsas a function of temperature
图4表明,FOX-7热分解首先出现峰对应的气体是NO2,说明FOX-7分解首先生成的是NO2气体。在所有气体产物中,HNCO的含量最高,NO含量最低,并且NO第二阶段浓度非常低,可以忽略不计。此外,所有的气体产物的含量都是第一阶段大于第二阶段,此外所有产物的含量在290 ℃后都达到第一阶段热分解前的水平,说明290 ℃之后不再有反应发生,即这几种气相产物成为FOX-7热分解的最终产物。
热分解气体产物的定量分析依据Beer-Lambert定律:
A=εbc
式中A是吸光度;ε为摩尔吸光系数;b为入射光通过样品光程;c为被测组分的浓度。
同一实验条件下光程b为定值,即浓度c只与吸光度A和气体种类ε相关,为了比较产物的浓度关系,以HNCO为基准,计算FOX-7热分解气相产物中其他气体的浓度与HNCO比,结果见表5。

表5 HNCO与其他气体的浓度关系Table 5 Concentration of HNCO and other gases
通过数据表明,一阶段主要产物HNCO∶CO2∶NO2∶NO含量比例约为10∶6∶4∶1,二阶段主要产物HNCO∶CO2∶NO2含量比例约为2∶2∶3,NO含量极低,可忽略不计。
2.2.2 催化剂对FOX-7热分解产物的影响
不添加催化剂和添加10%V2O5催化剂的FOX-7在227、290 ℃下的红外光谱图见图5。
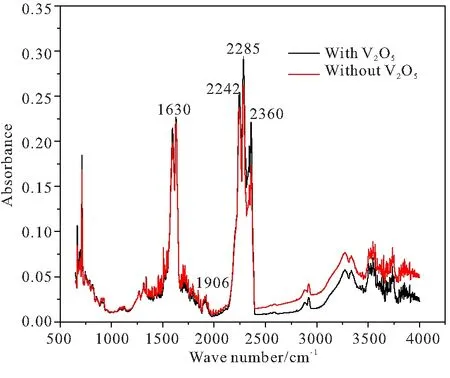
(a)227 ℃
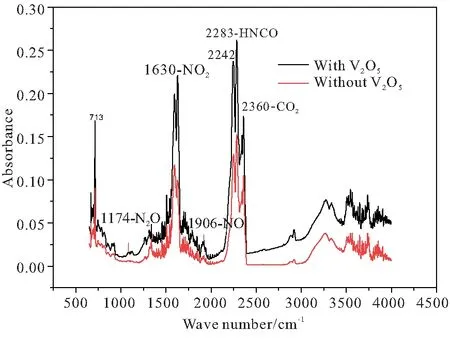
(b)290 ℃图5 添加和不添加V2O5催化剂FOX-7的红外光谱图Fig.5 IR of FOX-7 with and without V2O5
通过红外光谱图可以看到,除了NO、NO2、CO2、HNCO四种产物外,添加催化剂后在783、2229 cm-1处特征峰变得不明显,即添加V2O5改变了热分解历程,并且有新产物的生成,与气体标准红外特征峰比对可知,添加催化剂后不再有N2O、HCN产物生成。
2.3 FOX-7热分解键能计算



图6 FOX-7的球棍模型Fig.6 Ball-and-stick model of FOX-7

图7 热分解反应流程图Fig.7 Process of thermal decomposition reaction
从图7中可以看出,FOX-7首先发生C—NO2键断裂,生成中间体M1和NO2气体,M1经过一步重排后—NO2中的O转移到C上,生成酮基中间体M2,中间体M2受热,C—C键断裂,C—O键生成HNCO和过渡态TS1,TS1不稳定C—N键断裂生成HNCO和NH2-离子。通过能量计算可知,FOX-7热分解生成M2所消耗能量约为酮基中间体M2生成小分子所消耗的能量的1/2,这与DSC计算FOX-7热分解活化能结果相吻合(FOX-7热分解活化能一阶段为179 kJ/mol,二阶段为340 kJ/mol),因此可以判断在理论模拟中FOX-7热分解生成M2为FOX-7热分解的第一阶段,M2生成HNCO等小分子为FOX-7热分解的第二阶段。
基于此途径,1 mol FOX-7分解生成1 mol NO2和2 mol HCNO,并且NO2是起始生成,与红外光谱产物含量测试结果一致。反应过程中涉及到各个分子的最优结构如图8。

图8 过渡态、中间体及小分子的优化结构Fig.8 Optimal structure of transition states, intermediates and small molecules
基于量子化学理论,采用Gaussian 09程序计算FOX-7热分解途径,提出了一种FOX-7热分解历程,按照该途径1 mol FOX-7分解生成1 mol NO2和2 mol HCNO,理论计算结果与实验测试结果一致。
3 结论

(2)V2O5能影响FOX-7的热分解,添加V2O5催化剂后,FOX-7热分解峰提前,并且反应更充分,FOX-7第二阶段放热量大于第一阶段,添加催化剂后FOX-7热分解第二阶段的峰温提前,这是因为V2O5能加快FOX-7第一阶段热分解,放出更多能量,促进反应发生。对FOX-7的热分解有促进作用;此外,催化剂能改变反应历程,未添加催化剂时C—NO2发生断裂,添加催化剂后部分C—NO2键发生重排,导致热分解产物中N2O、HCN等气体不再明显观察到。
(3)采用Gaussian程序计算得出一种FOX-7热分解反应途径,根据能量计算分析出热分解生成的产物,按照该路径1 mol FOX-7生成2 mol HNCO和1 mol NO2,FOX-7热分解首先生成NO2,并且产物中HNCO含量最高,理论计算结果和红外实验测试结果一致。
