艾愈胶囊联合阿那曲唑对激素受体阳性老年乳腺癌患者肿瘤标志水平和免疫功能的影响
2023-11-14马驰骋
马驰骋
(河南理工大学第一附属医院 焦作 454000)
作为女性最常见的恶性肿瘤,乳腺癌主要是指发生于乳腺上皮组织的一种恶性肿瘤,早期多无明显症状,随着病情进展,可出现乳头溢液、乳腺肿块等症状,若未及时进行治疗,可逐渐累及肝肾等器官[1]。乳腺癌发病率位居女性恶性肿瘤的首位,而激素受体(HR)阳性占全部乳腺癌患者的60%以上,是指雌孕激素受体均呈阳性[2]。目前,临床对于HR 阳性乳腺癌的治疗以内分泌治疗为主,可有效延长生存时间,提升生活质量[3]。阿那曲唑是常见治疗药物之一,可有效调节患者内分泌环境,抑制肿瘤细胞生长,但容易损伤患者免疫功能,特别是老年患者[4]。近年来,中医药在恶性肿瘤的辅助治疗中显示出良好的应用前景[5]。艾愈胶囊属于一种中成药,具有解毒散结、补气养血等功效,适用于中晚期恶性肿瘤的辅助治疗。鉴于此,本研究从免疫功能、肿瘤标志物水平、中医证候积分、生活质量及不良反应等方面出发,探讨联合用药(艾愈胶囊+阿那曲唑)治疗HR 阳性老年乳腺癌的临床疗效及安全性。现报道如下:
1 资料与方法
1.1 一般资料 将2020 年6 月至2022 年5 月在河南理工大学第一附属医院接受治疗的80 例HR阳性老年乳腺癌患者纳入本研究,按照随机数字表法进行分组。对照组40 例,年龄61~84 岁,平均(68.96±4.38)岁;病理TNM 分期:Ⅰ期、Ⅱ期、Ⅲ期分别为15 例、18 例、7 例;病程1~9 年,平均(5.33±1.68)年。研究组40 例,年龄62~87 岁,平均(69.49±4.75)岁;病理TNM 分期:Ⅰ期、Ⅱ期、Ⅲ期分别为12 例、19 例、9 例;病程2~10 年,平均(5.49±1.57)年。两组资料(年龄、病理TNM 分期及病程等)相比,差异无统计学意义(P>0.05)。本研究经河南理工大学第一附属医院医学伦理委员会批准(伦理审批号:202000165)。
1.2 入组标准 (1)纳入标准:符合乳腺癌诊断标准[6],且经病理组织学、影像学等确诊;年龄>60 周岁;免疫组织化学检查结果显示HR 阳性;知情同意,依从性较好;自然停经超过1 年。(2)排除标准:近期内使用过相关药物治疗;对阿那曲唑等本研究所使用药物过敏;合并其他恶性肿瘤及严重器官组织功能障碍;预计生存时间不足3 个月;Karnofsky评分(KPS 评分)<60 分;治疗期间出现肿瘤复发、转移或死亡。
1.3 治疗方法 两组均给予常规补充维生素D、钙剂、饮食调节、运动管理等基础治疗。对照组采用阿那曲唑(国药准字H20050327)治疗,用法用量:口服,1 mg/次,1 次/d,治疗3 个月。研究组在上述基础上联合艾愈胶囊(国药准字Z20025336)治疗,用法用量:口服,3 粒/次,3 次/d,治疗3 个月。
1.4 观察指标 (1)临床疗效。经影像学和临床检查结果显示肿瘤病灶完全消失,且持续时间超过4周为完全缓解(CR);经影像学和临床检查结果显示肿瘤病灶缩小≥30%为部分缓解为进展(PR);经影像学和临床检查结果显示肿瘤病灶缩小<30%,或增大<20%为稳定(SD);经影像学和临床检查结果显示肿瘤病灶体积增大≥20%或出现新病灶为进展(PD)。客观缓解率=(CR 例数+PR 例数)/总例数×100%。(2)免疫功能。分别采集两组治疗前、治疗3 个月后血清样本,采用流式细胞仪对两组T 淋巴细胞亚群(CD3+、CD4+、CD8+、CD4+/CD8+)进行检测和计算。(3)肿瘤标志物水平。分别于治疗前、治疗3 个月后采用化学发光法检测两组癌胚抗原(CEA)、糖类抗原15-3(CA15-3)水平,采用酶联免疫吸附法(ELISA)检测两组组织多肽特异性抗原(TPS)水平。(4)中医证候积分。分别于治疗前、治疗3 个月后对两组食欲不振、神疲乏力、恶心呕吐等症状进行积分,每项症状按严重程度记0~3 分,满分42 分,评分越高症状越严重。(5)生活质量。分别于治疗前、治疗3 个月后采用KPS 评分进行评估,总分0~100 分,评分越高生活质量越好。(6)用药安全性。比较两组关节疼痛、乏力、腹泻、皮疹等发生情况。
1.5 统计学方法 采用SPSS23.0 软件分析处理数据,计量资料(中医证候积分、生活质量评分、免疫功能指标及肿瘤标志物水平等)以()表示,采用t检验;计数资料(临床疗效、用药安全性等)用%表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 临床疗效 客观缓解率相比(37.50% vs 60.00%),研究组较低(P<0.05)。见表1。
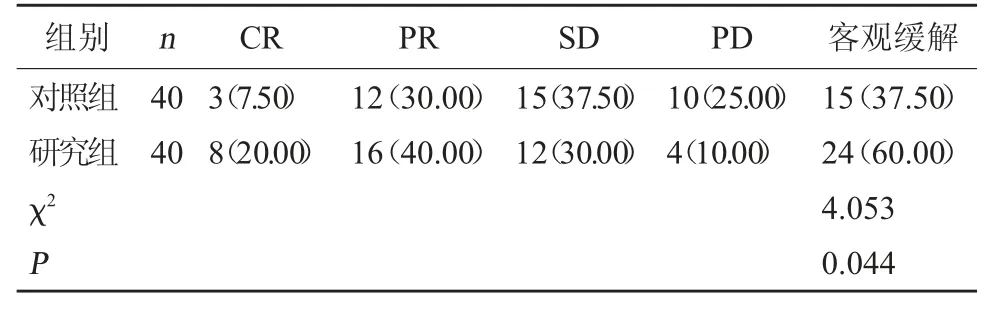
表1 两组临床疗效比较[例(%)]
2.2 免疫功能 两组治疗前免疫功能各项指标水平相比,差异无统计学意义(P>0.05);两组治疗3个月后CD3+、CD4+、CD4+/CD8+水平均显著升高,且研究组更高,而CD8+水平均显著降低,且研究组更低(P<0.05)。见表2。
表2 两组免疫功能各项指标水平比较()

表2 两组免疫功能各项指标水平比较()
注:与本组治疗前相比较,*P<0.05。
?
2.3 肿瘤标志物水平 两组治疗前肿瘤标志物各项指标水平相比,差异无统计学意义(P>0.05);两组治疗3 个月后CEA、CA15-3、TPS 水平均显著降低,且研究组更低(P<0.05)。见表3。
表3 两组肿瘤标志物各项指标水平比较()
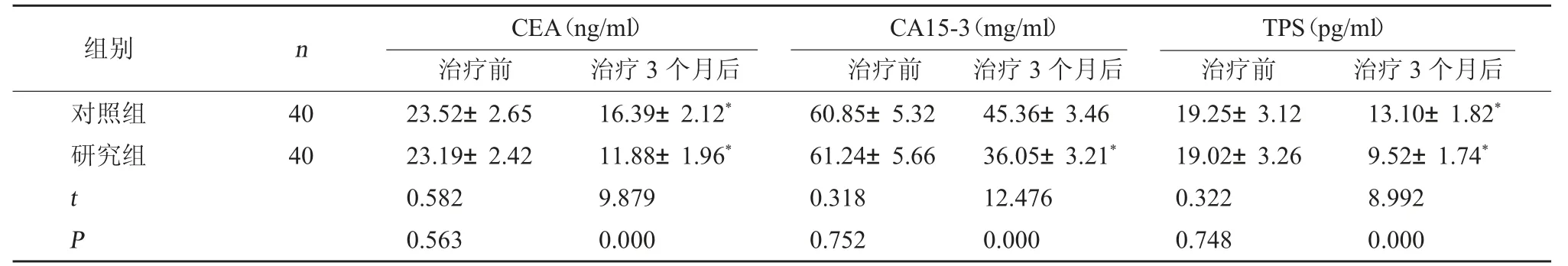
表3 两组肿瘤标志物各项指标水平比较()
注:与本组治疗前相比较,*P<0.05。
?
2.4 中医证候积分、生活质量 两组治疗前中医证候积分、生活质量各项指标水平相比,差异无统计学意义(P>0.05);两组治疗3 个月后中医证候积分均显著降低,且研究组更低,而KPS 评分均显著升高,且研究组更高(P<0.05)。见表4。
表4 两组中医证候积分、生活质量各项指标水平比较(分,)

表4 两组中医证候积分、生活质量各项指标水平比较(分,)
注:与本组治疗前比较,*P<0.05。
?
2.5 用药安全性 两组不良反应发生率比较,差异无统计学意义(P>0.05)。见表5。
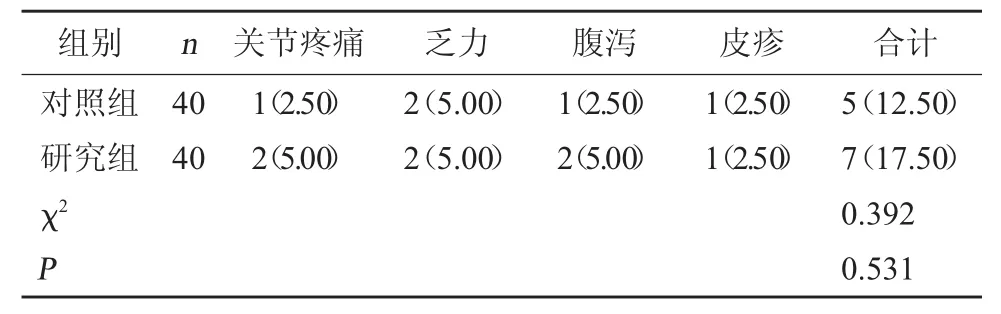
表5 两组用药安全性比较[例(%)]
3 讨论
近年来,我国乳腺癌患者患病人数不断增多,且有向年轻化发展的趋势,严重威胁患者生命安全[7]。目前,临床上超过一半的乳腺癌患者属于激素依赖型,肿瘤的发生和发展受到激素的调控,而雌孕激素可刺激乳腺肿瘤细胞的增殖与生长,约60%的患者HR 为阳性[8~9]。现阶段,临床针对HR 阳性老年乳腺癌患者多给予内分泌治疗,目的在于阻断或抑制雌激素来源,而患者血液中雌激素主要来自外周组织中芳香酶对肾上腺、卵巢中雄激素的转化[10]。由此可见,抑制芳香酶活性,减少雌激素转化,是治疗HR阳性老年乳腺癌的关键[11]。作为一种非甾体类芳香酶抑制剂,阿那曲唑可通过降低芳香酶活性,抑制雌激素转化,导致肿瘤细胞生长的内分泌环境发生改变,进而达到抑制肿瘤生长的目的[12]。但单独使用阿那曲唑进行治疗,疗效存在一定提升空间。
中医古籍中并无HR 阳性乳腺癌病名,多根据患者临床表现归属于“乳岩”范畴。中医认为,本病多因脏腑功能失调,正气不足,导致气血两虚,再加上情志内伤等,导致痰瘀互结,毒邪瘀结于乳络而发病。因此,本病的治疗以健脾补肾、清热解毒、益气养血等为原则[13]。本研究在阿那曲唑的基础上联合艾愈胶囊对HR 阳性老年乳腺癌患者进行治疗,结果显示,客观缓解率相比(37.50%vs 60.00%),研究组较低;两组治疗3 个月后中医证候积分均显著降低,且研究组更低,而KPS 评分均显著升高,且研究组更高(P<0.05)。这提示给予HR 阳性老年乳腺癌患者联合用药(艾愈胶囊+阿那曲唑)治疗,可有效减轻症状,促进生活质量提升,疗效确切。分析原因在于:艾愈胶囊主要由人参、当归等中药材组成,具有解毒散结、补气养血、健脾补肾等功效,与上述病机、治疗原则相吻合[14]。现代药理研究发现,艾愈胶囊具有增强机体免疫功能、保护骨髓造血功能及抑制肿瘤生长等多种作用[15]。
临床发现,受到放化疗、手术及疾病本身的影响,HR 阳性老年乳腺癌患者多伴有一定程度的免疫功能障碍[16]。通过检测治疗前后患者T 淋巴细胞亚群水平的变化情况,可有效掌握患者免疫功能恢复情况。血清肿瘤标志物是监测HR 阳性老年乳腺癌患者病情变化及评估预后的主要指标,具有价格低、操作简便等优势[17]。本研究结果显示,两组治疗3 个月后CD3+、CD4+、CD4+/CD8+水平均显著升高,且研究组更高,而CD8+、CEA、CA15-3、TPS 水平均显著降低,且研究组更低(P<0.05)。这表明联合用药可有效促进HR 阳性老年乳腺癌患者免疫功能恢复,降低肿瘤标志物水平。两组不良反应发生率比较,差异无统计学意义(P>0.05)。这说明联合用药安全性较好。综上所述,联合用药(艾愈胶囊+阿那曲唑)治疗HR 阳性老年乳腺癌疗效确切,可有效促进免疫功能恢复,降低肿瘤标志物水平,促进生活质量提升,且联合用药并未显著增加不良反应,优势较为明显,具有进一步推广和使用价值。
