绿原酸抑制巨噬细胞激活的机制研究Δ
2023-11-14郑薇郎静黄西凤肖锐白荷贾济中国人民解放军南部战区总医院麻醉科广州5050中国人民解放军西部战区总医院骨科成都60083
郑薇 ,郎静 ,黄西凤 ,肖锐 ,白荷 ,贾济 #(.中国人民解放军南部战区总医院麻醉科,广州 5050;.中国人民解放军西部战区总医院骨科,成都 60083)
巨噬细胞过度激活与多种炎症相关疾病的发生发展密切相关,包括川崎病、自身免疫性肝病、肾病和心肌疾病等[1—3]。巨噬细胞过度激活后,可释放多种促炎性细胞因子,包括肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、白细胞介素1β(interleukin 1β,IL-1β)和IL-6等。上述促炎性细胞因子可通过血液循环损伤体内多个脏器,继而造成脏器功能受损,甚至危及生命[4]。因此,可通过抑制巨噬细胞的过度激活,降低炎症反应水平,进而控制相关疾病的发生发展[5]。
绿原酸是富含于中药金银花中的一种苯丙素类化合物,具有抗炎、抗氧化、抗过敏和利胆等药理作用[6]。目前,关于绿原酸的相关研究多聚焦在抑制炎症反应方面。有研究报道,绿原酸的抗炎机制包括抑制巨噬细胞/小胶质细胞激活和调节p38分裂原激活的蛋白激酶/Toll样受体等细胞信号通路[7],但其详细抑炎机制尚不明确。骨髓细胞2表达的触发受体(triggering receptors expressed on myeloid cells-2,TREM2)是表达于巨噬细胞上的一种蛋白,可调控巨噬细胞激活程度,抑制炎症反应[8]。本研究使用经典致炎物质脂多糖(lipopolysaccharide,LPS)刺激小鼠RAW264.7巨噬细胞,模拟巨噬细胞激活[9],观察绿原酸对LPS所致巨噬细胞激活的影响和TREM2在其中的作用,为阐明绿原酸的抗炎机制提供实验室证据。
1 材料
1.1 主要仪器
Series 2型细胞培养箱购自美国Thermo Fisher Scientific公司;Infinite 200型酶标仪购自瑞士Tecan公司;Criterion型电泳仪和GelDoc Go型凝胶成像系统均购自美国Bio-Rad公司;FV10i型共聚焦显微镜购自日本Olympus公司。
1.2 主要药品与试剂
绿原酸原料药(批号327-97-9,纯度>95%)、DMEM细胞培养基(批号D5796)、胎牛血清(批号9014-87-7)、二甲基亚砜(dimethyl sulfoxide,DMSO)(批号67-68-5)和MTT(批号298-93-1)均购自美国Sigma-Aldrich公司;TNF-α、IL-1β和IL-6促炎性细胞因子检测试剂盒(批号分别为20220314、20220517、20220418)均购自中国南京建成生物工程研究所;兔抗小鼠诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)(批号ab178945)、核因子κB p65(nuclear factor κB p65,NF-κB p65)(批号ab32536)一抗和山羊抗兔IgG预吸附二抗(批号ab7090)均购自英国Abcam公司;TREM2小干扰RNA(TREM2-small interfering RNA,TREM2-siRNA)(批号HU079401)、乱序-siRNA(SC-siRNA,批号SIC001)和转染液(批号L3287)均购自瑞士Qiagen公司;Cy3标记的山羊抗兔荧光二抗(批号A0516)和青链霉素混合溶液(批号C0223)均购自中国碧云天生物技术有限公司。
1.3 细胞系
实验用小鼠RAW264.7巨噬细胞系获赠于中国科学院上海生命科学研究所。RAW264.7巨噬细胞在DMEM细胞培养基中培养,培养基含10%胎牛血清、10 U/mL的青霉素和10 μg/mL的链霉素。培养箱内空气含95%O2和5%CO2,温度为37 ℃,湿度为100%。每2~3 d更换培养基1次,每周以1∶4的比例传代2次。取对数生长期细胞进行后续实验。
2 方法
2.1 LPS造模浓度的筛选
2.1.1 细胞分组及处理
为确定适宜的LPS刺激强度,将细胞分为Control组和不同质量浓度(1、10、100 ng/mL,参考预实验结果设置)LPS处理组。细胞在含有上述药物的培养基/空白培养基内孵育24 h后,进行以下各项检测。
2.1.2 细胞培养上清液中IL-6水平的检测
将细胞接种于24孔板中,密度为5×105个/孔,24 h细胞贴壁后,按“2.1.1”项下方法分组(每组8个复孔)、给药、培养细胞,然后提取各孔细胞培养上清液200 μL置于离心管内,于4 ℃下5 000 r/min离心30 min。离心结束后,吸弃上清液150 μL,根据IL-6试剂盒说明书检测IL-6水平。
2.1.3 细胞中iNOS蛋白表达水平的检测
采用Western blot法检测细胞中iNOS蛋白的表达水平。将细胞接种于6孔板中,密度为1×106个/孔,24 h细胞贴壁后,按“2.1.1”项下方法分组(每组4个复孔)、给药、培养细胞。培养结束后,吸弃上层培养基,采用磷酸盐缓冲液(phosphate buffer saline,PBS)清洗3次(5 min/次),然后每孔加入细胞裂解液500 μL,在4 ℃下裂解5 min,采用细胞刮将细胞收集至清洁的离心管内,在4 ℃下以12 000 r/min离心30 min后,收集上清液,采用Bradford法进行蛋白定量。取蛋白进行高温变性后,进行聚丙烯酰胺凝胶电泳(电压120 V,电泳时间2 h),并转移至聚偏二氟乙烯膜上(转膜电流200 mA,转膜时间2 h),加入5%脱脂奶粉封闭非特异性抗原,4 ℃孵育过夜;加入稀释的iNOS、GAPDH一抗(稀释比例分别为1∶500、1∶1 000),在37 ℃下孵育4 h;洗膜后加入山羊抗兔IgG预吸附二抗(稀释比例为1∶1 000),室温孵育60 min;使用化学发光法显色后,采用凝胶成像系统成像,使用Image Lab软件分析各条带的灰度值,以iNOS蛋白与GAPDH蛋白的灰度值比值表示iNOS蛋白的表达水平。
2.2 绿原酸给药浓度的筛选
2.2.1 细胞分组及处理
参考相关文献中的绿原酸浓度[10],将细胞分为Control组、LPS处理组(10 ng/mL,按“2.1”项下结果设置,下同)和不同浓度绿原酸干预组(培养基分别含0.01、0.1、1 μmol/L 绿原酸和10 ng/mL LPS),每组8个复孔。将细胞在含有上述药物的培养基/空白培养基中常规孵育24 h后,进行以下各项检测。
2.2.2 细胞培养上清液中TNF-α、IL-1β水平的检测
按“2.1.2”项下方法接种细胞,常规培养,待细胞贴壁后,按“2.2.1”项下方法进行细胞分组、给药与培养,然后根据TNF-α和IL-1β试剂盒说明书检测细胞培养上清液中TNF-α、IL-1β水平。
2.2.3 细胞中iNOS、TREM2蛋白表达水平的检测
采用Western blot法检测细胞中iNOS、TREM2蛋白的表达水平。按“2.1.3”项下方法接种细胞,常规培养,待细胞贴壁后,按“2.2.1”项下方法进行细胞分组(每组4个复孔)、给药、培养,按“2.1.3”项下方法进行指标检测。本实验中iNOS、GAPDH、TREM2、β-actin一抗的稀释比例分别为1∶500、1∶1 000、1∶200、1∶1 000。以iNOS蛋白与GAPDH蛋白的灰度值比值表示iNOS蛋白的表达水平,以TREM2蛋白与β-actin蛋白的灰度值比值表示TREM2蛋白的表达水平。
2.2.4 细胞活力的检测
采用MTT法检测细胞活力。将细胞接种于96孔板中,密度为1×105个/孔,待细胞贴壁后,按“2.2.1”项下方法进行细胞分组(每组8个复孔)、给药和培养。培养结束后,每孔加入MTT溶液(5 mg/mL)20 μL,37 ℃孵育4 h后;吸弃上层培养基,每孔加入150 μL的DMSO,振荡15 min,待甲瓒完全溶解后,取空白孔加150 μL蒸馏水作为空白组,在490 nm波长处使用酶标仪检测各孔吸光度,计算细胞活力。细胞活力(%)=(实验组吸光度-空白组吸光度)/(Control组吸光度-空白组吸光度)×100%。
2.3 TREM2在绿原酸抑制巨噬细胞激活中的作用考察
2.3.1 转染TREM2-siRNA对巨噬细胞中TREM2蛋白表达水平的影响
将细胞接种于6孔板中,密度为1×106个/孔。接种24 h后,吸弃上层培养基,每孔加入含90 pmol的TREM2-siRNA转染液1 mL,37 ℃孵育6 h后,吸弃上层转染液;PBS常温清洗3次,每孔加入细胞裂解液200 μL,裂解30 min后,收集细胞;按“2.2.3”项下方法检测细胞中TREM2蛋白的表达水平。实验重复4次。
2.3.2 细胞分组及处理
为观察TREM2在绿原酸抑制巨噬细胞激活中的作用,将细胞分为Control组、LPS处理组(10 ng/mL LPS)、绿原酸+LPS组[培养基含1 μmol/L绿原酸(按“2.2”项下结果设置)和10 ng/mL LPS]、TREM2-siRNA+绿原酸+LPS组(细胞经TREM2-siRNA处理后,再经1 μmol/L绿原酸和10 ng/mL LPS处理)和SC-siRNA+绿原酸+LPS组(细胞经SC-siRNA处理后,再经1 μmol/L绿原酸和10 ng/mL LPS处理),每组8个复孔。在含有上述药物的培养基/空白培养基中孵育24 h后,进行以下各项检测。
2.3.3 干扰TREM2表达后细胞培养上清液中TNF-α、IL-1β水平的检测
按“2.1.2”项下方法接种细胞,常规培养,待细胞贴壁后,按“2.3.2”项下方法进行细胞分组、给药,根据TNF-α、IL-1β试剂盒说明书检测细胞培养上清液中TNF-α、IL-1β水平。
2.3.4 干扰TREM2表达后细胞中iNOS蛋白染色情况的检测
将细胞接种于共聚焦显微镜专用培养皿中,密度为1×105个/孔。接种24 h后,按“2.3.2”项下方法分组处理,吸去上层培养基,每孔加入4%多聚甲醛溶液1 mL固定,30 min后,PBS清洗3次,5 min/次;随后,每孔加入1%牛血清白蛋白1 mL包被非特异性抗原,30 min后,PBS清洗1次;每孔加入iNOS一抗(稀释比例为1∶100),在4 ℃下孵育12 h后,PBS清洗3次,5 min/次;每孔加入Cy3标记的山羊抗兔荧光二抗(稀释比例为1∶100)200 μL,常温避光孵育90 min;随后,每孔加入100 μL的DAPI染液标记细胞核(蓝色),常温避光孵育5 min后,PBS避光清洗3次,5 min/次;采用共聚焦显微镜在532 nm波长处进行观测,并随机选取视野拍照。
2.3.5 干扰TREM2表达后细胞中TREM2、iNOS和NFκB p65蛋白表达水平的检测
按“2.1.3”项下方法接种细胞,常规培养,待细胞贴壁后,按“2.3.2”项下方法分组、处理,每组4个复孔。培养结束后,按“2.1.3”项下方法操作检测TREM2、iNOS和NF-κB p65蛋白表达水平,iNOS、GAPDH、TREM2、βactin、NF-κB p65一抗的稀释比例分别为1∶500、1∶1 000、1∶200、1∶1 000、1∶200。以iNOS蛋白与GAPDH蛋白的灰度值比值表示iNOS蛋白的表达水平,以TREM2、NFκB p65蛋白与β-actin蛋白的灰度值比值分别表示TREM2、NF-κB p65蛋白的表达水平。
2.4 统计学方法
实验数据采用SPSS 20.0软件进行分析处理。所有数据均采用±s表示,组间差异采用单因素方差分析和Tukey多重比较检验进行分析。检验水准α=0.05。
3 结果
3.1 LPS造模浓度的筛选结果
与Control组[(7.25±2.22) pg/mL]比较,10、100 ng/mL LPS处理组细胞培养上清液中IL-6水平[(121.80±8.85)、(126.30±8.65) pg/mL]均显著升高(P<0.05)。与Control组(0.12±0.02)比较,10、100 ng/mL LPS处理组细胞中iNOS蛋白表达水平(0.84±0.06、0.86±0.04)均显著升高(P<0.05),且10、100 ng/mL LPS处理组间细胞中iNOS蛋白表达水平比较差异无统计学意义(P>0.05)。因此,本研究选择质量浓度为10 ng/mL的LPS进行后续实验。iNOS蛋白表达的电泳图见图1。

图1 不同质量浓度LPS作用下巨噬细胞中iNOS蛋白表达的电泳图
3.2 绿原酸给药浓度的筛选结果
结果(图2)显示,与Control组比较,LPS处理组培养基中TNF-α、IL-1β水平显著升高(P<0.05);与LPS处理组比较,0.01、0.1、1 μmol/L绿原酸干预组细胞培养上清液中TNF-α、IL-1β水平均显著降低(P<0.05)。与Control组比较,LPS处理组细胞中iNOS蛋白表达水平显著升高(P<0.05);与LPS处理组比较,0.1 μmol/L绿原酸干预组细胞中iNOS蛋白表达水平显著降低(P<0.05);与0.1 μmol/L绿原酸干预组比较,1 μmol/L绿原酸干预组细胞中iNOS表达水平显著升高(P<0.05),结果见图3A。与LPS处理组比较,0.1 μmol/L绿原酸干预组细胞中TREM2蛋白表达水平显著升高(P<0.05),结果见图3B。此外,上述各处理组间细胞活力比较差异无统计学意义(P>0.05),结果见图4。以上结果表明,0.1 μmol/L绿原酸可显著抑制LPS对巨噬细胞的激活,并提高TREM2蛋白表达水平,且未对细胞增殖产生显著影响,故本研究选择浓度为0.1 μmol/L的绿原酸进行后续实验。
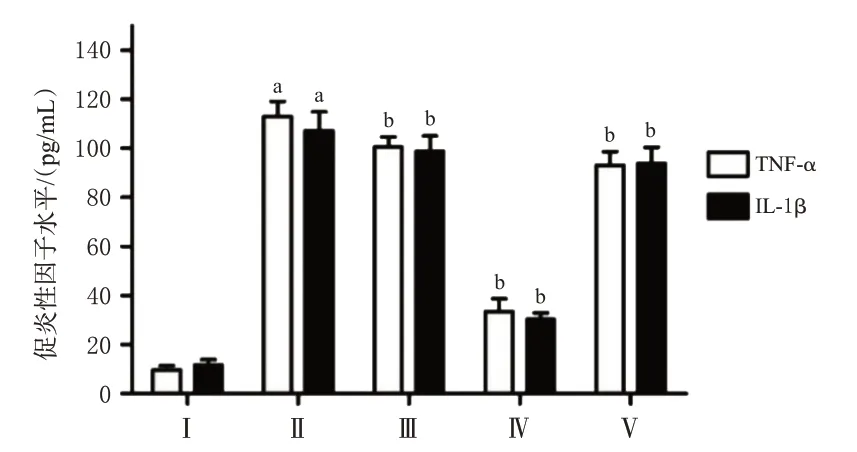
图2 不同浓度绿原酸对巨噬细胞中TNF-α、IL-1β水平的影响(±s,n=8)
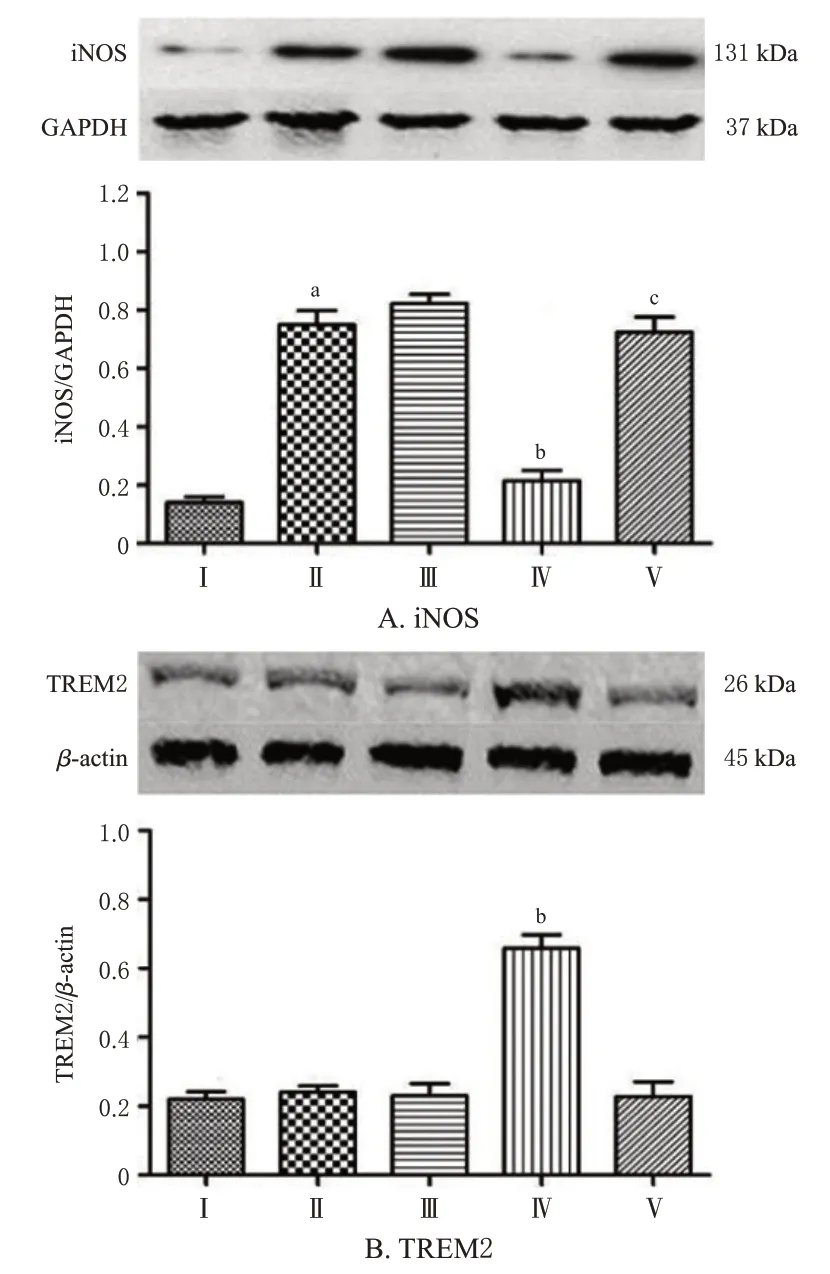
图3 不同浓度绿原酸对巨噬细胞中iNOS、TREM2蛋白表达水平的影响(±s,n=4)

图4 不同浓度绿原酸对巨噬细胞活力的影响(±s,
3.3 TREM2在绿原酸抑制巨噬细胞激活中的作用
3.3.1 转染TREM2-siRNA对巨噬细胞中TREM2蛋白表达水平的影响
结果(图5)显示,TREM2-siRNA可显著降低细胞TREM2蛋白表达水平(P<0.05),表明TREM2-siRNA的干扰有效,可用于后续实验。
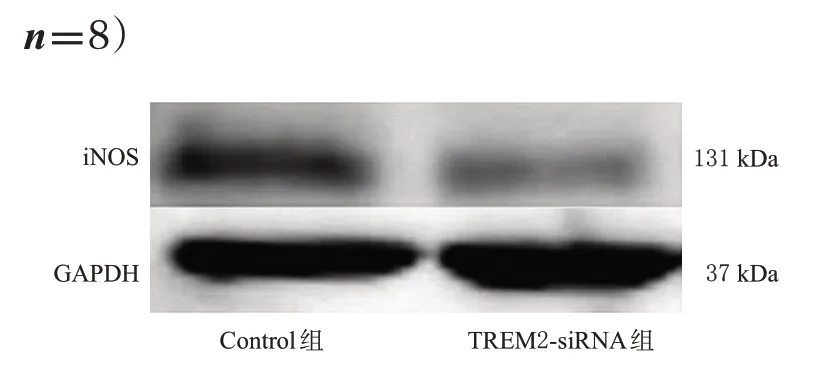
图5 转染TREM2-siRNA干扰细胞TREM2蛋白表达效果验证的电泳图
3.3.2 干扰TREM2表达后对TNF-α、IL-1β水平的影响
与Control组比较,LPS处理组培养基中TNF-α、IL-1β水平均显著升高(P<0.05);与LPS处理组比较,绿原酸+LPS组培养基中TNF-α、IL-1β水平均显著降低(P<0.05);与绿原酸+LPS组比较,TREM2-siRNA+绿原酸+LPS组细胞培养上清液中TNF-α、IL-1β水平均显著升高(P<0.05),而SC-siRNA未对绿原酸抑制TNF-α和IL-1β释放的作用产生显著影响(P>0.05)。结果见图6。

图6 干扰TREM2表达对TNF-α、IL-1β水平的影响(±s,n=8)
3.3.3 干扰TREM2表达对iNOS蛋白染色情况的影响
结果(图7)显示,LPS可明显增加巨噬细胞中iNOS蛋白表达水平(红色),绿原酸可明显降低iNOS蛋白表达水平,TREM2-siRNA显著逆转了绿原酸对iNOS蛋白表达水平的抑制作用,而SC-siRNA未对iNOS的蛋白表达水平产生明显影响。

图7 干扰TREM2表达对iNOS蛋白表达影响的免疫荧光染色图
3.3.4 干扰TREM2表达对TREM2、NF-κB p65和iNOS蛋白表达水平的影响
与Control组比较,LPS处理组细胞中iNOS和NFκB p65蛋白表达水平均显著升高(P<0.05);与LPS处理组比较,绿原酸+LPS组细胞中iNOS和NF-κB p65蛋白表达水平均显著降低、TREM2蛋白表达水平显著升高(P<0.05);与绿原酸+LPS组比较,TREM2-siRNA+绿原酸+LPS组细胞中iNOS和NF-κB p65蛋白表达水平均显著升高、TREM2蛋白表达水平显著降低(P<0.05),TREM2-siRNA明显逆转了绿原酸的上述作用;而SCsiRNA未对绿原酸产生的上述作用造成影响。以上结果表明,绿原酸可通过巨噬细胞TREM2介导,降低LPS引起的巨噬细胞激活。结果见图8、图9。
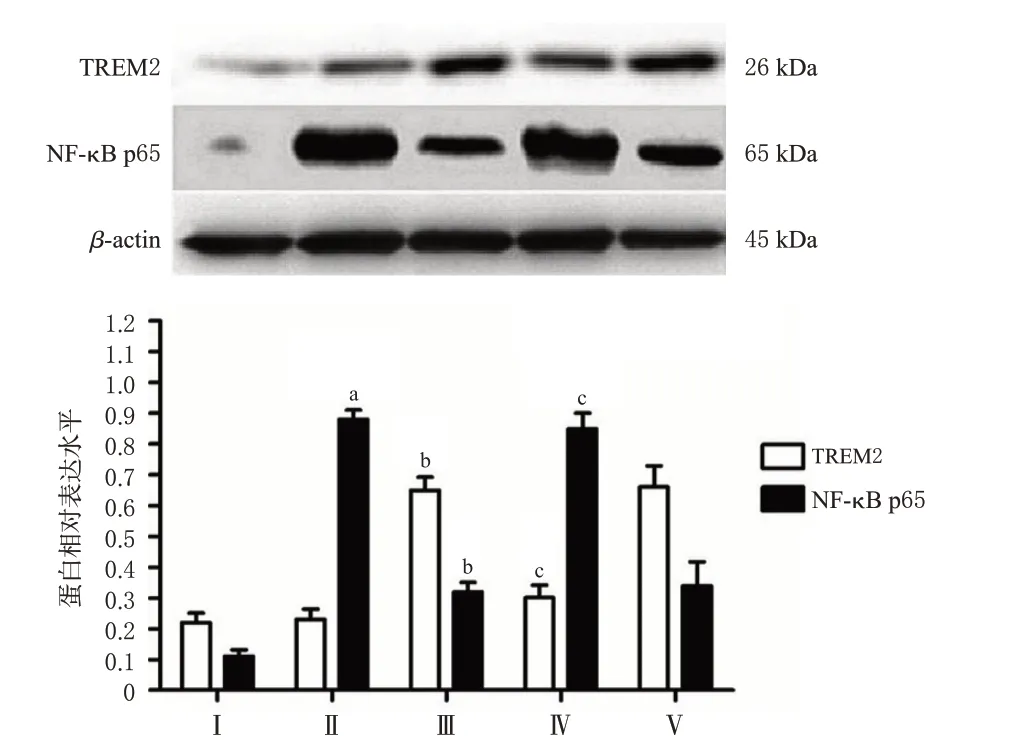
图8 干扰TRME2表达对TREM2和NF-κB p65表达的影响(±s,n=4)

图9 干扰TRME2表达对iNOS表达的影响(±s,n=4)
4 讨论
现代医学研究发现,绿原酸具有抗炎、抗肿瘤、抗氧化和心血管保护等作用[10],但目前其作用机制尚不十分明确,这也大大限制了绿原酸的临床应用。巨噬细胞是一种分布于人体血液循环和肺内的免疫细胞,在炎症反应过程中,巨噬细胞受到刺激后,可分泌大量促炎性细胞因子,如TNF-α、IL-1β和IL-6等,高浓度的促炎性细胞因子可增强人体内的炎症反应程度,对心、脑、肾、肝等多个脏器造成损伤。若巨噬细胞的引起的炎症反应得不到有效控制,可引起全身炎症反应综合征,甚至导致死亡[11]。因此,控制或抑制巨噬细胞的过度激活,被认为是治疗炎症相关疾病的关键环节。目前研究发现,巨噬细胞激活后可处于2种状态:经典激活状态(M1状态)和选择性激活状态(M2状态)。M1状态的巨噬细胞目前认为是有害的,而M2状态的巨噬细胞被认为是有益的。因此,将巨噬细胞调控至M2状态是治疗这类炎症反应相关疾病的关键环节[12—13]。本课题组使用LPS刺激巨噬细胞,引起细胞激活,观察使用绿原酸后对LPS引起巨噬细胞激活水平的影响。结果发现,绿原酸可显著减弱LPS对巨噬细胞的激活作用,降低巨噬细胞的炎症反应程度。促炎性细胞因子(如TNF-α和IL-6)分泌增加和iNOS蛋白表达上调,表明巨噬细胞处于M1激活状态;而绿原酸降低了巨噬细胞促炎性细胞因子分泌和iNOS蛋白表达水平,说明该药物减少了处于M1激活状态的巨噬细胞数量,具有明显的抗炎能力[14]。由于NFκB调控了很多炎症反应相关的基因,且巨噬细胞促炎性细胞因子分泌水平的高低,受NF-κB蛋白表达水平调控[14],因此,本研究检测了巨噬细胞中NF-κB p65的蛋白表达水平。结果发现,LPS刺激可明显升高巨噬细胞中NF-κB p65蛋白表达水平,而绿原酸可明显抑制LPS引起的NF-κB p65蛋白表达上调。以上结果表明,绿原酸可抑制LPS引起的巨噬细胞炎症反应。
髓样细胞触发受体(TREM)是在2000年被发现的一类免疫球蛋白超家族,目前已知TREM家族有3个成员,分别为TREM1、TREM2和TREM3[15]。其中,TREM1和TREM2是目前研究较多的2个TREM家族成员,其结构较为相似,但其功能大有不同——TREM1对炎症反应起着促进和放大的作用,而TREM2对炎症反应起着抑制的作用。研究表明,TREM2表达上调可抑制免疫细胞分泌炎症因子,减轻炎症损伤[16]。研究表明,TREM2基因敲除肺炎模型小鼠与野生型小鼠相比,前者肺炎的严重程度和死亡率显著降低,其机制可能是肺泡巨噬细胞上的TREM2基因敲除后,细胞吞噬能力显著增加,清除细菌等病原微生物的能力增强[17]。另一项研究表明,与巨噬细胞特性类似的小胶质细胞,其TREM2表达上调后,可显著抑制小胶质细胞激活,通过改善小胶质细胞激活状态,即降低M1状态的细胞数量,增加M2状态的细胞数量,减轻脑组织缺血后的炎症反应程度[17]。TREM2是调控炎症细胞(包括小胶质细胞和巨噬细胞)激活状态的重要靶点。早期研究提示,TREM2上调可抑制免疫细胞过度激活,从而抑制促炎性细胞因子分泌,最终降低炎症反应程度[7]。国外也有研究表明,TREM2可通过减轻巨噬细胞激活,减轻炎症反应[18]。在本研究中,研究者采用TREM2-siRNA干扰巨噬细胞的TREM2蛋白表达后,绿原酸在巨噬细胞中产生的抗炎作用被显著逆转。以上结果表明,绿原酸在LPS刺激下的巨噬细胞中产生的抑炎作用,可能是通过细胞上的TREM2蛋白介导的。
综上所述,绿原酸可显著抑制LPS对巨噬细胞的激活,其抗炎作用可能是通过巨噬细胞上的TREM2蛋白介导的。但本研究也有一些不足之处:首先,本研究采用巨噬细胞系作为研究对象,所得结论并非来源于动物或临床研究结果;其次,本研究仅观察了TREM2蛋白的作用,TREM1或TREM3在绿原酸抑制巨噬细胞激活中是否发挥了作用尚不明确。因此在后续研究中,还应采用更多实验对本研究结果进行进一步验证,并探索其更多的作用机制。
