UPLC法同时测定复方龙胆碳酸氢钠片中10种大黄蒽醌类成分及土大黄苷的含量Δ
2023-11-14陈学艳魏文芝张敏娟张耀元阿玉梅彭双青海省药品检验检测院西宁810016国家药品监督管理局中药藏药质量控制重点实验室西宁810016青海省中藏药现代化研究重点实验室西宁810016
陈学艳 ,魏文芝 ,张敏娟 ,张耀元 ,阿玉梅 ,彭双 [1.青海省药品检验检测院,西宁 810016;2.国家药品监督管理局中药(藏药)质量控制重点实验室,西宁 810016;3.青海省中藏药现代化研究重点实验室,西宁 810016]
复方龙胆碳酸氢钠片是由碳酸氢钠、龙胆膏(粉)、大黄膏(粉)、丁香油、薄荷油与适量辅料组成的中西药复方制剂,主要用于肝胃不和所致的胃胀反酸作痛、积食停滞、食欲不振、消化不良等症的治疗。组方中的大黄药材始载于《神农本草经》,为蓼科植物掌叶大黄RheumpalmatumL.、唐古特大黄R.tanguticumMaxim.ex Balf.或药用大黄R.officinaleBaill.的根和根茎,具有泻下攻积、清热泻火、利湿退黄之功效[1]。大黄中蒽醌类物质主要为大黄素型蒽醌,其在肠内亲和力高,可调节肠道蠕动,对胃肠道疾病有良好的疗效[2]。
据统计,2020年版《中国药典》(一部)中收载的150余个含大黄的复方制剂中,大黄的质量控制多采用显微、薄层色谱、高效液相色谱法;土大黄苷作为伪品大黄中的特征性成分,在大黄和大黄流浸膏中均不得检出[3]。本课题组前期采用超高效液相色谱-串联质谱(UPLCMS/MS)法测定了来自8家生产企业的45批次复方龙胆碳酸氢钠片,结果在10批次样品中检出了土大黄苷,检出率达22%[4]。因此,亟须建立一种高效的检测方法以控制含大黄制剂的质量。当采用液质联用技术时,由于中成药成分复杂,直接进样容易导致质谱污染,致使检测结果出现假阳性,并且高效液相色谱法分析时间长、溶剂消耗量大,不利于大批量及应急样品的快速检测[5—6]。鉴于此,本研究建立了UPLC法,并用该法同时测定了复方龙胆碳酸氢钠片中大黄素、大黄酸、大黄酚、芦荟大黄素、大黄素甲醚、芦荟大黄素-8-O-葡萄糖苷、大黄酸-8-O-β-D-葡萄糖苷、大黄素-8-O-葡萄糖苷、大黄素甲醚-8-O-β-D-葡萄糖苷、大黄酚-8-O-β-D-葡萄糖苷共10种发挥主要药理作用且含量较高的大黄蒽醌类成分以及伪品特征成分土大黄苷的含量,从而实现土大黄苷的快速筛查及大黄蒽醌类成分的准确测定,为含大黄复方制剂的质量控制提供参考。
1 材料
1.1 主要仪器
本研究所用的主要仪器包括AcQuity型UPLC仪(美国Waters公司),BS224S型万分之一电子天平、CP225D型十万分之一电子天平(德国Sartorius公司),KQ-500DE型数控超声仪(昆山市超声仪器有限公司),Milli-Q型超纯水系统(美国Millipore公司)等。
1.2 主要药品与试剂
40批复方龙胆碳酸氢钠片来自国内8家药品生产企业,每家企业的样品均有5个批次(样品编号从a1~a5至h1~h5,批号略),处方中大黄以大黄粉或大黄膏的形式投料,均相当于大黄原生药50 mg/片。对照品大黄素(批号110756-201512,纯度98.7%)、大黄酸(批号110757-201607,纯度99.3%)、大黄酚(批号110796-201621,纯度99.2%)、芦荟大黄素(批号110795-201710,纯度98.3%)、大黄素甲醚(批号110758-201616,纯度99.0%)、土大黄苷(批号110794-201708,供检查用)均购自中国食品药品检定研究院;对照品芦荟大黄素-8-O-葡萄糖苷(批号AF20042706,纯度98%)、大黄酸-8-O-β-D-葡萄糖苷(批号AF20030303,纯度98%)、大黄素-8-O-葡萄糖苷(批号AF20042708,纯度98%)、大黄素甲醚-8-Oβ-D-葡萄糖苷(批号AF20042709,纯度98%)、大黄酚-8-O-β-D-葡萄糖苷(批号AF20041628,纯度98%)均购自成都埃法生物科技有限公司;乙腈、甲醇均为色谱纯,水为纯化水,其余试剂均为分析纯。
2 方法与结果
2.1 11种成分的含量测定
2.1.1 对照品溶液的制备
分别精密称取上述11种对照品适量,分别加少量氯仿溶解后再加甲醇稀释,制成0.2 mg/mL的单一对照品储备液。精密量取各单一对照品储备液适量,加甲醇制成约含各成分10 μg/mL的混合对照品溶液。
2.1.2 供试品溶液的制备
取本品20片,称定质量,研细,取约相当于大黄原生药100 mg的细粉,精密称定。精密加入甲醇25 mL,称定质量,于25 ℃超声(功率250 W,频率40 kHz)提取60 min,放冷至室温,再称定质量,用甲醇补足减失的质量,经0.22 μm滤膜滤过,即得供试品溶液。
2.1.3 阴性样品溶液的制备
按复方龙胆碳酸氢钠片的处方比例,制成缺大黄药材的阴性样品,按“2.1.2”项下方法制得阴性样品溶液。
2.1.4 色谱条件
采用Agilent Eclipse Plus C18(3.0 mm×150 mm,1.8 µm)色谱柱,以乙腈(A)-0.1%磷酸溶液(B)为流动相进行梯度洗脱(0~10 min,20%A→60%A;10~11 min,60%A→80%A;11~15 min,80%A→85%A;15~18 min,85%A→20%A);流速为0.3 mL/min;检测波长为254 nm;柱温为30 ℃;进样量为5 µL;检测时间为20 min。
2.1.5 系统适用性试验及专属性考察
取上述混合对照品溶液、阴性样品溶液和供试品溶液(样品编号a1、b1、c1、d1、e1、f1、g1、h1)各5 μL,按“2.1.4”项下色谱条件进样测定,记录色谱图,见图1。结果表明,在该色谱条件下,理论板数均不小于33 820,各色谱峰与相邻峰的分离度均大于1.5,各成分测定不受其他组分的干扰,并且阴性样品在11种检测成分出峰时间处均未出现干扰峰。

图1 混合对照品、阴性样品和供试品的UPLC图
2.1.6 线性关系考察及检测限、定量限测定
分别精密吸取“2.1.1”项下11种单一对照品储备液,以甲醇逐步稀释制成各成分质量浓度均分别约为0.5、1.0、5.0、10.0、20.0 μg/mL的11种混合对照品溶液,其中大黄酚及大黄酚-8-O-β-D-葡萄糖苷的线性最高点质量浓度放宽至约50.0 μg/mL,土大黄苷放宽至约80.0 μg/mL。按“2.1.4”项下色谱条件进样测定,以峰面积为纵坐标(Y)、各对照品质量浓度为横坐标(X)绘制标准曲线,建立回归方程(表1)。结果表明,各成分在各自检测的质量浓度范围内与峰面积线性关系良好(r≥0.999 3)。
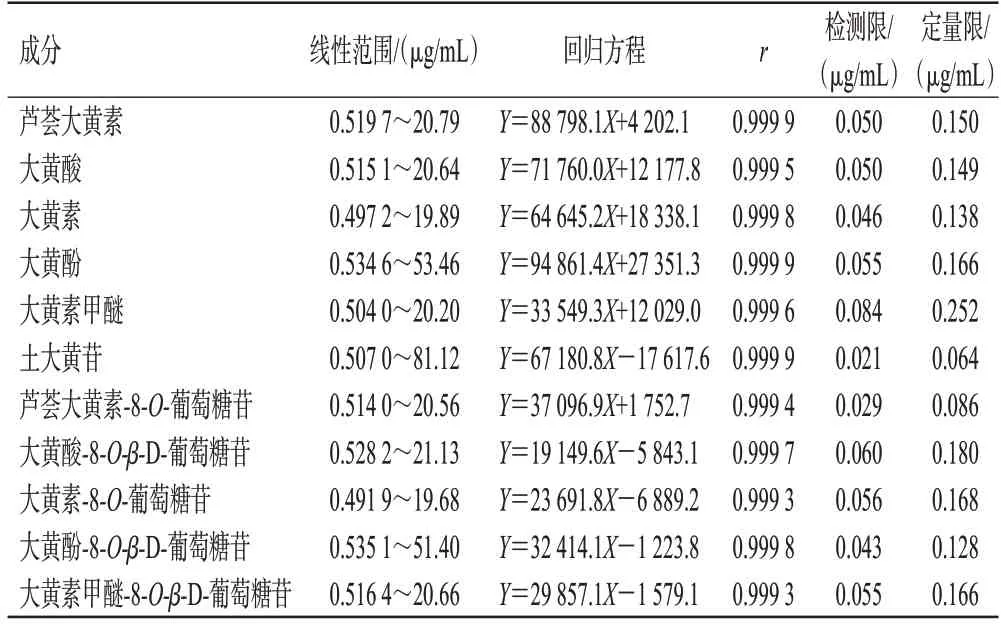
表1 芦荟大黄素等11种成分的线性关系考察结果及检测限、定量限
另按“2.1.1”项下方法稀释各成分的单一对照品储备液,按“2.1.4”项下色谱条件分别进样5~10 μL测定,以信噪比3∶1测得各成分的检测限;同法分别进样15~25 μL测定,以信噪比10∶1测得各成分的定量限。结果见表1。
2.1.7 精密度试验
精密吸取“2.1.1”项下混合对照品溶液5 μL,按“2.1.4”项下色谱条件连续进样测定6次,记录峰面积。结果显示,芦荟大黄素-8-O-葡萄糖苷、大黄酸-8-O-β-D-葡萄糖苷、土大黄苷、大黄素-8-O-葡萄糖苷、大黄酚-8-O-β-D-葡萄糖苷、大黄素甲醚-8-O-β-D-葡萄糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为1.02%、1.55%、0.61%、0.49%、0.90%、0.74%、1.18%、0.83%、0.86%、0.77%、1.32%(n=6),表明仪器精密度良好。
2.1.8 重复性试验
分别称取同一批样品(编号f1)6份,每份0.6 g,精密称定,置于50 mL具塞锥形瓶中,按“2.1.2”项下方法制备供试品溶液,按“2.1.4”项下色谱条件进样测定,记录峰面积,以外标法按峰面积计算样品含量。结果显示,样品中芦荟大黄素-8-O-葡萄糖苷、大黄酸-8-O-β-D-葡萄糖苷、大黄素-8-O-葡萄糖苷、大黄酚-8-O-β-D-葡萄糖苷、大黄素甲醚-8-O-β-D-葡萄糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的平均含量分别为0.020 2、0.021 5、0.175 9、0.136 7、0.016 6、0.012 3、0.014 5、0.018 7、0.189 0、0.084 5 mg/g,RSD分别为2.68%、1.72%、2.16%、2.66%、2.93%、2.04%、1.95%、1.55%、1.87%、1.36%(n=6)。另取样品(编号a1)同法操作,得样品中土大黄苷的平均含量为2.891 2 mg/g,RSD为0.83%(n=6)。上述结果表明本方法重复性良好。
2.1.9 稳定性试验
分别取按“2.1.2”项下方法制备的样品编号为f1和a1的供试品溶液,在室温下放置0、2、4、8、12、24 h后按“2.1.4”项下色谱条件进样测定,记录峰面积。结果显示,芦荟大黄素-8-O-葡萄糖苷、大黄酸-8-O-β-D-葡萄糖苷、土大黄苷、大黄素-8-O-葡萄糖苷、大黄酚-8-O-β-D-葡萄糖苷、大黄素甲醚-8-O-β-D-葡萄糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为1.21%、0.82%、1.99%、0.85%、0.77%、0.86%、1.52%、1.21%、0.82%、1.40%、0.83%(n=6),表明供试品溶液在室温下放置24 h内稳定。
2.1.10 加样回收率试验
称取已知含量的样品(编号f1、a1)各6份,每份0.30 g,精密称定,分别置于50 mL具塞锥形瓶中,精密加入各成分质量浓度约为样品含量100%的混合对照品溶液,按“2.1.2”项下方法制备供试品溶液,按“2.1.4”项下色谱条件进样测定,计算加样回收率。结果显示,各成分的平均加样回收率为96.82%~98.92%,RSD均不大于1.74%(n=6),表明本方法准确度良好。
2.1.11 样品含量测定
取各批次样品适量,分别按“2.1.2”项下方法制备供试品溶液,按“2.1.4”项下色谱条件进样分析,记录峰面积,以外标法按峰面积计算样品含量。每个样品测定3次,取平均值。结果见表2。
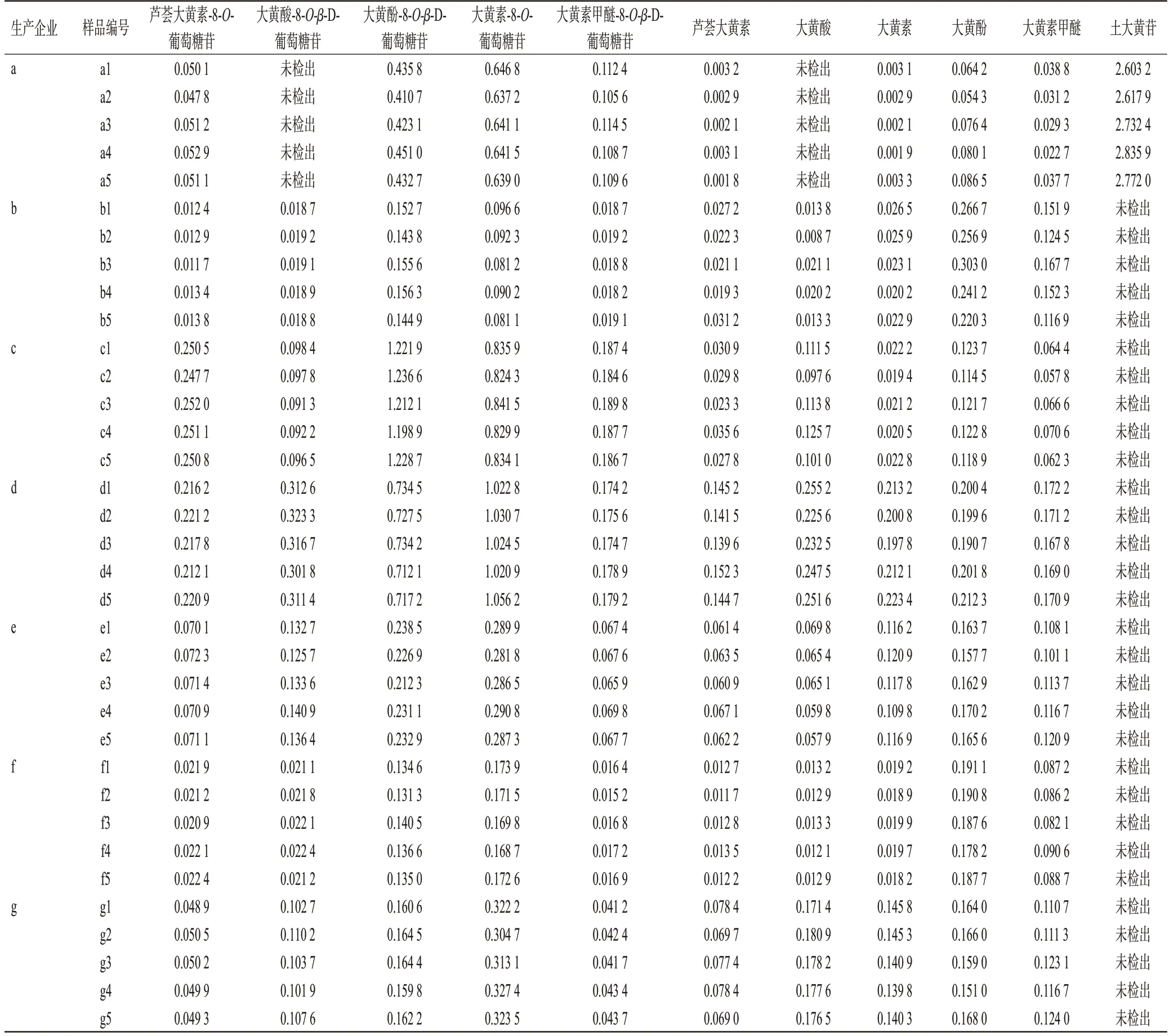
表2 40批样品中10种大黄蒽醌类成分及土大黄苷的含量测定结果(n=3,mg/g)
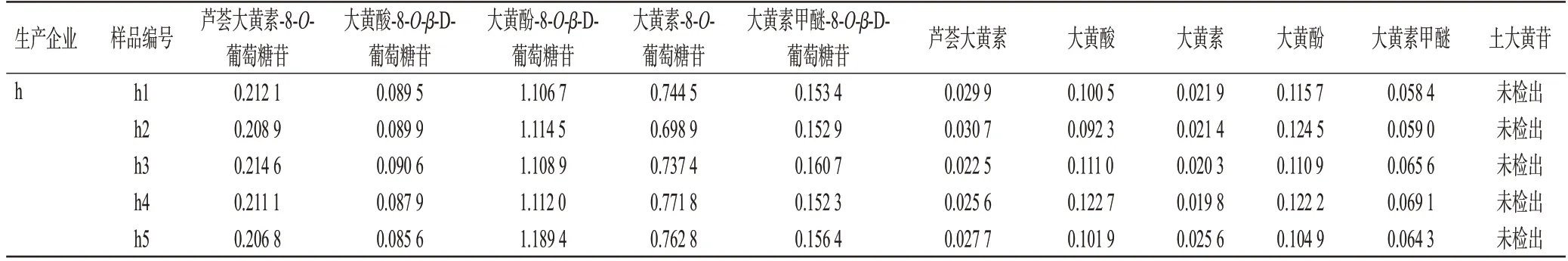
续表2
2.2 主成分分析
2.2.1 相关性分析
在进行主成分分析前,先利用SPSS 25.0软件进行KMO检验和Bartlett检验,得KMO值为0.635(>0.5)提示可以进行主成分分析;Bartlett检验结果显示,P<0.001,提示各变量间存在显著的相关性,可进行因子分析及各变量间的共性评价。
2.2.2 特征值和方差贡献率分析
利用SPSS 25.0软件对样品中11个指标成分进行主成分分析,结果见表3。由表3可知,前3个主成分的累计方差贡献率为95.533%,可反映样品中11个指标成分的大部分信息,因此提取这3个主成分对40批次样品中11个指标成分的含量进行综合分析,进而对该复方制剂进行质量评价[7—8]。

表3 主成分的特征值、方差贡献率及累计方差贡献率
2.2.3 不同生产企业样品的综合评价
采用SPSS 25.0软件,根据“成分矩阵”中各主成分对应的载荷,选择菜单中“转换”“计算变量”,得到特征向量,根据特征向量矩阵建立主成分分析模型。F1、F2、F3为3个主成分的得分,计算公式为:F1=向量1C1+向量2C2+向量3C3+……向量11C11,其中C1、C2、C3……C11分别为11个指标成分标准化后的变量。F2、F3同法计算。以各主成分的方差贡献率对主成分得分进行加权平均,得到综合得分(F):F=49.704F1+35.905F2+9.924F3,结果见表4。由表4可知,综合得分排前3名的分别为d、c、h企业样品,表明这3家生产企业投料用大黄药材的指标成分含量接近,且质量较优。
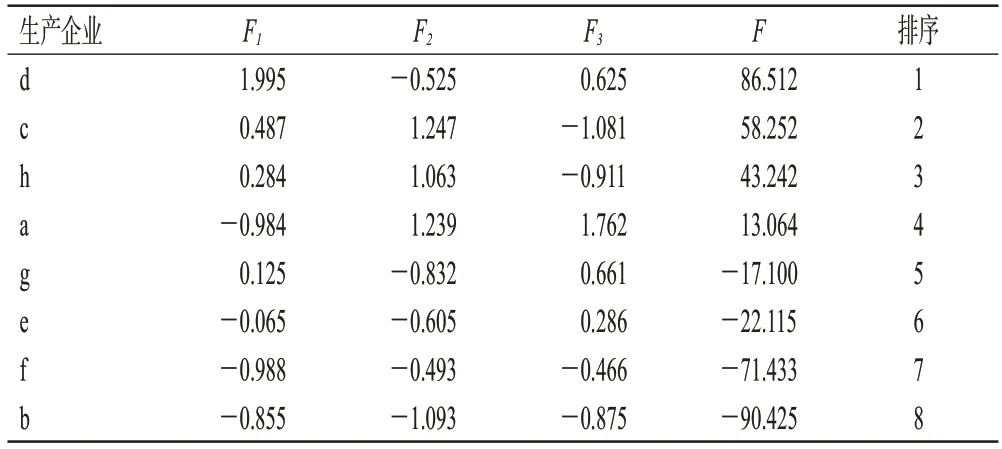
表4 8个生产企业样品的主成分分值、综合得分及排序
将40批样品中11个指标成分的含量测定结果导入SIMCA 14.1软件进行标准化处理,生成二维散点图,详见图2。由图2可知,40批样品可分成4类:a和d企业的样品分别自成一类,f、b、g、e企业的样品为一类,c、h企业的样品为一类。

图2 主成分分析的散点图
2.3 聚类分析
采用SPSS 25.0软件,将40批次样品中11个指标成分的含量经标准化处理后,以瓦尔德法、欧氏距离为度量标准进行聚类分析,输出垂直方向谱系图,结果见图3。由图3可知,当欧氏距离为14时,40批次样品可聚为4类:a和d企业的样品分别自成一类,f、b、g、e企业的样品为一类,c、h企业的样品为一类。聚类分析结果与主成分分析结果一致。

图3 8家生产企业40批次样品的聚类分析树状图
3 讨论
目前,业界对含大黄的复方制剂中大黄等多种处方成分的测定多采用高效液相色谱法,该法分析时间较长,约60~80 min。本研究采用小颗粒填料色谱柱(粒径<2 μm)结合超高压输液泵(压力>105 kPa),可同时测定复方龙胆碳酸氢钠片中10种大黄蒽醌类成分及1种伪品特征成分土大黄苷的含量,并可缩短分析时间至20 min,检测灵敏度高、准确性良好,可显著改善色谱峰展宽和拖尾的现象,实现在含大黄的复方制剂中土大黄苷的快速筛查及大黄蒽醌类成分的准确测定。同时,本研究考察了甲醇-水、乙腈-水、甲醇-0.1%磷酸溶液、乙腈-0.1%磷酸溶液等不同流动相系统的洗脱效果。结果发现,甲醇洗脱能力较乙腈弱,且色谱峰较宽影响分离度,存在大黄素-8-O-葡萄糖苷峰与大黄酚-8-O-β-D-葡萄糖苷峰、芦荟大黄素峰与大黄酸峰不能有效分离的情况;而采用乙腈洗脱时,大黄素甲醚-8-O-β-D-葡萄糖苷和大黄素甲醚的色谱峰峰形在以0.1%磷酸溶液为水相时较好,故最终采用乙腈-0.1%磷酸溶液为流动相进行梯度洗脱。在此流动相系统下,11个成分各相邻色谱峰的分离度均大于1.5,理论板数均不小于33 820。
本研究分别考察了甲醇体积分数为50%、70%、100%,提取时间为30、60、90 min的样品提取效果。结果发现,大黄素甲醚、大黄酸-8-O-β-D-葡萄糖苷和大黄素甲醚-8-O-β-D-葡萄糖苷等成分在甲醇体积分数大于70%且提取时间达30 min时,其含量才能逐渐增加,而提取60 min与提取90 min时的含量无明显差别。考虑到实际操作的可行性,本研究最终确定了文中提取方法,即采用100%甲醇超声提取60 min。
本研究应用主成分分析法提取的前3个主成分可以概括40批次样品中11个指标成分的大部分信息;利用综合得分排序,可得到d、c、h企业样品的综合质量较优。聚类分析和主成分分析结果一致,均将40批次样品分为4类:a和d企业的样品分别自成一类,c、h企业的样品为一类,f、b、g、e企业的样品为一类。a企业的样品中检出了伪品特征成分土大黄苷,且未检出大黄酸和大黄酸-8-O-β-D-葡萄糖苷,与其他企业样品质量差异较大,可判定该企业使用了伪品大黄投料,样品质量较差。
综上所述,本研究所建UPLC方法稳定、可靠,可用于同时测定复方龙胆碳酸氢钠片中10种大黄蒽醌类成分及土大黄苷的含量;结合主成分分析、聚类分析等化学计量学方法,可用于该制剂的质量控制。
