塑料粒子电极对电催化降解硝态氮增强作用的试验研究
2023-11-06褚龙威赵群芳李浩慷黄翀许振芹丁原红
褚龙威, 赵群芳, 李浩慷, 黄翀, 许振芹, 丁原红
(1.青岛科技大学 环境与安全工程学院, 山东 青岛 266000; 2.江苏裕隆环保有限公司, 江苏 宜兴 214200;3.宁阳县生态环境监控中心, 山东 宁阳 271411)
目前国内运行的各类污水处理厂大都面临着出水氨氮、 总氮波动或超标等问题, 需要对现有的污水处理工艺进行深度脱氮方面的升级或提标改造。很多水厂采用深床滤池等反硝化生物脱氮方案, 虽然有运行成本较低的优势, 但普遍具有操作复杂、工艺流程加长、 需要外加碳源、 降解速率慢和调试周期长等不足[1-2]。 若采用金属还原、 化学混凝沉淀等各种物化处理方案, 虽然脱氮效果显著, 但存在药剂耗量大、 运行成本高、 化学污泥产量大、 有二次污染等缺点[3]。
电催化反应用于硝态氮废水的深度脱氮, 除了极板和电耗, 没有化学药品投加和污泥产生, 被认为是一种绿色的污水脱氮技术。 采用铁/铜[4]或合金[5]做阴极可对硝态氮进行还原脱氮, 但除了可以将大部分硝态氮转化为氮气溢出水体实现废水的有效脱氮外, 硝态氮的电催化中间产物成分复杂, 作为溶解性氮化物仍然残留在水体中, 水体总氮仍然不能得到有效去除[6]。 目前三维电解反应器用于硝态氮的电催化降解, 可有效减少中间产物并提高总氮的去除率[7], 活性炭(AC)[8]、 氧化铝(Al2O3)[9]、钢渣[10]等材料均被探讨用于制备导电粒子, 参与硝态氮的电催化脱氮降解过程, 但这些作为导电粒子载体的材料本身, 普遍存在密度大、 混合搅拌动力消耗大、 制作和运行成本高[11]等缺陷。
本课题组采用塑料作为基体, 用于制备导电粒子, 与Ti/RuSn 电极一起构建三维电催化反应器,探究其对硝态氮电催化还原降解过程的影响作用。
1 材料与方法
1.1 试验装置
电催化脱氮试验装置如图1 所示, 采用Ti/RuSn电极作为阳极, 表面改性塑料粒子为粒子电极。 电解槽由有机玻璃制成, 尺寸为50 mm × 25 mm ×110 mm, 有效容积为120 mL, 极板间距为20 mm,电催化反应时间为0 ~2.5 h。 二维电催化反应过程时, 不投加塑料导电粒子; 三维电催化反应过程时, 投加一定量塑料导电粒子。
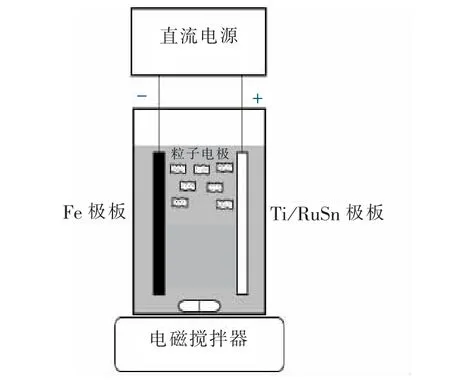
图1 电催化脱氮装置示意Fig.1 Electrocatalysis denitrification device
1.2 试验材料
塑料粒子电极材料来自移动床生物膜反应器(MBBR)中常用的塑料载体, 将其剪裁成相同尺寸的碎片, 浸泡于10% NaOH 溶液中90 ℃水浴30 min, 随后在去离子水中超声15 min, 再将其浸泡于10% 稀硫酸中, 经过相同的水浴和超声清洗过程后, 85 ℃下干燥30 min, 密封备用[12]。 称取0.05 g 高纯石墨烯、 0.15 g SnO2、 0.15 g RuCl3·xH2O、 0.03 g PdCl2, 量取10 mL 去离子水、 10 mL的聚四氟乙烯(PTFE)分散液在烧杯中混合均匀并超声搅拌30 min。 将超声完成的涂料使用小刷子反复多次均匀涂覆在碎片状的塑料表面上, 115 ℃下烘干2 h, 冷却至室温后重复以上操作3 遍, 将表面改性的碎片塑料再切割成5 mm×5 mm 左右的小碎片, 制得改性塑料粒子电极。
1.3 试验用水
模拟硝态氮废水为硝酸盐与去离子水配置的溶液, 其中主要目标污染物硝态氮的质量浓度为300 mg/L。
实际废水取自河北某化工厂的生产车间, 主要水质指标为: COD 3700 mg/L, 硝态氮238.59 mg/L, 氨氮76.61 mg/L, 总氮379.25 mg/L。
1.4 试剂与仪器
UV-1800 型紫外分光光度计, D-MAX 2500/PC 型X 射线衍射仪, 扫描电子显微镜SEMXMAX50, CHI600E 型电化学工作站。
1.5 试验方法
电催化脱氮试验在电磁搅拌器上进行, 反应一段时间后取样, 分析样品中总氮、 硝态氮、 亚硝态氮和氨氮的浓度, 考察各影响因素对硝态氮电催化降解效果的影响; 对电催化反应前后的极板电极和塑料粒子电极表面固体采样, 进行SEM、 XRD 表面特性分析; 对极板电极进行CV 电化学特征分析。
1.6 分析方法
硝态氮、 亚硝态氮、 氨氮浓度等都采用国标方法测定[13-15]。
2 结果与讨论
在三维电催化反应过程中, 塑料粒子电极的投加量、 氯化钠的浓度、 反应时间以及塑料粒子电极化学性能的稳定性都是影响硝态氮降解的关键因素。
2.1 塑料粒子电极对模拟废水的去除效果
2.1.1 塑料粒子电极投加量对硝态氮降解效果的影响
在硝态氮初始质量浓度为300 mg/L, 电压为10 V, 氯化钠投加量为0.1 g/L, 反应时间为2.5 h的条件下, 考察塑料粒子电极投加量对硝态氮催化降解效果的影响, 结果如图2 所示。
塔尔巴哈台所属厄鲁特蒙古共六千余人,十个人里一两个人共有两个骆驼、羊等,其他人几乎没有牛羊,从塔尔巴哈台到科布多所属青格里河等地途中,竟吃狗肉和饿死的人肉走过来的。[注]中国边疆史地研究中心、中国第一历史档案馆合编:《清代新疆满文档案汇编》280,“同治五年六月十六日呼图克图喇嘛棍噶扎勒参奏闻塔尔巴哈台城失陷情形折”,广西师范大学出版社,2012年,第7页。
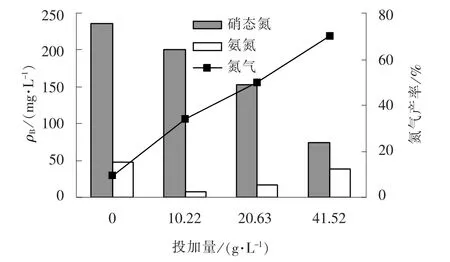
图2 塑料粒子电极投加量的影响Fig.2 Effect of plastic particle electrodes addition
由图2 可知, 随着塑料粒子电极投加量的提高, 硝态氮和总氮的去除率都有明显的提高, 当塑料粒子电极投加量为41.52 g/L 时, 硝态氮和总氮去除率达到最高, 分别为75.92% 和70.08%, 相比二维电解反应器(塑料粒子电极投加量为0), 其去除率分别提高了39.73%和45.39%, 并且产物中氨氮含量也处于较低的浓度水平。
塑料粒子电极表面负载有Ru 和Sn 等元素,对氨氮中的氮和水分子中的氧有良好的选择性, 可将氨氮吸附并转化为N2, 将水分子的H—O 键断裂生成H·[16], 如电化学方程式所示, 阴极表面会产生大量H·, H·攻击吸附在塑料粒子电极和阴极表面的, 使N—O 键断裂,还原为,在Ru 表面形成中间产物NOx。 2 种NOx相遇形成N2, 金属催化剂促进了硝态氮的电催化降解效果[17]:
2.1.2 氯化钠投加量对硝态氮降解效果的影响
电催化过程中电解质参与电子传递和脱氮反应过程, 在硝态氮初始质量浓度为300 mg/L, 电压为10 V, 反应时间为2.5 h, 塑料粒子电极投加量为41.52 g/L 的条件下, 考察氯化钠(氯离子)投加量对硝态氮降解效果的影响, 结果如图3 所示。
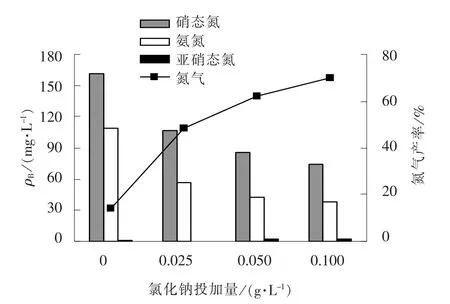
图3 氯化钠投加量的影响Fig.3 Effect of sodium chloride addition
由图3 可知, 相比于未投加氯化钠, 当氯化钠投加量为0.1 g/L 时, 硝态氮和总氮的去除率分别提高了28.69% 和50.79%, 而氨氮的质量浓度则从108.98 mg/L 下降至38.52 mg/L。
Ti/RuSn 阳极是具有很强氧化和析氯能力的DSA 阳极[18](钛基氧化物涂层或尺寸稳定阳极Dimensionally Stable Anode), 能够产生大量的·OH,有助于将氧化成N2[19]。 试验使用的塑料粒子电极的催化剂与Ti/RuSn 阳极采用相同成分, 但塑料粒子电极具有比Ti/RuSn 阳极更大的表面积, 增大了硝态氮等污染物与电极的接触面积, 可促进硝态氮更完全的电催化降解, 因此, 塑料粒子电极与Ti/RuSn 阳极构建的三维电极反应器理论上具有比二维电极反应器更好的处理效果。 氯离子易在Ti/RuSn 阳极被氧化为氯气、 次氯酸, 氨氮有可能被通过折点氯化的过程予以去除[20], 在反应过程中可实现Cl-→Cl2→HOCl →Cl-的氧化还原循环[21],可有效去除亚硝态氮或氨氮等硝态氮中间电催化产物, 实现对硝态氮的选择性电催化脱氮。 根据硝态氮去除效果, 确定氯化钠的投加量为0.1 g/L。
2.1.3 反应时间对硝态氮降解效果的影响
在硝态氮初始质量浓度为300 mg/L, 电压为10 V, 塑料粒子电极投加量为41.52 g/L, 氯化钠投加量为0.1 g/L 的条件下, 考察电催化反应时间对硝态氮电催化降解效果的影响, 结果如图4 所示。
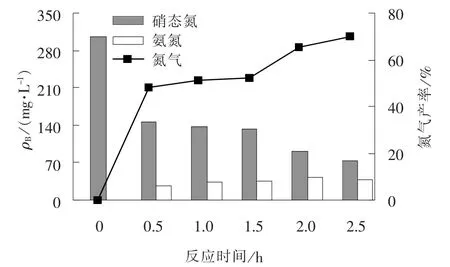
图4 反应时间的影响Fig.4 Effect of reaction time
由图4 可知, 随着反应时间的延长, 硝态氮和极板与塑料粒子电极的接触反应时间延长, 硝态氮和总氮去除率将逐渐提升, 当反应时间为2.5 h 时,硝态氮和总氮去除率分别为75.92% 和70.08%, 效果最佳。
2.1.4 塑料粒子电极使用次数对硝态氮降解效果的影响
塑料粒子电极性能的稳定性也是制约三维电催化反应器运行成本的重要因素。 在硝态氮初始质量浓度为300 mg/L, 电压为10 V, 塑料粒子电极投加量为41.52g/L, 氯化钠投加量为0.1 g/L, 反应时间为2.5 h 的条件下, 考察塑料粒子电极性能的稳定性, 结果如图5 所示。
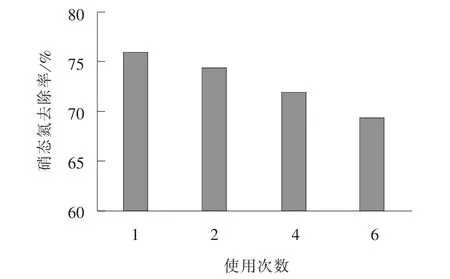
图5 塑料粒子电极使用次数的影响Fig.5 Effect of usage count of plastic particle electrode
由图5 可知, 随着重复使用次数的增加, 硝态氮的去除效率逐渐降低, 分析其原因是塑料粒子电极表面的催化剂部分脱落, 导致电催化过程对硝态氮的去除率整体下降。 在第6 次重复使用后, 三维电催化对硝态氮的降解效率仍能达到69.29%, 说明塑料粒子电极性能具有一定的稳定性。
2.2 塑料粒子电极对实际废水的适用性
在对硝态氮模拟废水电催化脱氮试验进行了基本运行参数的探索后, 在上述最佳试验条件下, 分别采用二维电催化反应器和三维电催化反应器对实际废水进行脱氮试验研究, 结果如图6 所示。
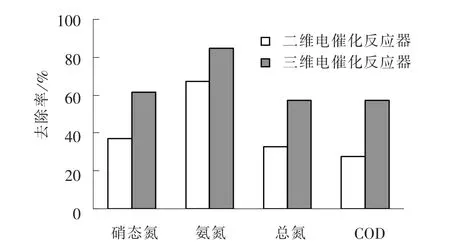
图6 二维和三维电催化反应器对实际废水的降解效果Fig.6 Effect of 2D and 3D electrocatalysis reactors on actual wastewater degradation
由图6 可以看出, 二维电催化反应器对硝态氮、氨氮、 总氮、 COD 的去除率分别为36.83%、 67.01%、32.81%、 27.41%, 而添加了塑料粒子电极的电催化反应器对硝态氮、 氨氮、 总氮和COD 的去除率相应地提升到了61.92% 、 85.07% 、 57.07% 和57.02%, 表明塑料粒子电极对实际废水中包括硝态氮在内的各种污染物的去除都有较为明显的增强效果。
2.3 自由基淬灭试验
塑料粒子电极的加入强化了对总氮的去除效果, 推测在三维电催化反应过程中有自由基参与硝态氮的降解过程。 叔丁醇是·OH 和H·的清除剂,考察叔丁醇的加入对硝态氮和总氮去除效果的影响, 结果如图7 所示。
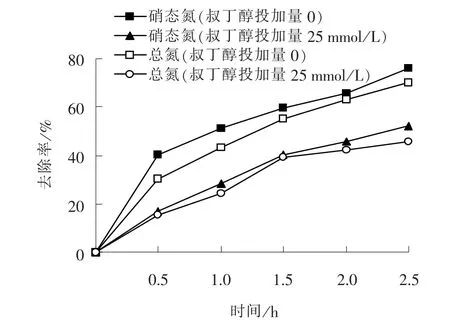
图7 投加叔丁醇对脱氮过程的影响Fig.7 Effect of tertiary butanol dosage on denitrification
由图7 可知, 当叔丁醇添加量为25 mmol/L时, 硝态氮去除率从75.92% 下降至52.05%, 总氮去除率从70.08%下降至45.50%, 可推测自由基贡献了24.58%的总氮去除率。
采用N,N-二乙基-1,4-苯二胺(DPD)分光光度法[22]测定电催化脱氮过程中的游离氯和总氯,随着反应的进行, 游离氯质量浓度呈现出递增的趋势, 最高可达55.56 mg/L, 而在初始氨氮质量浓度为30 mg/L 时, 自由氯则先增加后减少, 最后基本完全分解, 这说明自由基和氯离子参与了硝态氮的电催化脱氮[23], 反应方程式如下:
2.4 塑料粒子电极表征分析
塑料粒子电极负载了石墨烯、 Pd-Sn、 Ru-Sn双金属催化剂和Pd 的氧化物[24]。 Pd-Sn 活性位点可以有效提高硝酸盐的还原活性, Sn 可以促进到这一决定步骤[25]。 塑料粒子电极的XRD 图谱如图8 所示。
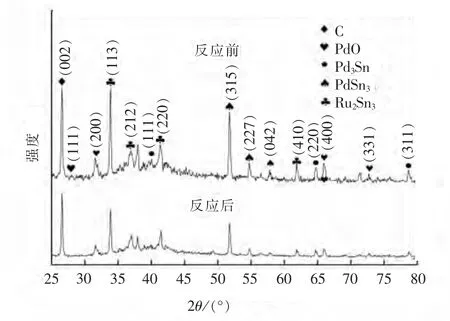
图8 塑料粒子电极反应前后的XRD 图谱Fig.8 XRD spectrum of plastic particles electrodes before and after reaction
由图8 可知, 反应前和反应后的XRD 谱图变化不大, 这说明塑料粒子电极具有一定的稳定性,反应后峰值降低, 表明催化剂的性能有一定程度的下降, 但仍保持较高的催化性能。
对表面改性塑料颗粒的原始状态、 涂层状态和使用状态进行SEM 表征, 结果如图9 所示。

图9 塑料粒子电极SEM 表征图片Fig.9 SEM phenogram of plastic particles electrodes
由图9 可以看出, 改性塑料基板的表面粗糙且起皱, 这增强了金属催化剂的负载量以及与主电极的传质能力。
3 结论
(1) 在模拟废水硝态氮的质量浓度为300 mg/L, 电压为10 V, 氯化钠投加量为0.1 g/L, 塑料粒子电极投加量为41.52 g/L, 反应时间为2.5 h 的条件下, 三维电催化过程对硝态氮和总氮的去除率分别为75.92% 和70.08%, 相比二维电催化反应器,相应的去除率分别提高了39.73% 和45.39%, 试验结果表明, 塑料粒子电极对硝态氮的电催化降解有增强作用。
(2) 塑料粒子电极表面负载的石墨烯、 Pd-Sn 和Ru-Sn 双金属催化剂, 自由基淬灭试验证明了·OH和H·的产生, 该自由基有利于促进还原硝态氮, 塑料粒子电极能增强降解去除实际废水中的硝态氮,并具有可重复利用性。
(3) 塑料粒子电极、 氯离子和Ti/RuSn 阳极,可协同促进硝态氮中间产物的进一步降解, 实现更高的硝态氮、 总氮去除率和氮气产率, 该技术具有一定的应用前景。
