日立7600检测血清淀粉样蛋白A的实验室性能验证
2023-11-06何一枭吴前星熊燏蔡群芳李秀文赫娜
何一枭 吴前星 熊燏 蔡群芳 李秀文 赫娜*
1 海南医学院热带医学院 (海南 海口 571199)
2 海南省肿瘤医院 (海南 海口 570312)
3 昆明医科大学海源学院 (云南 昆明 650000)
内容提要: 目的:日立7600型全自动生化分析仪检测血清淀粉样蛋白A的性能验证。方法:参照CLSI及CNAS有关检测系统性能验证文件方法通过实验对血清淀粉样蛋白A的精密度、正确度、线性范围、临床可报告范围、参考区间进行评价。结果:批间精密度变异系数分别为5.38%,2.29%,小于规定声称值10%;批内精密度变异系数分别为4.87%、1.82%,均小于规定声称值8%。正确度偏倚为-2.1%,<10%;临床可报告范围上限为3072mg/L;厂家说明书的线性范围、参考范围符合要求。结论:日立7600全自动生化分析仪搭载重庆中元生物技术有限公司血清淀粉样蛋白A试剂盒检测血清淀粉样蛋白A符合质量要求,能够为临床提供可靠的依据。
血清淀粉样蛋白A(Serum Amyloid A,SAA)是一种多基因编码的非特异性急性正向时相反应蛋白,人类编码该蛋白的基因序列集中在十一号染色体短臂上,长短为150kb,目前临床上检测的SAA均为SAA1和SAA2基因编码的急性期SAA(A-SAA)[1,2]。SAA半衰期短,当人体遭遇病毒感染、炎症刺激时,SAA比C反应蛋白和降钙素原更敏感,可在3~6h内升高100~1000倍,因而在感染性疾病的诊断和鉴别方面,SAA更受临床医生的青睐,在临床中的使用日益广泛[3-5]。有研究表明,SAA可以诱导基质金属蛋白酶表达、调节血管生成,在肿瘤细胞侵袭转移过程中起重要作用[6]。SAA在预示疾病加重及呼吸困难加重或痰液性状改变等程度变化优于C反应蛋白,对鉴别有呼吸衰竭危险的住院患者有帮助[7,8]。SAA还可以指导胃溃疡患者临床用药、在早期胃癌的诊断、鉴别诊断以及分期中具有重要作用,对评估胃癌患者的预后情况有重要应用价值[9]。此外,SAA在心血管疾病、2型糖尿病、银屑病、移植排斥反应等多种疾病的临床检测中亦发挥重要作用。
依据《医学实验室质量和能力认可准则》和ISO15189文件要求,临床实验室应对实验室内检测系统的检测性能进行验证[10-14]。因此,本研究为保证临床实验室检测SAA能够获得准确可靠的结果,遵照CNAS指南有关检测系统性能验证文件要求对本科室使用的日立7600全自动生化分析仪搭载重庆中元生物技术有限公司SAA试剂盒检测SAA的分析性能进行验证。
1.资料与方法
1.1 一般资料
样本来源:海南省肿瘤医院体检中心体检者的新鲜血清标本。样本处理1:分别混合、离心高浓度样本和低浓度样本,得到本实验所需的低值(Low,L)和高值(High,H)标本。按照以下配方配制混合标本:L,0.8L+0.2H,0.6L+0.4H,0.4L+0.6H,0.2L+0.8H,H,每份混合标本体积至少满足3次测定。样本处理2:用原厂技术资料文件注明的稀释液按照2、4、8、16倍稀释。样本处理3:排除糖尿病、心脏病、肾功能衰竭、血脂异常、更年期综合征人群,经临床诊断确认为健康成年人的血清样本。剔除脂血和溶血等不合格标本后,确保可用标本在各年龄段均有分布,随机抽取体检标本20例。
1.2 方法
1.2.1 对应参数信息
对应参数信息见表1。

表1. 对应参数信息(SAA中元)
1.2.2 精密度验证
参照EP15-A2文件测量样本,浓度水平参考线性范围和医学决定水平,标本量均保证在1mL以上。每个水平样本共完成15次测试量,分5d进行测量,测量3次/d,记录结果数据。计算批内精密度SD值、变异系数值;总精密度SD值、变异系数值。
1.2.3 正确度验证
参照EP9文件,选择厂家自带质控品,按实验室常规操作程序,进行SAA项目定标,然后测定厂家自带质控品3~5次,记录结果数据。计算均值,根据均值与靶值计算其偏倚,偏倚=(均值-靶值)/均值×100%。
1.2.4 线性范围验证
参照EP6A文件,选择接近线性范围下限和上限值的新鲜血清标本,经过混合处理后,在日立7600型全自动生化分析仪上按照常规操作步骤进行测量,按照浓度由低到高的顺序,每个浓度重复测定3次,全部实验和数据采集在同1个工作日完成。多项式回归分析将测定数据拟合为一次多项式模型,计算线性相关系数,根据R2≥0.975,0.97≥a≤1.03判断线性/非线性。
1.2.5 临床可报告范围验证
参照EP6A文件,选择分析测量范围内的高浓度标本。在日立7600上按照常规操作步骤进行测定,记录结果数据。将检测结果与标本稀释后的理论值对照,计算稀释回收率。偏倚=(均值-理论值)/均值×100%。
1.2.6 参考区间验证
参照EPC28文件,在日立7600上进行测定,要求0.5h内完成测定,记录结果数据。按照统计学区间计算法计算R值。R值=在参考区间内的测定值数量/参考区间验证人总数×100%。R值≥90%,则该参考范围区间可以直接使用。
2.结果与分析
2.1 精密度验证
日立7600检测SAA的精密度验证结果见表2。批内精密度均小于说明书中批内精密度规定声称值8%。批间精密度均小于说明书中总精密度最大限声称值10%。
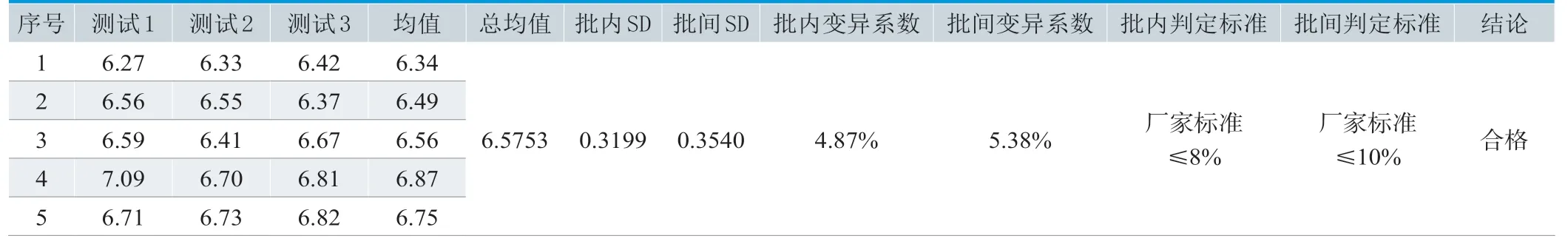
表2. 日立7600检测SAA L水平样品精密度验证结果
2.2 正确度验证
日立7600检测SAA的正确度验证结果见表3。正确度测定样本偏倚在-2.1%,测定值符合厂家说明书中提供的靶值之间的偏倚≤10%,正确度验证结果良好。
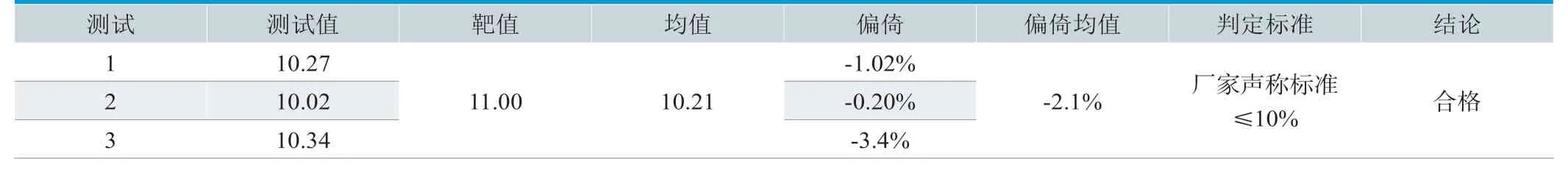
表3. 日立7600检测SAA正确度验证结果
2.3 线性范围验证
日立7600 检测SAA 的线性范围验证结果见表4,R2=0.9986。在2~240mg/L浓度范围内,R2>0.975,线性良好。
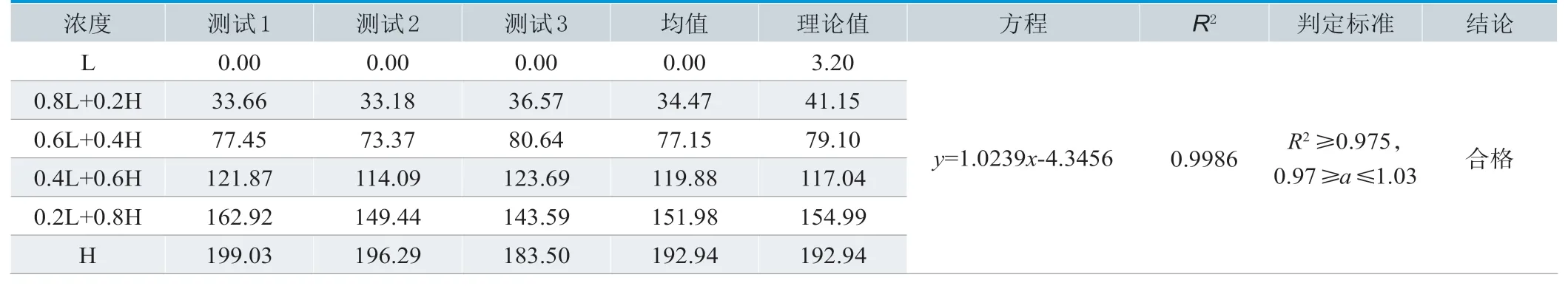
表4. 日立7600检测SAA线性范围验证结果
2.4 临床可报告范围验证l
日立7600 检测SAA 的临床可报告范围验证结果见表5。SAA 试剂盒最大稀释倍数为16 倍,故重庆中元生物技术有限公司生产的SAA 试剂盒可报告范围上限为192.01×16=3072mg/L。
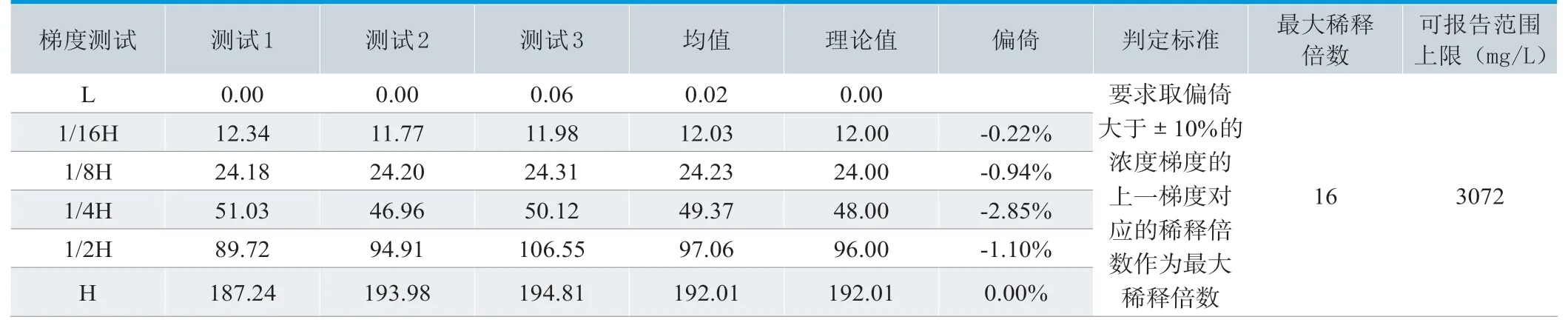
表5. 日立7600检测SAA可报告范围验证结果
2.5 参考区间验证
日立7600检测SAA的参考区间验证测试20次,结果分别为1.57、0.79、2.48、2.26、7.16、0.73、6.25、1.79、0.98、5.97、0.83、4.07、2.75、1.57、3.91、4.25、0.94、1.13、6.19、2.34。参考区间检测最大值7.16mg/L,最小值0.73mg/L,R值≥90%,符合标准,该参考范围区间可以使用。
3.讨论
在临床检验实验室中检测仪器和检测试剂都可能对系统的分析性能造成影响,检验结果是否准确直接影响到临床医生对患者的诊断、采用的治疗手段以及对预后情况的判断,因此定期地对系统进行性能验证及评价,以保证其能够满足临床实验室的要求[12-14]。ISO15189的相关文件明确要求,为确保检测系统能切合临床检测的需求,实验室必须验证其分析性能。故本研究依据医学实验室质量和能力认可准则要求,对7600生化分析仪搭载重庆中元生物技术公司SAA试剂盒检测SAA的分析性能进行评价。
现今SAA的检测方法主要包括胶乳增强免疫比浊法、酶联免疫吸附试验和胶体金法。经过对比发现,与酶联免疫吸附试验法和胶体金法相比,胶乳增强免疫比浊法不仅自动化程度高、更加简便快捷,而且灵敏度更高、线性范围更广,更适合应用于临床诊断,因此该方法在临床中广泛采用。本研究中所采用的重庆中元生物技术有限公司SAA试剂盒的检测方法即为胶乳增强免疫比浊法。现在市面上已有各种SAA检测试剂盒,解决了前几年只有西门子一家能够通过中国食品药品监督管理局审批的情况,可以满足市场需求。同时,也有很多学者自发研究了SAA的新检测方法和试剂,有望推动SAA检测的进一步发展。
日立7600是本科室所主要使用的生化分析仪,作者计划搭载重庆中元生物技术有限公司的SAA检测试剂盒,需对其检测分析性能进行验证。实验数据表明,本科室的日立7600搭载重庆中元生物技术有限公司SAA试剂检测的批内精密度均<8%,批间精密度均<10%满足要求。对试剂盒所配套的质控品进行测定,测定值与靶值之间的偏倚<10%,符合要求。线性范围测试采用高值标本,用低值血清分别对其进行5/5、4/5、3/5、2/5、1/5、0浓度稀释。以理论值为X轴,测定值为Y轴,绘制X-Y线性图。由线性图可以看出,SAA的线性良好,R2=0.9986。
在实际临床检验工作中,经常会对一些检测结果超过仪器线性的高值标本进行稀释。为了保证稀释之后的检测结果的准确性和可靠性,本研究对线性范围内的高值标本进行2、4、8、16倍稀释验证,稀释回收率均在偏差<10%的标准范围之内。稀释后的检测数据准确可靠,符合临床要求。参考区间是临床分析检验结果的重要依据,对临床上对检测结果的解释十分重要。本研究测定了本院20名健康体检者的血清SAA,90%以上的检测结果在参考区间之内,表明重庆中元生物技术有限公司的SAA试剂盒所提供的参考区间符合临床要求。
综上所述,本研究以重庆中元生物技术公司SAA试剂盒及临床标本为检测样本,为降低成本的同时提高可操作性,本研究设计采用简洁的方案,以现今学术科研认可的方法分析结果数据。结果表明,日本Hitachi公司7600型全自动生化分析仪搭载重庆中元SAA试剂检测性能良好,能够应用于临床检测。通过本研究,重庆中元SAA试剂盒可以在临床检验中推广使用,对临床疾病的诊断及鉴别诊断具有重要意义。
