煤沥青球预氧化的热转化机理及热力学特性研究
2023-11-03满梦瑶吴秋萍宋帅超程俊霞赖仕全朱亚明赵雪飞
满梦瑶,吴秋萍,宋帅超,程俊霞 ,赖仕全,朱亚明,赵雪飞
(辽宁科技大学 化工学院,辽宁 鞍山 114051)
0 引 言
煤沥青球是以煤焦油为原料并通过球化工艺处理所得到的产品,其最主要的用途在于制造球状活性炭。20世纪70年代,美国、德国等相继研制出1种新型的球形活性炭功能材料。相比于传统的粉末或不规则的颗粒活性炭,球形活性炭具备球形度好、表面光滑、机械强度高、负载密度高、孔径分布可控等优点[1]。基于其吸附解吸速度快、生理相容性好等优点,球形活性炭在环保、医疗、军事等诸多领域迅速得到广泛的应用。
对沥青球的氧化不熔化处理为制备沥青球形活性炭时的关键技术之一[2]。众所周知,未经预氧化处理的沥青球为热塑性固体,在后续工艺过程中因加热将发生熔融分解,对产品质量及形貌产生严重影响,因此探索沥青球氧化不熔化特性将对最终产品性能产生影响以及可为后续炭化、活化操作提供技术支撑。
目前沥青球的预氧化以空气做氧化剂的气相氧化为主[3]。在此过程中,沥青球发生氧化脱氢、分子间彼此交联等反应从而形成耐热的热固性结构,以确保在后处理加热过程中保持球形状态。但实际的预氧化过程是从沥青球的表面向内部逐渐扩散的过程,因此沥青球直径的大小将直接影响预氧化的效果。从预氧化的工艺研究角度出发,低温时化学键难以断裂,形成的活性位点少,预氧化难以发生;但高温状态大量活性组分产生,使得反应难以控制,且耗时耗能[4]。
为了研究预氧化的过程,管涛涛等[5]采用分子动力学模拟的方法以快速确定预氧化反应机理,从而确定预氧化过程桥键断裂及演化规律,进而指导工艺参数的确定。实际上,无论是在工艺参数上控制沥青球的预氧化过程,还是从模拟角度确定其反应机理,能量的变化是最有为性的体现。根据预氧化过程中能量的变化规律,推测其反应机理,控制其活性位点的形成,预氧化过程的可控性即可实现。反应过程中的动力学和热力学是最常见确定反应机理及计算能量变化的方法,且其具有应用范围广、计算数据的可靠性强的优点[6-7]。
为了快速揭示煤沥青球预氧化的机理,厘清其预氧化过程的特性,笔者利用热分析的方法对不同粒径的煤沥青球预氧化过程进行研究,从动力学和热力学角度运用KISSINGER机理函数模型研究其在预氧化过程中需求的能量变化情况,对活化能以及指前因子等参数进行求解,并通过Satava-Sastak分析法推导其化学反应机理,分析粒径对各参数的影响,详细探讨沥青球的预氧化行为,以期为更广泛、更高效地应用煤沥青球制备球形活性炭提供重要的理论依据。
1 实验部分
1.1 实验原料
实验原料采用国内某厂提供的1批煤沥青球,其基本性质见表1。将该沥青球筛分出4种不同粒径范围的球体,粒径分别为0.2~0.5、0.5~1.0、1.00~1.25、>1.25 mm。

表1 煤沥青球的基本性质
1.2 分析表征
利用美国TAQ-500热重分析仪,将4种样品在氧气气氛下由室温升至750 ℃进行热重分析实验,升温速率分别为 3、5、10、15 ℃/min,样品量为(4±0.3)mg。
1.3 动力学计算模型
化学反应动力学计算的基本假设依据为质量作用定律和Arrhenius定理,见式(1)、(2)[8]。
(1)
k=Aexp(-Ea/RT)
(2)
式中,c为产物的浓度,mol/L;t为时间,s;k(T)为速率常数的温度关系式;f(c)为反应机理函数;A为指前因子;Ea为活化能,kJ/mol;R为普适气体常数,其值为8.314 J/(mol·K)[9-10];T为热力学温度,K。
利用KISSINGER法计算煤沥青球预氧化过程的表观活化能及指前因子,见式(3):
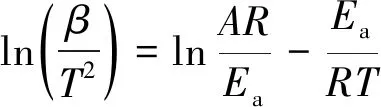
(3)
式中,β为升温速率,K/min。
KISSINGER法与其他模型方法相比,能够在未知转化率的前提下求得活化能与指前因子,快捷方便且所求机理函数的可靠程度较高。
2 结果与讨论
2.1 煤沥青球的热重分析
4种样品的TG-DTG曲线如图1所示,从图1中可看出几种样品曲线十分相似,随着温度的升高,整体呈现2个明显热解失重的台阶:第1阶段温度范围是150~400 ℃;第2阶段温度范围是460~640 ℃。根据前人对沥青球预氧化的研究,第1阶段属于预氧化不熔化的过程,该过程存在氧的扩散和氧化反应2个历程。在扩散历程中,沥青球本身轻组分发生脱除小分子反应后出现失重现象,但随着温度的升高,氧化反应开始发生,含氧官能团形成后开始增重。故此阶段存在失重和增重的平衡,导致此阶段的DTG出峰平缓,TG曲线下降有限。第2阶段在500 ℃以后出现剧烈的失重峰,该阶段应该是预氧化后的沥青球在高温下剧烈氧化,尤其在500~600 ℃,沥青球体发生脱烷基、脱氢等缩合反应以及球体内部发生的热分解速度均达到最大,造成该阶段的快速失重。最后该阶段以生成CO2和H2O而告终,而对应的TG曲线失重量几乎达到100%。
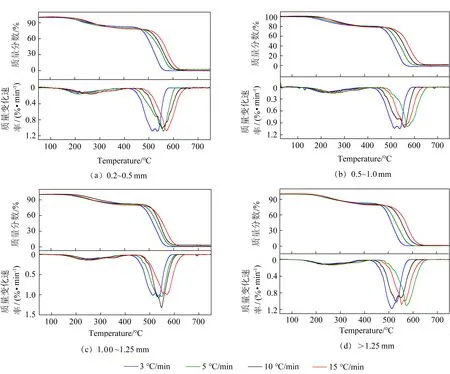
图1 4种不同粒径沥青球的TG/DTG曲线
2.2 煤沥青球热预氧化过程动力学分析
2.2.1表观活化能计算及指前因子求解
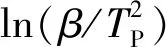
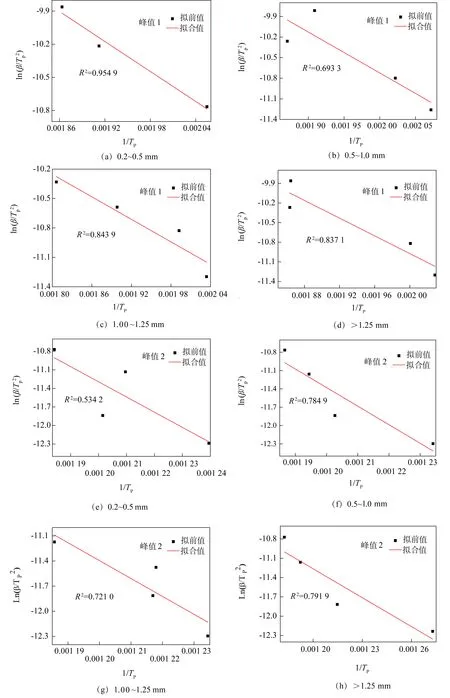
图2 4种不同粒径沥青球的拟合直线

表2 4种不同粒径沥青球在峰值1、2的活化能(Ea)和指前因子(A)
通过表2可得出以下认知:
(1) 同一物质在第2阶段所需的活化能普遍高于第1个失重阶段所需的活化能,其根本原因在于第1阶段氧气在样品中需充分扩散,而后沥青分子与氧发生氧化缩合反应形成大分子,且形成的大分子继续缩合形成大分子网,缩合反应本身更易放出热量,故此阶段反应的发生需要相对偏低的活化能。
(2)由于第2阶段主要发生的反应为含氧官能团以及大分子官能团的分解主要为CO2、CO、H2O等小分子的分解反应,因而所需的活化能偏高,因此导致所有样品在第2阶段的活化能普遍高于第1阶段。
(3)粒径对第1阶段活化能的需求影响更为明显,实际上由于沥青的组成较为复杂,与氧发生反应时其反应过程更为繁多杂乱,粒径的大小首先影响氧扩散,不同球径的沥青球中沥青分子与氧气的接触存在较大的差异,导致反应程度不完全一致,进而影响反应活化能的波动。
(4)沥青球的粒径越大,短时间内氧分子更难渗透至球体内部,在球体表面形成的含氧交联结构多且结构更加稳定,高温下不易分解。进入第2阶段后分解反应时,内部未发生预氧化的分子结构更易在活化能偏低时发生分解,导致该阶段的活化能随着煤沥青球样品粒径的增加而呈现下降的趋势。
反应的指前因子是影响活化能的重要因素,由于指前因子与反应物质本身的性质如构造、结构、电荷等有关,因此指前因子的数值在一定程度上可反映出样品反应的活性位点的数量,故而指前因子的求解对理解反应机理、控制反应速率和方向均具有重要的意义[13]。比较表2的4个指前因子可知,4种样品在第1阶段的指前因子的波动不大,说明反应活性位点之间基本不存在明显的差别[14]。而第2阶段的指前因子波动较大,且随着粒径增大有逐渐减小的趋势,说明第2阶段的分解反应受粒径大小的影响,粒径越大则其表面的含氧官能团越多,在相同温度下反应的稳定性越强则样品反应的活性位点数量越少。
2.2.2煤沥青球热转化机理判断
通过Satava-Sastak分析法按41种热解机理函数[15-16]分别计算出的数据与KISSINGER法计算出的平均活化能比较可知,第1阶段反应最合适的机理函数是第18号函数(Avrami-Erofeev equation,反应级数n=2),G(α)=[-ln(1-α)]2,机理函数模型为随机成核模型,随后生长;第2阶段反应最合适的机理函数是第2号函数(Valensi equation),G(α)=α+(1-α)ln(1-α),机理函数模型为随机成核模型,随后扩散。
2.3 煤沥青球热预氧化过程热力学分析
为了探讨4种样品在预氧化过程中的热力学性质,采用热力学参数的计算式(4)计算预氧化过程的热力学。样品在任意反应进程下对应的活化能(Ea)采用KISSINGER模型计算结果[17],特征温度(Ta)查找样品 TG/DTG 曲线对应数据,得到了各个样品在第1阶段和第2阶段的热力学参数,其中包括吉布斯自由能变(ΔG)、焓变(ΔH)、熵变(ΔS)[18-20]。
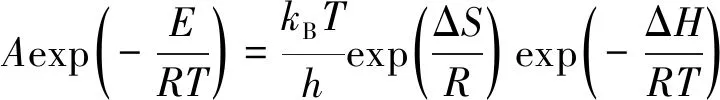
(4)
式中,h为Planck常量,其值通常为6.625×10-34J·s;kB为Boltzmann常量,其值为1.380 7×10-27J/K。
4种不同粒径煤沥青球样品在阶段1和阶段2的热力学参数如图3所示。
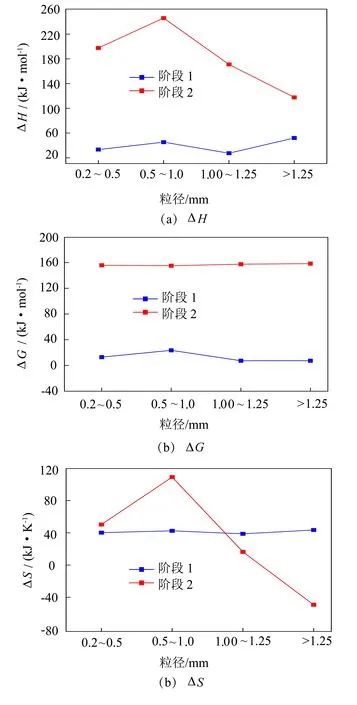
图3 4种不同粒径样品在阶段1和阶段2的热力学参数
由图3(a)可知,不同粒径的煤沥青球ΔH均大于0,说明煤沥青球的热转化反应过程在总体上表现为吸热过程。煤沥青球样品在第1阶段ΔH的变化规律并不明显,且数据较小,究其原因是因为沥青球在第1阶段的预氧化不熔化过程中,尽管沥青球的粒径存在差异,但氧的扩散历程与氧化反应历程程度在相同的温度下几乎一致,导致该过程所吸收的热量差异不很明显。但第2阶段的焓变明显增大,在此阶段发生剧烈的氧化反应则需吸收更多的热量。但随着沥青球球径的增加,所吸收的热量呈现出先增加后减小的趋势。在第1反应阶段中,沥青球的粒径越大,表面氧的交联反应程度越深;而进入第2反应阶段,剧烈的氧化反应发生始于表面的脱氧、脱小分子,故需吸收更多的热量。但沥青球径越大,沥青球内部未预氧化的结构越多,短时间内急速的氧化分解反应一旦发生,可迅速释放大量的热量,因而导致整体吸收热量降低[21]。因此,在第2阶段ΔH呈现先增加后减小的趋势。
整个过程中ΔG>0,说明煤沥青球的预氧化热分析的反应过程为非自发。由图3(b)可看出,4个样品在峰第1阶段的ΔG略有波动。沥青球的预氧化过程是1个复杂的反应过程,除了不断有新物质的生成,也会存在相的变化,而自由能ΔG在有相变的反应过程中实属相变驱动力[22]。从热重分析可知,第1阶段分解反应和聚合反应的同时发生,在此期间,又伴随着分解的气相小分子产生、小分子间聚合的液相物质形成以及氧原子交联固相物质的出现。由于其反应的基本物质为沥青和氧气,因此无论沥青球的粒径如何变化,ΔG的波动不会太大,而实际的计算数据也证实上述推测。而在第2阶段的ΔG差异很大,推测其原因可能是由于4种样品在该阶段均属于剧烈的氧化反应-燃烧,其本性是一样的,故吉布斯自由能的变化不大。总体上,第1阶段的ΔG普遍低于第2阶段,由此也充分说明以热分解为主的第2阶段反应在热力学上更难进行。
由于ΔS在第1阶段趋于稳定,说明沥青中原有的轻组分受热发生分解,表面的沥青分子与氧结合后聚合成含氧大分子,整个系统的混乱程度几乎保持一致,也即表现在ΔS数值上变化不大。粒径较小的样品在第1阶段与氧发生聚合的程度深,在第2阶段高温下发生分解反应时,逸出的含氧小分子相对较多,整个系统的紊乱程度大,因此,粒径越小则ΔS相对偏高。
3 结 论
以煤沥青球为研究对象,在氧气气氛中对不同粒径的煤沥青球进行不熔化处理,利用热失重仪模拟其预氧化过程,通过KISSINGER法及拟合计算得到煤沥青球在 2 个反应阶段中的表观活化能、指前因子和热力学参数(ΔH、ΔG、ΔS),并通过Satava-Sastak分析法及其41种机理函数的求解对比,探究煤沥青球粒径的大小对各参数以及热转化过程中能量需求的影响,综合以上方法分析得出结论:
(1)煤沥青球的热失重过程根据热失重曲线的明显变化分成 2 个阶段,第 2 阶段的活化能普遍高于第 1 阶段的活化能。球体粒径对热失重第 1 阶段活化能的影响更为明显,但指前因子的波动不大,反应活性位点基本无明显的差别。热失重第 2 阶段的活化能随着粒径的增加呈现下降的趋势,指前因子逐渐减小,活性位点数量减少,稳定性增强。
(2)从对热力学各参数ΔH、ΔG、ΔS的分析可得出,煤沥青球热解反应是非自发的吸热反应,粒径对ΔH、ΔS有一定影响,不同反应阶段对ΔG造成影响,而粒径对其影响不大,即从总体上归纳第1阶段属于热分解过程,第2阶段属于热缩聚过程。
(3)煤沥青球热转化过程的第1阶段符合第18号机理函数,机理函数模型为随机成核模型,随后生长;第2阶段符合第2号机理函数,机理函数模型为随机成核模型,随后扩散。
