综合化学实验:Fascaplysin类生物碱的命名、合成及表征
2023-11-02卢爱党王瑞虎刘运亭姜艳军
卢爱党,王瑞虎,刘运亭,姜艳军
河北工业大学化工学院,天津 300130
生态文明绿色发展,化学首当其冲,“化学的绿色化”已成为世界各国化学发展的主要目标和方向[1];遵循绿色化学理念,实现化学实验的绿色化不仅是社会可持续发展的需要,是培养学生环境保护意识的基本要求,也是化学化工专业培养人才的必然趋势[2-4]。
1 实验简介
1.1 实验背景及内容
1988年,Roll等人[5]首次从海绵FascaplysinopsisBergquist sp中提取并鉴定生物碱fascaplysin,该化合物为五元杂环季铵盐类化合物。研究发现生物碱fascaplysin具有广泛的生物学活性,包括抗细菌、抗真菌、抗病毒、抗肿瘤等[6]。1992年,Gibble等人[7]首次对fascaplysin生物碱进行全合成,具体合成路线见图1,共需要七步,总收率为57%。后续有文献报道了多种生物碱fascaplysin的合成方法[8-11],其中吴安心教授课题组通过I2/DMSO组合试剂介导下进行一锅法全合成天然产物fascaplysin尤为高效[11]。此外,鉴于学时限制,讲授IUPAC (国际纯粹与应用化学联合会)有机化学命名法的知识较少,学生即便通过Chemdraw获得化合物的英文名称,遇到复杂有机物如并环化合物时往往对名称中各部分组成缺乏基本的认知。本文通过在专业实验中引入综合化学实验——“Fascaplysin类生物碱的命名、合成及表征”,利用科学前沿研究成果设计绿色的有机合成路线,在实验教学过程中介绍利用I2/DMSO组合试剂介导下一锅法实现杂环化合物的高效合成[10-13],并学习并环化合物的命名规则。
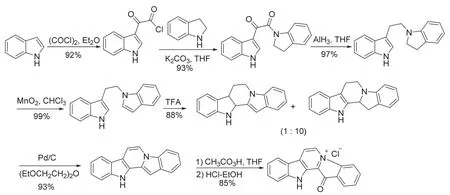
图1 Fascaplysin的首次全合成
1.2 实验目的
通过开展“Fascaplysin类生物碱的命名、合成及表征”实验,达到以下教学目的:
(1) 查阅和使用I2/DMSO组合体系作为工具化试剂在有机合成中的应用,实现绿色化学理念在有机合成化学实验教学中的渗透。
(2) 学习并环有机化合物的命名原则。
(3) 掌握β-咔啉杂环体系的构筑,巩固酮的α-卤代反应、Kornblum氧化和Menschutkin反应等反应机理,熟悉部分官能团的相互转化。
(4) 巩固和强化加热反应、真空抽滤、封管实验等基础操作技能,学会利用薄层层析法(TLC)检测及分析反应进程。
(5) 学会使用核磁共振数据处理软件(MestRe-C),并能够结合核磁共振波谱分析化合物结构。
1.3 实验原理
Fascaplysin类生物碱的合成反应路线见图2,具体各步反应机理如图3所示:(1) 第一步,分子碘促进芳基甲基酮化合物1进行碘代得到α-碘代芳基酮化合物A以及HI,随后α-碘代芳基酮A在DMSO作用下发生Kornblum氧化反应得到α-芳基酮醛化合物B;在反应体系中加入色胺2后,色胺分子中氨基进攻α-芳基酮醛中的醛基发生加成而后脱水形成亚胺C,溶液中的H+促使亚胺生成亚胺正离子D并发生分子内加成反应,经氧化经历中间体E和F后得到目标产物β-咔啉3;(2) 第二步,化合物3结构中β-咔啉N原子在230 °C条件下进攻苯基官能团的C―X碳原子发生Menschutkin反应(亲核取代反应)实现分子内关环得到季铵盐化合物4[11,14]。
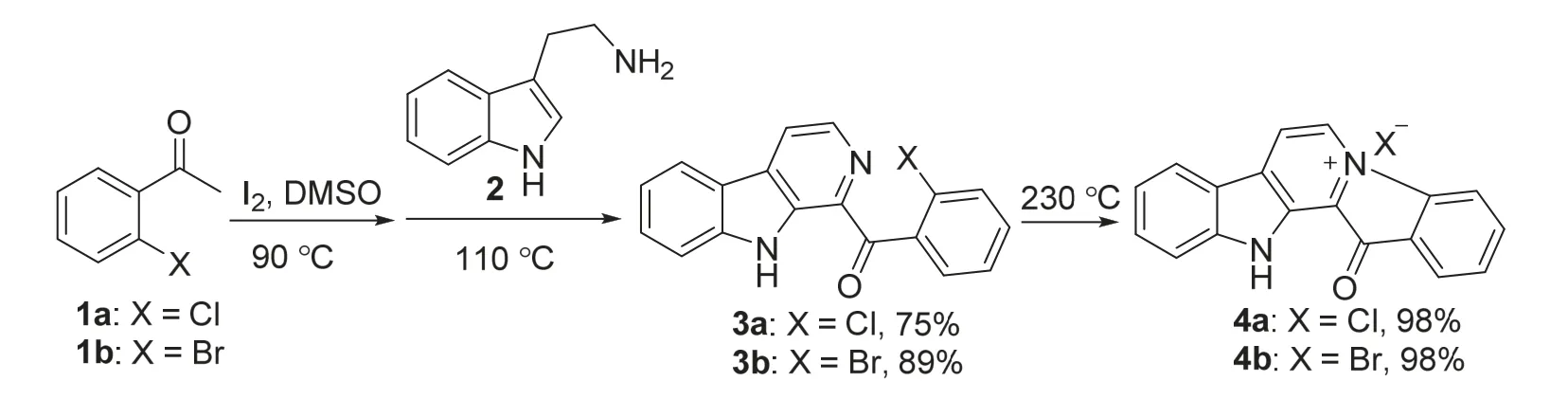
图2 Fascaplysin类生物碱的合成
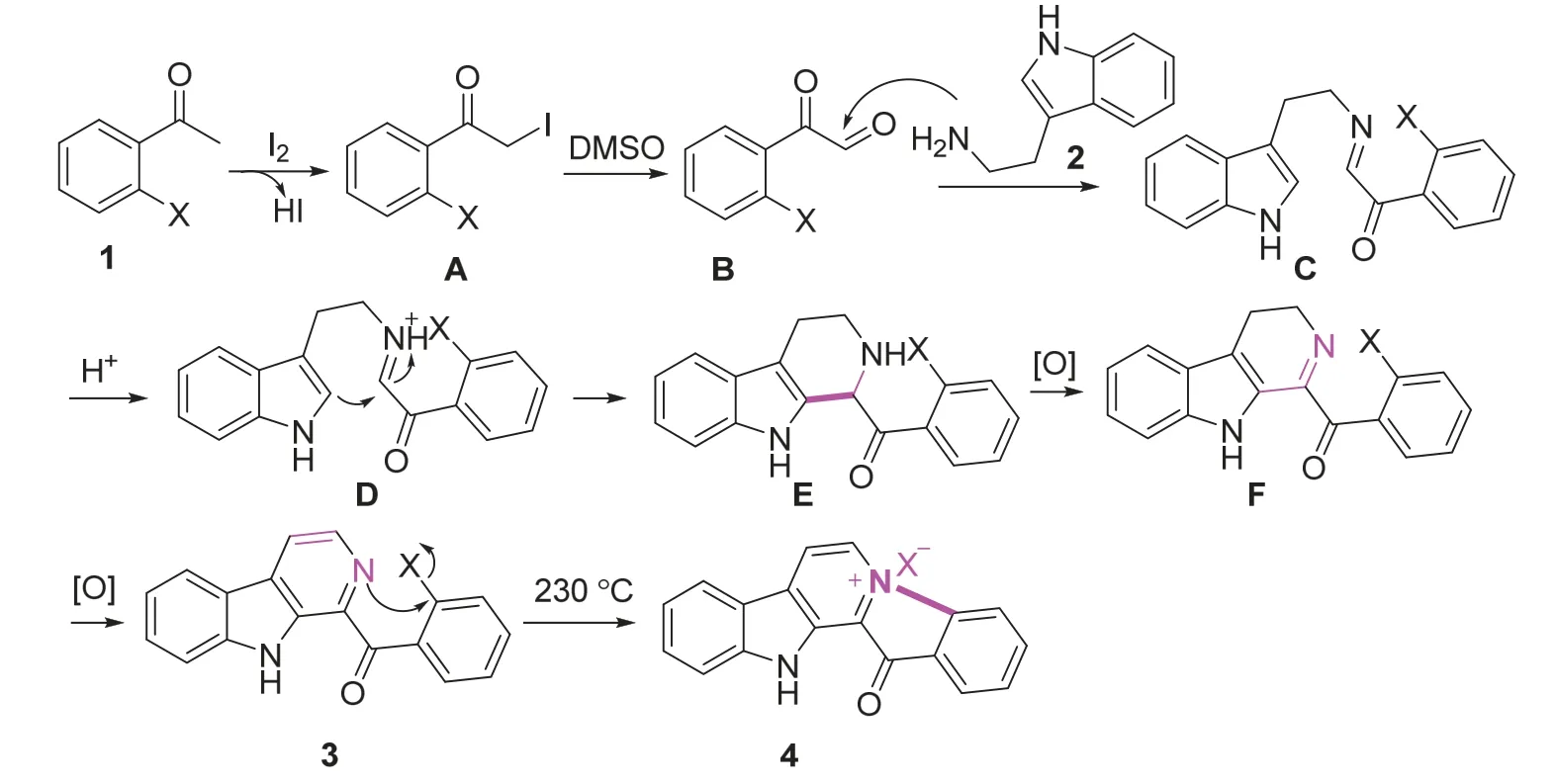
图3 合成Fascaplysin类生物碱的反应机理
2 教学过程的组织与实施
2.1 实验教学计划
我校应用化学“专业实验”课程在第七学期第1-4教学周(共计80学时),实验内容包括必做实验和选做实验两种类型,学生除完成必做实验(每个实验一般为4-8学时)外,还必须完成2个难度略有增加的选做实验(实验学时控制为8-16学时,每个选做实验由提供该实验的教师单独讲授),其中“Fascaplysin类生物碱的命名、合成及表征”综合化学实验需8学时,其中Fascaplysin类生物碱的命名及实验过程讲解(1学时)、合成实验(4学时)、软件使用及数据分析(1学时)、实验总结及讨论(2学时);选择该实验的同学,可以独立完成,也可2人组队共同完成。
2.2 实验准备阶段
上课前教师设计并提出引导性问题,让同学们提前预习并做好课上随时抽查。针对“Fascaplysin类生物碱的命名、合成及表征”综合化学实验提出的引导性问题见表1,引导和培养学生独立学习和解决问题的能力。

表1 引导性问题及其设计目标
2.3 实验实施阶段
2.3.1 试剂和仪器
实验药品:2’-氯苯乙酮、2’-溴苯乙酮、单质碘、二甲亚砜(DMSO)、无水乙醇、色胺,所有试剂均为分析纯,购于天津广达试剂公司。
实验仪器:98-3型数显磁力搅拌器(天津讯赫科技有限公司)、Bruker Plus 400 M型核磁共振波谱仪(德国Bruker)、ME303E型电子天平(梅特勒-托利多)、Waters 3100 Mass-Dector型质谱仪(Waters公司)、WFH-204B型三用紫外分析仪(上海驰唐电子有限公司)、X-4数字显示显微熔点测定仪(巩义市予华仪器有限公司)。
2.3.2 实验操作
2.3.2.1 化合物3的制备
将2’-氯苯乙酮或2’-溴苯乙酮(10 mmol)溶于DMSO (25 mL)中,磁力搅拌下加入单质碘(2.5 g,10 mmol),加热反应体系至90 °C条件下继续反应1 h (体系呈黑色),向混合液中加入色胺(1.6 g,10 mmol)后继续在110 °C下反应,TLC检测原料消失后停止加热(约1.5 h)。待反应液冷却至室温后搅拌条件下滴加蒸馏水(约20 mL),有大量黄色沉淀生成,通过抽滤后用无水乙醇洗涤即可得到产物。
3a:黄色固体,收率75%,熔点为204-206 °C (文献[15]204-206 °C);1H NMR (400 MHz, CDCl3)δ10.45 (s, 1H, NH), 8.57 (d,J= 4.8 Hz, 1H, ArH), 8.20-8.16 (m, 2H, ArH), 7.64-7.59 (m, 3H, ArH), 7.52-7.35 (m, 4H, ArH);13C NMR (DMSO-d6, 100 MHz)δ196.7, 142.4, 139.8, 138.3, 135.8, 135.7, 131.8,131.5, 130.6, 130.0, 129.8, 129.6, 127.2, 122.4, 121.0, 120.4, 120.2, 113.6。
3b:黄色固体,收率89%,208-210 °C (文献[11]190-192 °C);1H NMR (DMSO-d6, 400 MHz)δ12.24 (s, 1H, NH), 8.45 (s, 2H, ArH), 8.33 (d,J= 7.7 Hz, 1H, ArH), 7.85 (d,J= 8.2 Hz, 1H, ArH), 7.73 (d,J=7.9 Hz, 1H, ArH), 7.58-7.65 (m, 2H), 7.47 (t,J= 7.7 Hz, 1H, ArH), 7.35 (t,J= 7.1 Hz, 1H, ArH);13C NMR (DMSO-d6, 100 MHz)δ196.9, 142.0, 141.4, 137.9, 135.33, 135.1, 132.3, 131.3, 131.1, 129.5, 129.2,127.2, 122.0, 120.5, 120.0, 119.7, 119.0, 113.2。
2.3.2.2 化合物4的制备
称取化合物3 (0.15 g)至Schlenk瓶中,抽换N2气三次,然后磁力搅拌条件下封管加热至230 °C反应10 min,体系中黄色固体逐渐变成红棕色固体产品。
4a:红棕色(升华至瓶口处为黄色固体),收率98%,熔点为235-237 °C (文献[11]230-232 °C);1H NMR (DMSO-d6, 400 MHz)δ13.54 (s, 1H, NH), 9.60 (d,J= 7.2 Hz,1H, ArH), 9.18 (d,J= 6.5 Hz, 1H,ArH), 8.58 (d,J= 7.2 Hz, 1H, ArH), 8.50 (d,J= 7.6 Hz, 1H, ArH), 8.08 (d,J= 7.1 Hz, 1H, ArH), 8.03 (t,J= 7.8 Hz, 1H, ArH), 7.90 (t,J= 7.2 Hz, 1H, ArH), 7.82 (d,J= 8.3 Hz, 1H, ArH), 7.74 (t,J= 7.6 Hz, 1H,ArH), 7.54 (t,J= 7.8 Hz, 1H, ArH);13C NMR (DMSO-d6, 100 MHz)δ182.4, 147.2, 147.0, 140.5, 137.1,134.3, 131.4, 131.1, 126.8, 125.6, 124.4, 124.1, 123.1, 123.0, 120.4, 119.5, 115.7, 113.8;HRMS (ESI):m/z[M-Cl]+calcd for C18H11NO2+:271.0866;found:271.0857。
4b:红棕色(升华至瓶口处为黄色固体),收率为98%,熔点为238-240 °C;1H NMR (DMSO-d6,400 MHz)δ13.52 (s, 1H, NH), 9.67 (d,J= 5.5 Hz, 1H, ArH), 9.19 (d,J= 5.1 Hz, 1H, ArH), 8.58 (d,J= 7.7 Hz, 1H, ArH), 8.52 (d,J= 8.0 Hz, 1H, ArH), 8.08 (d,J= 6.6 Hz, 1H, ArH), 8.02 (t,J= 7.5 Hz, 1H, ArH),7.88 (t,J= 7.2 Hz, 1H, ArH), 7.81 (d,J= 8.0 Hz, 1H, ArH), 7.75 (t,J= 7.3 Hz, 1H, ArH), 7.54 (t,J= 7.1 Hz, 1H, ArH);13C NMR (DMSO-d6, 100 MHz)δ182.4, 147.2, 146.9, 140.5, 137.1, 134.3, 131.4, 131.1,126.8, 125.6, 124.5, 124.1, 123.1, 123.0, 120.5, 119.5, 115.7, 113.8;HRMS (ESI):m/z[M-Br]+calcd for C18H11NO2+:271.0866;found:271.0853。
本阶段,学生综合运用了有机化学中的加热、抽滤、封管反应和TLC检测等实验操作,合成了并环化合物Fascaplysin类生物碱,练习并掌握一种β-咔啉杂环构筑的方法,巩固酮的α-卤代反应、Kornblum氧化、Pictet-Spengler反应等反应机理,熟悉部分官能团的相互转化。
2.4 结果与讨论
2.4.1 化合物4的命名
含最大非累积双键数环系的二度空间表示式中,两个相邻环共有两个原子和一根键者成为并环[16],对于fascaplysin生物碱并环化合物的核心结构(如图4A)命名大体流程为:确定并环组成环系及其高位顺序→找出并环构词及并合位置的标识→编号→命名。
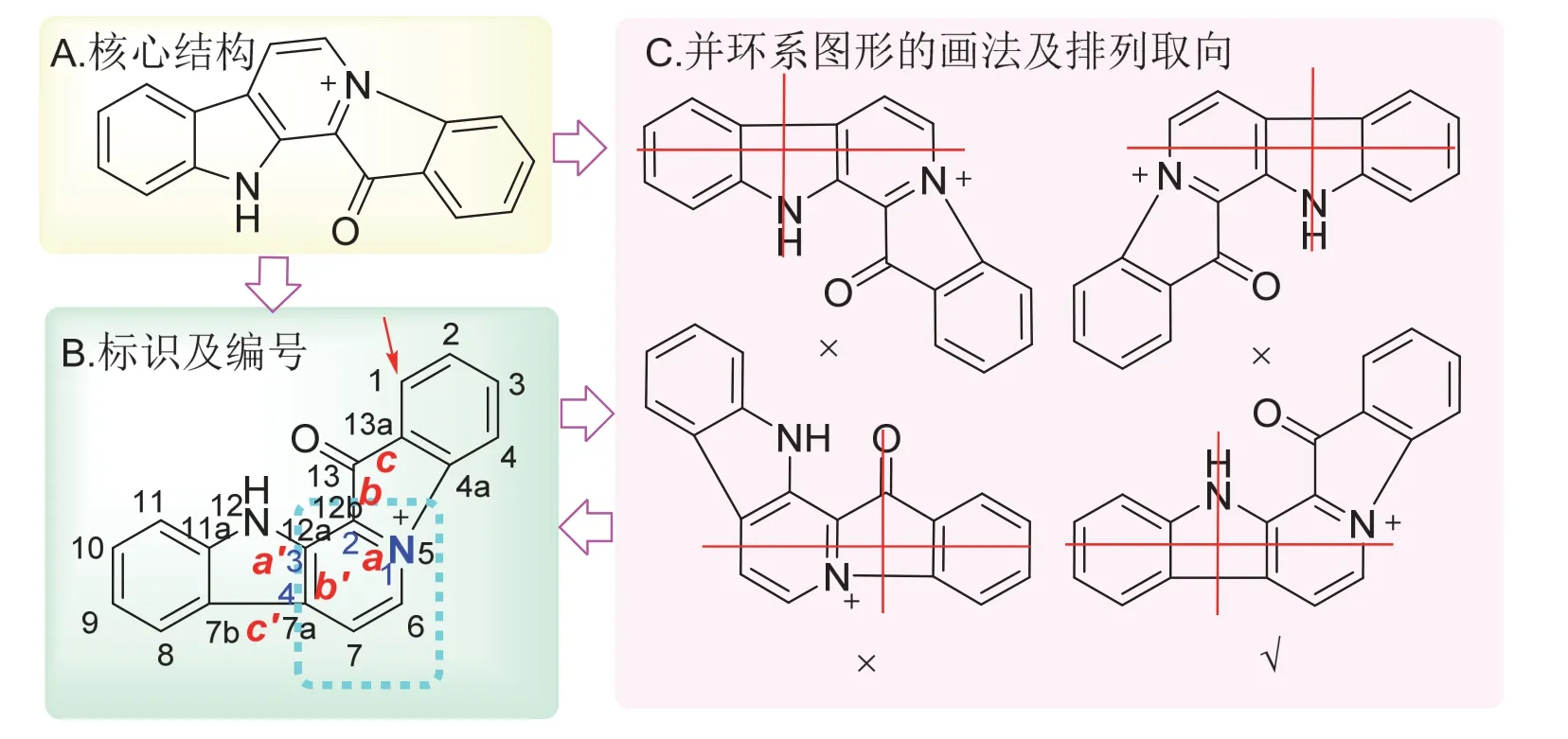
图4 生物碱fascaplysin的命名
(1) 确定并环组成环系及其高位顺序:Fascaplysin类生物碱核心结构包括两个吲哚和一个吡啶结构单元,吲哚高于吡啶,位高者为主体,因此确定主体为吲哚、拼合体(介体)为吡啶。
(2) 找出并环构词及并合位置的标识:吲哚与吡啶通过两个相邻原子以邻位并合的方式并合,采用加连缀字“并”的并环命名法进行命名[16];对主体环组分的周边进行标记(用斜体小写的拉丁字母),如图4B中周边标记红色符号“a,b,a’,b’,…”所示;并环中拼合体环组分周边的位次标识(用数字)如图4B中蓝色符号“1,2,3,4,…”所示,一个吲哚单元与吡啶共用吡啶结构N-1及C-2两个原子,另一个吲哚单元与吡啶共用吡啶结构的C-3及C-4两个原子;因此,并环构词为“并[1,2-a: 3,4-b’]”。
(3) 编号[16]:首先,在进行编号前,需要按并环命名的并环环系规则将它们的环系结构在二维空间中表达,对于横向并环系的排列取向应尽可能多的环在一横向轴上且在一横排上环数最多,如图4C所示,右上区环数最多,左下区环数最少;其次,对并环周边原子编号,从最顶端的环开始(如有多个环时则从其中最右端的环),并从此环反时针计最远的非公共原子起始(如图4B红色箭头标识处),再按顺时针方向计数,计数时包括公共杂原子(如图4B中蓝色标记氮原子),周边公共碳原子不进入数字编号内,公共碳原子以前一个碳原子的数字编号加拉丁字母a、b、c等进行标识,如7a、7b等;详细编号见图4B所示。
(4) 命名:利用IUPAC英文命名法对Fascaplysin类生物碱进行命名为chloride 13-oxo-12,13-dihydropyrido[1,2-a:3,4-b’]diindol-5-ium (4a) 或 bromide 13-oxo-12,13-dihydropyrido[1,2-a:3,4-b’]diindol-5-ium (4b),中文有机化合物命名在基本原则上与国际命名规则一致,4a和4b中文名称为氯化或溴化13-氧代-12,13-二氢吡啶并[1,2-a:3,4-b’]二吲哚-5-盐。
2.4.2 化合物4的绿色化合成
Anastas和Warner提出理想的绿色化学反应需具备高选择性、高产率、100%的原子经济性等12项原则[17]。在实验方案的讲解过程中,通过合成路线的对比选择绿色、经济、高效的合成方法,实现最大的原子利用率及零排放。文献[7]报道图1所示Fascaplysin生物碱合成路线,共需要七步反应,所用试剂超过20种,虽然总收率达到57%,但是原子利用率很低;对比本实验方案,第一步反应所用原料及溶剂只有2’-氯苯乙酮或2’-溴苯乙酮、单质碘、二甲亚砜(DMSO)、色胺和无水乙醇,溶剂DMSO也可以在反应结束后进行减压蒸馏或低温真空蒸发的方法进行回收,第二步反应在无溶剂真空条件下发生分子内关环,原子经济性高达100%,合成路线共计两步,化合物4a和4b的总收率分别为73%和87%。因此,本实验可以满足绿色化实验教学的要求,而且新颖高效的反应类型降低了实验操作的难度和对环境的污染。提问与思考:(1) I2/DMSO组合体系在有机合成中还有哪些方面的应用?(2) 图3所示的反应历程中间体B到E的过程为Pictet-Spengler反应,如果利用该反应为关键步骤合成Fascaplysin生物碱,实验路线如何进行设计?
2.4.3 化合物4的结构表征
化合物3中N-2原子在230 °C下进攻苯基官能团的C―X碳原子发生亲核取代反应实现分子内关环制备季铵盐化合物4。学生得到仪器室测试数据后,在教师指导下对测试样品的1H NMR和13C NMR进行分析和确认目标产物的化学结构。根据NMR谱图5 (DMSO-d6)及文献报道[5,11],以4a为例进行分析确认:Fascaplysin生物碱含有10个均与sp2杂化碳原子形成的C―H键(δ7.5-9.7)以及17个处于芳香区域的碳原子(δ113-148),含有两个邻位取代的苯环和一个孤立的AB体系;确定δ13.54处的单峰为NH的氢,δ9.60 (d,J= 7.2 Hz)、9.18 (d,J= 6.5 Hz)、8.58 (d,J= 7.2 Hz)、8.50 (d,J= 7.6 Hz)、8.08(d,J= 7.1 Hz)和7.82 (d,J= 7.1 Hz)处6个双重峰分别为H-7 (b)、H-6 (c)、H-8 (d)、H-4 (e)、H-1 (f)和H-11 (i)所处氢的信号峰,δ8.03 (t,J= 7.8 Hz)、7.90 (t,J= 7.2 Hz)、7.74 (t,J= 7.6 Hz)和7.54 (t,J=7.8 Hz)处4个三重峰分别H-3 (g)、H-10 (h)、H-9 (j)、和H-9 (k)所处的氢;13C NMR谱图中确定在δ182.4处为羰基碳信号峰,其余为芳香区域碳信号峰;化合物4a的高分辨质谱(HRMS)中有明显的分子离子峰271.0863,计算分子式C18H11N2O+[M-Cl-]+的值为271.0877,两者完全符合。提问及思考:(1) 化合物4a和4b分别为氯化和溴化季铵盐,通过哪些方法对其进行鉴别?(2) Fascaplysin生物碱结构中有多个C―H键,如何确定各自在核磁共振氢谱中的化学位移?

图5 化合物4a的核磁共振氢谱(A)和碳谱(B)谱图
2.4.4 注意事项及预防措施
本实验经过四轮的开展,总结注意事项及预防措施主要有三点:① 在制备化合物3的过程中,反应体系经过加热后,会有少许臭味生成(原因是DMSO在加热条件下会有二甲硫醚生成)。可以通过在加热前加入1.5倍量的双氧水进行消除,或在通风橱中进行实验操作,亦可通过反应过程中增加尾气吸收装置(吸收液为5%的次氯酸钠溶液)且在反应结束滴加水的过程替换为5%的次氯酸钠溶液进行消除。② 在制备化合物3的过程中,后续滴加水的量需要进行控制,加入水量过少沉淀无法生成;加入水量过多,会造成反应器底部生成大量粘稠固体;因此需要进行缓慢滴加,注意观察体系现象,待有沉淀生成时即可停止加水。经验证,最好控制溶剂DMSO与水的滴加体积比为1 : 0.6-1 : 1。③ 化合物4的合成过程中,反应如果在敞口下进行也可得到目标化合物,但是产物颜色为黑色;若经抽换氮气处理封管加热得到的产物为红棕色;另外,如果化合物3干燥不彻底,会有少量乙醇残留,需要在密封前进行预热。
3 教学效果及评价
本实验要求学生除了需要完成生物碱fascaplysin的命名、合成及表征,还要练习实验数据的整理以及实验报告的撰写。实验报告内容包括实验操作的详细步骤、目标化合物(1H NMR和13C NMR)谱图解析。通过书写实验记录、分析实验数据和撰写实验报告,提升学生理解、推理和探究能力,并培养学生严谨的科学态度。另外,实验内容结合有机化学前沿研究,将I2/DMSO组合体系引入到实验教学中,利用碘代、Kornblum氧化、Menschutkin反应合成Fascaplysin类生物碱,引导学生自主学习I2/DMSO组合试剂介导下构建杂环化合物的反应系统,开拓学生科研视野。
通过实施教学实验,积极调动学生进行文献调研与总结-实验准备及操作-产物分离与纯化-产物表征与分析-数据处理与报告撰写等,还可以培养学生追踪学科研究动态、分析比较实验方法和独立完成综合性实验的能力,为后续的创新性综合实验、毕业论文及其他科研训练打下坚实的基础。此外,该实验内容与本专业有机化学、精细化学品合成、仪器分析等课程的理论教学结合紧密,利用化学原理从源头上减少和消除有机合成对环境的污染,提高原子经济性,适合作为本科高年级学生开展综合化学实验。
