基于“大学化学”的科创培育模式探索
2023-11-02周苇鹿现永田东亮
周苇,鹿现永,田东亮
北京航空航天大学化学学院,北京 100191
“新工科”建设是在“卓越工程师教育培养计划”的基础上,由教育部提出的一项持续深化工程教育改革的重大行动计划,目的是要培养科学基础厚、工程能力强的高素质复合型人才[1]。化学作为自然科学的中心学科之一,具有理论基础、交叉性强的特点,更是促进能源、环境、材料、生物、信息科学等诸多领域前沿研究的基础学科[2]。我们所处的时代具有知识量大、信息迭代快的特点,积极推进“新工科”的建设,让老的知识在这个飞速发展的时代展现新的活力,主动应对新一轮科技革命和产业革命,适应国家战略人才培养的需求,就必须注重“两性一度”,将“应试”知识挖掘拓展为“实用”知识[3]。
北京航空航天大学化学学院承担的“大学化学”课程面向航空航天大类大一新生开设,涵盖基本化学原理和物质结构等内容,具有知识抽象、公式繁多、自成体系等特点。此课程一方面学生在学习过程中易于感觉枯燥,容易产生厌学怠学等情绪;另一方面课程知识体系与实际应用贯通不足,交叉融合不够,知识的实用性有待挖掘与拓展[4]。如何让知识与能源或环境等现今社会关注的热点研究接轨,通过对化学知识延伸并与本科生科研实践联系,既有助于学生明晰其应用价值,利于培养学生的学习兴趣,变被动学习为主动学习,更能在此过程中培养学生的科研创新能力,提高其发现问题与解决问题的能力。显然,这类探索是非常有必要的。
1 基于“大学化学”的科创培育模式
北京航空航天大学有着鼓励本科生参与科研训练与实践的传统。北航“冯如杯”竞赛始创于1990年,以我国航空先驱冯如先生命名,每年4-5月举办,目前已经举办过32届,学生参与面广、参与积极性高,是北航一年一度的科技盛会,也是引导广大学生开展创新实践与科研活动的重要平台。科研微课题则是同时处于教学一线和研究一线的教师为本科生的培养,结合个人专业所长,自主设置的科研训练与实践的平台。比如,笔者近年为本科生提供的科研微课题“纳米电催化剂的制备与制氢研究”,围绕着备受关注的绿色能源——氢能,开展研发高性能低成本的电解水纳米催化剂,以实现高能量转换效率,降低氢能成本。
“大学化学”课程的改革即以上述实践活动为契机,教师凝练出可进行科研创新的知识点,补充交叉领域的背景知识或前沿进展,进行课堂知识拓展,引导与激发学生的学习兴趣。对应的知识点,教师可设置不同的微课题,通过自愿加入或教师鼓励等模式,为有兴趣与潜力的学生提供3-6个月时间的科研微课题。经过科研训练与实践,一方面加深了课堂知识,另一方面架构了化学知识与实际应用之间的联系,最后也锻炼了学生的实践动手能力。课程结束后,部分学生会坚持下去,将微课题做深,为参加“冯如杯”科技作品竞赛打下基础。通过将课堂、微课题与竞赛相串联,打通从知识学习到科研训练的本科生培养环节,形成了“课堂-微课题-竞赛”人才连续化培育模式,在教学改革与科研创新方面均取得了较好成效。
图1为连续化培养模式,主要包括三部分内容:以教师授课为主的课堂知识凝练环节,随着知识点的凝练逐步拓展出的科研微课题项目,以及学生经过微课题实践后为竞赛做准备的更高层次的科研创新训练。其中,“大学化学”知识发散、理论性强,易于凝练出可拓展的知识点,如图1提及的四点:电解水与超电势、阿伦尼乌斯公式、化学电源、沉淀的转换。从第一点“电解水与超电势”可探讨如何降低电解水体系的超电势,进而发展到“电解水催化剂的研究”。阿伦尼乌斯公式(Arrhenius equation)是我们熟悉的表征化学反应动力学的公式,把动力学的研究放在具体的科研场景中,会带来一些创新研究,所以这里也可设置一个微课题。“化学电源”包括一次电池、二次电池与连续电池。考虑现今“能源革命”的背景,它可以挖掘出许多重要的微课题,我们则重点关注目前极具前景的锂/钠离子电池[5,6],并为之设置了一个能源方向的微课题。而在环境领域,水污染及处理一直都是社会关注的重心,这里可以借助“水溶液化学”中的“沉淀的转换”有关的溶度积的知识点,进行去除重金属离子的纳米吸附剂的研究。如图1所示,知识点凝练拓展出微课题,微课题的进展促使竞赛作品的诞生。同时利用微课题的实践情况,可以调整课堂知识讲授;将科技竞赛中存在的问题反馈给微课题,依据反馈结果随时对前面环节进行相应的动态调整。“课堂-微课题-竞赛”的培育模式不仅有利于探究化学知识与其他学科交叉创新的可能性,更重要的是,利用科研过程中收获的丰富知识反哺课堂,再通过多轮次培育模式进行知识精炼,让“大学化学”越来越接地气。

图1 “课堂-微课题-竞赛”的连续化培养模式图
2 创新实验案例
除了图1列举的4个例子,基于“大学化学”的学科知识还可以凝练出更多有意义的课题,这些亟待熟悉大学化学课堂并活跃在科研第一线的教师的实践总结。这里就上述提及的“纳米电催化剂的制备与制氢研究”这个微课题孵化出的两个创新实验案例“电解与电催化制氢催化剂的研究”及“阿伦尼乌斯公式的创新应用”,进行简单介绍,希望为同行的教学研究起到抛砖引玉的效果。
2.1 电解与电催化制氢催化剂的研究
“大学化学”中“电化学”内容主要包括原电池与电解两部分。电解内容中,电解水会存在超电势(overpotential),通常到1.8 V以上才能实现水的分解。越高的分解电压,意味着产生同样量的氢气需要更多的电能,也就是氢气成本更高。因此,降低超电势是电解水亟待解决的问题。
在此时的教学内容中,首先分析超电势产生的多种原因以及降低超电势的途径。同时可以提及“双碳”目标,介绍温室气体效应带来的危害。减少高碳化石能源的利用,发展零碳的氢能是最直接的途径。我国在风力、太阳能、水力发电领域极具优势,但这些能源形式受季节影响,具有不稳定性。为了保证能源的稳定且持续供应,需要将通过清洁能源获得的电量加以储存,而氢能是一类优异的化学储能形式。电解水制氢则提供了一种规模化清洁制氢的途径[7]。但为了降低氢能成本,需要提高电能向氢能的能量转换效率。因此,水到渠成地引入发展高性能电催化剂,通过降低超电势,实现高的能量转换效率的研究意义。
通过上述背景知识的介绍,有些本科生表现出极大兴趣,会主动询问相应的研究,笔者会推荐合适的文献让他们阅读,并吸收他们加入之后的“科研微课题”,参与到科研训练中。水电解的反应包括两个半电池反应,即正极的析氧反应(oxygen evolution reaction,OER)和负极的析氢反应(hydrogen evolution reaction,HER)。再根据E=φ+-φ-的公式,查得标准状态下的EӨ为1.23 V。即电解水在某电流密度下的真实电势值减去1.23 V,即为超电势。而析氧和析氢电催化剂则是在电极表面提供丰富的活性位点,通过形成中间相,降低反应的活化能垒,进而使得整个反应的超电势降低。图2为以博士生为副导师带领本科生开展的科研结果示意图,即利用研制的插层型NiFe-LDH (层状双氢氧化物)和异质结磷化物分别作为OER和HER催化剂,让通常高于1.8 V的分解电压降至1.5 V以下,使得一节干电池即可驱动水的电解,有效提高了能量转换效率[8]。也有本科生参与研究正负极催化剂的匹配,进行电化学性能调控的研究[9]。
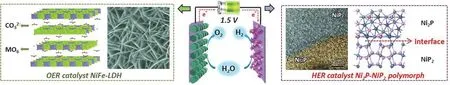
图2 催化剂辅助电解水的科研结果图例
在之后的课堂中,我们秉承“从学生中来,到学生中去”的思想,将取得的研究结果,再作为拓展知识在课堂中介绍,很容易引起学习者的知识共鸣。化学是一门注重基础理论和实验的学科,将基础理论拓展到与社会息息相关的新能源领域,再将得到的实验结果作为案例重新引入课堂,通过基础知识与创新实验的融合与验证,不仅丰富了“大学化学”氧化还原知识体系的内容,加强对“超电势”概念的理解,更有助于创新教学内容、激发学生的学习兴趣、强化学生的思维能力。
2.2 阿伦尼乌斯公式的创新应用
1885年Hood根据经验指出活化能具有指数形式的温度依赖性,但未给出具体的公式[10]。1889年,类比热力学的van’t Hoff方程,Arrhenius将活化能视为发生反应所需克服的能垒,基于实验数据归纳出阿伦尼乌斯公式[11-13]。碰撞理论认为速率常数k与[T1/2exp(-E/RT)]成正比;过渡态理论认为k与[Texp(-E/RT)]成正比。结合二者,总结公式如下:k=k0Tmexp(-E/RT)。其中,m是一个附加参数,通常在0 <m< 1的范围内,特殊情况下m> 1。其中,与指数项[exp(-E/RT)]相比,公式中Tm对k的影响非常小[14]。后来用指前因子A代替k0Tm,一般情况下认为温度对A影响不大。
阿伦尼乌斯公式广泛应用在食品、生物等领域中,用于研究化学反应中温度对速率的影响规律,以及寻找合适的反应温度等。由于该模型要求速率随温度单调增加,对于特殊反应,如具有最佳温度的酶促反应和微生物生长研究则会受限,因为酶或微生物在高温下易失活。此时的阿伦尼乌斯公式则需要一定的校正,才能适用[15]。这是讲化学反应动力学有关的活化能和阿伦尼乌斯公式涉及到的历史背景,有助于学生理解van’t Hoff方程和Arrhenius公式存在T1和T2两个温度时形式的类似,以及在特殊体系此公式的温度适用范围。
显然,阿伦尼乌斯公式是前人在若干实验数据的基础上归纳的用以揭示反应动力学的经验式。教师引导学生将之拓展到电化学反应体系,并结合目前热门的氢能领域电解水制氢催化剂的研制,用以考察不同催化剂下水分解反应的反应能垒的高低,借以筛选能有效降低反应能垒的更优异的催化剂。这部分知识的拓展在课堂完成,鼓励学生去查找早期关于阿伦尼乌斯公式的研究与应用。并结合后面开展的“科研微课题”,带领感兴趣的学生加入到高性能催化剂的筛选中。如,在碱性电解液中,析氢基元反应步骤如下[16],
其中,*号代表催化剂的活性位点。根据反应速率不同,可能是Volmer-Heyrovsky的析氢步骤,也可能是Volmer-Tafel的析氢步骤。其中,Volmer步骤即水裂解过程通常被认为是限速步,是此电催化体系最需要跨过的能垒。首先,我们通过合适温度范围内的变温实验,利用阿伦尼乌斯公式求得此体系的能垒值Ea。但由于实验过程是将催化剂涂覆到电极表面,涂覆剂的制备、涂覆量、涂覆手法等均会影响测试结果,存在一定测试误差。为了更好地揭示催化剂的催化效果,我们对单片层催化剂进行扫描电化学显微镜(SECM)的变温测试,同样利用阿伦尼乌斯公式,可以求得单片层催化剂表面水裂解步骤的能垒。甚至,我们可以通过密度泛函理论计算(DFT),依据上述反应式(1),构建催化剂的原子模型结构,计算水吸附、水劈裂、释放OH-各个步骤的表面能,通过这些能量差,得到理想状态的活化能的数值。上述研究分别从宏观体相(电化学实验)和微纳尺度(单片层测试),利用阿伦尼乌斯公式,获得催化体系的活化能数值。且与目前热门的计算化学(原子分子尺度的DFT计算)得到的活化能数值,互为验证。如图3所示,将这三类方法结合,我们验证了复合型催化剂NiCoP@MXene较单一成分的催化剂NiCoP,对Volmer基元反应步骤的活化能降低了16.0%-22.1%,提出了一种筛选催化剂的跨尺度验证的可靠方法[16]。将这部分研究内容引入课堂,可以加深学生对阿伦尼乌斯公式的深度理解,对化学过程中的动力学研究在原子分子尺度上有更感性的认识,加深课堂印象,启发学生以后的科学创新研究。

图3 基于Arrhenius公式进行科研创新的图例
3 结语
笔者用课堂知识的凝练、带领本科生做科研微课题及参加科技竞赛的经历,证实了“课堂-微课题-竞赛”的连续化培养模式的可行性。一方面,将教学与科研连接,是一类高效的人才培育模式,并且前面学生获奖或参与科学研究的成功经验会激发低年级学生的学习热情。另一方面,从化学基础知识中挖掘出来的微课题,经过孵化产生的创新实验案例,被重新引入课堂,极大丰富并优化了“大学化学”的知识体系,顺应“新工科”的培育需求,赋予了化学知识新的生命力。
