低分子肝素钠联合醋酸地塞米松基于PAR-2/TRPV1信号通路治疗小鼠瘙痒模型的有效性
2023-11-01李仰琪赵晓岚梁艳华柯娅楠沈秀玲叶兴东
李仰琪,赵晓岚,梁艳华,柯娅楠,沈秀玲,叶兴东
瘙痒是一种可使人产生不快的主观症状,易引发搔抓欲望,其发病机制尚未完全阐明。近年临床发现瘙痒的外周敏化机制主要是组胺依赖及非组胺依赖性的瘙痒信号通路,其中蛋白酶激活受体2(PAR-2)途径可介导瘙痒,瞬时感受器电位香草酸受体1(TRPV1)是该途径的下游信号。有研究表明,非组胺依赖性瘙痒神经信号传导与TRPV1或TRPA1耦联神经通路有关[1]。TRPV1的初级传入C纤维的子集可根据受体的表达与瘙痒原敏感性分为3组[2-4]。TRPV1作为各刺激的整合器,在瘙痒、疼痛及皮肤神经源性炎症的发生发展中发挥着重要作用[5-6]。本研究基于PAR-2/TRPV1信号通路探讨低分子肝素钠联合醋酸地塞米松治疗小鼠瘙痒模型的有效性,现报道如下。
1 对象与方法
1.1 研究对象 于选取6周龄C57小鼠48只,体质量(25±5)g,在标准环境下饲养,昼夜12 h∶12 h,均衡饮食,自由饮水。采用随机数字表法将24只制成干皮症(AEW)慢性瘙痒小鼠模型,剩余24只制成DNFB过敏性皮炎急性瘙痒小鼠模型。将AEW慢性瘙痒、DNFB过敏性皮炎急性瘙痒小鼠模型按照随机数字表法分为模型对照组、地塞米松组、肝素组、联合用药组,每组6只。
1.2 建模与干预方法 小鼠AEW慢性瘙痒、DNFB过敏性皮炎急性瘙痒模型构建参考文献[7-8]。治疗方法:模型对照组仅在小鼠脱毛部位给予0.9%氯化钠溶液;地塞米松组在小鼠脱毛部位涂抹醋酸地塞米松乳膏(本院自制)0.1 g;肝素组在小鼠脱毛部位涂抹低分子肝素钠软膏(山东博士伦福瑞达制药有限公司生产)0.1 g;联合用药组在小鼠脱毛部位涂抹醋酸地塞米松乳膏、低分子肝素钠软膏各0.1 g。各组小鼠用药频率均为2次/d,持续干预7 d。
1.3 观察指标与方法 (1)瘙痒次数:于干预前、干预7 d后,分别将各组小鼠置于聚丙烯树脂玻璃盒子内,在安静环境下用摄像机记录小鼠1 h内对颈背部的抓挠次数,测试当天选取3个不同的时间点记录,取平均值。(2)PAR-2、TRPV1蛋白表达量:干预7 d后,观察小鼠皮损、抓挠情况,而后采取颈椎脱臼法处死所有小鼠,取小鼠造模区皮肤,提取蛋白并根据BCA法进行蛋白定量,待抗体孵育完成清洗,行ECL化学发光法进行目的蛋白条带灰度分析,采用Western blotting检测PAR-2、TRPV1蛋白表达量。

2 结 果
2.1 瘙痒次数比较 在AEW慢性瘙痒、DNFB过敏性皮炎急性瘙痒小鼠模型中,干预前,4组小鼠瘙痒次数比较,差异无统计学意义(P>0.05);干预7 d后,联合用药组、肝素组、地塞米松组小鼠瘙痒次数均少于模型对照组,且联合用药组小鼠瘙痒次数少于肝素组、地塞米松组(P<0.05),见表1。
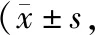
表1 4组小鼠模型干预前后瘙痒次数比较次,n=6)
2.2 PAR-2、TRPV1蛋白表达量比较 干预7 d后,在AEW慢性瘙痒小鼠模型中,肝素组、联合用药组TRPV1蛋白表达量低于模型对照组,联合用药组低于地塞米松组、肝素组(P<0.05);地塞米松组、肝素组、联合用药组PAR-2蛋白表达量低于模型对照组,联合用药组低于地塞米松组、肝素组(P<0.05)。干预7 d后,在DNFB过敏性皮炎急性瘙痒小鼠模型中,肝素组、联合用药组TRPV1、PAR-2蛋白表达量低于模型对照组,联合用药组低于地塞米松组、肝素组(P<0.05),见表2。
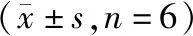
表2 4组小鼠模型干预后TRPV1、PAR-2蛋白表达量比较
3 讨 论
急性瘙痒提示环境存在有害物质,如昆虫、有毒植物或其他刺激物,同时激发抓挠,以清除瘙痒原并减轻瘙痒感。慢性瘙痒则可能是一种伴随皮肤或系统病变的免疫异常表现,虽然多数瘙痒症状由组胺信号介导,但还有其他神经通路[9],如来自植物毛霉的针刺通过非组胺依赖途径引起的强烈瘙痒[10-11]。此外,免疫细胞可释放多种致痒原,引起瘙痒、银屑病及湿疹等,而抗组胺药物在治疗瘙痒方面无效。大多数病理生理瘙痒症对抗组胺药物并不敏感,治疗靶点尚未确定[12]。皮肤病、全身性疾病、神经系统疾病、精神疾病等均可导致瘙痒症状,常表现为急性或慢性形式(持续时间≥6周)。
慢性瘙痒的治疗是临床的一项挑战,中重度瘙痒患者的生活质量显著降低。而瘙痒的潜在生理学非常复杂,包括角质形成细胞和感觉神经元等以及某些免疫细胞的浸润。有研究表明,角质层细胞、神经纤维与各种免疫细胞(如角质形成细胞、T细胞、嗜碱粒细胞、嗜酸粒细胞和肥大细胞)之间存在显著影响,皮肤和脊髓神经元或不同免疫细胞上受体之间的相互作用对瘙痒传播起着重要作用。
TRPV1广泛分布于皮肤重要结构细胞的细胞膜上,包括角质形成细胞、成纤维细胞及皮脂腺细胞,以及树突状细胞、肥大细胞等功能细胞的细胞膜上,多种炎性皮肤病的发生、发展与内外源性刺激介导的TRPV1活化密切相关,该受体活化可进一步导致神经肽或促炎性递质释放,该通道的活化或阻断在慢性炎性皮肤病治疗中的靶点作用也日益凸显。TRPV1是瘙痒信号传导的重要分子。背根神经节细胞对PAR-2和5-羟色胺的反应大于对组胺的反应,提示慢性干性皮肤的瘙痒神经信号途径可能是内源性激活剂的释放促使PAR-2和5-羟色胺受体2A激活,致敏发送瘙痒信号的神经元,加重瘙痒症状,此过程并不依赖组胺的释放。相关研究证实,PAR-2神经源性机制参与皮肤炎症和瘙痒,TRPV1属于瞬时受体电压感受器家族成员之一,存在于中枢神经系统和外周神经系统。目前已有研究证实PAR-2在外周神经系统及中枢神经系统的脊髓及大脑中存在表达,因此,PAR-2信号途径也可刺激中枢神经系统脊髓水平段的神经肽释放,CGRP受体和SP受体(NK1P)激活后,促使痒觉效应直接传达至中枢神经系统。此外,神经元表面的PAR-2活化后,神经元发生以钙离子为主的跨膜离子流动,细胞内钙离子浓度改变,TRPV1活性增强,PAR-2与TRPV1以协同作用的方式相互影响,增强瘙痒感觉。
肝素是三磷酸肌醇(IP3)受体特异性拮抗剂,其中低分子肝素分子量小,易透过细胞膜进入细胞内拮抗IP3受体,从而抑制PAR-2激活诱导的钙离子浓度上升。本研究结果显示,干预7 d后,在所有瘙痒小鼠模型中,联合用药组瘙痒次数少于肝素组、地塞米松组;在AEW慢性瘙痒小鼠模型中,肝素组、联合用药组TRPV1蛋白表达量低于模型对照组,联合用药组低于地塞米松组、肝素组,地塞米松组、肝素组、联合用药组PAR-2蛋白表达量低于模型对照组,联合用药组更低于地塞米松组、肝素组;在DNFB过敏性皮炎急性瘙痒小鼠模型中,肝素组、联合用药组TRPV1、PAR-2蛋白表达量低于模型对照组,联合用药组更低于地塞米松组、肝素组,表明低分子肝素钠与醋酸地塞米松均可明显改善瘙痒小鼠皮肤瘙痒症状,且联合用药效果优于单一用药,同时低分子肝素钠可显著降低小鼠皮肤PAR-2/TRPV1通路蛋白的表达,且联合醋酸地塞米松对该通路的抑制效果更加显著,本实验结果进一步验证了低分子肝素钠联合醋酸地塞米松可通过阻断PAR-2/TRPV1信号通路改善瘙痒小鼠的瘙痒程度,PAR-2/TRPV1非组胺依赖通路可能是低分子肝素钠发挥作用的重要机制。
综上所述,低分子肝素钠软膏可通过阻断PAR-2/TRPV1信号通路改善瘙痒小鼠的瘙痒症状,将其与醋酸地塞米松联合治疗对该通路的抑制效果更加显著。随着对PAR-2及TRPV1生物学功能的深刻认识,以及其在炎症性瘙痒性皮肤病发病机制中的深入探讨,研发更具有特异性的PAR-2或TRPV1拮抗肽应用于瘙痒性皮肤病的治疗终将成为可能。
利益冲突:所有作者声明无利益冲突。
