羟基磷灰石改性甘蔗叶对水中刚果红的吸附特性研究
2023-10-30柳富杰张馨月潘莉莉
柳富杰,张馨月,苏 龙,潘莉莉
(1.广西科技师范学院食品与生化工程学院,广西 来宾 546119;2.广西科技师范学院广西现代蔗糖业发展研究院,广西 来宾 546119)
中国已成为世界上染料产量最多的国家,近年来的产量约占世界总产量的70%[1]。合成染料在我国主要应用于纺织、皮革、化妆品、造纸、印刷、制药和食品等行业[2],这些行业产生的废水中,含有一定量具有致癌性、致突变性、有毒的染料[3],其中的刚果红是一种常用的阴离子偶氮染料,常以钠盐形式存在。刚果红具有高稳定性和难降解性,刚果红废水排放到环境中,除了会造成严重的环境污染问题,还会引起癌症、基因突变、肺部和肾脏感染等诸多健康问题[4]。因此在刚果红废水排放之前,要采取必要的处理措施,以降低其危害。研究者对染料废水的处理技术做了相关的研究,目前处理有机染料废水的有效方法,主要分为物理法和化学法,具体有吸附法[5]、絮凝法[6]、膜分离法[7-8]和光催化[9]等。相较于其它方法,吸附法是一种更为经济有效的方法,具有成本低、可得性好、操作简单、去除效率高等优点,因此被广泛用于处理染料废水[10]。
农业废弃物具有数量丰富、易于收集的特点,近年来国内外学者对农业废弃物的吸附性能进行了广泛的研究[11]。甘蔗叶主要由纤维素、半纤维素及木质素等组成,含有能够吸附重金属离子的官能基团如羟基和羧基等,是一种天然且物美价廉的植物吸附剂[12]。但甘蔗叶表面缺乏吸附阴离子染料刚果红的基团,为此本研究用羟基磷灰石对甘蔗叶进行表面改性,以提高其吸附性能。
本文以甘蔗叶(Sugarcane leaf,SCL)为原料,采用共沉淀法在甘蔗叶上负载羟基磷灰石(hydroxyapatite,HA)后,得到的羟基磷灰石改性甘蔗叶(HA@SCL)可以增强对刚果红的吸附能力。改变pH值、初始浓度、吸附温度和吸附时间,进行吸附实验,研究不同的因素对刚果红吸附效果的影响,并探究了再生效果,以期为有机染料废水的处理提供一种解决方案。
1 材料与方法
1.1 材料与仪器
原料:甘蔗叶,洗涤烘干后粉碎,过0.074mm筛,备用。
药品:碳酸钠、无水氯化钙、氯化钠、磷酸二氢钾、盐酸、氢氧化钠(均为分析纯)。
722S型可见光分光光度计,PHS-3E型台式pH计,Bruker ALPHA型傅立叶红外光谱,TESCAN MIRA LMS型扫描电镜。
1.2 羟基磷灰石改性甘蔗叶(HA@SCL)的制备
在烧杯中加入9.0g甘蔗叶和60mL蒸馏水,用0.1mol·L-1的氢氧化钠溶液调节pH至10,然后将混合物置于60℃恒温水浴中搅拌。搅拌过程中加入120mL浓度为0.25mol·L-1的氯化钙溶液,然后缓慢滴加120mL浓度为0.15mol·L-1的磷酸二氢钾溶液,再继续搅拌3h,在室温下静置老化12h。老化结束后过滤,用去离子水洗涤数次后,在真空干燥箱中60℃下烘干,烘干后用研钵研磨后过0.15mm筛,得到羟基磷灰石改性甘蔗叶(HA@SCL)。
1.3 等电点的测定
配制0.01mol·L-1的氯化钠溶液,用盐酸溶液和氢氧化钠溶液分别调节pH为3.0~11.0。取20mL不同pH值的氯化钠溶液加入装有0.06g HA@SCL的锥形瓶中,在恒温振荡器中,150r·min-1、25℃下恒温振荡48h,震荡结束后直接测定pH值。
1.4 不同因素对吸附去除刚果红的影响
1.4.1 染料溶液酸度的影响
配制浓度为200mg·L-1的刚果红溶液,用0.1mol·L-1的盐酸和氢氧化钠溶液将刚果红溶液的pH分别调节至2.0~12.0。取50 mL不同pH值的刚果红溶液倒入150mL锥形瓶中,分别加入0.05g吸附剂,在恒温振荡器中,150r·min-1、25℃下震荡吸附3h。吸附完成后离心,取上清液,在波长为498nm的分光光度计中测定剩余浓度,按式(1)和式(2)计算吸附容量qe和吸附率η。
式中,C0和Ce分别为刚果红的初始浓度和平衡浓度,mg·L-1;qe为刚果红到达平衡时的吸附容量,mg·g-1;η为吸附率,%;V为刚果红溶液的体积,L;m为吸附剂的质量,g。
1.4.2 吸附时间的影响
配置pH=4.0、浓度分别为200、250、300mg·L-1的刚果红溶液。取50mL不同浓度的刚果红溶液加入0.05g吸附剂,吸附时间分别设置为2~800min。吸附完毕后离心,取上清液测定溶液的剩余浓度。
1.4.3 染料初始浓度的影响
配制浓度分别为200~700 mg·L-1的刚果红溶液,调节pH=4.0,取50mL不同浓度的刚果红溶液,分别加入0.05g甘蔗叶和0.05g的HA@SCL,吸附完毕后离心,取上清液测定溶液的剩余浓度。
1.4.4 吸附剂的循环再生实验
取pH=4.0、浓度为250mg·L-1的刚果红溶液50mL于锥形瓶中,加入0.5g的HA@SCL,振荡吸附完成后,过滤收集吸附剂。将收集到的吸附剂在0.2mol·L-1的氢氧化钠溶液中解吸8h,完成后用蒸馏水洗涤,烘干后得到再生的吸附剂。使用再生的吸附剂重复进行吸附解吸过程,以研究其再生性能。
2 结果与讨论
2.1 吸附材料的表征结果
2.1.1 扫描电镜分析
图1是甘蔗叶和HA@SCL的SEM图。图1(a)中,改性前的甘蔗叶表面相对平整光滑,表面的纳米小颗粒较少;图1(b)中,改性后的HA@SCL表面变得粗糙,原有的平整表面被破坏,表面有许多层状物质,该现象与Fan等人[13]的研究结果一致。这些层状纳米颗粒可能是纳米羟基磷灰石。

图1 甘蔗叶和HA@SCL的SEM图Fig. 1 SEM images of sugarcane leaves and HA@SCL
2.1.2 XRD谱图分析
为了进一步确认HA@SCL上形成的纳米小颗粒物质,对改性前后的甘蔗叶和羟基磷灰石进行了XRD分析,结果见图2。羟基磷灰石的XRD谱图中,11.6°、20.8°、23.4°、29.2°和34.1°处的晶体衍射峰,分别与羟基磷灰石的标准图卡(JCPDS,NO11-0293)在(020)、(-121)、(040)、(-112)、(022)晶面上的特征峰相对应,说明羟基磷灰石主要以CaPO3(OH)2·H2O的形式存在。改性后,HA@SCL的XRD谱图的对应位置上,出现了羟基磷灰石的特征衍射峰,说明HA@SCL表面生成了羟基磷灰石,扫描电镜图上的纳米小颗粒物质是羟基磷灰石。
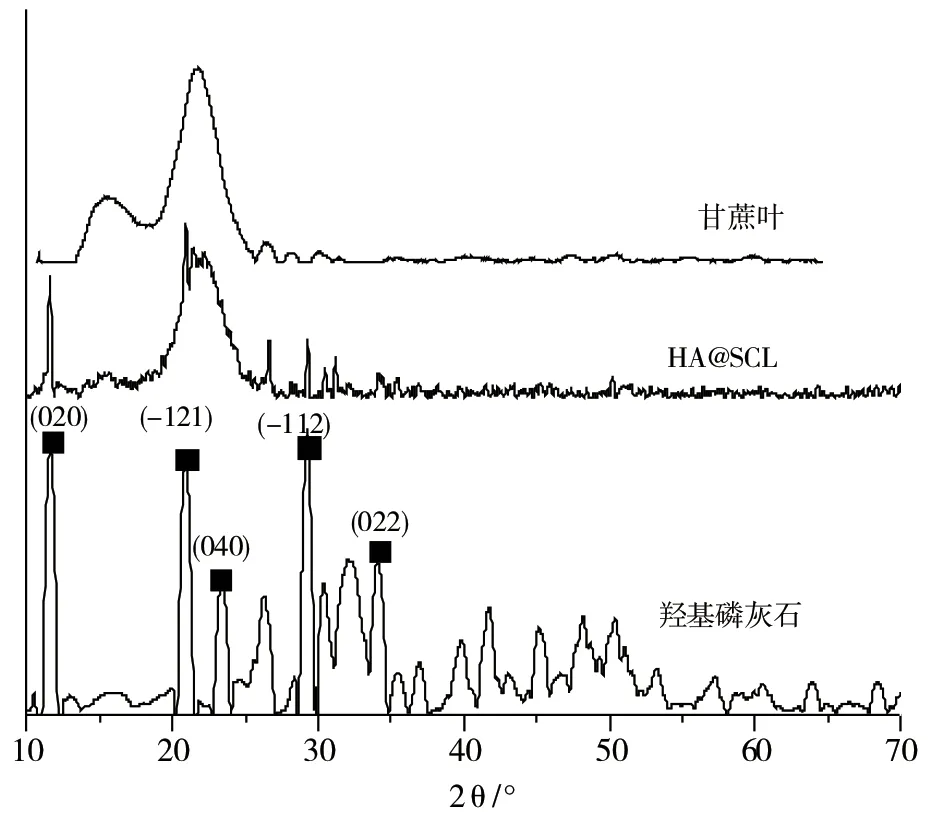
图2 改性前后的甘蔗叶和羟基磷灰石的XRD谱图Fig. 2 XRD patterns of sugarcane leaves and hydroxyapatite before and after modification
2.2 吸附实验结果与分析
2.2.1 吸附剂的等电点及pH对刚果红吸附性能的影响
吸附材料在溶液中的等电点直接影响其在不同pH溶液中的表面带电性[14]。HA@SCL的等电点实验结果见图3。由图3可知,HA@SCL的等电点pHzpc=7.68,当溶液的pH>7.68时,HA@SCL在溶液中表面带负电;当溶液的pH<7.68时,HA@SCL在溶液中表面带正电[15]。

图3 HA@SCL的等电点Fig.3 Isoelectric point of HA@SCL
溶液pH是影响吸附材料吸附性能的关键因素之一。图4显示了不同的溶液初始pH下,HA@SCL对刚果红的吸附性能。如图4所示,相比其他的初始pH,溶液初始pH=2时的吸附性能较低,可能是在较低的pH下,HA@SCL表面的羟基磷灰石发生了溶解而导致的。溶液初始pH在3~7范围内时,HA@SCL对刚果红有较好的吸附能力,吸附容量约为163.65 mg·g-1;溶液初始pH在8~12范围变化时,HA@SCL对刚果红的吸附容量,随着pH的升高而降低。这是因为HA@SCL的等电点为7.68,溶液pH在3~7时,吸附剂表面带正电,对阴离子染料刚果红的吸附能力较强[16];溶液pH在8~12时,吸附剂表面带负电,且随着pH升高,电负性增强,由此导致其对刚果红的吸附性能降低。
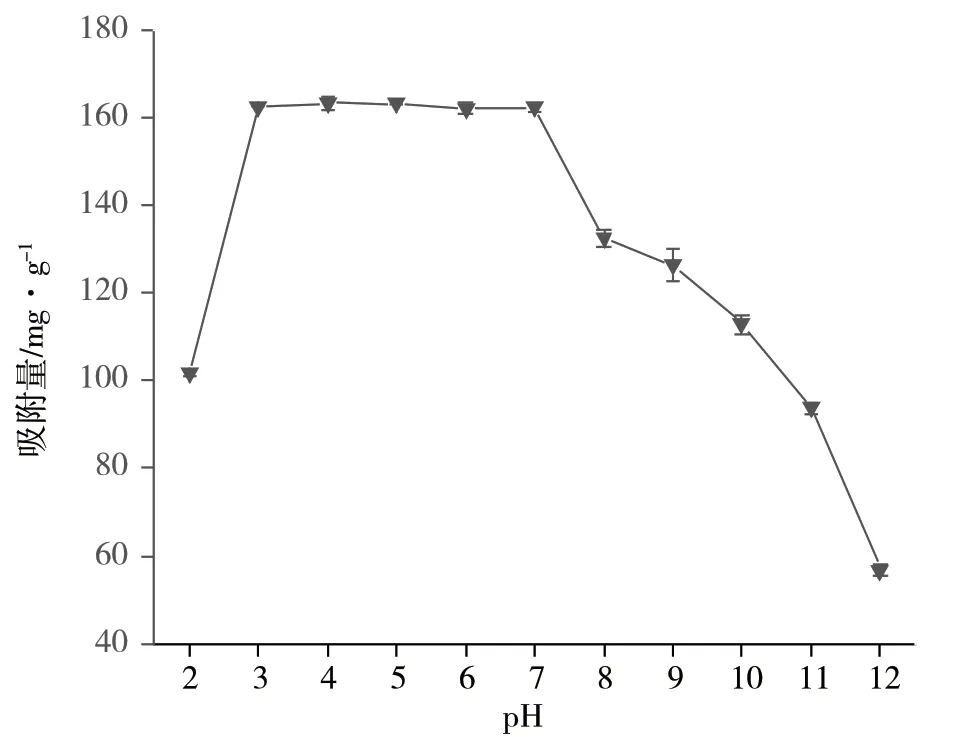
图4 pH对刚果红吸附性能的影响Fig.4 effect of pH on the adsorption property of Congo red
2.2.2 吸附时间对刚果红吸附性能的影响及吸附动力学研究
吸附时间是影响吸附剂吸附效果的重要因素之一。如图5所示,在刚果红初始浓度分别为200、250和300 mg·L-1的溶液中,平衡时HA@SCL对刚果红的吸附容量分别为163.70、187.01、201.86 mg·g-1。随着初始浓度增加,吸附容量呈升高的趋势;平衡时的吸附率分别为81.85%、74.80%、67.29%,呈现降低的趋势。这说明提高刚果红的浓度有利于提高HA@SCL的吸附容量,但会降低吸附率。由图5可知,随着时间延长,HA@SCL对刚果红的吸附量增加,达到吸附平衡后不再增加。在吸附初期(<120 min),HA@SCL吸附量的增加速度较快,吸附曲线较陡峭,之后吸附速度减慢,360 min时逐渐接近吸附平衡。原因是吸附初期溶液中刚果红的浓度较高,同时吸附剂表面空余的吸附位点也较多,溶液中的刚果红与吸附位点迅速结合;随着吸附位点减少,后期的吸附速度出现下降,之后吸附速度与解吸速度达到平衡,吸附容量保持稳定。

图5 吸附时间对刚果红吸附性能的影响Fig. 5 Effect of the adsorption time on the adsorption performance of Congo red
吸附动力学模型是研究吸附机理的重要方法之一。采用常用的准一级动力学模型[(式3)]、准二级动力学模型[(式4)]和颗粒内扩散动力学模型[(式5)],对不同的改性时间下,HA@SCL对刚果红的吸附容量数据进行拟合[17],拟合结果见图6,具体拟合参数见表1。

表1 吸附动力学拟合参数Table 1 The parameter of adsorption kinetics

图6 准一级动力学模型(a)和准二级动力学模型(b)拟合图Fig. 6 Fitting diagram of QFO kinetic (a) and QSO kinetic (b) model
式中,qt和qe分别是吸附剂对刚果红在t时刻和平衡时的吸附量,mg·g-1;k1和k2分别为准一级和准二级的吸附速率常数;kd为颗粒内扩散模型的速率常数;c为吸附过程中刚果红与吸附剂之间的边界层的厚度。
从图6和表1可知,由初始浓度分别为200、250和300mg·L-1的刚果红吸附数据拟合得到的参数中,准二级动力学模型的理论吸附量qe2均比准一级模型qe1更接近实验值。此外,准二级动力学模型拟合参数中的相关系数R2均大于0.98,比准一级更高,均说明准二级动力学模型可以更好地描述HA@SCL吸附刚果红的过程,吸附过程主要由化学吸附控制。由颗粒内扩散模型的拟合参数可知,在不同初始浓度的刚果红的吸附过程中,刚果红与HA@SCL之间的边界层厚度均不为零,说明该吸附过程由颗粒内扩散和边界层扩散共同控制[18]。
2.2.3 初始浓度对刚果红吸附性能的影响及等温吸附线研究
刚果红的初始浓度是影响吸附剂吸附效果的重要因素之一。如图7所示,在刚果红初始浓度为150~600mg·L-1的溶液中,随着刚果红的初始浓度提高,HA@SCL和甘蔗叶对刚果红的吸附量随之增大,但吸附率随之降低。这是因为随着刚果红的初始浓度增大,传质推动力增大,吸附量增加,但HA@SCL和甘蔗叶上的吸附位点有限,所以吸附率下降。采用常用的Langmuir方程[(式6)]和Freundlich等温线方程[(式7)][19-20]对图7的数据进行拟合,得到的模型参数见表2。

表2 等温吸附线的拟合参数Table 2 The fitting parameters of isothermal adsorption line
式中,Ce为吸附后溶液中刚果红的剩余浓度,mg·L-1;qe为吸附剂的平衡吸附量,mg·g-1;kL为Langmuir等温线模型与吸附能有关的常数;kF是Freundlich 等温线模型与吸附容量相关的常数;n为Freundlich等温线模型与温度相关的常数。
由表2可知,由HA@SCL和甘蔗叶对刚果红的吸附数据拟合得到的Langmuir的相关系数R2,大于Freundlich模型,说明HA@SCL和甘蔗叶吸附刚果红的过程,更符合Langmuir等温线模型,该过程为单分子层吸附。拟合得到的HA@SCL吸附刚果红的Freundlich模型中的n为5.1282(2<n<10),说明该吸附过程属于优惠吸附,易于进行。HA@SCL对刚果红的理论吸附量为270.27mg·g-1,相比未改性的甘蔗叶提高了59.46%。
2.2.4 再生性能研究
收集吸附后的HA@SCL,用氢氧化钠溶液进行再生,再生实验结果见图8。由图8可知,HA@SCL对刚果红的初次吸附量为187.13mg·g-1,再生5次后的吸附量为163.21mg·g-1,是初次吸附量的87.22%,说明HA@SCL在使用过程中具有良好的再生性能。

图8 再生实验结果Fig.8 regeneration test results
3 结论
本文以甘蔗叶为原料,采用共沉淀法对甘蔗叶进行表面改性,制备得到了HA@SCL,并用于水中刚果红的吸附。使用XRD和扫描电镜表征了HA@SCL的表面形貌,通过吸附实验探究了其对刚果红的吸附特性,得出以下结论:
1)XRD和SEM的表征结果说明,改性过程成功地将羟基磷灰石引入甘蔗叶表面,制备得到了HA@SCL。
2)吸附实验结果表明,在pH=3~7的范围内,HA@SCL对刚果红均有较高的吸附量,并在360min时达到吸附平衡。吸附过程符合Langmuir等温吸附模型和准二级吸附动力学模型,说明该吸附过程主要为单分子层吸附,受到化学吸附控制。
3)HA@SCL对刚果红的理论吸附量为270.27mg·g-1,相比未改性的甘蔗叶提高了59.46%。再生实验结果表明,HA@SCL再生5次后的吸附量为163.21mg·g-1,表明HA@SCL具有良好的再生性能。
