研究硼替佐米联合地塞米松、来那度胺化疗方案治疗多发性骨髓瘤的安全性
2023-10-27蔡亚云丁琳琳陈婷何国民
蔡亚云,丁琳琳,陈婷,何国民
南通大学附属如皋医院血液介入科,江苏如皋 226500
血液肿瘤类型多样,恶化程度高,其中多发性骨髓瘤较常见,此类肿瘤和浆细胞代谢有较高相关性,一般在中老年人群中出现,有浆细胞无限增生的特点,多数患者伴随免疫球蛋白异常分泌的情况,诱发多器官损伤[1]。化学物质接触、辐射、感染等都可能造成多发性骨髓瘤,当前治疗方案有骨髓移植、免疫治疗等,但缓解率始终维持在较低水平,多数患者生存周期较短,为提升缓解率,常经化疗辅助抑制浆细胞增殖[2-3]。硼替佐米使用频率高,经使用后能有效抑制蛋白酶,可使骨髓肿瘤细胞走向凋亡,快速减轻骨髓瘤相关症状,地塞米松则有较好的新生血管抑制作用,能防止骨髓瘤加重[4]。但上述两种化疗药物的辅助效果有限,仍有骨髓瘤反复加重的情况,近年来那度胺得到使用,其化学结果被证实与沙利度胺有较高相似性,可维持较强免疫调节机制,能阻止血管新生,提高抗肿瘤强度[5]。对此,本研究以2022 年3月—2023 年3 月南通大学附属如皋医院血液介入科42 例多发性骨髓瘤患者为研究对象,重点是分析硼替佐米+地塞米松+来那度胺化疗的安全性。现报道如下。
1 资料与方法
1.1 一般资料
以本院多发性骨髓瘤患者42 例为研究对象,根据双色球法分组,参考组、化疗组均21 例。参考组:年龄45~80 岁,平均(62.81±2.09)岁;男13 例,女8 例;Ⅰ期10 例,Ⅱ期7 例,Ⅲ期4 例;病程1~10 个月,平均(5.79±1.64)个月。化疗组:年龄46~81 岁,平均(63.03±2.42)岁;男12 例,女9 例;Ⅰ期9 例,Ⅱ期8 例,Ⅲ期4 例;病程1~11 个月,平均(6.23±1.55)个月。组间资料对比,差异无统计学意义(P>0.05)。具有可比性。医院医学伦理委员会已批准本研究。
1.2 纳入与排除标准
纳入标准:①病理结果为多发性骨髓瘤;②未行其他骨髓瘤治疗;③同意研究;④各化疗药物可耐受;⑤生存期评估后预计在半年以上。
排除标准:①难治性多发性骨髓瘤者;②有重度心血管病变者;③非骨髓瘤造成的慢性肾脏病者;④对各化疗方案不配合者;⑤血管状态极差,不适宜化疗者。
1.3 方法
参考组:以硼替佐米(国药准字H20204018;规格:3.5 mg)+地塞米松(国药准字H41021038;规格:0.75 mg)为所用方案,硼替佐米使用1.3 mg/m²的剂量,治疗途径为皮下注射,d1、8、15、22 应用。地塞米松使用40 mg/周的剂量,口服20 mg gd×2 d。28 d为1 个化疗周期,共化疗3 个周期。
化疗组:增加来那度胺(国药准字:H20193115;规格:25 mg)治疗,其中硼替佐米以及地塞米松需保持和参考组相同的使用方案,在来那度胺使用期间,需维持单次25 mg 的剂量,经口服途径完成治疗,化疗1~21 d 时均进行口服,口服时间为早上,1 次/d。维持和参考组相同的化疗周期。
1.4 观察指标
①生化指标:化疗前后采集静脉血,采集前确保骨髓瘤患者处于空腹状态,在3 000r/min 的数据下处理标本,处理时间为10 min,在全自动分析仪中放入得到的血清标本,实施各指标的检测即可,具体有β2-微球蛋白(β2-microglobulinβ, β2-MG)、单克隆蛋白(M 蛋白),同时要统计各组患者的骨髓瘤细胞比例。
②免疫指标:化疗前后采集静脉血,采集前提和标本离心数据均与生化指标检验保持一致,仅荧光原位杂交技术完成指标检测,有CD3+、CD8+以及CD4+等。
③安全性:对不良反应实施评估,具体有脱发、恶心呕吐等,还需统计白细胞减少等发生情况。
1.5 统计方法
以SPSS 26.0 统计学软件为计算软件,计量资料均符合正态分布,采用(±s)表示,行t检验,计数资料采用例数(n)和率(%)表示,进行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者生化指标比较
化疗后,3 项生化指标,与化疗前相比均下降,且化疗组低于参考组,差异有统计学意义(P<0.05)。见表1。
表1 两组患者生化指标比较(±s)

表1 两组患者生化指标比较(±s)
组别化疗组(n=21)参考组(n=21)t 值P 值β2-MG(μg/mL)化疗前11.02±1.59 11.24±1.04 0.531 0.599化疗后3.08±0.55 6.19±0.76 15.192<0.001 M 蛋白(g/L)化疗前51.77±5.08 51.19±5.48 0.356 0.724化疗后22.05±3.96 27.24±3.81 4.328<0.001骨髓瘤细胞比例(%)化疗前37.92±3.05 37.44±3.31 0.489 0.628化疗后14.08±2.89 18.93±2.55 5.767<0.001
2.2 两组患者免疫指标比较
化疗后,化疗组CD3+和CD4+高于参考组,CD8+低于参考组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者免疫指标比较[(±s),%]
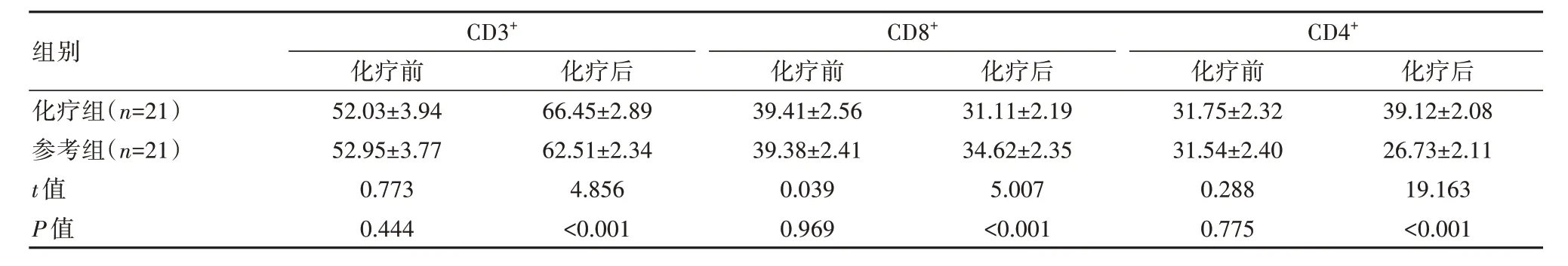
表2 两组患者免疫指标比较[(±s),%]
组别化疗组(n=21)参考组(n=21)t 值P 值CD3+CD8+CD4+化疗前52.03±3.94 52.95±3.77 0.773 0.444化疗后66.45±2.89 62.51±2.34 4.856<0.001化疗前39.41±2.56 39.38±2.41 0.039 0.969化疗后31.11±2.19 34.62±2.35 5.007<0.001化疗前31.75±2.32 31.54±2.40 0.288 0.775化疗后39.12±2.08 26.73±2.11 19.163<0.001
2.3 两组患者安全性比较
化疗组、参考组不良反应总发生率比较,差异无统计学意义(P>0.05)。见表3。
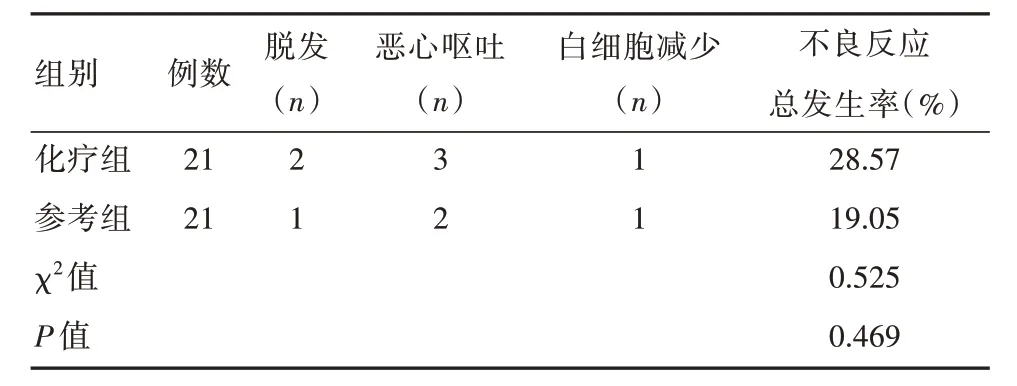
表3 两组患者安全性比较
3 讨论
多发性骨髓瘤较为特殊,为浆细胞恶性增殖所致,表现为单克隆免疫球蛋白水平升高,而正常免疫球蛋白分泌不足,在骨髓瘤发展期间有广泛性浸润的问题,多数患者生存期短[6]。化疗为骨髓瘤常见治疗方案,往常使用硼替佐米以及地塞米松完成化疗。硼替佐米使用时间长,作为双肽基硼酸盐类似物,可达到较好肿瘤细胞粘附因子阻碍机制,同时能抑制生长因子分泌,提高肿瘤细胞敏感度,保持较高骨髓瘤缓解率[7]。此药可在细胞核因子kB 表达中维持较好阻碍机制,能增强肿瘤细胞杀伤效果,但此药会抑制神经因子生长,阻止神经因子的分化,常诱发各类神经病变,降低了抗肿瘤治疗安全性[8-9]。糖皮质激素在各类病变中均有使用,应用在多发性骨髓瘤治疗时,能增强蛋白质抑制效果,可保持较好蛋白质分解状态,增强硼替佐米疗效。以硼替佐米为基础,辅以地塞米松可达到一定的肿瘤杀伤机制,但此类骨髓瘤存在骨质破坏严重的情况,无法维持较好磷钙代谢状态,常降低抗肿瘤效果,需调整化疗方案[10]。来那度胺被证实有较好效果,此药能缩短肿瘤细胞凋亡时间,有效抑制细胞增殖,可提高骨髓瘤缓解率,常被应用于多发性骨髓瘤治疗中,但临床对来那度胺的安全性研究较少[11]。
本研究中,化疗组、参考组不良事件间发生率分别为28.57%、19.05%,两者对比差异无统计学意义(P>0.05)。毛沛沛等[12]的研究中,观察组、对照组不良事件间发生率分别为25.00%、29.17%,两者对比差异无统计学意义(P>0.05)。即联合化疗方案安全性高,能减少骨髓瘤治疗不良事件。辅以来那度胺治疗,能增强免疫调节机制,此药可增强NK 细胞识别能力,有效杀伤肿瘤细胞,并能对肿瘤细胞周期停滞发挥一定引导作用,有效抑制新生血管,防止骨髓瘤加重[13]。作为免疫调节药物,来那度胺可对浆细胞微环境进行有效攻击,达到较好肿瘤细胞凋亡机制,还能防控新生血管,一般不会产生神经毒性,安全性高,可降低多发性骨髓瘤治疗风险[14]。以硼替佐米、地塞米松为基础,增加来那度胺治疗,能增强抗肿瘤机制,有效降低骨髓瘤细胞比例,同时能缓解破骨细胞损害问题,改善多发性骨髓瘤预后[15]。
综上所述,硼替佐米+地塞米松+来那度胺的方案有多重优势,缓解率高、免疫调节机制好、抗肿瘤效果强等,且能控制用药安全问题,建议多发性骨髓瘤患者选择。
